Escolar Documentos
Profissional Documentos
Cultura Documentos
Segunda Lei Da TermodinÂmica
Enviado por
Juliane Froncheti de MouraDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Segunda Lei Da TermodinÂmica
Enviado por
Juliane Froncheti de MouraDireitos autorais:
Formatos disponíveis
A SEGUNDA LEI DA TERMODINMICA
ENTROPIA
Santo ngelo, 23 de junho de 2014
Universidade Regional Integrada do Alto Uruguai e das Misses
Qumica Industrial
Fsico-Qumica I
Mquina a vapor 1769 (James Watt).
Calor como energia 1842 (Primeira Lei da
Termodinmica.
Segunda Lei da Termodinmica origem em 1824 por
Carnot (rendimento das mquinas trmicas).
calor como um fluido indestrutvel, ao transferir-se
da fonte quente para a fonte fria , era capaz de produzir
trabalho.
2
Mquina sistema que sofre transformaes
cclicas que podem ser repetidas indefinidamente.
Movimentao sem atrito converso de
quantidades ilimitadas de uma forma de trabalho
em outra .
Processo inverso inverso do ciclo da mquina
3
GERADOR E MOTOR ELTRICO
Figura pag. 280
4
Figura 1 Esquema de gerador e motor eltrico
ESQUEMA DE MQUINA TRMICA
Um reservatrio de calor no igual a um reservatrio
de trabalho.
5
Figura 2 Esquema de mquina trmica
EM RESUMO...
Enquanto se verifica perfeita reversibilidade na
converso de uma forma de trabalho em outra,
mediante processos cclicos e isotrmicos do
sistema, a converso de trabalho em calor
irreversvel nas mesmas condies.
6
SEGUNDA LEI DA TERMODINMICA:
IMPOSSIBILIDADE DE MQUINAS PERFEITAS
Enunciado de Kelvin-Plank (mquinas trmicas):
impossvel um processo cclico de converso
completa de calor em trabalho a partir de um nico
reservatrio trmico. (eficincia e < 1)
7
Enunciado de Clausius (refrigeradores):
impossvel um processo cclico que resulte
na transferncia completa de calor de um corpo frio
para um corpo quente. (desempenho Kp < )
SEGUNDA LEI DA TERMODINMICA:
IMPOSSIBILIDADE DE MQUINAS PERFEITAS
8
MQUINAS TRMICAS
A converso contnua de
calor em trabalho s
possvel em mquinas
trmicas.
U = 0 (energia interna
nula);
-w = q = q
1
+ q
2
9
MQUINA TRMICA
10
Rendimento - a razo entre o resultado colhido e
o investimento feito.
Rendimento termodinmico ()
Razo entre o trabalho produzido (-w), ao trmino
de um ciclo, e o calor recebido da fonte quente
(Q
1
).
= -w =Q
1
+ Q
2
Q
1
Q
1
MQUINAS TRMICAS
11
Exemplo 1:
Um motor vapor realiza um trabalho de 12kJ
quando lhe fornecido uma quantidade de calor
igual a 23kJ. Qual a capacidade percentual que o
motor tem de transformar energia trmica em
trabalho?
MQUINAS TRMICAS
12
MQUINA FRIGORFICA
A irreversibilidade que caracteriza a transferncia
de calor de uma fonte quente, de temperatura t
1
,
para uma fonte fria, de temperatura t
2
.
A transferncia de calor de uma fonte fria a um
fonte quente, s possvel a custa do consumo de
trabalho num dispositivo chamado mquina
frigorfica ou bomba trmica.
13
uma mquina
trmica de ciclo
invertido.
Uma quantidade de
calor Q
2
, retirada da
fonte fria t
2
, e
transferida a fonte
quente t
1
, a custa do
consumo de trabalho,
w.
Q
1
+ Q
2
+ W = 0
MQUINA FRIGORFICA
14
A eficincia de um mquina frigorfica definida
pela razo entre o calor Q
2
subtrado da fonte fria e
o trabalho consumido:
MQUINA FRIGORFICA
= Q
2
= Q
2
w
-(Q
1
+ Q
2
)
15
O TEOREMA DE CARNOT
Carnot mostrou que todas as mquinas trmicas,
que funcionem reversivelmente entre as mesmas
temperaturas da fonte quente e da fonte fria,
possuem o mesmo rendimento e este s depende
das temperaturas das fontes e no da natureza do
agente transformador.
16
O CICLO DE CARNOT
D-se o nome de ciclo de Carnot (ou mquina de
Carnot) a um ciclo de duas temperaturas e reversvel
constitudo de duas isotermas e duas adiabticas.
17
O CICLO DE CARNOT
O ciclo da Carnot num diagrama P-V
18
O CICLO DE CARNOT
O rendimento do ciclo de Carnot a razo entre o
trabalho produzido e o calor recebido da fonte
quente.
O rendimento tanto maior quanto mais alta a
temperatura da fonte quente e mais baixa a
temperatura da fonte fria.
= Q
1
+ Q
2
= T
2
- T
1
Q
1
T
2
19
O CICLO DE CARNOT
Exemplo 2:
Comparar o rendimento termodinmico de
duas mquinas a vapor, a primeira operando com
vapor dgua a presso de 1 atm (100C) e a
segunda com vapor dgua a presso de 50 atm
(265C). Em ambos os casos, a temperatura do
condensador de 35C.
20
O CICLO DE CARNOT
O ciclo de Carnot invertido corresponde a uma mquina
frigorfica ou bomba trmica cuja eficincia ser
expressa por:
O trabalho consumido para transferir uma certa
quantidade de calor Q
2
da fonte fria para a fonte quente
ser:
O w ser tanto maior quanto maior for a diferena de T
entre as duas fontes, e ser nulo quando T
1
= T
2
= Q
2
= Q
2
= T
2
w Q
1
+Q
2
T
1
-
T
2
w = Q
2
T
1
-
T
2
T
1
21
O CICLO DE CARNOT
Exemplo 3:
Calcular o trabalho necessrio para transferir
400 J do interior de um refrigerador domstico a
0C para o ar exterior a 25C, supondo
funcionamento reversvel.
22
PROPRIEDADES DO CICLO DE CARNOT
A razo q/T (J.K
-1
) entre o calor recebido
isotermicamente pelo sistema e a temperatura na
qual recebido chama-se quantidade reduzida de
calor.
Em todo o ciclo de Carnot, nula a soma das
quantidades reduzidas de calor recebidas pelo
sistema.
qr = 0
T
23
A FUNO DA ENTROPIA
24
A FUNO DA ENTROPIA
Processos endotrmicos e exotrmicos espontneos
25
ENTROPIA
Definio:
Todos estes processos respeitam a Primeira Lei da
Termodinmica.
Qualquer um dos processos mencionados poderia
ocorrer em ambas as direes sem contrariar a
Primeira Lei.
Os sistemas tendem a aumentar sua desordem ao
mesmo tempo em que procuram minimizar sua
energia.
26
ENTROPIA
a medida da desordem de um sistema, definida
como:
A Entropia uma funo de estado.
27
ENTROPIA
Para calcular o acrscimo de entropia de um
sistema entre dois estados ligados por um processo
irreversvel, um dos seguintes recursos pode ser usado:
Se apresentar uma sequncia de etapas reversvel
entre os mesmos estados usa-se a equao S = q
r
/T
Estabelecida a dependncia funcional entre entropia
e outras variveis de estado de um sistema, pode-se
calcular S em funo dessas variveis.
28
CRIAO A ENTROPIA NOS PROCESSOS
IRREVERSVEIS
Uma transformao de um sistema entre dois
estados (1 e 2) ser:
S = S
2
S
1
Em processos reversveis, o acrscimo de
entropia S do sistema igual a entropia recebida,
mas em processos irreversveis, a entropia
recebida inferior ao acrscimo S, porque a
entropia foi criada no interior do sistema pela
prpria irreversibilidade do processo.
29
CRIAO A ENTROPIA NOS PROCESSOS
IRREVERSVEIS
Representando entropia criada por e a entropia
recebida por S, teremos:
S = S +
Onde:
= 0 num processo reversvel
> 0 num processo irreversvel
A entropia no uma propriedade
conservativa, a no ser nos processos reversveis.
30
Exemplo 4:
Seja 0,409 mol de um gs ideal que ocupa o
volume de um litro sob a presso de 10 bar a 25C.
O gs, em contato com um reservatrio de calor a
25C, expande a uma presso final de 1 bar, sendo
de 25C a temperatura final. Calcular o acrscimo
de entropia, lembrando que, na transformao
isotrmica de um gs ideal. U = 0
31
VARIAO DE ENTROPIA DE UM SISTEMA SIMPLES
Variao da entropia com a temperatura e presso
Permite calcular a variao de entropia de uma
substncia, entre duas temperaturas, permanecendo a
presso constante (geralmente 1 bar).
Exigncia: conhecimento da funo C
p
(T)
Tratando-se de um gs, tem-se para um mol:
C
p
= + T + T
2
(valores tabelados)
32
Para gases:
S
p
= ln T
2
+ (T
2
T
1
) + 1 (T
2
2
T
1
2
)
T
1
2
Se o intervalo de temperatura for pequeno, ou
se for usada uma capacidade trmica mdia entre
a temperaturas consideradas tem-se:
S
p
= n <C
p
> ln T
2
T
1
33
Exemplo 5:
Um mol de H2 (g) aquecido sob presso
constante de 1 bar de 25C a 200C. Calcular o
acrscimo de entropia do gs:
a) Considerando a variao de C
p
com a
temperatura;
b) Admitindo para C
p
um valor mdio igual a 30
J.mol
-1
K
-1
34
Para os slidos
A capacidade trmica molar varia com a
temperatura segundo:
C
p
= a + bT - cT
2
(valores tabelados)
S
p
= a ln T
2
+ b (T
2
T
1
) + 1 c (T
2
-2
T
1
- 2
)
T
1
2
Exemplo 6:
Um mol de CaO(s) aquecido sob presso
constante de 27C a 527C. Calcular o acrscimo de
entropia do slido.
35
VARIAO DE ENTROPIA DE UM GS IDEAL
Gases ideais so sistemas simples e admite-se que as
capacidades trmicas Cv e Cp so independentes da
temperatura.
Variao de entropia com a temperatura e com o volume
S = n C
V
ln T
2
+ n R ln V
2
T
1
V
1
A variao de entropia corresponde a uma variao
finita de temperatura e volume.
36
Variao de entropia com a temperatura e a presso
S = n C
p
ln T
2
- n R ln V
2
T
1
V
1
Exemplo 7:
Um mol de gs diatmico (C
p
= 29,3 J.mol
-1
K
-1
)
aquecido de 25C a 100C sob presso constante e
comprimido isotermicamente de 1 bar a 3 bar.
Calcular o acrscimo de entropia do gs.
37
DIFERENAS ENTRE C
P
E C
V
A diferena entre as capacidades trmicas a
presso constante e a volume constante, de um
sistema simples dada por:
C
p
C
v
=
2
TV
No caso dos gases ideais, = 1/T e = 1/P,
resultando:
C
p
C
v
= PV = nR
T
38
DIFERENAS ENTRE C
P
E C
V
Exemplo 8:
Calcular a diferena C
p
C
v
para o cobre, a
25C, sabendo que, nessa temperatura, = 49,2 x
10
-6
K
-1
, = 7,75 x 10
-12
Pa
-1
e a densidade 8930
kg.m
3
.
39
ENTROPIA DE MUDANA DE FASE
Tratando-se de uma substncia pura, a entropia de
mudana de fase pode ser considerada como o
acrscimo de entropia que acompanha a
transferncia de um mol de substncia de uma a
outra fase em equilbrio, a temperatura e presso
constantes.
Tem-se ento:
S = S
2
S
1
40
ENTROPIA DE MUDANA DE FASE
Notando-se que o processo :
a) Reversvel, porque ocorre em equilbrio ( = 0);
b) Isotrmico e isobrico;
c) Termelstico (w = 0)
Tratando-se de um processo reversvel e
isotrmico, tem-se:
S = q
r
= H
T T
41
ENTROPIA DE MUDANA DE FASE
Exemplo 9:
A fuso de um mol de gua a 0C e presso
de 1 atm:
H
2
O (s) = H
2
O (l) H = 6017 J.mol
-1
A vaporizao de um mol de gua a 25C, sob
a prpria presso de vapor, que de 0,0313 atm:
H
2
O (l) = H
2
O (g, 0,0113 atm) H = 43990 J.mol
-1
42
ENTROPIA DE MISTURA
Considerada como o acrscimo de entropia que
acompanha a formao de uma soluo, a partir os
componentes puros, a temperatura e presso
constantes.
No processo de mistura, cada componente sofre
uma diluio e, portanto, um aumento de desordem
e de entropia, embora a energia permanea
constante.
S = S (soluo) S (componentes puros)
43
ENTROPIA DE MISTURA
Para um numero qualquer de mol de gases ideais,
tem-se:
S = -R n ln x
Para um nmero qualquer de massa, tem-se:
S = M C
P
ln T
2
T
1
44
ENTROPIA DE MISTURA
Exemplo 10:
Qual o acrscimo de entropia por mol que
acompanha a formao de uma mistura cuja
composio em volume 79% de nitrognio, 20%
de oxignio e 1% de argnio, a temperatura e
presso constantes, admitindo-se comportamento
ideal dos gases
45
ENTROPIA DE MISTURA
Exemplo 11:
Cem gramas de gua a 100C so
adicionados a 50 gramas de gua a 25C, sob
presso constante, em recipiente adiabtico.
Admite-se que o calor especfico da gua seja
independente da temperatura e igual a 4,184 kJ.
Kg
-1
K
-1
. Calcular a temperatura final e a entropia
criada no processo.
46
ENTROPIA DE MISTURA
Exemplo 12:
Dois recipientes de paredes adiabticas, como
no exemplo anterior, contm cada qual um mol de
gs ideal na mesma presso de 1 bar, mas,
enquanto a temperatura no primeiro recipiente de
27C no segundo d 327C. Abrindo a vlvula, o
sistema atinge o equilbrio. Determinar a entropia
criada no processo quando os gases so idnticos
e quando so diferentes supondo que , em ambos
os casos, Cp = 21 J. mol
-1
K
-1
47
Você também pode gostar
- Ativ. Adaptadas Ciências - 3º AnoDocumento88 páginasAtiv. Adaptadas Ciências - 3º AnoAninha Ribeiro100% (3)
- 30 Dias de Noite - História Pronta Storytelling PDFDocumento16 páginas30 Dias de Noite - História Pronta Storytelling PDFOscar Moura100% (1)
- Gases ideais: leis de Boyle, Charles e Gay-LussacDocumento2 páginasGases ideais: leis de Boyle, Charles e Gay-LussacJuliane Froncheti de MouraAinda não há avaliações
- Introdução à análise técnica e fundamentos básicos do mercado financeiroDocumento63 páginasIntrodução à análise técnica e fundamentos básicos do mercado financeiroRodrigo MatioliAinda não há avaliações
- Liturgia de São João CrisóstomoDocumento35 páginasLiturgia de São João CrisóstomoPereiraManoelAinda não há avaliações
- 3 - Soluções ReaisDocumento4 páginas3 - Soluções ReaisJuliane Froncheti de MouraAinda não há avaliações
- Potenciometria - Aula PráticaDocumento1 páginaPotenciometria - Aula PráticaJuliane Froncheti de MouraAinda não há avaliações
- Segurança em LaboratórioDocumento16 páginasSegurança em LaboratórioJuliane Froncheti de MouraAinda não há avaliações
- 2 - Termodinâmica Dassoluções Não-Eletrolíticas - Soluções IdeaisDocumento3 páginas2 - Termodinâmica Dassoluções Não-Eletrolíticas - Soluções IdeaisJuliane Froncheti de MouraAinda não há avaliações
- 1 - Equilíbrio Líq-VaporDocumento3 páginas1 - Equilíbrio Líq-VaporJuliane Froncheti de MouraAinda não há avaliações
- 1 - Equilíbrio Líq-VaporDocumento3 páginas1 - Equilíbrio Líq-VaporJuliane Froncheti de MouraAinda não há avaliações
- Segurança em LaboratórioDocumento3 páginasSegurança em LaboratórioJuliane Froncheti de MouraAinda não há avaliações
- Aula Prática - Preparo de SoluçõesDocumento1 páginaAula Prática - Preparo de SoluçõesJuliane Froncheti de MouraAinda não há avaliações
- Espectroscopia de Absorção Atômica - Forno de GrafiteDocumento11 páginasEspectroscopia de Absorção Atômica - Forno de GrafiteJuliane Froncheti de MouraAinda não há avaliações
- Calorimetria - Aula Prática 1Documento1 páginaCalorimetria - Aula Prática 1Juliane Froncheti de MouraAinda não há avaliações
- Espectometria de Absorção Atômica - FaasDocumento8 páginasEspectometria de Absorção Atômica - FaasJuliane Froncheti de MouraAinda não há avaliações
- Cromatografia Líquida de Alta EficiênciaDocumento10 páginasCromatografia Líquida de Alta EficiênciaJuliane Froncheti de MouraAinda não há avaliações
- Apostila Química Orgânica ExperimentalDocumento18 páginasApostila Química Orgânica ExperimentalJuliane Froncheti de MouraAinda não há avaliações
- Determinação de Cr6+ por espectrofotometriaDocumento12 páginasDeterminação de Cr6+ por espectrofotometriaJuliane Froncheti de MouraAinda não há avaliações
- Físico-Química II - Soluções IdeaisDocumento1 páginaFísico-Química II - Soluções IdeaisJuliane Froncheti de MouraAinda não há avaliações
- Equilíbrio QuímicoDocumento3 páginasEquilíbrio QuímicoJuliane Froncheti de MouraAinda não há avaliações
- Espectroscopia de Absorção Molecular UV-vísDocumento65 páginasEspectroscopia de Absorção Molecular UV-vísJuliane Froncheti de Moura100% (1)
- Aula Experimental 01Documento1 páginaAula Experimental 01Juliane Froncheti de MouraAinda não há avaliações
- Corrosão de ligas metálicas experimentoDocumento2 páginasCorrosão de ligas metálicas experimentoJuliane Froncheti de MouraAinda não há avaliações
- Gases ideais e misturasDocumento3 páginasGases ideais e misturasJuliane Froncheti de MouraAinda não há avaliações
- Cinética QuímicaDocumento4 páginasCinética QuímicaJuliane Froncheti de MouraAinda não há avaliações
- Cxjme0z51tbc5j55il11wt45Isotermas de Frendlich e BETDocumento3 páginasCxjme0z51tbc5j55il11wt45Isotermas de Frendlich e BETJuliane Froncheti de MouraAinda não há avaliações
- Comportamento de GasesDocumento3 páginasComportamento de GasesJuliane Froncheti de MouraAinda não há avaliações
- Exercícios Gases Lei do Gás IdealDocumento1 páginaExercícios Gases Lei do Gás IdealJuliane Froncheti de MouraAinda não há avaliações
- 2 - Combustiveis - CombustaoDocumento18 páginas2 - Combustiveis - CombustaoGilmar DemenekAinda não há avaliações
- Aula Prática - Preparo de SoluçõesDocumento1 páginaAula Prática - Preparo de SoluçõesJuliane Froncheti de MouraAinda não há avaliações
- Equação de NernstDocumento1 páginaEquação de NernstJuliane Froncheti de MouraAinda não há avaliações
- Lista de Exercícios - 1 TermodinâmicaDocumento1 páginaLista de Exercícios - 1 TermodinâmicaJuliane Froncheti de MouraAinda não há avaliações
- Aula4 2Documento37 páginasAula4 2Lucas AssisAinda não há avaliações
- Manto PeridotíticoDocumento367 páginasManto Peridotítico19-2011ºB Ana Sofia Ferreira DuarteAinda não há avaliações
- Farmacologia cardiovascular: tratamentos e mecanismos de açãoDocumento5 páginasFarmacologia cardiovascular: tratamentos e mecanismos de açãoLARA GONÇALVES DA SILVAAinda não há avaliações
- Artigo - DesignDocumento15 páginasArtigo - DesignFábio Henrique Lucas da CostaAinda não há avaliações
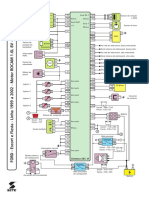
- FORD Escort Fiesta Linha 1999 A 2002 Motor ROCAM 1.6L 8V Sistema EEC VIDocumento1 páginaFORD Escort Fiesta Linha 1999 A 2002 Motor ROCAM 1.6L 8V Sistema EEC VICristianoAinda não há avaliações
- 59,37 Aderir Aderir 15,52 : Quanto Tenho A Pagar? Débito Na Minha Conta A Partir deDocumento3 páginas59,37 Aderir Aderir 15,52 : Quanto Tenho A Pagar? Débito Na Minha Conta A Partir deRose Mery de Jesus GomesAinda não há avaliações
- As 10 Novas Habilidades para o Trabalho PDFDocumento5 páginasAs 10 Novas Habilidades para o Trabalho PDFFabrício ZandonáAinda não há avaliações
- Circuito Elétrico Simulado 2Documento3 páginasCircuito Elétrico Simulado 2mlcsdrAinda não há avaliações
- SerDocumento8 páginasSerDiego BeckAinda não há avaliações
- O Alicerce de Seu CasamentoDocumento4 páginasO Alicerce de Seu CasamentoRafael PaixãoAinda não há avaliações
- Alimentação na BíbliaDocumento21 páginasAlimentação na BíbliaRav Yehunatan Mikhail ZaytsAinda não há avaliações
- NBR 1002 - Mascaras de Protecao Respiratoria de Uso Nao ProfissionalDocumento42 páginasNBR 1002 - Mascaras de Protecao Respiratoria de Uso Nao ProfissionalKildere AlmeidaAinda não há avaliações
- Transtorno de LinguagemDocumento8 páginasTranstorno de LinguagemmetalliraphaAinda não há avaliações
- Guia Corrimão DuploDocumento12 páginasGuia Corrimão DuploAndre VidalAinda não há avaliações
- Frater Achad - 31 Hinos A Deusa Das Estrelas (PT)Documento18 páginasFrater Achad - 31 Hinos A Deusa Das Estrelas (PT)Caléu N. MoraesAinda não há avaliações
- Ferramentas essenciais para eletricistasDocumento3 páginasFerramentas essenciais para eletricistasHeloisa RomãoAinda não há avaliações
- Oração Do EnriquecimentoDocumento11 páginasOração Do EnriquecimentodradivinhaAinda não há avaliações
- Dízimo Mirim: Ensinando a Prática do Dízimo na CatequeseDocumento8 páginasDízimo Mirim: Ensinando a Prática do Dízimo na CatequesegracyynhaAinda não há avaliações
- Spink - Frezza - Práticas DiscursivasDocumento23 páginasSpink - Frezza - Práticas DiscursivasClara RodriguesAinda não há avaliações
- IbamaDocumento17 páginasIbamaanon_700777709Ainda não há avaliações
- Sumariospnmgulsumariospdf23o20sumario PDFDocumento96 páginasSumariospnmgulsumariospdf23o20sumario PDFpedro manjarres figueredoAinda não há avaliações
- Relatório parcial de Psicologia ExperimentalDocumento16 páginasRelatório parcial de Psicologia ExperimentalGEOVANA RISSATO GARCIAAinda não há avaliações
- Plano de Aula Geo7 07und02Documento15 páginasPlano de Aula Geo7 07und02Cristian Chaves RodriguesAinda não há avaliações
- Bioinsumos Na Agricultura BrasileiraDocumento100 páginasBioinsumos Na Agricultura BrasileiraJOAO LUCAS XAVIER AZEVEDOAinda não há avaliações
- Gazeta de AustinDocumento8 páginasGazeta de AustinAndre de SouzaAinda não há avaliações
- A Mulher No Terceiro Milênio - Rose MuranoDocumento205 páginasA Mulher No Terceiro Milênio - Rose MuranoEdilson SouzaAinda não há avaliações