Escolar Documentos
Profissional Documentos
Cultura Documentos
Cap 2 - Sist Fe-C
Enviado por
Tales NascimentoDescrição original:
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Cap 2 - Sist Fe-C
Enviado por
Tales NascimentoDireitos autorais:
Formatos disponíveis
Universidade Federal de Ouro Preto
Escola de Minas
Departamento de Engenharia Metalúrgica e de Materiais
Tratamento Térmico dos
Metais
Capítulo 2 – Sistema Ferro-Carbono
Prof. Dr. Geraldo Lúcio de Faria
e-mail:geraldofaria@ufop.edu.br ou geraldolfaria@yahoo.com.br
Laboratório de Tratamentos Térmicos e Microscopia Óptica (LTM)
https://geraldolfaria.wixsite.com/ltmemufop 1
Capítulo 2 –Sistema Fe-C O Elemento Fe
1. O Elemento Ferro
• Metal de Transição;
• Número atômico: 26;
• Massa molar: 55,85g/mol;
• Apresenta o fenômeno de alotropia ou polimorfismo;
• Constituinte de ligas metálicas de extrema importância.
Prof. Dr. Geraldo Lúcio de Faria 2
Capítulo 2 –Sistema Fe-C O Elemento Fe
Alotropia e Polimorfismo do Fe
Resfriamento Aquecimento
(Refroidissement) (Chauffage)
Ferro Líquido
Ar5 Ac5
1538oC
Fe d
(CCC) Ar4 Ac4
1394oC
Temperatura (oC)
Fe g
(CFC) Ar3 Ac3
912oC
Paramagnético
Ar2 Ac2
Fe a
770oC
(CCC)
Ferromagnético
20oC
Tempo Obs.: A - Arrêt
Prof. Dr. Geraldo Lúcio de Faria 3
Capítulo 2 –Sistema Fe-C O Elemento Fe
Fe a - CCC
Número de átomos por célula unitária: 1+(1/8)x8 = 2 átomos
Relação entre parâmetro de rede a e raio atômico r :
Fator de empacotamento (F.E.): F.E. = 0,679, ou seja, 68% ocupado por átomos
Os espaços vazios caracterizam interstícios octaédricos e tetraédricos.
Prof. Dr. Geraldo Lúcio de Faria 4
Capítulo 2 –Sistema Fe-C O Elemento Fe
Fe g - CFC
Número de átomos por célula unitária: 6x(1/2)+(1/8)x8 = 4 átomos
Relação entre parâmetro de rede a e raio atômico r :
Fator de empacotamento (F.E.): F.E. = 0,74 , ou seja, 74% ocupado por átomos
Os espaços vazios caracterizam interstícios octaédricos e tetraédricos.
Prof. Dr. Geraldo Lúcio de Faria 5
Capítulo 2 –Sistema Fe-C O Elemento Fe
Interstícios
Octaédricos Tetraédricos
Fe a - CCC Fe g - CFC
Prof. Dr. Geraldo Lúcio de Faria 6
Capítulo 2 –Sistema Fe-C O Elemento Fe
Curva Dilatométrica
Transformação Fe a para Fe g
Calculo do Volume molar (CCC)
Calculo do Volume molar (CFC)
Prof. Dr. Geraldo Lúcio de Faria 7
Capítulo 2 –Sistema Fe-C Soluções Sólidas de Fe
2. Soluções Sólidas de Ferro
Sistema de Grande
Sistema Fe-C
Importância
Solvente Soluto
Vejamos algumas características importantes:
Relação (ri/rm)
Estrutura F.E.
Octaédrico Tetraédrico
CFC 0,414 0,225 0,74
CCC 0,154 0,291 0,68
ri – Raio do átomo intersticial;
rm – Raio do átomo da matriz;
Prof. Dr. Geraldo Lúcio de Faria 8
Capítulo 2 –Sistema Fe-C Soluções Sólidas de Fe
Vejamos outras características importantes:
Ferro Carbono
Intersticial Substitucional
Temperatura Raio Fe
Estrutura Raio do
(oC) (Å) Raio do vão Raio do C (Å) a
vão ± 15% do Raio
tetraédrico 15oC
octaédrico do Fe (Å)
(Å)
(Å)
500 CCC 1,25 0,19 0,36 1,06-1,44
1000 CFC 1,29 0,53 0,29 1,10-1,48 0,71
Baixa solubilidade do C:
a – máximo de 0,02% (727oC);
g – máximo de 2% (1148oC);
Prof. Dr. Geraldo Lúcio de Faria 9
Capítulo 2 –Sistema Fe-C Diagrama Ferro-Grafita
3. Diagrama Ferro-Grafita
A combinação de carbono e ferro, em equilíbrio termodinâmico, dará origem a
diferentes fases para as diversas temperaturas avaliadas. Este diagrama de fases de
equilíbrio termodinâmico é o diagrama Ferro-Grafita:
Tempos infinitamente grandes para que os processos difusionais ocorram.
Prof. Dr. Geraldo Lúcio de Faria 10
Capítulo 2 –Sistema Fe-C Diagrama Ferro-Cementita
4. Diagrama Ferro-Cementita
Diagrama Ferro-Cementita ≠ Diagrama de Equilíbrio
Fase Metaestável – Cementita (Fe3C)
Baixo coeficiente de Equilíbrio
difusão do C no Fe: Tempo muito longo Termodinâmico
D = 2,9x10-19cm2/s (Grafita)
À Temperatura Ambiente
Equilíbrio
Fase Metaestável
Taxas infinitamente lentas Termodinâmico
Cementita (Fe3C)
(Grafita)
Prof. Dr. Geraldo Lúcio de Faria 11
Capítulo 2 –Sistema Fe-C Diagrama Ferro-Cementita
Estrutura Cristalina da Cementita (Fe3C):
A cementita possui uma estrutura
cristalina ortorrômbica. Na figura
ao lado os átomos de ferro são
representados pelas esferas azuis e
os de carbono pelas pretas.
Prof. Dr. Geraldo Lúcio de Faria 12
Capítulo 2 –Sistema Fe-C Diagrama Ferro-Cementita
A4
Acm
A3
A1
Prof. Dr. Geraldo Lúcio de Faria 13
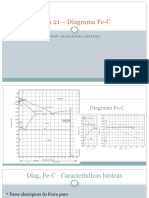
Capítulo 2 –Sistema Fe-C Diagrama Ferro-Cementita
Significado das Linhas:
A1 – Temperatura de reação eutetóide g a + Fe3C;
A2 – Transformação magnética da fase a a 770oC;
A3 – Transformação da fase g para a fase a;
Acm – Indica a transformação da fase g para Fe3C;
A4 – Transformação da fase g em d;
Liquidus – Acima desta linha existe somente líquido;
Solidus – Abaixo desta linha todo o material está no estado sólido.
Prof. Dr. Geraldo Lúcio de Faria 14
Capítulo 2 –Sistema Fe-C Soluções Sólidas de Fe
Hipoeutetóide
Aço
Aço Ferro Fundido Ferro Fundido
Hipereutetóide Hipoeutético Hipereutético
Prof. Dr. Geraldo Lúcio de Faria 15
Capítulo 2 –Sistema Fe-C Aços e Ferros Fundidos
5. Aços e Ferros Fundidos
Prof. Dr. Geraldo Lúcio de Faria 16
Capítulo 2 –Sistema Fe-C Aços e Ferros Fundidos
Prof. Dr. Geraldo Lúcio de Faria 17
Capítulo 2 –Sistema Fe-C Aços e Ferros Fundidos
Classificação Teor de C
Aço Extra Doce < 0,15%
Aço Doce 0,15% - 0,30%
Aço Meio-doce 0,30% - 0,40%
Aço Meio-Duro 0,40% - 0,60%
Aço extraduro 0,60% - 1,20%
Prof. Dr. Geraldo Lúcio de Faria 18
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
6. Constituintes do Aço Resfriado Lentamente e Suas
Propriedades Mecânicas
Aços Hipoeutetóides (C < 0,76%);
FOCO Aços Eutetóides (C = 0,76%);
Aços Hipereutetóides (C > 0,76%).
Neste sub-capítulo iremos estudar alguns resfriamentos bem lentos para três
composições distintas de aços, porém não lentas o suficiente para tornar
possível a formação da grafita.
Prof. Dr. Geraldo Lúcio de Faria 19
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Resfriamento 1: Aço Hipoeutetóide – 99,5% de Fe e 0,05% de C inicialmente a 1100oC.
Supondo que Co = 0,5% de C, teremos:
• c – Existe apenas a fase g em equilíbrio
com 0,5% de C.
• d – Co-existem as fases g e a nucleada.
• e – Co-existem as fases g e a.
• f – A fase g se transforma em lamelas
alternadas de a e Fe3C.
• Este constituinte formado de lamelas
alternadas de a e Fe3C é denominado
PERLITA.
• À temperatura ambiente, teremos a
primário (ou proeutetóide) e perlita.
Prof. Dr. Geraldo Lúcio de Faria 20
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Imagem de Aço Hipoeutetóide Resfriado “Lentamente”
Micrografia obtida com o auxílio de um microscópio óptico
de luz refletida (600X).
Prof. Dr. Geraldo Lúcio de Faria 21
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Resfriamento 2: Aço Eutetóide – 99,23% de Fe e 0,76% de C inicialmente a 1100oC.
Supondo que Co = 0,76% de C, teremos:
• a – Existe apenas a fase g em equilíbrio
com 0,76% de C.
• b –A fase g se transforma em lamelas
alternadas de a e Fe3C.
• Este constituinte formado de lamelas
alternadas de a e Fe3C é denominado
PERLITA.
• À temperatura ambiente, teremos apenas
a perlita.
Prof. Dr. Geraldo Lúcio de Faria 22
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Imagens de Aço Eutetóide Resfriado “Lentamente”
Imagem obtida com microscópio óptico de Imagem obtida com microscópio eletrônico
luz refletida (500X). de varredura (12000X).
Prof. Dr. Geraldo Lúcio de Faria 23
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Resfriamento 3: Aço hipereutetóide – 98,5% de Fe e 1,5% de C inicialmente a 1100oC.
Supondo que Co = 1,5% de C, teremos:
• g – Existe apenas a fase g em equilíbrio
com 1,5% de C.
• h – Co-existem as fases g e Fe3C nucleada.
• i – A fase g se transforma em lamelas
alternadas de a e Fe3C.
• Este constituinte formado de lamelas
alternadas de a e Fe3C é denominado
PERLITA.
• À temperatura ambiente, teremos Fe3C
primário (ou proeutetóide) e perlita.
Prof. Dr. Geraldo Lúcio de Faria 24
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Imagem de Aço Hipereutetóide Resfriado “Lentamente”
Micrografia obtida com o auxílio de um microscópio óptico
de luz refletida (1000X).
Prof. Dr. Geraldo Lúcio de Faria 25
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Comparativo:
• Quanto menor o teor de C, maior a
fração de ferrita proeutetóide;
• Quanto mais próximo da composição
eutetóide, maior a fração de perlita;
• Quanto maior o teor de C (<2,14,
>0,76) maior a fração de cementita
proeutetóide.
Prof. Dr. Geraldo Lúcio de Faria 26
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Falemos um pouco sobre as fases g, a, Fe3C e do constituinte Perlita:
g – Austenita: Solução sólida intersticial de C no Fe no sistema CFC. Se caracteriza por ser
dúctil, paramagnético e estável em temperaturas elevadas;
a – Ferrita: Solução sólida intersticial de C no Fe no sistema CCC. Se caracteriza por ser
dúctil, ferromagnético em temperaturas inferiores a 770oC, e estável em baixas
temperaturas;
Fe3C – Cementita: É um carboneto de ferro. Se caracteriza por ser um material duro e
quebradiço;
Prof. Dr. Geraldo Lúcio de Faria 27
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Perlita: A perlita não é uma fase, e sim uma mistura de duas fases, ferrita e cementita,
que ocorre sob a forma de lamelas alternadas e paralelas. Se caracteriza por ser
resistente e tenaz;
Modelo de Mehl
Prof. Dr. Geraldo Lúcio de Faria 28
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Modelo de Mehl para a decomposição da Austenita
Austenita em Perlita
a
Fe3C
Prof. Dr. Geraldo Lúcio de Faria 29
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
É importante ressaltar que o diagrama Fe-Fe3C apresentado é o de ligas livres de
outros elementos químicos que não o Fe e o C. A presença de outros elementos
pode implicar em alterações das linhas de contorno dos campos austeníticos e
ferríticos.
Elementos Elementos
Estabilizadores da Estabilizadores da
Austenita Ferrita
Elementos Elementos
g-gêneos a-gêneos
A2 – Campo B1 – Campo B2 – Campo
A1 – Campo
Austenítico Austenítico Fechado Austenítico
Austenítico Aberto
Expandido Contraído
(Ni, Mn e Co) (Si, Al, Be, P, Ti, V e
(C e N) Mo) (B, S, Ta, Zr e Nb)
Prof. Dr. Geraldo Lúcio de Faria 30
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
A-I) Campo Austenítico Aberto;
A-II) Campo Austenítico Expandido;
B-I) Campo Austenítico Fechado;
B-II) Campo Austenítico Contraído.
Prof. Dr. Geraldo Lúcio de Faria 31
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Efeito de Elementos de Liga no campo de
estabilidade de g em um sistema binário.
Prof. Dr. Geraldo Lúcio de Faria 32
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Efeito de Elementos de Liga na Efeito de Elementos de Liga na
Composição Eutetoide. Temperatura Eutetoide.
Prof. Dr. Geraldo Lúcio de Faria 33
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Efeito de Elementos de Liga no campo
de estabilidade da austenita (a) Mn,
(b) Mo, (c) Cr e (d) Ti.
Prof. Dr. Geraldo Lúcio de Faria 34
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Elementos Fortes Formadores de Carbonetos:
Os carbonetos do grupo I possuem
estruturas cristalinas complexas,
semelhantes à da cementita. Em
geral eles são formados por
elementos metálicos
substitucionais, como por exemplo
o Cr que pode formar o Cr23C6. As
estruturas do grupo II são mais
Representação esquemática das posições simples e são geralmente formadas
na tabela periódica de elementos fortes por metais instersticiais, como
formadores de carbonetos em aços. exemplo pode-se citar:TiC, WC,
NbC, Mo2C.
Prof. Dr. Geraldo Lúcio de Faria 35
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Em geral, a morfologia dos compostos de
estruturas cristalinas mais simples se
formam de forma mais finamente
dispersas (VC, NbC, TiC, TaC)
Morfologias típicas de carbonetos em um
aço com elevada concentração destes
compostos intermetálicos. Em geral, a morfologia dos compostos de
estruturas cristalinas mais complexas se
formam de forma mais grosseira (M7C3,
M6C e M23C6)
Prof. Dr. Geraldo Lúcio de Faria 36
Capítulo 2 –Sistema Fe-C Aço Resfriado Lentamente
Entalpias de formação de boretos,
carbonetos e nitretos a 298,15K
DHf/kJMol-1
Prof. Dr. Geraldo Lúcio de Faria 37
Capítulo 2 –Sistema Fe-C Alterações nas Linhas de Transformação
7. Efeito de Resfriamento e Aquecimento nas Linhas de
Transformação
Ac – Arrêt de Chauffage
Ar – Arrêt de Refroidissement
Prof. Dr. Geraldo Lúcio de Faria 38
Capítulo 2 –Sistema Fe-C Alterações nas Linhas de Transformação
8. Efeito de Elementos de Liga nas Linhas de
Transformação – Temperaturas Críticas
Geralmente as temperaturas críticas de um dado aço são determinadas
experimentalmente, por exemplo por meio de experimentos de dilatometria. No
entanto, algumas equações empíricas têm sido desenvolvidas por meio de regressões
para se calcular estas temperaturas. Abaixo são apresentadas duas importantes
equações:
Ac3 = 910 – 203.(C)1/2 – 15,2Ni + 44,7Si +104V + 31,5Mo + 31,1W
Ac1 = 723 – 10,7Mn – 16,9Ni + 29,1Si +16,9Cr + 290As + 6,38W
Prof. Dr. Geraldo Lúcio de Faria 39
Capítulo 2 –Sistema Fe-C Frações Volumétricas das Fases
9. Determinação das Frações em Peso das Fases
Informação Importante Fração de Ferrita e de
Cementita na Perlita
Tomemos:
Fração de Ferrita:
Fração de Cementita:
Conclusão:
A perlita é constituída por 89% de
ferrita e 11% de cementita.
Ca (0,008%C) C0 (0,76%C) Ccm (6,67%C)
Prof. Dr. Geraldo Lúcio de Faria 40
Capítulo 2 –Sistema Fe-C Frações Volumétricas das Fases
Ao estudarmos um aço hipoeutetóide com 0,5% de C teremos:
Fração Total de Ferrita e de Cementita (A):
Ferrita total = 93%
B
Cementita = 7%
c
Fração de Ferrita Proeutetóide e Perlita (B):
A
c
Ca (0,008%C) C0 (0,5%C) Ccm (6,67%C)
Como, assim:
Ferrita Proeutetóide = 35%
Logo, teremos 35% de ferrita proeutetóide, 58% Perlita= 65%
de ferrita eutetóide e 7% de cementita.
Prof. Dr. Geraldo Lúcio de Faria 41
Capítulo 2 –Sistema Fe-C Velocidade de Resfriamento
10. Efeito da Velocidade de Resfriamento na Fração em
Peso da Ferrita e da Perlita
Se um aço for resfriado lentamente, mas não o suficiente para a formação da grafita, com
o auxílio da microscopia óptica e com a aproximação da fração volumétrica pela fração
em peso, pode-se estimar o teor de carbono do mesmo:
a - proeutetóide
Sabemos que:
Se Ce = 0,76% de C, podemos escrever que
Perlita
Portanto, conhecendo a fração de perlita proeutetóide,
podemos calcular o teor de carbono da liga (C0).
Prof. Dr. Geraldo Lúcio de Faria 42
Capítulo 2 –Sistema Fe-C Velocidade de Resfriamento
Entretanto se o resfriamento for mais rápido, esta estimativa não poderá ser feita, pois a
quantidade de ferrita será menor do que a prevista pelo diagrama Fe-Fe3C.
Modelo comparado e validado experimentalmente para um aço hipoeutetóide com
0,4% de C.
Prof. Dr. Geraldo Lúcio de Faria 43
Capítulo 2 –Sistema Fe-C Ferro Fundido
11. Ferro Fundido – EXTRA
Como vimos:
Hipoeutetóide
Hipereutetóide
Aço
Ferro Fundido Ferro Fundido
Aço
Hipoeutético Hipereutético
Prof. Dr. Geraldo Lúcio de Faria 44
Capítulo 2 –Sistema Fe-C Ferro Fundido
Resfriemos três composições de Ferro Fundido:
Prof. Dr. Geraldo Lúcio de Faria 45
Capítulo 2 –Sistema Fe-C Ferro Fundido
Ferro Fundido Eutético: Ferro Fundido Branco (4,3% de C)
T = 1147oC: Temperatura Eutética
L (4,3%C) Ledeburita (Nódulos de austenita em matriz de cementita). 1147oC
T = 727oC: Temperatura Eutetóide
g+Fe3C
g (0,76%C) Ledeburita (Nódulos de perlita em matriz de cementita).
727oC
a+Fe3C
Prof. Dr. Geraldo Lúcio de Faria 46
Capítulo 2 –Sistema Fe-C Ferro Fundido
Ferro Fundido Hipoeutético: (2,11<%C<4,3)
g+Fe3C
727oC
a+Fe3C
Prof. Dr. Geraldo Lúcio de Faria 47
Capítulo 2 –Sistema Fe-C Ferro Fundido
Ferro Fundido Hipereutético: (%C>4,3)
Prof. Dr. Geraldo Lúcio de Faria 48
Capítulo 2 –Sistema Fe-C Ferro Fundido
Ferro Fundido Cinzento Ferro Fundido Nodular
3,4%C, 2,5%Si 3,4%C, 2,5%Si, 0,03%Mg
A adição de Si favorece A adição de Mg ajuda
a decomposição da na formação da grafita
cementita em grafita. na forma nodular.
Prof. Dr. Geraldo Lúcio de Faria 49
Capítulo 2 –Sistema Fe-C Termodinâmica Inoxidáveis
12. Termodinâmica Inoxidáveis – EXTRA
1600 L+d L
1500 1,00
Ferrita Austenita Ferrita
1400
d
1300
Fração em massa
Temeperatura (°C)
1200 0,10
1100
g a+g
1000
M23C6
900
0,01
800
M23C6
700
600 a
0,00
500 400 500 600 700 800 900 1000 1100 1200 1300 1400 1500 1600
7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26
Cr (% em peso)
T (°C)
Diagramas de Fases no Equilíbrio do aço inoxidável ferrítico 410D: 0,011%C 11,1%Cr, 0,533%Mn, 0,526%Si, 0,305%Ni, 0,013%N.
Prof. Dr. Geraldo Lúcio de Faria 50
Capítulo 2 –Sistema Fe-C Termodinâmica Inoxidáveis
Diagrama de Fases Primárias no Equilíbrio do aço inoxidável Duplex UNSS32304: 0,02%C, 1,35%Mn, 0,39%Si, 22,45%Cr,
3,63%Ni, 0,44%Mo e 0,13%N.
Prof. Dr. Geraldo Lúcio de Faria 51
Você também pode gostar
- 2019 - 2b - 2 - Estruturas 2Documento7 páginas2019 - 2b - 2 - Estruturas 2Eduardo AquinoAinda não há avaliações
- Diagrama de Ferro CarbonoDocumento10 páginasDiagrama de Ferro CarbonoricardomochoAinda não há avaliações
- Lista de Exercicio Transformacao Isotermica TTT e TRCDocumento8 páginasLista de Exercicio Transformacao Isotermica TTT e TRCJoão Memoria100% (1)
- Aula Diagrama Fe C 7Documento33 páginasAula Diagrama Fe C 7Rafael SantosAinda não há avaliações
- Pignata - Estruturas de Aço para EdifíciosDocumento322 páginasPignata - Estruturas de Aço para EdifíciosRogério Mattes100% (2)
- Aços e MicroestruturasDocumento35 páginasAços e MicroestruturasMidori PitangaAinda não há avaliações
- 9.0 - Cap.09 DIAGRAMA DE FASES RES. 16.1.pptx (Salvo Automaticamente)Documento78 páginas9.0 - Cap.09 DIAGRAMA DE FASES RES. 16.1.pptx (Salvo Automaticamente)Carlos Eugenio Fortes TeixeiraAinda não há avaliações
- Aula05 - Diagrama de Fases Ferro Carbono PDFDocumento39 páginasAula05 - Diagrama de Fases Ferro Carbono PDFEugenio ManuelAinda não há avaliações
- Aula05 - Diagrama de Fases Ferro CarbonoDocumento39 páginasAula05 - Diagrama de Fases Ferro CarbonoTaci AlvesAinda não há avaliações
- Diagramas Transformaçoes FaseDocumento37 páginasDiagramas Transformaçoes Fasekaka**Ainda não há avaliações
- Aula 07 - Diagrama Fe-CDocumento37 páginasAula 07 - Diagrama Fe-CVitoria MarianaAinda não há avaliações
- Ferro CarbonoDocumento33 páginasFerro CarbonoccsygnnpoAinda não há avaliações
- Sebenta Materiais de EngenhariaDocumento133 páginasSebenta Materiais de EngenhariaPedro FerreiraAinda não há avaliações
- CIEN0004 - Diagrama de Fase Fe-C (2019.1)Documento32 páginasCIEN0004 - Diagrama de Fase Fe-C (2019.1)Fernanda OliveiraAinda não há avaliações
- 2 Lista de ExercíciosDocumento11 páginas2 Lista de ExercíciosEltonAinda não há avaliações
- MCM II - RevisãoDocumento19 páginasMCM II - RevisãoEdimilson RodriguesAinda não há avaliações
- MTT1 Aula1Documento18 páginasMTT1 Aula1João Pedro LimaAinda não há avaliações
- Aula 10 - Metalurgia Da Soldagem - PPIDocumento72 páginasAula 10 - Metalurgia Da Soldagem - PPIJohnAinda não há avaliações
- ITEM 2 - DIAGRAMA Fe - C PDFDocumento20 páginasITEM 2 - DIAGRAMA Fe - C PDFSoraia SandesAinda não há avaliações
- Aços - Tratamentos TérmicosDocumento9 páginasAços - Tratamentos Térmicossergioeq2000Ainda não há avaliações
- 3º Lista de Exercícios de MetalurgiaDocumento5 páginas3º Lista de Exercícios de Metalurgiaewerton diegoAinda não há avaliações
- Ferrita de WidmanstaettenDocumento15 páginasFerrita de WidmanstaettenSylvio Kaschner SeraphimAinda não há avaliações
- ENG1015 A Os Diagramas Fe C e A Os EspeciaisDocumento33 páginasENG1015 A Os Diagramas Fe C e A Os EspeciaisAndre FrançaAinda não há avaliações
- Acos Versao AtualizadaDocumento272 páginasAcos Versao AtualizadaManuel VianaAinda não há avaliações
- 21-Diagrama Ferro - CarbonoDocumento19 páginas21-Diagrama Ferro - CarbonoLucas SeverinAinda não há avaliações
- Aula 4-Diagrama Ferro Carbono e TT ReduzidoDocumento42 páginasAula 4-Diagrama Ferro Carbono e TT ReduzidoJulia de OliveiraAinda não há avaliações
- 1a Prova 20201Documento2 páginas1a Prova 20201matheus miguelAinda não há avaliações
- Aula 3 - Diagrama de Equilibrio Fe-CDocumento64 páginasAula 3 - Diagrama de Equilibrio Fe-CLorena FerreiraAinda não há avaliações
- TT03Documento11 páginasTT03Bruno VazAinda não há avaliações
- Diagrama Ferro CarbonoDocumento74 páginasDiagrama Ferro CarbonoWanderley Fonseca100% (1)
- 1.3 - Capítulo 1 - Diagrama de Fases Fe-CDocumento68 páginas1.3 - Capítulo 1 - Diagrama de Fases Fe-CGLAUCIO DOS SANTOS SILVAAinda não há avaliações
- 3 Lista de ExercíciosDocumento8 páginas3 Lista de ExercíciosEltonAinda não há avaliações
- Aula 4Documento55 páginasAula 4Jordan OliveiraAinda não há avaliações
- Apostila Aço e Ferro FundidoDocumento48 páginasApostila Aço e Ferro FundidoMauricio CamargoAinda não há avaliações
- MicroestruturasDocumento11 páginasMicroestruturasFrenzy BritoAinda não há avaliações
- Diagrama de FasesDocumento20 páginasDiagrama de FasesDenilsonRobertoAinda não há avaliações
- Diagrama de Equilibrio Fe-CDocumento19 páginasDiagrama de Equilibrio Fe-Ctcosta88Ainda não há avaliações
- Diagrama de Ferro CarbonoDocumento25 páginasDiagrama de Ferro CarbonoToninho PorpinoAinda não há avaliações
- Exercicios de CienciasDocumento13 páginasExercicios de CienciasMarilis MaguengueAinda não há avaliações
- Sebenta Materiais de EngenhariaDocumento96 páginasSebenta Materiais de EngenhariaDuarte FonsecaAinda não há avaliações
- Estudo Dirigido 3Documento6 páginasEstudo Dirigido 3rodrigoAinda não há avaliações
- Interstícios OctaédricosDocumento10 páginasInterstícios OctaédricosFernanda FischerAinda não há avaliações
- 04.4.CTM-Metais IV-Tratamentos TérmicosDocumento45 páginas04.4.CTM-Metais IV-Tratamentos TérmicosMiguel Queiros100% (1)
- Aula 11 ICM - Diagramas de Fases - 2018.2Documento46 páginasAula 11 ICM - Diagramas de Fases - 2018.2Ana Flavia BAinda não há avaliações
- METALURGIADocumento9 páginasMETALURGIAlucasqsms04Ainda não há avaliações
- Materais de Construção Mecânica Aula 21 - Diagrama de Fases Diagrama Fe-CDocumento25 páginasMaterais de Construção Mecânica Aula 21 - Diagrama de Fases Diagrama Fe-CGiovanna VerasAinda não há avaliações
- Aula7 8Documento52 páginasAula7 8Matheus Yuri Sasaki FranzoniAinda não há avaliações
- Aços e Seus Tratamentos TérmicosDocumento90 páginasAços e Seus Tratamentos TérmicosAngelo LeãoAinda não há avaliações
- Exercício - Metais CompletoDocumento2 páginasExercício - Metais CompletoBeatriz CalimanAinda não há avaliações
- Lista de Exercícios AV2Documento10 páginasLista de Exercícios AV2Carlos Brandão0% (1)
- 2-Exercicios Fe-C PDFDocumento5 páginas2-Exercicios Fe-C PDFEduardo MendesAinda não há avaliações
- 1014005-Diagramas de Fases Ferro-CementitaDocumento49 páginas1014005-Diagramas de Fases Ferro-CementitaHenrique ToziAinda não há avaliações
- Aula 6 Diagrama Fe CDocumento33 páginasAula 6 Diagrama Fe CMárcio FerreiraAinda não há avaliações
- Desenvolvendo Um Datalogger E Armazenando No Arquivo Formato Csv Para Medir Contador Geiger Com PicNo EverandDesenvolvendo Um Datalogger E Armazenando No Arquivo Formato Csv Para Medir Contador Geiger Com PicAinda não há avaliações
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- Desenvolvendo Um Datalogger Para Medir Contador Geiger Com PicNo EverandDesenvolvendo Um Datalogger Para Medir Contador Geiger Com PicAinda não há avaliações
- Aços Inoxidáveis - Corrosão E Métodos Para DetecçãoNo EverandAços Inoxidáveis - Corrosão E Métodos Para DetecçãoAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Metalurgia básica para ourives e designers: Do metal à joiaNo EverandMetalurgia básica para ourives e designers: Do metal à joiaAinda não há avaliações
- Cap 3 - Transf Fase Fora Do EquilDocumento72 páginasCap 3 - Transf Fase Fora Do EquilTales NascimentoAinda não há avaliações
- Cap 4 - Recoz de RecristDocumento56 páginasCap 4 - Recoz de RecristTales NascimentoAinda não há avaliações
- Cap 1 - PirometriaDocumento45 páginasCap 1 - PirometriaTales NascimentoAinda não há avaliações
- Cap 0 - IntroduçãoDocumento16 páginasCap 0 - IntroduçãoTales NascimentoAinda não há avaliações
- Na - 04 - Lajes CompletaDocumento41 páginasNa - 04 - Lajes CompletaAgatha ShirleyAinda não há avaliações
- Relatório 3 - PressãoDocumento11 páginasRelatório 3 - PressãoMatheus RossiniAinda não há avaliações
- Catalogo Tec Vidro 2022 1Documento22 páginasCatalogo Tec Vidro 2022 1simons79Ainda não há avaliações
- Catálogo de Válvulas DataDocumento75 páginasCatálogo de Válvulas DataLeonardo PestanaAinda não há avaliações
- Planilha Sem TítuloDocumento11 páginasPlanilha Sem TítuloMatheus Neves CarvalhoAinda não há avaliações
- ATERRAMENTO - Projeto Atua AsslDocumento6 páginasATERRAMENTO - Projeto Atua AsslFAGNER AZEVEDO azevedoAinda não há avaliações
- PLANOS DE AÇÃO ANUAL para Manutenção - 2022Documento50 páginasPLANOS DE AÇÃO ANUAL para Manutenção - 2022Empresa DaluAinda não há avaliações
- Teste Fenômenos de TransporteDocumento8 páginasTeste Fenômenos de TransporteGuilherme PrataAinda não há avaliações
- Steelman Construcao CivilDocumento208 páginasSteelman Construcao CivilLucas Pereira de Jesus0% (2)
- Manual de ProcedimentosDocumento9 páginasManual de ProcedimentosRoger GevaerdAinda não há avaliações
- 3VA23257MN320DA0 Datasheet PTDocumento6 páginas3VA23257MN320DA0 Datasheet PTClayton CostaAinda não há avaliações
- Ged 15994Documento19 páginasGed 15994Lucas Costa Honório da SilvaAinda não há avaliações
- Patologia Coberturas FrançaDocumento16 páginasPatologia Coberturas Françadalton de lara stellaAinda não há avaliações
- Cabo Opgw Desempenho Descarg AtmosfDocumento6 páginasCabo Opgw Desempenho Descarg AtmosfWilliam CruzAinda não há avaliações
- (Aula 8) Domínios de DeformaçõesDocumento20 páginas(Aula 8) Domínios de DeformaçõesTiago AraujoAinda não há avaliações
- Relatório 3 - Termostato EletrônicoDocumento7 páginasRelatório 3 - Termostato EletrônicoFelipe BizioAinda não há avaliações
- Comportamento Estrutural Vigas e Concreto e CarbonoDocumento317 páginasComportamento Estrutural Vigas e Concreto e CarbonoSol SAinda não há avaliações
- Cap. 3-Mecanismo de Formação Do Cavaco Mota (11.1)Documento41 páginasCap. 3-Mecanismo de Formação Do Cavaco Mota (11.1)Tulismar LacerdaAinda não há avaliações
- Aula 13 PDFDocumento43 páginasAula 13 PDFDiego Fernandes do NascimentoAinda não há avaliações
- Ensaios Mecânicos e MacrográficoDocumento78 páginasEnsaios Mecânicos e MacrográficoAnderson Mathias da Silva100% (1)
- Testes e Resolução BA1Documento56 páginasTestes e Resolução BA1João Sidónio Freitas100% (3)
- Moldes AreiaDocumento58 páginasMoldes AreiaJose Graciano100% (1)
- Catalogo MekalDocumento103 páginasCatalogo MekallecapasAinda não há avaliações
- Aula 4 DosagemDocumento27 páginasAula 4 DosagemArteplena HomeDesignAinda não há avaliações
- FlexaoSimples PDFDocumento80 páginasFlexaoSimples PDFmarcosvictor17Ainda não há avaliações
- Anexo III - TreinamentoDocumento10 páginasAnexo III - Treinamentojohn KotowskiAinda não há avaliações
- Parecer TecnicoDocumento21 páginasParecer TecnicoROBERTO DE ALMEIDA GUERRAAinda não há avaliações
- Trabalho Sobre Mancais (REV)Documento18 páginasTrabalho Sobre Mancais (REV)Vitor AlmeidaAinda não há avaliações