Escolar Documentos
Profissional Documentos
Cultura Documentos
Lista de Exercícios - Espectros
Enviado por
Kely MacêdoTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Lista de Exercícios - Espectros
Enviado por
Kely MacêdoDireitos autorais:
Formatos disponíveis
UNIVERSIDADE FEDERAL RURAL DE PERNAMBUCO
DEPARTAMENTO DE QUÍMICA
Disciplina: Química Geral I II Semestre Letivo de 2019
Turmas: LQI e LQII
LISTA DE EXERCÍCIOS
ESPECTROSCOPIA
1) O que significa dizer que a energia é quantizada?
2) Calcule e compare a energia de um fóton de comprimento de onda de 3,3 μm com um
de comprimento de onda de 0,154 nm.
3) Uma estação de rádio AM transmite a 1.440 kHz, e sua parceira FM transmite a 94,5
MHz. Calcule e compare a energia dos fótons emitidos por essas duas estações de rádio.
4) Um tipo de queimadura de sol ocorre com a exposição à luz UV de comprimento de
onda na vizinhança de 325 nm. Qual a energia de um fóton com esse comprimento de
onda?
5) Nos termos da teoria de Bohr para o átomo de hidrogênio, qual processo ocorre quando
seus átomos excitados emitem energia radiante com determinados comprimentos de
onda e apenas aqueles comprimentos de onda?
6) Um átomo de hidrogênio ‘expande-se’ ou ‘contrai-se’ ao mover-se de seu estado
fundamental para um estado excitado?
7) Quando a transição eletrônica, n=4 para n=2, ocorre no hidrogênio, a energia é emitida
ou absorvida?
8) Umas das linhas de emissão do átomo de hidrogênio tem comprimento de onda de 93,8
nm. Em qual região do espectro eletromagnético essa absorção é encontrada?
9) Para n=4, quais são os possíveis valores de l?
10) Para l=2, quais são os possíveis valores de ml?
11) Dê os valores para n, l e ml para (a) 3p; (b) 2s; (c) 4f; (d) 5d.
12) Quais as seguintes alternativas representação combinações impossíveis de n e l: (a)1p;
(b) 4s; (C) 5f; (d) 2d?
13) Qual o número máximo de elétrons que podem ocupar cada um dos seguintes subníveis:
(a) 3d; (b) 4s; (c) 2p; (d) 5f?
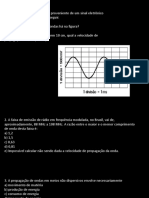
14) Considere as duas ondas mostradas a seguir, que representam duas radiações
eletromagnéticas:
(a) Qual o comprimento de onda da onda A? E da onda B?
(b) Qual a frequência da onda A? E da onda B?
(c) Identifique as regiões do espectro eletromagnético às quais as ondas A e B pertencem.
15) Certos elementos emitem luz de um comprimento de onda específico são queimados.
Historicamente, os químicos utilizavam tais comprimentos de onda de emissão para
determinar se certos elementos estavam presentes em uma amostra. Alguns
comprimentos de onda característicos para alguns desses elementos são:
Ag 328,1 nm Fe 372,0 nm
Au 267,6 nm K 404,7 nm
Ba 455,4 nm Mg 285,2 nm
Ca 422,7 nm Na 589,6 nm
Cu 324,8 nm Ni 341,5 nm
(a) Determine quais elementos emitem radiação na parte visível do espectro.
(b) Qual elemento emite fótons de energia mais alta? E de energia mais baixa?
(c) Ao ser queimada, uma amostra de substância desconhecida emite luz de frequência
6,59 x 1014 s-1. Qual desses elementos provavelmente está na amostra?
16) Os raios do sol que causam o bronzeamento e as queimaduras estão na porção
ultravioleta do espectro eletromagnético. Esses raios são categorizados por
comprimento de onda: a chamada radiação UV-A tem comprimentos de onda na faixa
de 320-380 nm, enquanto a radiação UV-B tem comprimentos de onda na faixa 290-320
nm.
(a) Calcule a frequência de luz que tem comprimento de onda de 320 nm.
(b) Quais são mais energéticos, fótons de radiação UV-A ou de radiação UV-B?
(c) A radiação UV-B do sol é considerada maior causadora de queimaduras em
humanos do que a radiação UV-A. Essa observação é consistente com sua resposta
ao item anterior?
Você também pode gostar
- Treinamentos Energia SolarDocumento285 páginasTreinamentos Energia SolarHallyson Aquino100% (1)
- Exercícios Quantica I ResolvidoDocumento7 páginasExercícios Quantica I ResolvidoJosevandro MagalhãesAinda não há avaliações
- Química Geral I - Teoria Atômica de DaltonDocumento14 páginasQuímica Geral I - Teoria Atômica de DaltonSimony OliveiraAinda não há avaliações
- 2018.1 - Fisica Moderna - Lista de Exercícios 2 - Quantização Da Carga Luz e Energia - Propriedades Corpusculares Da RadiaçãoDocumento2 páginas2018.1 - Fisica Moderna - Lista de Exercícios 2 - Quantização Da Carga Luz e Energia - Propriedades Corpusculares Da RadiaçãoFábio Lima100% (1)
- Lista de Exercícios de Estrutura AtômicaDocumento2 páginasLista de Exercícios de Estrutura AtômicaGabriela FernandesAinda não há avaliações
- Interferência e difração da luzDocumento27 páginasInterferência e difração da luzLucas MachadoAinda não há avaliações
- Lista de Exercícios 1 QG 2019Documento2 páginasLista de Exercícios 1 QG 2019vinicius souzaAinda não há avaliações
- Lista 1Documento3 páginasLista 1Agatha PozzatiAinda não há avaliações
- Topico5 ListaExercíciosDocumento3 páginasTopico5 ListaExercíciosRebeca TavaresAinda não há avaliações
- 6-Lista Exercicios Geral 1 - Espectro Atomico PDFDocumento2 páginas6-Lista Exercicios Geral 1 - Espectro Atomico PDFCarolLessaAinda não há avaliações
- Lista de Exercícios Quimica Geral (Superior)Documento9 páginasLista de Exercícios Quimica Geral (Superior)Ian Pereira100% (1)
- Lista #3 Modelos Atomicos PDFDocumento3 páginasLista #3 Modelos Atomicos PDFgiovannaAinda não há avaliações
- LISTA 02-Arquitetura AtômicaDocumento7 páginasLISTA 02-Arquitetura AtômicaMarcsAinda não há avaliações
- Teorias de Física QuânticaDocumento17 páginasTeorias de Física QuânticaGildoAinda não há avaliações
- ListaDocumento2 páginasListaAlice M.AlmeidaAinda não há avaliações
- 1a Lista de Exercícios QUI125 PDFDocumento3 páginas1a Lista de Exercícios QUI125 PDFLucas SfredoAinda não há avaliações
- Lista de Exercícios de Espectroscopia AtômicaDocumento2 páginasLista de Exercícios de Espectroscopia AtômicaMattia Silva ValsangiacomoAinda não há avaliações
- Problemas de Física Atômica e NuclearDocumento5 páginasProblemas de Física Atômica e NuclearjoanaAinda não há avaliações
- Química exercícios onda comprimentoDocumento1 páginaQuímica exercícios onda comprimentoÊnio BruceAinda não há avaliações
- Espectroscopia UV-Vis: Fundamentos e AplicaçõesDocumento187 páginasEspectroscopia UV-Vis: Fundamentos e AplicaçõesAnonymous UYDJtUnAinda não há avaliações
- 04 - Aula 2 - Lista 2Documento1 página04 - Aula 2 - Lista 2Diego Feijó de AbreuAinda não há avaliações
- Lista de Exercícios de Química e Ciências dos MateriaisDocumento2 páginasLista de Exercícios de Química e Ciências dos MateriaisRafaela GomesAinda não há avaliações
- Lista de Exercícios de Química Geral com Radiação e Configurações EletrônicasDocumento1 páginaLista de Exercícios de Química Geral com Radiação e Configurações EletrônicasValdivam CardozoAinda não há avaliações
- Espectroscopia de Absorçaõ e EmissãoDocumento27 páginasEspectroscopia de Absorçaõ e EmissãoNatasha CabralAinda não há avaliações
- Fundamentos QuímicaDocumento2 páginasFundamentos QuímicaTatiane Takeshita0% (1)
- Lista de problemas de física quântica com radiação e efeitos fotoelétricoDocumento4 páginasLista de problemas de física quântica com radiação e efeitos fotoelétricoMaycon OliveiraAinda não há avaliações
- Ap 11Documento2 páginasAp 11BeneditoAinda não há avaliações
- 1 e 2 Listas de Exercícios de Química Geral (Com Respostas) - Estrutura AtômicaDocumento7 páginas1 e 2 Listas de Exercícios de Química Geral (Com Respostas) - Estrutura AtômicacarlosAinda não há avaliações
- Exercício Avaliativo - 1Documento2 páginasExercício Avaliativo - 1fabi32Ainda não há avaliações
- Lista de Exercícios Física QuânticaDocumento2 páginasLista de Exercícios Física QuânticaFelipe GohAinda não há avaliações
- Rede de difracção: resolução de dobletes e espectrosDocumento3 páginasRede de difracção: resolução de dobletes e espectrosBeneditoAinda não há avaliações
- Brown e Holmes. Capitulo 6 Exerccios e Respostas Do Livro.Documento15 páginasBrown e Holmes. Capitulo 6 Exerccios e Respostas Do Livro.Rafael CarvalhoAinda não há avaliações
- Exercícios Física 9o anoDocumento2 páginasExercícios Física 9o anoMaria Do Carmo Cardoso BezerraAinda não há avaliações
- Ficha exercícios ondas eletromagnéticasDocumento2 páginasFicha exercícios ondas eletromagnéticasCarlos MugabeAinda não há avaliações
- Química Geral: Teoria AtômicaDocumento33 páginasQuímica Geral: Teoria AtômicaLarissa CamargoAinda não há avaliações
- LISTA DE EXERCÍCIOS IQG 111 Com GabaritoDocumento12 páginasLISTA DE EXERCÍCIOS IQG 111 Com GabaritomichelAinda não há avaliações
- Ondas Electromagneticas e Radiacao Do Corpo Negro 12a ClasseDocumento2 páginasOndas Electromagneticas e Radiacao Do Corpo Negro 12a ClasseAdriano Allan DjamboAinda não há avaliações
- Exercícios - Estrutura Atómica - Química Geral - LEB - 18Documento12 páginasExercícios - Estrutura Atómica - Química Geral - LEB - 18Melissa CoutoAinda não há avaliações
- Física Moderna I - Lista de ExercíciosDocumento2 páginasFísica Moderna I - Lista de ExercíciosCauê FerreiraAinda não há avaliações
- 2a Lista de Exerc Cios de F Sica Moderna 1 - 2Documento3 páginas2a Lista de Exerc Cios de F Sica Moderna 1 - 2Giuliano RidolfiAinda não há avaliações
- Espectro eletromagnético e estrutura atômicaDocumento3 páginasEspectro eletromagnético e estrutura atômicaEduardoRaphaelAinda não há avaliações
- Espect Rosco PiaDocumento11 páginasEspect Rosco PiaAndre Tomas ChanganaAinda não há avaliações
- Atividade 2 - Efeito Fotoeletrico.Documento2 páginasAtividade 2 - Efeito Fotoeletrico.ccnm - IFPE - Campus RecifeAinda não há avaliações
- Exercicicos - CorrDocumento3 páginasExercicicos - CorrJoão Paulo Sousa100% (1)
- Lista de Exerccios de Modelos Atmicos Estrutura Eletrnica e Propriedades PerDocumento2 páginasLista de Exerccios de Modelos Atmicos Estrutura Eletrnica e Propriedades PerPedro Henrique De Almeida AlvesAinda não há avaliações
- Relatório 3 - Linhas Espectrais de Emissão e Modelos AtômicosDocumento29 páginasRelatório 3 - Linhas Espectrais de Emissão e Modelos AtômicosLuara De Andrade Gonçalves100% (1)
- Lista de problemas de física quânticaDocumento4 páginasLista de problemas de física quânticaRafael CampoyAinda não há avaliações
- Transformaçoes - Lista de Exerccios 1Documento4 páginasTransformaçoes - Lista de Exerccios 1John SaucerAinda não há avaliações
- Ficha - Exercicios - Física Moderna - 2020Documento2 páginasFicha - Exercicios - Física Moderna - 2020HonestoAlarcoFranciscoMambrançaAinda não há avaliações
- 5 - EspectrosDocumento7 páginas5 - Espectrosjulianapalma2008Ainda não há avaliações
- Teste de chama e luminescência: identificação químicaDocumento2 páginasTeste de chama e luminescência: identificação químicaEmanuel Vieira TavaresAinda não há avaliações
- Lista Exerc Estrutura (Cap 1)Documento2 páginasLista Exerc Estrutura (Cap 1)CarlosAinda não há avaliações
- 2022 - LabModerna - Roteiros CompiladosDocumento74 páginas2022 - LabModerna - Roteiros CompiladosJ Camila JabsAinda não há avaliações
- Lista de Exercícios 1 - Modelos Atômicos e Tabela PeriódicaDocumento3 páginasLista de Exercícios 1 - Modelos Atômicos e Tabela Periódicalara.coutinhoAinda não há avaliações
- Ondas eletromagnéticas FMDocumento6 páginasOndas eletromagnéticas FMHenrique AraujoAinda não há avaliações
- Tarefa 1Documento2 páginasTarefa 1Luhan MaurilioAinda não há avaliações
- Tomografia Computadorizada: Bases Físico - MatemáticasNo EverandTomografia Computadorizada: Bases Físico - MatemáticasAinda não há avaliações
- Desenvolvendo Um Datalogger E Armazenando No Arquivo Formato Csv Para Medir Contador Geiger Com PicNo EverandDesenvolvendo Um Datalogger E Armazenando No Arquivo Formato Csv Para Medir Contador Geiger Com PicAinda não há avaliações
- Alteração Da LDBDocumento4 páginasAlteração Da LDBFelipe Dalenogare AlvesAinda não há avaliações
- TCC - Jerusa Ferreira de AlmeidaDocumento41 páginasTCC - Jerusa Ferreira de AlmeidaKely MacêdoAinda não há avaliações
- Educação Inclusiva Na PráticaDocumento210 páginasEducação Inclusiva Na PráticaLúcia DantasAinda não há avaliações
- Exercício EspectroscopiajjjjjjjjjjjjjjjDocumento28 páginasExercício EspectroscopiajjjjjjjjjjjjjjjKely MacêdoAinda não há avaliações
- Guia Didático - Série - Ensino de Química - Nº 013 - Eloi Caçador Ferreira Sá 1512202000000000000001Documento166 páginasGuia Didático - Série - Ensino de Química - Nº 013 - Eloi Caçador Ferreira Sá 1512202000000000000001Kely MacêdoAinda não há avaliações
- Ond SonDocumento47 páginasOnd SonjoaovasAinda não há avaliações
- Relatório 05 - Rede de DifraçãoDocumento3 páginasRelatório 05 - Rede de DifraçãoFelipe BacelarAinda não há avaliações
- AULA - Dioptro, Lâminas e PrismasDocumento6 páginasAULA - Dioptro, Lâminas e PrismasMurilo Carlos PresottoAinda não há avaliações
- Ficha Trabalho18 SantillanaDocumento3 páginasFicha Trabalho18 SantillanaAnaAinda não há avaliações
- 3 Avaliação Deondas-1Documento1 página3 Avaliação Deondas-1Ruan AssunçãoAinda não há avaliações
- Medição de Espessura e Técnicas Dms 2Documento43 páginasMedição de Espessura e Técnicas Dms 2Али АленкарAinda não há avaliações
- Níveis de pressão sonora e potência sonora em dBDocumento34 páginasNíveis de pressão sonora e potência sonora em dBMarcelo CunhaAinda não há avaliações
- Exercícios de Revisão Do 9º AnoDocumento2 páginasExercícios de Revisão Do 9º AnoAndrey TeixeiraAinda não há avaliações
- Aula 6 - Fontes Sonoras, Ressonância e Filtros AcústicosDocumento24 páginasAula 6 - Fontes Sonoras, Ressonância e Filtros AcústicosLuiz SalomãoAinda não há avaliações
- FQ SomDocumento4 páginasFQ SomCarlaSampaio100% (2)
- Ondulatoria - EnEMDocumento24 páginasOndulatoria - EnEMmarcosnunesspotifyAinda não há avaliações
- Padrões de Ondas de Elliott e Relacionamentos de Fibonacci Guia de Referência Central PDFDocumento20 páginasPadrões de Ondas de Elliott e Relacionamentos de Fibonacci Guia de Referência Central PDFEduardo LimaAinda não há avaliações
- Polarização de Ondas EletromagnéticasDocumento4 páginasPolarização de Ondas EletromagnéticasBreno SoaresAinda não há avaliações
- Tubo Kunt PDFDocumento4 páginasTubo Kunt PDFbininha89Ainda não há avaliações
- Ondas eletromagnéticas e teorema de PoyntingDocumento2 páginasOndas eletromagnéticas e teorema de PoyntingHugo CaetanoAinda não há avaliações
- Gerador de ondas estacionárias: relação entre força, comprimento de onda e densidadeDocumento9 páginasGerador de ondas estacionárias: relação entre força, comprimento de onda e densidadeLara Danna MarquesAinda não há avaliações
- OndasDocumento4 páginasOndasBianca FalcãoAinda não há avaliações
- Espectros atômicos revelam elementos químicosDocumento13 páginasEspectros atômicos revelam elementos químicosTeresa BernardoAinda não há avaliações
- Falha de Rolamentos Fase 3 BPFIDocumento1 páginaFalha de Rolamentos Fase 3 BPFILuisSilvaAinda não há avaliações
- M13 Ondas Electromagnéticas e A Sua ReflexãoDocumento7 páginasM13 Ondas Electromagnéticas e A Sua ReflexãoExplicadora ClaudiaAinda não há avaliações
- Certificados Proteção RadiológicaDocumento14 páginasCertificados Proteção RadiológicaRolando CostaAinda não há avaliações
- CST em Radiologia: raios X, efeito fotoelétrico e modelos atômicosDocumento7 páginasCST em Radiologia: raios X, efeito fotoelétrico e modelos atômicosCelso Queiroz100% (1)
- Reflexão e Refração de OndasDocumento24 páginasReflexão e Refração de OndasDanilo MattosAinda não há avaliações
- Resumos Moles e Espetros (Inclui Espetro de Hidrogénio)Documento3 páginasResumos Moles e Espetros (Inclui Espetro de Hidrogénio)Madalena PimentaAinda não há avaliações
- Física - Óptica - Índice de RefraçãoDocumento9 páginasFísica - Óptica - Índice de RefraçãoFísica Concurso VestibularAinda não há avaliações
- Como Funciona o Sistema de RadiodifusaoDocumento4 páginasComo Funciona o Sistema de RadiodifusaoCaíqueCézarAinda não há avaliações
- Ondas Otica Interf DifracaoDocumento3 páginasOndas Otica Interf DifracaoGabrielli RovedaAinda não há avaliações
- Acústica - Mapa MentalDocumento3 páginasAcústica - Mapa MentalVinicius KaioAinda não há avaliações