Escolar Documentos
Profissional Documentos
Cultura Documentos
Masas Atómica y Masa Molecular para Primer Grado de Secundaria
Enviado por
Mercedes RojasTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Masas Atómica y Masa Molecular para Primer Grado de Secundaria
Enviado por
Mercedes RojasDireitos autorais:
Formatos disponíveis
MASAS ATÓMICA Y MASA MOLECULAR
Las unidades químicas de masa son aquellas relaciones II. MASA MOLECULAR (M)
cualitativas y cuantitativas que se producen entre los La masa molecular de un compuesto químico,
compuestos químicos y los elementos que la constituyen. se determina sumando las masas atómicas de los
elementos que lo forman.
I. MASA ATÓMICA DE UN ELEMENTO
(mA)
Tambien se le conoce como peso atómico (PA). M(compuesto) = Suma m.A. elementos
La masa atómica de un elemento tiene como químicos
unidad al uma (unidad de masa atómica).
1 uma = 1/12 masa 12C = 1,66 x 10–24g Ejemplos:
Determina la masa molecular de los siguientes
compuestos.
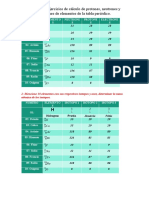
Las masas atómicas de los diversos elementos
químicos se encuentran en la tabla periodica, a. H2O mA (H) = 1 uma
debes de recordar las masas atómicas del C,H,O,N mA (O) = 16 uma
Elemento Símbolo Masa atómica
químico M = 2(1) + 1(16)
Carbono C 12 uma M = 2 + 16
Hidrógeno H 1 uma M = 18 uma
Oxígeno O 16 uma
Nitrógeno N 14 uma b. C3H8 mA (C) = 12 uma
mA (H) = 1 uma
Masas atómicas de los elementos más
M = 3(12) + 8(1)
importantes en uma
M = 36 + 8
Metales No metales M = 44 uma
Ca = 40 Li = 7 P = 31 Br = 80
Fe = 56 Mg = 24 S = 32 B = 11 c. HNO3 mA (H) = 1 uma
Al = 27 Zn = 65 Cl = 35,5 I = 127 mA (N) = 14 uma
Ag = 108 K = 39 mA (O) = 16 uma
Na = 23
M = 1(1) + 1(14) + 3(16)
En los examenes M = 1 + 14 + 48
de admisión de M = 63 uma
las universidades,
no te darán las d. H2SO4 mA (H) = 1 uma
masas atómicas mA (S) = 32 uma
del C,H,O,N, mA (O) = 16 uma
pero sí de los
demás elementos M = 2(1) + 1(32) + 4(16)
químicos. M = 2 + 32 + 64
M = 98 uma
Trabajando en clase
Integral a) M H2O = _________________
1. La masa atómica del oxígeno (O) es: b) M CO = _________________
c) M N2O3 = _________________
Resolución: d) M FeO = _________________
La mA (O) = 16 e) M SO = _________________
2. La masa atómica del carbono (C) es: 8. Si el compuesto E2O tiene M = 30 uma, calcula la
masa atómica de E.
3. Calcula la masa molecular del CH4
Resolución:
4. Calcula la masa molecular del NH3
M : E2O = 30
2(E) + 16 = 30
UNMSM 2E = 14
E = 7 uma
5. Calcula la masa molecular del SO3
(S = 32 uma). Rpta.: mA (E) = 7 uma
Resolución:
MSO3: 1(32) + 3(16) UNI
M = 32 + 48
M = 80 uma 9. Si el compuesto EO tiene masa molecular igual a
28 uma, calcula la masa atómica de E.
6. Calcula la masa molecular del N2O3
10. Compuesto que presenta la mayor masa molecular
7. Calcula la masa molecular de las siguientes a) CH4 c) NH3 e) SO2
sustancias. (Fe = 56 uma; S = 32 uma) b) CO2 d) H2O
Você também pode gostar
- Masas Atómica y Masa Molecular Primer Grado de SecundariaDocumento2 páginasMasas Atómica y Masa Molecular Primer Grado de SecundariaAlexander VergaraAinda não há avaliações
- 5to Quimica Cartilla 1Documento2 páginas5to Quimica Cartilla 1Soledad ParedesAinda não há avaliações
- Masas Atómica y Masa Molecular para Primer Grado de SecundariaDocumento2 páginasMasas Atómica y Masa Molecular para Primer Grado de Secundariavirginia hidalgoAinda não há avaliações
- 22 Unidades Quimicas de MasaDocumento4 páginas22 Unidades Quimicas de MasaRomulo FranciscoAinda não há avaliações
- Aula 3:: - Correção Dos Exercícios - Métodos Científicos - Massa MolecularDocumento26 páginasAula 3:: - Correção Dos Exercícios - Métodos Científicos - Massa MolecularLorena Nunes FerreiraAinda não há avaliações
- Quimca 9cDocumento5 páginasQuimca 9cWalter BlerraAinda não há avaliações
- Unidades Químicas de MasaDocumento15 páginasUnidades Químicas de MasahablabienpsAinda não há avaliações
- Microsoft Word 3 Masa Atómica y Molecular para Tercer Grado de SecundariaDocumento4 páginasMicrosoft Word 3 Masa Atómica y Molecular para Tercer Grado de SecundariaJhordan CallenzAinda não há avaliações
- 1col-Massa e MolDocumento32 páginas1col-Massa e MolWeberBraganteAinda não há avaliações
- Masa Atómica para Cuarto de PrimariaDocumento2 páginasMasa Atómica para Cuarto de PrimariaJose QuispeAinda não há avaliações
- Unidades Quimicas de Masa IDocumento4 páginasUnidades Quimicas de Masa IMilagros Andrea Pedraza MoyaAinda não há avaliações
- Grandezas Químicas - Documentos GoogleDocumento5 páginasGrandezas Químicas - Documentos GoogleAline Vanessa Silva SantosAinda não há avaliações
- Massa MolecularDocumento4 páginasMassa MolecularPATRICIA FERREIRA SILVEIRAAinda não há avaliações
- Grandezas QuímicasDocumento29 páginasGrandezas Químicasjosue02282007Ainda não há avaliações
- Balanceamento e EstequiometriaDocumento26 páginasBalanceamento e EstequiometriaBruno RaffaelAinda não há avaliações
- 3 Introducao A EstequiometriaDocumento26 páginas3 Introducao A Estequiometriareidosgnomos97Ainda não há avaliações
- En Este Artículo Haremos El Desarrollo de Ejercicios Sobre Masa Molar y Masa MolecularDocumento2 páginasEn Este Artículo Haremos El Desarrollo de Ejercicios Sobre Masa Molar y Masa MolecularDavidAinda não há avaliações
- Teoria Atomico-Molecular e Fórmula CentesimalDocumento15 páginasTeoria Atomico-Molecular e Fórmula CentesimalPedrão 360Ainda não há avaliações
- Masa Atómica y Molecular para Tercer Grado de SecundariaDocumento4 páginasMasa Atómica y Molecular para Tercer Grado de SecundariaLeandroCarlosManayayAinda não há avaliações
- Aula de Química - 2 SérieDocumento12 páginasAula de Química - 2 SérieLUDYMILLA MAYELLE PEREIRA GOMESAinda não há avaliações
- Cálculos - Químicos Massa - MolecularDocumento14 páginasCálculos - Químicos Massa - MolecularPaulo GouveiaAinda não há avaliações
- Cap. 1 - Unidades de Medida Da QuímicaDocumento18 páginasCap. 1 - Unidades de Medida Da QuímicaGatos CatsAinda não há avaliações
- Qumica Semana 02 Ciclo IIDocumento3 páginasQumica Semana 02 Ciclo IIMOYA HINOSTROZA YAN DICKAinda não há avaliações
- Mod 09 Aula 01Documento17 páginasMod 09 Aula 01Marcelo Batista SilvaAinda não há avaliações
- Aula de QuimicaDocumento6 páginasAula de QuimicaOrlando FirmezaAinda não há avaliações
- Prova de Avaliação nº3-CC-V1 e V3Documento7 páginasProva de Avaliação nº3-CC-V1 e V3dr.joao alcobiaAinda não há avaliações
- Ejercicios de Masa Molar 2015Documento2 páginasEjercicios de Masa Molar 2015Haydee ParedesAinda não há avaliações
- EstequiometriaDocumento2 páginasEstequiometriaLa MangaAinda não há avaliações
- Mol, Massa Molecular e EstequiometriaDocumento63 páginasMol, Massa Molecular e EstequiometriaKeila DiasAinda não há avaliações
- Aprovar Ano05 Livro13 011Documento1 páginaAprovar Ano05 Livro13 011Aprovar UEA ApostilasAinda não há avaliações
- Cálculo de Massa MolecularDocumento7 páginasCálculo de Massa MolecularLadyjones301Ainda não há avaliações
- Unidade II: Quantidade em Química Sumário: Massa MolarDocumento31 páginasUnidade II: Quantidade em Química Sumário: Massa MolarEsmeralda gomesAinda não há avaliações
- Semana 06 UqmDocumento7 páginasSemana 06 UqmKaroll Sthefany Moreno GuevaraAinda não há avaliações
- Quimica IDocumento13 páginasQuimica IfirminogaabrielAinda não há avaliações
- 10FQA Ficha Trab Ini Q1.1 - N.º 2Documento2 páginas10FQA Ficha Trab Ini Q1.1 - N.º 2Miguel Do Carmo VinagreAinda não há avaliações
- APFQI - Aula 2 - Grandezas-parteIDocumento10 páginasAPFQI - Aula 2 - Grandezas-parteIRobson RaduanAinda não há avaliações
- Balanceamento e Estequiometria SS2Documento29 páginasBalanceamento e Estequiometria SS2Bruno RaffaelAinda não há avaliações
- 10FQA Ficha Trab Ini Q1.1 - N.º 2Documento4 páginas10FQA Ficha Trab Ini Q1.1 - N.º 2pedro afonsoAinda não há avaliações
- Grandezas QuímicasDocumento17 páginasGrandezas QuímicasjvrrsalaverryAinda não há avaliações
- EstequiometriaDocumento35 páginasEstequiometriapedroaurino88Ainda não há avaliações
- Aula3 Mol e Massa Molar PDFDocumento53 páginasAula3 Mol e Massa Molar PDFCleber José de SouzaAinda não há avaliações
- Massas e MedidasDocumento49 páginasMassas e MedidasozikaaapedrinhoAinda não há avaliações
- 2 - Processos e Variáveis de Processo - SHS 0352Documento12 páginas2 - Processos e Variáveis de Processo - SHS 0352lala.laura.soaresAinda não há avaliações
- PáginaDocumento6 páginasPáginamafaldaAinda não há avaliações
- Recuperação Trimestral - 2º ADMDocumento2 páginasRecuperação Trimestral - 2º ADMkarla amorimAinda não há avaliações
- Formulas Quim2.Documento14 páginasFormulas Quim2.Vitoria MenezesAinda não há avaliações
- Mod - 08 - Reações QuímicasDocumento14 páginasMod - 08 - Reações QuímicasAline F da CostaAinda não há avaliações
- Massa e Tamanho Dos AtomosDocumento11 páginasMassa e Tamanho Dos AtomosnmnicolauAinda não há avaliações
- FT5 Mole 2022 CorreçãoDocumento3 páginasFT5 Mole 2022 Correçãojonas47Ainda não há avaliações
- Reações Químicas - Aula 03Documento25 páginasReações Químicas - Aula 03Igor FernandoAinda não há avaliações
- 01.reações Químicas-Mar 2024Documento27 páginas01.reações Químicas-Mar 2024adoniascarvalho2004Ainda não há avaliações
- Aula 1 Grandezas - 2 CamilDocumento48 páginasAula 1 Grandezas - 2 CamilAl Eduarda Barreto 4519 1O3Ainda não há avaliações
- Exercc3adcios Atomc3adstica Correc3a7c3a3oDocumento4 páginasExercc3adcios Atomc3adstica Correc3a7c3a3oPriscilla Pitizker DamacenoAinda não há avaliações
- Massas Moleculares: Cálculos QuímicosDocumento17 páginasMassas Moleculares: Cálculos QuímicosElany PereiraAinda não há avaliações
- Ficha 1.2 - 10FQADocumento2 páginasFicha 1.2 - 10FQABiaAinda não há avaliações
- FT 1QDocumento4 páginasFT 1QLeticia RussoAinda não há avaliações
- Atividade 1 TM QS 2020Documento3 páginasAtividade 1 TM QS 2020Renato Vieira de SáAinda não há avaliações
- Estequiometria (Conceitos Fundamentais)Documento16 páginasEstequiometria (Conceitos Fundamentais)Carina SiqueiraAinda não há avaliações
- ESTEQUIOMETRÍADocumento37 páginasESTEQUIOMETRÍApedroAinda não há avaliações
- Etapas Do Projeto de PesquisaDocumento2 páginasEtapas Do Projeto de Pesquisajoao vitorAinda não há avaliações
- Sas2018 4Documento17 páginasSas2018 4jgabrielcdaviAinda não há avaliações
- Aula 6 - Recursos CinesioterapêuticosDocumento9 páginasAula 6 - Recursos CinesioterapêuticosVeronica luz anselmoAinda não há avaliações
- ANIM-012 - Manual Tosa Cocker SpanielDocumento15 páginasANIM-012 - Manual Tosa Cocker SpanielMarcos CelestinoAinda não há avaliações
- Programa de Hipertrofia Feminina GRATIS Nivel 1 MescladoDocumento11 páginasPrograma de Hipertrofia Feminina GRATIS Nivel 1 MescladoCasa na VilaAinda não há avaliações
- Guia de Identificação Das Pastagens Nativas Do Pantanal (2019)Documento223 páginasGuia de Identificação Das Pastagens Nativas Do Pantanal (2019)Andreia CostaAinda não há avaliações
- Apostila Projeção Da Consciência - Waldo VieiraDocumento12 páginasApostila Projeção Da Consciência - Waldo VieiraRanilson Angelo100% (1)
- Óquio: Istema Etro ErroviárioDocumento96 páginasÓquio: Istema Etro ErroviárioJLAinda não há avaliações
- Curso Técnico de RestauraçãoDocumento2 páginasCurso Técnico de RestauraçãoVítorFernandoMarquesCoitoAinda não há avaliações
- Check List BPFDocumento11 páginasCheck List BPFcassilda_carvalho@hotmail.comAinda não há avaliações
- Apresentação TCC TamboreadorDocumento39 páginasApresentação TCC TamboreadorAllery SamAinda não há avaliações
- Guia Local v1810 - CE Crateus - 06-11-2018Documento22 páginasGuia Local v1810 - CE Crateus - 06-11-2018Marcelo ClaroAinda não há avaliações
- 3258 Boletim Tecnico Eucatex SiliconeDocumento3 páginas3258 Boletim Tecnico Eucatex Siliconeedgar m paivaAinda não há avaliações
- Ficha Rakan (ATUAL)Documento3 páginasFicha Rakan (ATUAL)Fiky ColdAinda não há avaliações
- 002 - Criminologia AMBIENTALDocumento19 páginas002 - Criminologia AMBIENTALf_f_claudio100% (2)
- Noção Intuitiva de LimitesDocumento14 páginasNoção Intuitiva de LimitesThayla CastroAinda não há avaliações
- Prova Teorica NR 06Documento2 páginasProva Teorica NR 06Lih AssisAinda não há avaliações
- Relatório de Levantamento MaterialDocumento2 páginasRelatório de Levantamento MaterialHeltonsubrg SystemAinda não há avaliações
- Requisição de PessoalDocumento2 páginasRequisição de PessoalComa Bem RefeiçõesAinda não há avaliações
- Regência Nominal Na Construção Do Texto.Documento25 páginasRegência Nominal Na Construção Do Texto.carlosjanssenrs100% (1)
- Equações DiferenciaisDocumento45 páginasEquações DiferenciaisDarkArkangel2Ainda não há avaliações
- Proced Criar NOVA CONTA No FusionSolar MONODocumento4 páginasProced Criar NOVA CONTA No FusionSolar MONOCharles CardosoAinda não há avaliações
- BOVINOCULTURADocumento85 páginasBOVINOCULTURAJuliana MouraAinda não há avaliações
- Patologia Das ConstruçõesDocumento2 páginasPatologia Das ConstruçõesAldenilo VieiraAinda não há avaliações
- Cartilha FNS - Acesso A Recursos Da Saúde 2022Documento166 páginasCartilha FNS - Acesso A Recursos Da Saúde 2022vieiraianaAinda não há avaliações
- RESGATE HISTÓRICO DE UMA COMUNIDADE: Um Olhar Sobre A História e Os Patrimônios Culturais Material e Natural Do Bairro Ponte AltaDocumento39 páginasRESGATE HISTÓRICO DE UMA COMUNIDADE: Um Olhar Sobre A História e Os Patrimônios Culturais Material e Natural Do Bairro Ponte AltaPeterson Mendes PaulinoAinda não há avaliações
- Endometriose 2021Documento16 páginasEndometriose 2021Nathalia Vasconcelos Barroso Todt AragãoAinda não há avaliações
- Classificacao Geral Vestibular UeaDocumento991 páginasClassificacao Geral Vestibular UeamartinselanildaAinda não há avaliações
- Yago CastroDocumento21 páginasYago CastroYago CastroAinda não há avaliações
- AutoP03158216425 PDFDocumento1 páginaAutoP03158216425 PDFwitalo taveiraAinda não há avaliações