Escolar Documentos
Profissional Documentos
Cultura Documentos
Cinetica Quimica
Enviado por
Daniel VictorTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Cinetica Quimica
Enviado por
Daniel VictorDireitos autorais:
Formatos disponíveis
Curso do DaN – Caderno 01 – 2024.
Essa reação é um exemplo de desidratação, __________ em
que a espécie química representada por __________ atua
01 como catalisador.
As lacunas do texto são preenchidas, respectivamente, por:
A decomposição do peróxido de hidrogênio (H2O2) é uma a) intramolecular e C2H5OH2+
reação que ocorre de acordo com a equação: b) intermolecular e H+
c) intermolecular e C2H5OH2+
2 H2O2 (aq) 2 H2O( ) O2 (g) d) intramolecular e H+
e) intramolecular e H2O
Para estudar a cinética da decomposição do peróxido de
hidrogênio, foram preparadas soluções com concentrações
diferentes, as quais foram submetidas a diferentes 03
temperaturas, sendo que em uma das soluções foi
adicionado um catalisador. A tabela apresenta as diferentes
O cientista Richard Feynman, prêmio Nobel de Física em
condições a que as soluções foram submetidas e o tempo
1965, fez comentários sobre o processo de combustão em
necessário para iniciar a decomposição do H2O2 em cada
uma entrevista chamada Fun to Imagine. Segundo ele, à
caso.
primeira vista, é impressionante pensar que os átomos de
carbono de uma árvore não entram em combustão com o
Tempo oxigênio da atmosfera de forma espontânea, já que existe
Concentração para uma grande afinidade entre essas espécies para a formação
Experimento de Temperatura iniciar a de CO2. Entretanto, quando a reação tem início, o fogo se
H2O2 liberação espalha facilmente.
de O2
5 Essa aparente contradição pode ser explicada pois
1 10 mol/L 30 °C
minutos a) a reação depende de um processo que concentre o
2 10 mol/L 50 °C 1 minuto carbono para ocorrer.
8 b) o fogo torna a reação desfavorável.
3 5,0 mol/L 30 °C
minutos c) o fogo depende da presença de CO2 para começar.
4 5,0 mol/L 30 °C 1 minuto d) o átomo de carbono da árvore é muito mais resistente ao
5 O2 do que os átomos de carbono dispersos no fogo.
5 5,0 mol/L 50 °C
minutos e) a reação precisa de uma energia de ativação para
começar.
A solução em que foi adicionado um catalisador é a do
experimento de número
a) 1.
b) 2. 04
c) 4.
d) 3. Considere a reação de decomposição da amônia,
e) 5. equacionada abaixo:
02 2NH3(g) N2(g) 3H2(g)
O polímero conhecido como “plástico verde” é o
polietileno produzido a partir do eteno proveniente do Utilizando-se métodos adequados de análise, foi possível
etanol, um recurso renovável, em vez do eteno proveniente verificar as concentrações de amônia ao longo do tempo de
do petróleo, um material fóssil. reação:
A reação de obtenção do eteno a partir do etanol se dá pelo [NH3] (mol L–1) 8,0 4,0 2,0 1,0
seguinte mecanismo: Tempo (h) 0 1 2 3
Etapa 1: C2H5OH H C2H5OH2 Com base nesses dados, assinale o que for correto.
01) A velocidade de decomposição da amônia entre 0 e 1
Etapa 2: C2H5OH2 C2H4 H2O H hora é de 4,0 mol L–1/h.
02) A velocidade da reação de decomposição da amônia ao
Reação global: C2H5OH C2H4 H2O longo de cada intervalo de tempo estudado é constante.
Assistente Unit 2024.1
Curso do DaN – Caderno 01 – 2024.1
04) A velocidade de formação do nitrogênio entre 1 e 2 02) O valor da constante de velocidade (k) é de
horas é de 1,0 mol L–1/h. aproximadamente 1,5 mol L-1 s-1.
08) A velocidade de formação do hidrogênio entre 2 e 3 04) A ordem da reação em relação ao SO2(g) é 2.
horas é de 1,5 mol L–1/h. 08) A lei de velocidade para a reação é dada por: v = k
[SO2]2 [O3]0.
16) Quando as concentrações de SO2(g) e de O3(g) forem
iguais e valerem 1,00 mol L-1 cada, a velocidade inicial
será igual a 1,5 mol L-1 s-1.
05
Considere a reação de decomposição da amônia,
equacionada abaixo:
07
2NH3(g) N2(g) 3H2(g)
O estudo cinético de determinado processo químico
Utilizando-se métodos adequados de análise, foi possível permitiu a construção de coordenadas de reação como a
verificar as concentrações de amônia ao longo do tempo de ilustrada no gráfico.
reação:
[NH3] (mol L–1) 8,0 4,0 2,0 1,0
Tempo (h) 0 1 2 3
Com base nesses dados, assinale o que for correto.
01) A velocidade de decomposição da amônia entre 0 e 1
hora é de 4,0 mol L–1/h.
02) A velocidade da reação de decomposição da amônia ao
longo de cada intervalo de tempo estudado é constante.
04) A velocidade de formação do nitrogênio entre 1 e 2
horas é de 1,0 mol L–1/h.
08) A velocidade de formação do hidrogênio entre 2 e 3
horas é de 1,5 mol L–1/h.
De acordo com a análise do gráfico, verifica-se que:
a) a reação ocorre pelo caminho II devido à presença de um
catalisador liberando energia, diferentemente do
caminho I, que é endotérmico.
b) quando a reação ocorre pelo caminho I, o reagente A2 é
06
consumido mais rapidamente do que quando ocorre pelo
caminho II.
c) a reação é endotérmica, sendo absorvida a energia dada
Considere a reação química representada a seguir: por (x – z) por mol de A2 consumido.
d) devido à atuação do catalisador, o caminho II apresenta
menor energia de ativação, igual a y, do que o caminho I,
SO2(g) O3(g) SO3(g) O2(g)
cuja energia de ativação é dada por x.
e) a reação é exotérmica e libera energia dada por (x + z)
Um estudo de velocidade dessa reação foi realizado a 298 por mol de A2 consumido.
K. Os dados que foram obtidos a partir desse estudo são
mostrados na tabela a seguir:
[SO2], mol Velocidade inicial, mol L-
[O3], mol L-1
L-1 1 -1
s
0,25 0,40 0,118
0,25 0,20 0,118
0,75 0,20 1,062
A partir dos dados contidos na tabela, assinale o que for
correto.
01) A ordem da reação em relação ao O3(g) é 1.
Assistente Unit 2024.1
Curso do DaN – Caderno 01 – 2024.1
08 10
O airbag, componente de segurança passiva dos veículos
automotores, possui um balão de ar muito resistente que O uso de catalisadores em processos químicos é usual e
contém, entre outras substâncias, o sólido azida de sódio muito importante. Grandes investimentos são realizados
(NaN3). Quando ocorre uma colisão, os sensores tanto por empresas quanto por órgãos públicos visando a
distribuídos em partes especificas dos veículos transmitem síntese de materiais que atuem como catalisadores cada vez
um impulso elétrico (faísca) que provoca a rápida mais seletivos e eficientes. Dessa forma, busca-se atingir a
decomposição desse sólido, em gás nitrogênio (N2), inovação tecnológica de materiais e processos químicos.
responsável por inflar o airbag, e o sólido sódio (Na),
conforme a equação da reação: Os catalisadores aumentam a velocidade da reação
química, porque
a) permitem que reações não espontâneas se tornem
2NaN3 (s) 3N2 (g) 2Na(s)
espontâneas.
tempo (min) NaN3 (mol) b) permitem que a reação se desenvolva por um caminho de
0 0,8 reação exotérmico.
c) permitem que a reação se desenvolva por um caminho de
10 0,5 menor energia de ativação.
d) promovem o aumento da energia cinética dos reagentes.
Considerando a reação de decomposição e os dados da e) permitem que a reação se desenvolva por um caminho de
tabela, a velocidade média de formação do gás nitrogênio, reação em fase homogênea.
no intervalo entre 0 e 10 minutos, é igual a
a) 5,0 10 4 mol s1.
b) 3,0 10 3 mol s1.
c) 7,5 10 2 mol s1.
d) 5,0 10 2 mol s1.
e) 7,5 10 4 mol s1.
09
Certa reação ocorre pela combinação de três reagentes „A‟,
„B‟ e „C‟. Ao se dobrar a concentração do reagente „A‟,
mantendo-se constantes os valores de concentração dos
outros dois reagentes, a velocidade da reação dobra. Ao se
dobrar a concentração do reagente „B‟, mantendo-se
constantes os valores de concentração dos outros dois
reagentes, a velocidade da reação não se altera. Ao se
dobrar a concentração do reagente „C‟, mantendo-se
constantes os valores de concentração dos outros dois
reagentes, a velocidade da reação quadruplica.
Em relação à velocidade da reação, assinale a alternativa
CORRETA:
a) A equação de velocidade da reação é V = K
[A]2[B]1[C]44.
b) A equação de velocidade da reação é V = K
[A]1[B]0[C]2.
c) A equação de velocidade da reação é V = K
2[A]+[B]+4[C].
d) A equação de velocidade da reação é V = K [A]-2[B]-
1
[C]-4.
Assistente Unit 2024.1
Curso do DaN – Caderno 01 – 2024.1
Questões Abertas
1 12
Os conversores catalíticos são a opção mais comum para o
A amônia é produzida pelo conhecido processo Haber- controle das emissões de gases poluentes pelos motores de
Bosch a partir dos gases nitrogênio e hidrogênio, segundo a combustão interna dos automóveis, acelerando a conversão
equação (não balanceada) a seguir: dos óxidos de nitrogênio em gases nitrogênio e oxigênio.
Uma reação química que pode ser usada para a conversão
N2(g) H2(g) NH3(g) do óxido nítrico em gases não poluentes á a reação deste
gás com hidrogênio, resultando nos gases nitrogênio e água,
como mostra a equação química abaixo:
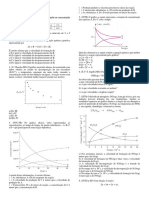
O gráfico a seguir se refere às concentrações de reagentes e
produto para um experimento de síntese da amônia.
2 NO(g) 2 H2(g) N2(g) 2 H2O(g)
A cinética desta reação na temperatura de 1250 C
encontra-se representada na tabela abaixo, a qual indica a
influência da concentração dos reagentes na velocidade da
reação, obtida através de três experimentos executados sob
as mesmas condições:
Velocidad
Experiment [NO] (mol L) [H2 ] (mol L) e inicial
o
(mol L s)
1 0,10 0,04 0,025
2 0,20 0,04 0,10
3 0,20 0,08 0,20
Considerando a lei de velocidade das reações químicas,
pede-se:
Com base nesses dados:
a) Escreva a equação da velocidade desta reação e calcule a
a) Escreva a equação balanceada da síntese da amônia. velocidade quando a concentração de NO for de
b) Associe as curvas A, B e C com as substâncias N2, H2 e 0,30 mol L e a concentração de H2 for igual a
NH3. 0,10 mol L.
c) Qual a velocidade média de consumo de H2 entre 0 e 60 b) Explique por que ocorre o aumento da velocidade de
minutos. reação quando aumentamos a concentração dos
d) Qual a velocidade média de formação de NH3 entre 60 e reagentes.
120 minutos?
Assistente Unit 2024.1
Você também pode gostar
- Est Dirigido Cineticaqui-1Documento6 páginasEst Dirigido Cineticaqui-1Zoé AraújoAinda não há avaliações
- Lista 1.cinética QuímicaDocumento6 páginasLista 1.cinética Químicagiovannaluiza1323Ainda não há avaliações
- Alfa - Módulo 37Documento23 páginasAlfa - Módulo 37Jackson Rodrigo Sousa PintoAinda não há avaliações
- Exercicios de Fisico-QuimicaDocumento2 páginasExercicios de Fisico-QuimicaFellipe LimaAinda não há avaliações
- Cine TicaDocumento37 páginasCine TicaWingston WalterAinda não há avaliações
- Cinètica Quimica 1Documento6 páginasCinètica Quimica 1Débora SaraAinda não há avaliações
- Exe CineticaDocumento26 páginasExe CineticaJhonatas GouveiaAinda não há avaliações
- Azdoc - Tips Exe CineticaDocumento10 páginasAzdoc - Tips Exe CineticaAlana SantosAinda não há avaliações
- Cinética QuímicaDocumento2 páginasCinética QuímicasrfesjiunAinda não há avaliações
- Lista 8 - Cinética Química - Físico-Química - Cursinho VitorianoDocumento9 páginasLista 8 - Cinética Química - Físico-Química - Cursinho Vitorianoana biaAinda não há avaliações
- Cinética QuimicaDocumento26 páginasCinética QuimicaTais Kaspary SchmittAinda não há avaliações
- Atividade Avaliativa de Cinética Química ProfDocumento1 páginaAtividade Avaliativa de Cinética Química ProfClebson RamosAinda não há avaliações
- Atividade Cinética II SGDocumento7 páginasAtividade Cinética II SGademairmoreiraAinda não há avaliações
- Cinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesDocumento72 páginasCinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesrafelAinda não há avaliações
- Cinetica-Quimica EXERCICIOSDocumento2 páginasCinetica-Quimica EXERCICIOScarlostucupiAinda não há avaliações
- Química GeralDocumento3 páginasQuímica GeralMonica januarioAinda não há avaliações
- 50 20cin C3 A9tica 20qu C3 ADmicaDocumento26 páginas50 20cin C3 A9tica 20qu C3 ADmicaDouglas Sousa0% (1)
- Apostila Tecnico Operaçao Junior-Operador-PetrobrasDocumento22 páginasApostila Tecnico Operaçao Junior-Operador-Petrobrasvmdesousa100% (1)
- Alfa - Módulo 37 PDFDocumento21 páginasAlfa - Módulo 37 PDFLuiza FreitasAinda não há avaliações
- 2009 FinalDocumento6 páginas2009 FinaliolaAinda não há avaliações
- Exe Cinetica PDFDocumento29 páginasExe Cinetica PDFnatale_carvalhoAinda não há avaliações
- Lista de Exercícios Modelo - Cinética Química (Part 1)Documento2 páginasLista de Exercícios Modelo - Cinética Química (Part 1)AlexandreAinda não há avaliações
- Exercícios Cinética Química LivretoDocumento8 páginasExercícios Cinética Química LivretoJoão Ribeiro Franco NetoAinda não há avaliações
- Velocidade Das Reações - ÍtaloDocumento8 páginasVelocidade Das Reações - ÍtaloItalo PiresAinda não há avaliações
- 31583Documento14 páginas31583Leondenes Rodrigues IzidoroAinda não há avaliações
- Química 2 Ano - Iii Unid - Cinética QuímicaDocumento41 páginasQuímica 2 Ano - Iii Unid - Cinética QuímicaJuca GordoAinda não há avaliações
- Reação QuímicaDocumento11 páginasReação QuímicaFranco PontesAinda não há avaliações
- Lista de Exercícios - CinéticaDocumento5 páginasLista de Exercícios - CinéticaGleison MendesAinda não há avaliações
- Lista de Exercícios - Cinética QuímicaDocumento4 páginasLista de Exercícios - Cinética QuímicaMary Eduarda MoraesAinda não há avaliações
- Lista 10 Geral 2023-2Documento6 páginasLista 10 Geral 2023-2yjb46zys2hAinda não há avaliações
- CálculosestequiométricoDocumento8 páginasCálculosestequiométricompedroleesilvaAinda não há avaliações
- Cinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesDocumento72 páginasCinética Química - Expressão e Cálculo Da Velocidade - 130 Questõesani_matrixx4733100% (1)
- Cinetica Quimica UniDocumento6 páginasCinetica Quimica UnicarlostucupiAinda não há avaliações
- Treino Segunda SerieDocumento7 páginasTreino Segunda SeriekauaAinda não há avaliações
- Aula 1 VelocidadesDocumento3 páginasAula 1 VelocidadesDaniel MatheusAinda não há avaliações
- Lista Complementar de Exercícios: Ensino Médio 3º AnoDocumento10 páginasLista Complementar de Exercícios: Ensino Médio 3º AnogabezmirandaAinda não há avaliações
- Lista de Exercícios - Cinética 2Documento4 páginasLista de Exercícios - Cinética 2Gleison MendesAinda não há avaliações
- Class AppDocumento5 páginasClass AppThaayna BarroosAinda não há avaliações
- Exercícios - Cinética QuímicaDocumento4 páginasExercícios - Cinética QuímicaIara DaherAinda não há avaliações
- Exercícios CineticaEquilibrioDocumento3 páginasExercícios CineticaEquilibrioVandice75Ainda não há avaliações
- Cinetica ExercDocumento3 páginasCinetica ExercCamila BarreirosAinda não há avaliações
- Lista de Cinética IDocumento2 páginasLista de Cinética IRtyu IuytAinda não há avaliações
- Cinética Química IDocumento50 páginasCinética Química IArthur ViníciusAinda não há avaliações
- Lista de Exercicios Cinetica Quimica EQM061Documento13 páginasLista de Exercicios Cinetica Quimica EQM061Mariana DomicianoAinda não há avaliações
- EXAME 2ANO QuimicaDocumento3 páginasEXAME 2ANO QuimicaBruna MartinsAinda não há avaliações
- Quimica ADocumento10 páginasQuimica Ahelenaquevedo64Ainda não há avaliações
- Físico-Química - Cinética Química (20 Questões)Documento10 páginasFísico-Química - Cinética Química (20 Questões)Ciencias PPT100% (1)
- Exercício de CinéticaDocumento7 páginasExercício de CinéticaIsaque MouraAinda não há avaliações
- Cinética QuímicaDocumento37 páginasCinética QuímicaGleisonAinda não há avaliações
- Lista CinéticaDocumento18 páginasLista Cinéticamoitinhamhsp2Ainda não há avaliações
- 21Documento5 páginas21gabezmirandaAinda não há avaliações
- Avaliação Cinética e TermoquímicaDocumento5 páginasAvaliação Cinética e TermoquímicaLuciane Azevedo DiasAinda não há avaliações
- EXERCÍCIOS-12 CLASSEdocxDocumento6 páginasEXERCÍCIOS-12 CLASSEdocxRanked PlayerAinda não há avaliações
- Exercà Cios Rec 2 CertifDocumento2 páginasExercà Cios Rec 2 CertifMin YoongiAinda não há avaliações
- Cinetica CompletaDocumento5 páginasCinetica CompletaConta ReservaAinda não há avaliações
- Questões CinéticaDocumento1 páginaQuestões Cinéticarubens.costaAinda não há avaliações
- Cine TicaDocumento37 páginasCine TicaLala AssisAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- 15 03Documento5 páginas15 03Daniel VictorAinda não há avaliações
- Notes 240129 092237 240301 095006Documento1 páginaNotes 240129 092237 240301 095006Daniel VictorAinda não há avaliações
- CraseDocumento4 páginasCraseDaniel VictorAinda não há avaliações
- Unit Unificado Cad 2 2022 FinalDocumento21 páginasUnit Unificado Cad 2 2022 FinalDaniel VictorAinda não há avaliações
- Lista de Exercício BalanceamentoDocumento1 páginaLista de Exercício Balanceamentoklebert.dantasAinda não há avaliações
- Cinetica Lista 1Documento3 páginasCinetica Lista 1luisparoAinda não há avaliações
- Aula PotássioDocumento18 páginasAula PotássiojoicessmmAinda não há avaliações
- Cromatografia SupercríticaDocumento11 páginasCromatografia Supercríticajean.pinheiroAinda não há avaliações
- Lista 2 Exercicios Pre Vestibular Revisão UfrgsDocumento21 páginasLista 2 Exercicios Pre Vestibular Revisão UfrgscontatojaysroutineAinda não há avaliações
- Atividade 02 - Saúde - Química Analítica e Instrumental - 51-2024Documento5 páginasAtividade 02 - Saúde - Química Analítica e Instrumental - 51-2024admcavaliniassessoriaAinda não há avaliações
- A Lei de LavoisierDocumento6 páginasA Lei de Lavoisierpedropaulosales9Ainda não há avaliações
- Relatório Aulas Práticas OFCDocumento11 páginasRelatório Aulas Práticas OFCfranconitiagoAinda não há avaliações
- Exercícios Quimica - 2023Documento4 páginasExercícios Quimica - 2023solanthales7Ainda não há avaliações
- NBR 12653 - Materiais Pozolânicos - RequisitosDocumento10 páginasNBR 12653 - Materiais Pozolânicos - RequisitosMusicas boasAinda não há avaliações
- Euq - 2023-1Documento23 páginasEuq - 2023-1Andre TeixeiraAinda não há avaliações
- Combustíveis Fósseis e Energia NuclearDocumento21 páginasCombustíveis Fósseis e Energia NuclearbeneditaAinda não há avaliações
- 4-Segunda e Terceira Lei Da TermodinâmicaDocumento55 páginas4-Segunda e Terceira Lei Da TermodinâmicaAnny NascimentoAinda não há avaliações
- Estequiometria e Balanceamento 1Documento11 páginasEstequiometria e Balanceamento 1Rebeca SáAinda não há avaliações
- Fispq 60 Limpa Vidros Coperalcool Codigo 780 781 782 Rev00Documento15 páginasFispq 60 Limpa Vidros Coperalcool Codigo 780 781 782 Rev00christianlima365Ainda não há avaliações
- Misturas Homogêneas e Heterogêneas - Ef06ci01Documento20 páginasMisturas Homogêneas e Heterogêneas - Ef06ci01Augusto Pereira100% (1)
- Material de Apoio para ProvasDocumento13 páginasMaterial de Apoio para ProvascradogodAinda não há avaliações
- Materiais Cerâmicos - EstruturaDocumento8 páginasMateriais Cerâmicos - EstruturaErick GomesAinda não há avaliações
- Plano de Aula de Ligações Iônicas e CovalentesDocumento3 páginasPlano de Aula de Ligações Iônicas e CovalentesDrico AraújoAinda não há avaliações
- MineraisDocumento33 páginasMineraisaluno26507100% (1)
- Lab Quim 23 - 24 - QuestionáriosDocumento14 páginasLab Quim 23 - 24 - QuestionáriosAfonso MacedoAinda não há avaliações
- Prova Paulista 1anoDocumento7 páginasProva Paulista 1anoWelton Vanzei TeixeiraAinda não há avaliações
- Amino Acid OsDocumento51 páginasAmino Acid OspabsbarbosasoaresAinda não há avaliações
- AminofilinaDocumento1 páginaAminofilinacelmorcelliAinda não há avaliações
- Aspectos Quantitativos: QuímicaDocumento20 páginasAspectos Quantitativos: Química00001122915858spAinda não há avaliações
- Fas 2 (Rpe)Documento4 páginasFas 2 (Rpe)Maria CoutoAinda não há avaliações
- Aula7 - 1 Série - ExperimentosDocumento15 páginasAula7 - 1 Série - ExperimentosSara MarquiAinda não há avaliações
- Atomística e DistribuiçãoDocumento17 páginasAtomística e DistribuiçãoRebeca SáAinda não há avaliações
- Lava Roupas InvictoDocumento7 páginasLava Roupas InvictokathelyndinizAinda não há avaliações
- Resumo Concentraà à o Comum e MolarDocumento1 páginaResumo Concentraà à o Comum e Molarmarianomiguel483Ainda não há avaliações