Escolar Documentos
Profissional Documentos
Cultura Documentos
Castro-Silva Et Al 2009
Enviado por
lorena amorimDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Castro-Silva Et Al 2009
Enviado por
lorena amorimDireitos autorais:
Formatos disponíveis
Panorama atual do uso de xenoenxertos na prática
odontológica
Current overview of the use of xenograft in dentistry
Igor Iuco CASTRO-SILVA1, Willian Fernando ZAMBUZZI2, José Mauro GRANJEIRO3
RESUMO ABSTRACT
O reparo de perdas ósseas severas é, ainda, um grande Repair of severe bone loss is still a major challenge for
desafio na Medicina Regenerativa, onde o osso autógeno Regenerative Medicine, where the bone graft is the gold
continua sendo o padrão-ouro a despeito de apresentar standard in spite of some disadvantages such as need
desvantagens como necessidade de segundo sítio cirúrgico for second surgical site and morbidity. Alternatively, the
e morbidade. Alternativamente, o xenoenxerto acelular properly processed acellular and deproteinized bovine
e desproteinizado de origem bovina, adequadamente xenograft, presenting biocompatibility and osteoconductive
processado e apresentando-se biocompatível e properties, plays an important role in bone repair. Based
osteocondutor, ocupa um papel de destaque no auxílio ao on histomorphometric analysis, in vivo studies and clinical
reparo ósseo. Estudos in vivo e clínicos baseados em análise trials showed better performance compared to alloplastic
histomorfométrica demonstraram melhor performance em materials and allograft, possibly because of the inherent
relação aos materiais aloplásticos e alógenos, possivelmente properties of natural apatite and biologically designed porous
em função das propriedades inerentes da apatita natural architecture. Recent studies have evaluated the association
e, ainda, da arquitetura porosa naturalmente desenhada. of the xenograft, growth factors and stem cells aiming to
Estudos recentes tem avaliado a associação de xenoenxertos attribute autograft properties to xenograft. We conclude
a fatores de crescimento e células osteoprogenitoras com that xenografts handled appropriately, will show physico-
o intuito de aproximar a resposta tecidual ao xenoenxerto chemical properties and adequate biological behavior helping
à do enxerto autógeno. Conclui-se que xenoenxertos to repair bone defects, demonstrating safety, applicability
adequadamente processados possuem características físico- and satisfactory clinical predictability.
químicas e comportamento biológico favoráveis ao reparo
ósseo, demonstrando segurança, aplicabilidade e satisfatória Key words: Transplantation, heterologous. Bone
previsibilidade clínica. transplantation. Biocompatible materials.
Palavras-chave: Transplante heterólogo. Transplante
ósseo. Materiais biocompatíveis.
Endereço para correspondência:
José Mauro Granjeiro
Hospital Universitário Antônio Pedro - Laboratório de Bioengenharia, Biomateriais e Mineralização Biológica
Rua Marquês do Paraná, 303 - 4. andar - Emergência - Unidade de Pesquisa Clínica
24033-900 - Niterói - Rio de Janeiro - Brasil
E-mail: jmgranjeiro@gmail.com
Recebido: 05/12/2009
Aceito: 17/12/2009
1. Mestre em Patologia Buco-Dental. Pesquisador do Núcleo de Terapia Celular, Unidade de Pesquisa Clínica, Hospital Universitário Antônio Pedro, Universidade Federal
Fluminense, Niterói, RJ, Brasil.
2. Pós-Doutorando em Enzimologia do Departamento de Bioquímica, Instituto de Biologia, Universidade Estadual de Campinas, Campinas, SP, Brasil.
3. Professor Adjunto do Departamento de Biologia Celular e Molecular, Instituto de Biologia, Universidade Federal Fluminense, Niterói, RJ, Brasil. Professor Visitante da
Faculdade de Odontologia de Bauru, Universidade de São Paulo, Bauru, SP, Brasil.
70 Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009
ARTIGOS CIENTÍFICOS
Castro-Silva II, Zambuzzi WF, Granjeiro JM
INTRODUÇÃO de tecidos ou órgãos devem ser, obrigatoriamente, livres de
patógenos conhecidos. Para os xenoenxertos de origem bovina,
a preocupação com a encefalopatia espongiforme bovina
O reparo de perdas ósseas severas é ainda um grande (BSE) foi descartada com base nos seguintes aspectos: 1) uso
desafio na Medicina Regenerativa moderna, especialmente em de animais livres da BSE; 2) processamento adequado do osso
cirurgia craniomaxilofacial e ortopédica. A opção de tratamento com substâncias alcalinas capazes de remover o príon, agente
é o uso de enxertos ósseos que, de acordo com sua similaridade etiológico da BSE, potencialmente existente; 3) extração da
genética, podem se classificar em: autógenos (mesmo indivíduo matéria-prima dos tecidos a partir de sítios com mínimo risco de
doador e receptor), alógenos (indivíduos doador e receptor de transmissão da BSE: os ossos e tendões. No caso particular do
mesma espécie), xenógenos (indivíduos doador e receptor de Brasil, não há registros de BSE, tornando os materiais produzidos,
espécies diferentes), ou aloplásticos (sintéticos). desde que convenientemente processados, adequados para uso
Embora o autoenxerto seja considerado a primeira opção como osteosubstitutos.
para enxertos ósseos ou “padrão-ouro” devido ao seu potencial
osteogênico, osteoindutor e osteocondutor, sua disponibilidade PROCESSAMENTO DO BIOMATERIAL
é baixa, incorre em maiores custos operacionais e morbidade Os xenoenxertos são predominantemente de origem
(sensibilidade aumentada) do sítio doador a curto e longo prazo. bovina15,17-18, 20-22,25, mas também podem derivar de suínos23 ou
A previsibilidade de resultados clínicos com a utilização de equinos7, sendo sua matéria-prima obtida pelo processamento
substitutos ósseos alógenos, xenógenos e aloplásticos levam a de ossos longos20, tendão20, pericárdio27, submucosa intestinal23
considerar essas opções como válidas para o processo de reparo ou outros sítios anatômicos.
tecidual, devido a ausência de reabsorção em volume, ao sítio O processamento de um biomaterial osteosubstituto
cirúrgico unitário e ao melhor pós-operatório6. xenógeno permite alternativas interessantes quanto às
Diversas empresas estrangeiras produzem materiais formas isoladas ou conjugadas dos seguintes constituintes
osteosubstitutos de origem xenógena há cerca de 20 anos, biológicos: fração orgânica do osso (desmineralizada, com
as quais detém 80% do mercado mundial de enxertos ósseos potencial osteoindutor), fração cortical ou medular inorgânica
dentários. Paralelamente, empresas nacionais também têm desproteinizada, na forma de grânulos ou blocos, ou ainda,
investido no desenvolvimento de materiais biocompatíveis como membrana reabsorvível desmineralizada15. Por vezes, a
capazes de aumentar e/ou acelerar o reparo ósseo. As dispersão dos grânulos pode dificultar a implantação do material
aplicações mais comuns dos xenoenxertos em Odontologia e a associação com um aglutinante (como colágeno) seria uma
são os tratamentos de defeitos periodontais19, sítios pós- estratégia interessante. Dentre os implantes xenogênicos de
extração dentária9, levantamento de seio maxilar9 e aumento origem bovina, os produzidos com o osso esponjoso revestem-
de rebordo alveolar8. se de particular interesse devido a sua arquitetura constituída
O objetivo deste trabalho é revisar as características e de poros biologicamente desenhados que favorecem a invasão
propriedades dos xenoenxertos e as avaliações físico-químicas celular e vascular até o centro do defeito29.
e biológicas fundamentais para a validação de um xenoenxerto O processamento do xenoenxerto, com tratamento mecânico
bovino seguro para o emprego na terapia de defeitos ósseos. e químico, via álcalis e solventes orgânicos, para remoção de
debris, células e sangue, e ácido clorídrico 0,6M, resultou em
osso bovino desmineralizado biocompatível e biodegradável30.
A temperatura de desproteinização do osso cortical
REVISÃO DE LITERATURA bovino influencia na resposta tecidual. O tratamento térmico
a 1.000 °C resultou em maior intensidade de fibrose e reação
granulomatosa do tipo corpo estranho de baixa renovação,
REGULAMENTAÇÕES contendo macrófagos e células gigantes multinucleadas, porém
A Organização Internacional de Padronização (ISO), através não exibindo indícios de atuarem na sua degradação. Por outro
da norma 10993 e seus subitens, compilou as fases pré-clínicas lado, o tratamento a 100 °C promoveu maior interação com as
necessárias para caracterização de biomateriais, desde os células gigantes e exibiu sinais de biodegradação após 60 dias
estudos físico-químicos29 até os biológicos (in vitro e in vivo)11. de implantação17. Temperatura superiores a 700 °C permitem a
Por outro lado, a Sociedade Americana de Testes e Materiais completa eliminação do conteúdo protéico e manutenção das
(ASTM) contribuiu para padronizar os métodos para avaliação da característica naturais da fração mineral do osso bovino, resultado
composição do osso inorgânico bovino para implantes cirúrgicos2 em grânulos com boa estabilidade mecânica do material, livre de
e, no cenário nacional, a Agência Nacional de Vigilância Sanitária espículas e fragmentos micrométricos prejudiciais ao processo
(ANVISA) é o órgão responsável por autorizar a comercialização de reparo e biocompatível5,12.
de dispositivos para a saúde. Uso de blocos de osso bovino inorgânico sinterizado em
A Organização Mundial de Saúde26 e o Conselho de Bioética defeitos de tamanho crítico em porcos da índia (Cavia aperea)
de Nuffield14 determinam que animais utilizados como fonte mostrou, em relação ao tratamento com coágulo sanguíneo
Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009 71
Panorama atual do uso de xenoenxertos na prática odontológica
(controle), após 180 dias de pós-operatório, o valor médio de
espessura vertical do enxerto igual a 279%, osseointegrado
às bordas do defeito, uma espessura vertical 3,8 vezes
superior e um volume total de aumento ósseo 148% maior,
demonstrando a propriedade de osteocondução e reabsorção
lenta do xenoenxerto4.
CARACTERIZAÇÃO FÍSICO-QUÍMICA
Dentre as técnicas de avaliação pela norma ISO, destacam- Figura 1 - Características físico-químicas e morfológicas de
se: para parâmetros físicos, a microscopia ultra-estrutural da Osseus®. (A) FTIR; (B) difração de raios X. (C) micrografia
superfície do material (microscopia eletrônica de varredura eletrônica de varredura exibindo a uniformidade estrutural
- MEV), mensuração de porosidade (BET) e de rugosidade dos grânulos, presença de poros na estrutura do biomaterial e
ausência de fragmentos micrométricos.
(perfilometria ou microscopia de força atômica) e avaliação
tridimensional (microscopia confocal). A análise química
é feita através de difração de raio X (DRX), MEV acoplado à
espectroscopia por energia dispersiva de Raios X (MEV-EDS) ou CARACTERIZAÇÃO BIOLÓGICA
por infravermelho transformada por Fourier (FTIR)5. FTIR é uma
ferramenta útil para avaliação de um biomaterial implantável; CITOCOMPATIBILIDADE
detecta modificação química de hidroxiapatita pela troca de A análise da toxicidade a curto prazo (24 horas) dos materiais
íons entre o ambiente biológico e a apatita, como a inclusão de implantáveis aponta a existência de resíduos tóxicos solúveis no
carbonato 28 dias após enxerto3. xenoenxerto se houver morte de 15% ou mais das células11.
A caracterização físico-química de materiais osteosubstitutos Processamento do osso bovino inadequado pode resultar em
é fundamental, pois parâmetros como cristalinidade, área materiais citotóxicos15, mas a remoção completa de proteínas,
superficial e composição do biomaterial influenciam o reparo debris celulares e lipídios resulta em enxertos inorgânicos na
ósseo e sua taxa de degradação após implantação; produtos forma granular biocompatíveis12,18. É importante a utilização de
com área de superfície baixa associada à cristalinidade alta controle positivo e negativo a fim de orientar a interpretação
decorrente de tratamento térmico (sinterização) podem ser dos resultados in vitro, tornando-os relativos a materiais cujos
assumidos como não-absorvíveis, embora elevadas concentração efeitos biológicos sejam muito bem conhecidos e reproduzíveis
de carbonato atenuem esta tendência5. Xenoenxertos (Figura 2)12.
desproteinizados, constituídos por apatitas naturais, sinterizadas
ou não, têm boas propriedades físicas e químicas (Figura 1)12.
Entretanto, o controle do processo de produção é determinante
para a qualidade dos biomateriais; o estudo mostrou que
dentre seis diferentes hidroxiapatitas (2 naturais/bovinas e 4
sintéticas) comerciais disponíveis no mercado brasileiro, apenas
um dos produtos (HA natural) apresentou concordância nas
propriedades físicas e químicas determinadas no estudo e as
presentes na bula do produto5.
Figura 2 - Gráfico do número relativo de célula em função da
concentração do extrato do pó de titânio (controle negativo),
fenol 2% (controle positivo) e do Osseus® mostrando que o
xenoenxerto proporcional citotoxicidade da ordem de 10 a
15%, não significativamente diferente do titânio, em oposição
à forte citotoxicidade do fenol 2%.
BIOCOMPATIBILIDADE
A caracterização biológica in vivo mostra em sítios ectópicos
(músculo ou tecido subcutâneo) o padrão de resposta celular e
72 Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009
ARTIGOS CIENTÍFICOS
Castro-Silva II, Zambuzzi WF, Granjeiro JM
em sítios ortotópicos (calvária, tíbia, fêmur ou rádio) o padrão realizando experimentos em coelhos, observou acidentalmente
de reparo ósseo, em diferentes modelos animais experimentais um fenômeno de indução óssea, o qual denominou-se
(camundongo, rato, cobaia, porco-da-índia, porco, coelho, cão e osteoindução. Neste processo células progenitoras multipotentes
ovelha). O enxerto ósseo ideal deve possuir características como são persuadidas a diferenciarem-se em osteoblastos capazes
biocompatibilidade, capacidade osteocondutora, osteoindutora, de produzir osso, tornando-se evidente a diferenciação de
resistência e plasticidade29, porém estas propriedades não foram células-tronco mesenquimais em osteoblastos maduros na
reunidas, ainda, em um único material. área do defeito1. São exemplos deste processo a matriz óssea
O osso inorgânico bovino medular é bem tolerado pelo desmineralizada16 e as proteínas morfogenéticas ósseas10.
tecido conjuntivo de ratos, evoluindo a respostas tecidual para Por sua vez, a osteocondução se refere ao crescimento ósseo
a formação de fibrose, mas livre de reações adversas severas ordenado sobre a superfície do biomaterial implantado1. Alguns
(presença discreta de células gigantes), após 60 dias da autores definem osteocondução como o processo pelo qual o
implantação, com desaparecimento de neutrófilos, linfócitos, material implantado serve como arcabouço para migração e a
plasmócitos em período tardio, não estimulando a resposta adesão de células osteoprogenitoras e endoteliais, contribuindo
imunológica e sendo considerado biocompatível (Figura 3)12,28. para a aposição de um novo tecido ósseo1.
A associação de osso cortical inorgânico e colágeno liofilizado, Por fim, a osteopromoção refere-se ao princípio de utilizar
ambos de origem bovina, pode resultar em um biomaterial barreiras mecânicas que evitam a proliferação do tecido conjuntivo
biocompatível e não imunogênico. adjacente em meio ao defeito ósseo, permitindo que o mesmo
A resposta tecidual a um biomaterial cerâmico engloba seja povoado por células osteoprogenitoras24. Esta exclusão
basicamente as fases da inflamação (aguda: células tecidual é realizada com o uso de membranas (barreiras físicas),
polimorfonucleares, mastócitos, macrófagos; crônica: células que podem ser absorvíveis ou não. As membranas, rígidas ou
gigantes multinucleadas e mastócitos) e reparo, caracterizado com reforço de titânio, são capazes de promover a formação de
por alterações vasculares (maior densidade de microvasos) e quantidade significativa de novo osso e manter espaço suficiente,
maior taxa de proliferação. sem a adição de material de preenchimento. Isso ocorre devido
à sua capacidade de “efeito tenda”, principalmente quando
fixadas com pequenos parafusos, pois o maior problema das
membranas sem reforço de titânio é a manutenção do espaço
para a neoformação óssea. Clinicamente, estes atributos
conferem uma técnica de regeneração óssea guiada (ROG), a
qual é indicada no tratamento de defeitos ósseos, para aumentar
a altura e largura da crista óssea, entre outras indicações13.
CONCLUSÃO
Especificamente no campo da Odontologia, biomateriais
podem ser aplicados como enxertos ósseos em cirurgia
regenerativas ou corretivas, em procedimentos destinados a
restaurar o tecido ósseo perdido durante a doença periodontal
ou lesões endodônticas, no preenchimento alveolar de dentes
extraídos, com o objetivo de evitar a redução do volume do
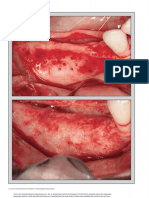
Figura 3 - Fotomicrografias após 9 semanas de implantação rebordo alveolar, em levantamento de assoalho do seio maxilar
de Osseus® no tecido subcutâneo de ratos. Grânulos de entre outras utilizações.
xenoenxertos (*) no tecido conjuntivo denso constituído por
discreto infiltrado inflamatório de células mononucleares
O desenvolvimento biotecnológico, iniciado na década de 50
(cabeça de seta), vasos sanguíneos (seta). Aumentos de 10 (A) e e notavelmente acelerado a partir dos anos 90, trouxe avanços
40 (B) vezes. Coloração: hematoxilina e eosina. significativos para o emprego de biomateriais em tratamentos
envolvendo a remodelação óssea. Juntamente com estas inovações,
novos riscos terapêuticos e outras questões também surgiram
EVENTOS BIOLÓGICOS ALIADOS À BIOCOMPATIBILI- para desafiar profissionais com diferentes formações, que devem
DADE convergir seus esforços para trabalhar questões multidisciplinares
Uma vez biocompatível, a resposta tecidual aos diferentes como características químicas, físicas e comportamento biológico.
biomateriais, pode exibir propriedades como osteocondução, Assim, no presente momento, biomateriais estão sujeitos a normas
osteoindução e osteopromoção. Pioneiro, Urist em 1965, específicas para testes e avaliação.
Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009 73
Panorama atual do uso de xenoenxertos na prática odontológica
Esta interação entre diferentes segmentos da ciência é de REFERÊNCIAS
extrema importância para um maior benefício ao paciente,
desde que, cada biomaterial apresenta algum tipo de limitação 1. Albrektsson T, Johansson C. Osteoinduction, osteoconduction and
e especificidade. Particularmente, os fosfatos de cálcio de origem osseointegration. Eur Spine J. 2001;10(Suppl 2):S96-101.
natural têm se destacado como materiais biocompatíveis capazes 2. American Society for Testing and Materials. F1581: standard
de auxiliar o tecido ósseo e minimizar ou eliminar a necessidade specification for composition of anorganic bone for surgical
de enxerto autógeno em diversos casos. implants. West Conshohocken: The Society; 2008.
Nesta revisão foi possível reunir características acerca dos 3. Calasans-Maia MD, Santos SRA, Rossi AM, Granjeiro JM. In vivo
biomateriais xenogênios, principalmente aqueles de origem behavior of hydroxyapatite evaluated by attenuated total reflection
bovina. Baseado no que foi abordado, concluímos que materiais infrared microscopy (ATR-FTIR). Key Eng Mater. 2009;396:61-4.
osteosubstitutos originados de ossos de animais adequadamente 4. Cestari TM, Granjeiro JM, Assis GF, Garlet GP, Taga R. Bone repair
processados resultam em biomateriais biocompatíveis e and augmentation using block of sintered bovine-derived anorganic
parcialmente absorvíveis, favorecendo a regeneração do defeito bone graft in cranial bone defect model. Clin Oral Implants Res.
ósseo. Além disso, a utilização de materiais de origem bovina 2009; 20(4):340-50.
posiciona o Brasil em lugar de destaque no cenário mundial, uma 5. Conz MB, Granjeiro JM, Soares GA. Physicochemical characterization
vez que detém um dos maiores rebanhos de bovinos do mundo. of six commercial hydroxyapatites for medical-dental applications
as bone graft. J Appl Oral Sci. 2005;13(2):136-40.
6. Daelemans P, Hermans M, Godet F, Malevez C. Autologous bone
graft to augment the maxillary sinus in conjunction with immediate
endosseous implants: a retrospective study up to 5 years. Int J
Periodontics Restorative Dent. 1997;17(1):27-39.
7. Di Stefano DA, Artese L, Iezzi G, Piattelli A, Pagnutti S, Piccirilli M, et
al. Alveolar ridge regeneration with equine spongy bone: a clinical,
histological, and immunohistochemical case series. Clin Implant
Dent Relat Res. 2009;11(2):90-100.
8. Gonçalves F, Granjeiro JM, Cestary TM, Taga R, Oliveira RC, Zanetti
RV, et al. Recuperação de rebordo alveolar com enxerto xenogênico
composto Gen-Tech®. Relato de caso clínico. ImplantNews.
2005;2(5):491-7.
9. Gonçalves F, Hohn A, Granjeiro JM, Silva IIC, Taga R, Cestari TM,
et al. Regeneração óssea em odontologia com a utilização do
substituto ósseo composto xenogênico Gen Mix. ImplantNews.
2009;6(4):373-9.
10. Granjeiro JM, Oliveira RC, Bustos-Valenzuela JC, Sogayar MC, Taga
R. Bone morphogenetic proteins: from structure to clinical use. Braz
J Med Biol Res. 2005;38(10):1463-73.
11. International Organization for Standardization. 10993. Biological
evaluation of medical devices. Part 5: Tests for in vitro cytotoxicity.
Geneve: The Organization; 2009.
12. Jardelino CL, Takamori ER, Santos SRA, Rossi AM, Granjeiro JM.
Biocompatibility of bovine anorganic xenograft. Key Eng Mater.
2009;396-8:3-6.
13. Jovanovic SA, Nevins M. Bone formation utilizing titanium-
reinforced barrier membranes. Int J Periodontics Restorative Dent.
1995;15(1):56-69.
14. Nairne P. Animal to human transplants: the ethics of
xenotransplantation. London: Nuffield Council on Bioethics; 1996.
15. Oliveira RC, Menezes R, Cestari TM, Taga EM, Taga R, Buzalaf MAR,
et al. Tissue response to a membrane of demineralized bovine
cortical bone implanted in the subcutaneous tissue of rats. Braz
Dent J. 2004;15(1):3-8.
16. Oliveira RC, Oliveira FHG, Cestari TM, Taga R, Granjeiro JM.
Morphometric evaluation of the repair of critical-size defects using
demineralized bovine bone and autogenous bone grafts in rat
74 Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009
ARTIGOS CIENTÍFICOS
Castro-Silva II, Zambuzzi WF, Granjeiro JM
calvaria. Clin Oral Implants Res. 2008;19(8):749-54. anorganic bovine bone graft. Braz Dent J. 2006;17(4):274-8.
17. Oliveira RC, Sicca CM, Silva TL, Cestari TM, Kina JR, Oliveira DT, 30. Zambuzzi WF, Oliveira RC, Piozzi R, Cestari TM, Taga R, Buzalaf
et al. Avaliação histológica e bioquímica da resposta celular ao MAR, et al. Avaliação histológica do implante do osso fetal bovino
enxerto de osso cortical bovino previamente submetido a altas acelular e desmineralizado em subcutâneo de ratos. Rev Bras
temperaturas. Efeito da temperatura no preparo de enxerto Ortop. 2006;41(6):227-32.
xenógeno. Rev Bras Ortop. 2003;38(9):551-60.
18. Oliveira RC, Sicca MC, Silva TL, Cestari TM, Oliveira DT, Buzalaf
MAR, et al. Efeito da temperatura de desproteinização no preparo
de osso cortical bovino microgranular: avaliação microscópica e
bioquímica da resposta celular em subcutâneo de ratos. Rev Fac
Odontol Bauru. 1999;7(3/4):85-93.
19. Richardson CR, Mellonig JT, Brunsvold MA, McDonnell HT, Cochran
DL. Clinical evaluation of Bio-Oss®: a bovine-derived xenograft
for the treatment of periodontal osseous defects in humans. J Clin
Periodontol. 1999;26(7):421-8.
20. Rodrigues CV, Serricella P, Linhares AB, Guerdes RM, Borojevic R,
Rossi MA et al. Characterization of a bovine collagen-hydroxyapatite
composite scaffold for bone tissue engineering. Biomaterials.
2003;24(27):4987-97.
21. Sicca CM, Corotti MV, Sgarbosa SHPV, Cestari TM, Cavalcanti
MGP, Ferreira PM, et al. Comparative histomorphometric and
tomographic analysis of maxillary sinus floor augmentation in
rabbits using autografts and xenografts. J Biomed Mater Res B
Appl Biomater. 2008;86(1):188-96.
22. Sicca CM, Oliveira RC, Silva TL, Cestari TM, Oliveira DT, Buzalaf MAR,
et al. Avaliação microscópica e bioquímica da resposta celular a
enxertos de osso cortical bovino em subcutâneo de ratos: efeito do
tamanho da partícula. Rev Fac Odontol Bauru. 2000;8(1/2):1-10.
23. Suckow MA, Voytik-Harbin SL, Terril LA, Badylak SF. Enhanced bone
regeneration using porcine small intestinal submucosa. J Invest
Surg. 1999;12(5):277-87.
24. Taga ML, Granjeiro JM, Cestari TM, Taga R. Healing of critical-size
cranial defects in guinea pigs using a bovine bone-derived resorbable
membrane. Int J Oral Maxillofac Implants. 2008;23(3):427-36.
25. Teixeira CR, Rahal SC, Volpi RS, Taga R, Cestari TM, Granjeiro JM, et
al. Tibial segmental bone defect treated with bone plate and cage
filled with either xenogeneic composite or autologous cortical bone
graft. An experimental study in sheep. Vet Comp Orthop Traumatol.
2007;20(4):269-76.
26. World Health Organization. Report of WHO consultation on
xenotransplantation. WHO, 1997 [cited 2008 Aug 8]. Available from:
http://www.who.int/zoonoses/resources/xenotransplantation/en/
27. Yamatogi RS, Rahal SC, Granjeiro JM, Taga R, Cestari TM, Lima
AFM. Microscopic evaluation of biologic membrane association
from bovine origin implanted subcutaneously in rats. Cienc Rural.
2005;35(4):837-42.
28. Zambuzzi WF, Oliveira RC, Alanis DG, Menezes R, Letra AMG, Cestari
TM, et al. Microscopic analisys of porous microgranular bovine
anorganic bone implanted in rat subcutaneous tissue. J Appl Oral
Sci. 2005;13(4):382-6.
29. Zambuzzi WF, Oliveira RC, Pereira FL, Cestari TM, Taga R, Granjeiro
JM. Rat subcutaneous tissue response to macrogranular porous
Innov Implant J, Biomater Esthet, São Paulo, v. 4, n. 3, p. 70-75, set./dez. 2009 75
Você também pode gostar
- 15323-Texto Do Artigo-60267-2-10-20220701Documento8 páginas15323-Texto Do Artigo-60267-2-10-20220701Marcos SilvaAinda não há avaliações
- 009POR - Uso de Osso Xenógeno em Bloco para Manutenção de Alvéolo Pós-ExtraçãoDocumento8 páginas009POR - Uso de Osso Xenógeno em Bloco para Manutenção de Alvéolo Pós-ExtraçãoMarcela ResendeAinda não há avaliações
- Portfólio 4Documento6 páginasPortfólio 4João Pedro GarciaAinda não há avaliações
- Bio OssDocumento4 páginasBio OssDeyvison MendesAinda não há avaliações
- Articulo GenmixDocumento7 páginasArticulo GenmixOscar Ortiz IntriagoAinda não há avaliações
- BiomateriaisDocumento89 páginasBiomateriaisLetíciaFigueiredoAinda não há avaliações
- BiomateriaisDocumento36 páginasBiomateriaisannaAinda não há avaliações
- Áreas Doadoras de Enxertos ÓsseosDocumento30 páginasÁreas Doadoras de Enxertos ÓsseosDanilo ChequerAinda não há avaliações
- Histologia e Fisiologia Do Enxerto Ósseo Autógeno Revisão de LiteraturaDocumento5 páginasHistologia e Fisiologia Do Enxerto Ósseo Autógeno Revisão de LiteraturaGabriel MuraAinda não há avaliações
- Caracterização Físico-Química de 12 BiomateriaisDocumento6 páginasCaracterização Físico-Química de 12 BiomateriaisRob ColeAinda não há avaliações
- Avaliação Histológica Do Biovidro Particulado Na Reparação de DefeitoDocumento6 páginasAvaliação Histológica Do Biovidro Particulado Na Reparação de DefeitoMofi JairAinda não há avaliações
- Reconstrução Óssea em Cirurgia Ortognática - Enxertos Autógenos Vs Biomateriais - Issn 1678-0817 Qualis b2Documento11 páginasReconstrução Óssea em Cirurgia Ortognática - Enxertos Autógenos Vs Biomateriais - Issn 1678-0817 Qualis b2joseaugusto19901Ainda não há avaliações
- Definicoes PR0TESESDocumento4 páginasDefinicoes PR0TESESEduarda de Macedo SilvaAinda não há avaliações
- 152 Enxerto Sseo Na Reabilitao Dos MaxilaresDocumento11 páginas152 Enxerto Sseo Na Reabilitao Dos MaxilaresDr. Jalisson VicenteAinda não há avaliações
- Biomateriais Aplicados A ImplantodontiaDocumento10 páginasBiomateriais Aplicados A ImplantodontiaCarolina L. Carvalho100% (1)
- The Tissue Bioengineering in Favor of The Rehabilitation of Individuals With Cleft Lip and PalateDocumento6 páginasThe Tissue Bioengineering in Favor of The Rehabilitation of Individuals With Cleft Lip and PalateAuri Paiva89Ainda não há avaliações
- Aumento de Cume Horizontal Com Uma Membrana de Colageno e Uma Combinação de Osso Autogeno ComentDocumento10 páginasAumento de Cume Horizontal Com Uma Membrana de Colageno e Uma Combinação de Osso Autogeno ComentBianca MarcheziAinda não há avaliações
- Prótese FixaDocumento7 páginasPrótese FixaerikysilvaAinda não há avaliações
- Art. 1 Traduzido 01Documento15 páginasArt. 1 Traduzido 01Guilherme MaccariniAinda não há avaliações
- Programa Biologia Ossea - ViolinDocumento8 páginasPrograma Biologia Ossea - ViolinAlcides ManoelAinda não há avaliações
- Regeneracao Ossea Guiada e Suas AplicacoDocumento8 páginasRegeneracao Ossea Guiada e Suas AplicacoramoAinda não há avaliações
- Khoury TraduzidoDocumento11 páginasKhoury TraduzidoTiago CarvalhoAinda não há avaliações
- Membrana Lumina Coat e UnianDocumento108 páginasMembrana Lumina Coat e UnianEVANDRO FRANCO DA ROCHAAinda não há avaliações
- Fixacoes Zigomaticas Utilizando Carga ImediataDocumento8 páginasFixacoes Zigomaticas Utilizando Carga Imediatarebekamotta816Ainda não há avaliações
- ROG Com Uso de Membrana Nao Reabsorvivel Boneheal em Alveolos Pos Exodontia Relato de CasoDocumento7 páginasROG Com Uso de Membrana Nao Reabsorvivel Boneheal em Alveolos Pos Exodontia Relato de CasoFelipeGuzanskyMilaneziAinda não há avaliações
- Nihms-1651723-2 en PTDocumento49 páginasNihms-1651723-2 en PTThiago SoaresAinda não há avaliações
- Artigo Tipos de Implantes e Perda ÓsseaDocumento7 páginasArtigo Tipos de Implantes e Perda ÓsseaEmmanuelVAinda não há avaliações
- Anais Do IX ENNEC, Rev. Cir. Traumatol. Buco-Max-Fac v14.n2, Suplemento 1. ISSN 1808-5210 1Documento257 páginasAnais Do IX ENNEC, Rev. Cir. Traumatol. Buco-Max-Fac v14.n2, Suplemento 1. ISSN 1808-5210 1Caio GonçalvesAinda não há avaliações
- Aula Rog CiospDocumento88 páginasAula Rog CiospAlex Martins AlbaneseAinda não há avaliações
- Banco de Tecido Ósseo Como Alternativa para Enxertia em OdontologiaDocumento41 páginasBanco de Tecido Ósseo Como Alternativa para Enxertia em OdontologiaAlexandre Sant Ana100% (1)
- ARTIGO 12-Enxerto Bovino-Levantamento Asoalho de Seio PDFDocumento5 páginasARTIGO 12-Enxerto Bovino-Levantamento Asoalho de Seio PDFPedro Maria Crizul Barreto100% (1)
- NecroseDocumento6 páginasNecroseMarcela ResendeAinda não há avaliações
- A02v67n4 PDFDocumento6 páginasA02v67n4 PDFDanielaAinda não há avaliações
- HACa e Quitosana PDFDocumento6 páginasHACa e Quitosana PDFGeorge MacêdoAinda não há avaliações
- Biomateriais Aplicados A ImplantodontiaDocumento10 páginasBiomateriais Aplicados A ImplantodontiaSergio S SouzaAinda não há avaliações
- ImplantNewsPerio - International JournalDocumento12 páginasImplantNewsPerio - International JournalMarco TeixeiraAinda não há avaliações
- 1555 4221 1 PBDocumento18 páginas1555 4221 1 PBQuirino NetoAinda não há avaliações
- Aumento Do Rebordo AlveolarDocumento9 páginasAumento Do Rebordo AlveolarTarsila LopesAinda não há avaliações
- Bion N OvationDocumento20 páginasBion N OvationJuan Carlos Ramirez VelezAinda não há avaliações
- Geistlich Alvéolo Pós ExtraçãoDocumento32 páginasGeistlich Alvéolo Pós ExtraçãoFelipe TitoAinda não há avaliações
- Comparação Entre Enxerto Ósseo Autólogo, Homólogo Congelado e Homólogo Liofilizado em Modelo de Cranioplastia em RatosDocumento107 páginasComparação Entre Enxerto Ósseo Autólogo, Homólogo Congelado e Homólogo Liofilizado em Modelo de Cranioplastia em RatosJonathan NevesAinda não há avaliações
- Comparativo de Terapêuticas Utilizando Implantes Curtos e Enxertos Interposicionais em Mandíbula Posterior: Revisão de LiteraturaDocumento41 páginasComparativo de Terapêuticas Utilizando Implantes Curtos e Enxertos Interposicionais em Mandíbula Posterior: Revisão de LiteraturaAndré SilvaAinda não há avaliações
- Enxerto ÓsseoDocumento22 páginasEnxerto ÓsseoRafael NascimentoAinda não há avaliações
- BiomateriaisDocumento22 páginasBiomateriaisRaquel Filgueira de Souza FerreiraAinda não há avaliações
- ENXERTO ÓSSEO AUTÓGENO ProntoDocumento25 páginasENXERTO ÓSSEO AUTÓGENO ProntoFranklin Nascimento100% (1)
- Preservação Alveolar e Instalação Tardia de Implante Dentário: Relato de CasoDocumento8 páginasPreservação Alveolar e Instalação Tardia de Implante Dentário: Relato de Casoaskovazul83Ainda não há avaliações
- BiomateriaisDocumento81 páginasBiomateriaisLuis Aliaga0% (1)
- Mall PosicionadpsDocumento4 páginasMall PosicionadpsXIOMARA YASMITH REYES PALOMINOAinda não há avaliações
- 3 Proteses Orteses BiomateriaisDocumento19 páginas3 Proteses Orteses BiomateriaisRui AbreuAinda não há avaliações
- Utilização Clínica Do Lumina-Porous para Enxerto Ósseo Heterógeno em Seio Maxilar: Estudo Preliminar Com Relato de Dois Casos ClínicosDocumento14 páginasUtilização Clínica Do Lumina-Porous para Enxerto Ósseo Heterógeno em Seio Maxilar: Estudo Preliminar Com Relato de Dois Casos ClínicosDiego SiqueiraAinda não há avaliações
- Prevalência Dos Materiais Utilizados para Osteossíntese de Fraturas Faciais em João Pessoa/PBDocumento5 páginasPrevalência Dos Materiais Utilizados para Osteossíntese de Fraturas Faciais em João Pessoa/PBTalvane SobreiraAinda não há avaliações
- Sistemas de Retenção para OverdenturaDocumento7 páginasSistemas de Retenção para OverdenturaJuliane DeluqueAinda não há avaliações
- Regeneração Tecidual GuiadaDocumento29 páginasRegeneração Tecidual GuiadaAna Flavia Prates FonsecaAinda não há avaliações
- Universidade Federal Do Rio Grande Do Sul Faculdade de VeterináriaDocumento26 páginasUniversidade Federal Do Rio Grande Do Sul Faculdade de Veterináriamilton96rubroAinda não há avaliações
- Utilizacao Da Tecnica de Tunel para Reconstrucao Maxilar Com Osso Homogeno Relato de Caso 1Documento7 páginasUtilizacao Da Tecnica de Tunel para Reconstrucao Maxilar Com Osso Homogeno Relato de Caso 1Jorge Luiz Amorim CarreiroAinda não há avaliações
- REGENERACAO OSSEA GUIADA COM MEMBRANAS NAO ABSORVIveisDocumento20 páginasREGENERACAO OSSEA GUIADA COM MEMBRANAS NAO ABSORVIveisRaquel machadoAinda não há avaliações
- Biomateriais Com Aplicação Na Regeneração ÓsseaDocumento8 páginasBiomateriais Com Aplicação Na Regeneração ÓsseaLeticia VasconcellosAinda não há avaliações
- A Terapia Com Bisfosfonatos E A Osteonecrose Dos MaxilaresNo EverandA Terapia Com Bisfosfonatos E A Osteonecrose Dos MaxilaresAinda não há avaliações
- Reações teciduais frente à movimentação dentária ortodóntica e suas implicações clínicasNo EverandReações teciduais frente à movimentação dentária ortodóntica e suas implicações clínicasEditora PUC MinasAinda não há avaliações
- Comparação das técnicas All-On-Four® e Four-On-Pillars em reabilitação de maxila edêntula atrófica: análise de elementos finitos 2DNo EverandComparação das técnicas All-On-Four® e Four-On-Pillars em reabilitação de maxila edêntula atrófica: análise de elementos finitos 2DAinda não há avaliações
- Aula 1 Introdução À Química AnalíticaDocumento50 páginasAula 1 Introdução À Química AnalíticaFrancine FábregaAinda não há avaliações
- 01 - (Fuvest SP) : 03 - (ESCS DF)Documento22 páginas01 - (Fuvest SP) : 03 - (ESCS DF)Cesar WagnerAinda não há avaliações
- Trabalho ImpermeabilizantesDocumento13 páginasTrabalho Impermeabilizantescaio benficaAinda não há avaliações
- Aula Dens - Óssea Parte IDocumento57 páginasAula Dens - Óssea Parte IJamile Barros50% (2)
- Man Dpc650Documento16 páginasMan Dpc650Pedro Ohana100% (5)
- 1° Lista de Exercícios - Drenagem 2 Semestre - 2018 - Resolvida - 9 e 10Documento4 páginas1° Lista de Exercícios - Drenagem 2 Semestre - 2018 - Resolvida - 9 e 10Mario MachadoAinda não há avaliações
- Filtro Gel Rexroth - BFSKDocumento4 páginasFiltro Gel Rexroth - BFSKFelipe VenturiniAinda não há avaliações
- Natureza Fisica Dos PrecipitadosDocumento19 páginasNatureza Fisica Dos Precipitadoscharmpenelope100% (2)
- Energia Solar FotovoltaicaDocumento11 páginasEnergia Solar FotovoltaicaDiegoAinda não há avaliações
- Buchas PDFDocumento20 páginasBuchas PDFLuiz Gabriel Alves de DeusAinda não há avaliações
- NBR 9574Documento2 páginasNBR 9574Jacqueline AndradeAinda não há avaliações
- Gessos Odontológicos PDFDocumento4 páginasGessos Odontológicos PDFVanessa MarquesAinda não há avaliações
- Atlas de Mineralogia MicroDocumento25 páginasAtlas de Mineralogia MicroMônica de PaulaAinda não há avaliações
- Sarfam BeauplexDocumento0 páginaSarfam BeauplexicraoAinda não há avaliações
- ESTM006-17: Materiais Poliméricos: Universidade Federal Do ABCDocumento51 páginasESTM006-17: Materiais Poliméricos: Universidade Federal Do ABCLaura FerreiraAinda não há avaliações
- Aula 12 Estruturas Isostáticas - Vigas Gerber PDFDocumento11 páginasAula 12 Estruturas Isostáticas - Vigas Gerber PDFDiego Souza0% (1)
- Petro08 008 8Documento13 páginasPetro08 008 8Wellington de MattosAinda não há avaliações
- Conceitos e Classificações de Jazigos MineraisDocumento12 páginasConceitos e Classificações de Jazigos MineraisAnonymous IabqZQ1tkAinda não há avaliações
- Aula 4 - Haletos e Compostos AromáticosDocumento26 páginasAula 4 - Haletos e Compostos AromáticospaulossmateusjrAinda não há avaliações
- Estudo Dirigido III - Proteínas - Estrutura e FunçãoDocumento2 páginasEstudo Dirigido III - Proteínas - Estrutura e FunçãoDaniel MarquesAinda não há avaliações
- Aula 1 Equilibrio Ácido BaseDocumento71 páginasAula 1 Equilibrio Ácido BaseFlávia CastroAinda não há avaliações
- Execícios Resolvidos - RadioatividadeDocumento11 páginasExecícios Resolvidos - RadioatividadeRômulo Barbosa100% (1)
- Água DuraDocumento4 páginasÁgua DuravanS2tutyAinda não há avaliações
- Escoamento Sob PressãoDocumento21 páginasEscoamento Sob PressãoEverton GadelhaAinda não há avaliações
- Quimica OrganicaDocumento4 páginasQuimica OrganicaJacinto FaustinoAinda não há avaliações
- Praguicidas em AlimentosDocumento13 páginasPraguicidas em AlimentosMilanaSilvaAinda não há avaliações
- Primeira Errata Da FB6Documento12 páginasPrimeira Errata Da FB6CAMILA ROBERTA OLIVEIRA DA SILVAAinda não há avaliações
- Fermentação SemicontínuaDocumento4 páginasFermentação SemicontínuaFernando RodriguesAinda não há avaliações
- Steelman Construcao CivilDocumento208 páginasSteelman Construcao CivilLucas Pereira de Jesus0% (2)
- FISPQ - Cloreto de SodioDocumento4 páginasFISPQ - Cloreto de SodioluciaAinda não há avaliações