Escolar Documentos
Profissional Documentos
Cultura Documentos
Novo11Q - (Teste 3 - Mai18)
Enviado por
Isabel Vilhena FerreiraTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Novo11Q - (Teste 3 - Mai18)
Enviado por
Isabel Vilhena FerreiraDireitos autorais:
Formatos disponíveis
Teste 3
Duração: 90 min
NOME ___________________________________________________________ Turma _______ Número _______
Consulte a Tabela Periódica, a tabela de constantes e o formulário sempre que necessário.
Nos itens de escolha múltipla selecione a letra da única opção que permite obter uma afirmação correta
ou que responda corretamente à questão formulada.
Nos itens de construção que envolvam cálculos numéricos é obrigatório apresentar todas as etapas de
resolução.
Junto de cada item, entre parênteses, apresenta-se a respetiva cotação.
GRUPO I
As cloraminas são responsáveis pelo cheiro caraterístico e pelo ardor nos olhos provocado pela água
de piscinas, que são erradamente associados ao excesso de cloro. A sua formação deve-se a reações
entre o cloro, usado como desinfetante, e derivados do amoníaco, proveniente de resíduos
libertados pelos banhistas.
1. A tricloramina, NCℓ3, é uma cloramina cuja formação em meio aquoso pode ser traduzida
simplificadamente pela reação:
NH3 (aq) + 3 Cℓ2 (aq) ⇌ NCℓ3 (aq) + 3 HCℓ (aq)
1.1 (8p) A equação química representa uma reação ... e um equilíbrio químico ...
(A) completa ... homogéneo.
(B) completa ... heterogéneo.
(C) incompleta ... homogéneo.
(D) incompleta ... heterogéneo.
1.2 (8p) Escreva a expressão da constante de equilíbrio para a reação representada.
1.3 (12p) Calcule a massa de cloro, Cℓ2, que deve reagir para que se formem de 0,235 mol de
tricloramina.
2. A cloramina liberta-se da água da piscina para a atmosfera, onde também tem efeitos adversos.
O valor limite de exposição para a cloramina na atmosfera é 1,5 mg/m3.
2.1 (12p) Admita que se libertaram 1,50 g de cloramina, que se acumularam numa camada de ar
com 750 m3 sobre a superfície da piscina. Determine se foi ou não ultrapassado o valor limite
de exposição nesta camada de ar.
Editável e fotocopiável © Texto | Novo 11Q 1
2.2 (8p) A ordem de grandeza do valor limite de exposição para a cloramina, quando expresso em
μg/m3, é
(A) 103.
(B) 106.
(C) 10–3.
(D) 100.
2.3 (12p) Para se acumular junto à superfície da piscina, a cloramina deve ter uma densidade
superior à do ar, que é 1,16 g dm–3, a 27 °C. A essa temperatura o volume molar de um gás é
24,6 dm3 mol–1. Calcule a densidade da cloramina, a 27 °C.
3. A formação da tricloramina representada é uma reação de oxidação-redução.
3.1 (8p) Nesta reação, o cloro, Cℓ2, é
(A) oxidado, pois há aumento do número de oxidação de Cℓ.
(B) oxidado, pois há diminuição do número de oxidação de Cℓ.
(C) reduzido, pois há aumento do número de oxidação de Cℓ.
(D) reduzido, pois há diminuição do número de oxidação de Cℓ.
3.2 (8p) É de esperar que o amoníaco, NH3, seja o agente
(A) oxidante, por sofrer redução.
(B) redutor, por sofrer oxidação.
(C) oxidante, por sofrer oxidação.
(D) redutor, por sofrer redução.
4. Os valores recomendáveis para o pH da água de uma piscina situam-se no intervalo
compreendido entre 7,2 e 7,8. Se o pH for superior ou inferior, deve ser ajustado para que volte a
situar-se dentro deste intervalo.
4.1 (8p) Qual das amostras seguintes ajustará mais facilmente o pH de uma água cujo valor inicial
do pH seja 9?
(A) 1 mol Ca(OH)2
(B) 1 mol H2SO4
(C) 1 mol NaOH
(D) 1 mol HCℓ
2 Editável e fotocopiável © Texto | Novo 11Q
4.2 (8p) Uma água com pH igual a 7,2 tem uma concentração de H3O+ (aq) que é ... vezes ... que a
concentração de H3O+ (aq) numa água com pH igual a 7,8.
(A) 0,6 ... maior
(B) 4 ... menor
(C) 4 ... maior
(D) 0,6 ... menor
GRUPO II
O amoníaco, NH3, é uma matéria-prima amplamente utilizada na indústria para a preparação de
muitas outras substâncias.
Em solução aquosa, o amoníaco (Kb = 1,8 × 10−5) reage com a água, comportando-se como uma base
de Brønsted e Lowry.
1. (8p) Escreva a equação química que traduz a reação referida no texto.
2. Num laboratório existe uma solução aquosa de amoníaco
de concentração desconhecida, armazenada num balão
volumétrico de 100 cm3. Mediu-se o pH da solução a 25 °C,
obtendo-se o valor apresentado na figura.
2.1 (8p) Indique entre que valores está contido o pH da
solução.
2.2 (12p) Determine a concentração de amoníaco presente
na solução referida.
GRUPO III
O ácido clorídrico, HCℓ (aq), formado, por exemplo, durante a síntese da tricloramina oxida com
facilidade uma grande variedade de metais. É importante, por isso, que na indústria se utilizem
reatores e outros equipamentos feitos de materiais adequados, para que estes não sejam
deteriorados por ação do ácido clorídrico.
Para averiguar que metal(ais) poderia(m) ser utilizado(s) no revestimento
interno de um reator onde ocorre a formação de HCℓ (aq), foram
mergulhadas lâminas idênticas de cobre, estanho, níquel, ferro e zinco em
50 cm3 de uma solução de HCℓ (aq), como ilustra a figura.
Editável e fotocopiável © Texto | Novo 11Q 3
A série eletroquímica seguinte apresenta uma lista ordenada de algumas espécies por ordem
crescente de tendência para ceder eletrões.
Pt Au Ag Cu H2 Pb Sn Ni Fe Cr Zn Mn Aℓ Mg Ca Na K
Maior tendência para ceder eletrões
1. (8p) A série eletroquímica apresentada, dispõe as espécies por
(A) ordem crescente de poder oxidante.
(B) ordem crescente de poder redutor.
(C) menor tendência para se oxidarem.
(D) maior tendência para se reduzirem.
2. (12p) Conclua, justificando, qual(ais) dos metais testados pode(m) ser utilizado(s) no revestimento
interno de um reator, de modo a que não seja deteriorado por ação de HCℓ (aq).
3. (8p) Preveja, com base na série eletroquímica apresentada, se ocorrerá uma reação de oxidação-
-redução após a adição de uma solução de
(A) Cr3+ a um prego de ferro.
(B) Mg2+ a um prego de ferro.
(C) Fe2+ a uma lata de zinco.
(D) Zn2+ a um fio de prata.
GRUPO IV
Um modo alternativo de desinfetar a água de piscinas envolve a utilização de sistemas que libertam
iões cobre (II), Cu2+, e prata, Ag+, que asseguram efeitos bactericidas. O cobre tem também a
capacidade de destruir algas. Nestes casos, o teor de iões prata na água pode atingir 0,10 mg/L e o
de ião cobre 2,0 mg/L.
1. (8p) O teor de cobre, quando expresso em partes por milhão (em massa), é
(A) 2,0 × 10−3 ppm.
(B) 2,0 × 103 ppm.
(C) 0,2 ppm.
(D) 2,0 ppm.
4 Editável e fotocopiável © Texto | Novo 11Q
2. (16p) Verifique se há precipitação de cloreto de prata, AgCℓ, caso existam 6,0 kg de ião cloreto,
Cℓ−, uma piscina com 1,0 × 103 m3 de água, a 25 °C.
Ks(AgCℓ, 25 °C) = 1,77 × 10–10 M(Ag+) = 107,87 g mol–1 M(Cℓ–) = 35,45 g mol–1
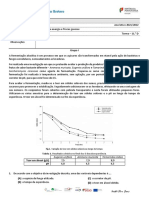
3. (8p) O gráfico abaixo mostra a variação da solubilidade de AgCℓ em soluções aquosas de NaCℓ de
concentração crescente.
Que efeitos podem justificar a diminuição no início, e o aumento no final, da solubilidade de
AgCℓ (s)?
(A) O efeito do ião comum, seguido da formação de iões complexos.
(B) A formação de iões complexos, seguido da acidificação por NaCℓ (aq).
(C) O efeito do ião comum, seguido da acidificação por NaCℓ (aq).
(D) A formação de iões complexos, seguido do efeito do ião comum.
4. (12p) Escreva a equações das semirreações de oxidação que traduzem a formação de Ag + e Cu2+ a
partir dos respetivos metais.
5. (8p) O cobre é um metal com maior poder redutor do que a prata, pelo que
(A) os iões cobre têm maior poder redutor do que os iões prata.
(B) os iões cobre têm menor poder redutor do que os iões prata.
(C) os iões cobre têm menor poder oxidante do que os iões prata.
(D) os iões cobre têm maior poder oxidante do que os iões prata.
Editável e fotocopiável © Texto | Novo 11Q 5
Você também pode gostar
- Novo11Q Critérios Específicos Classificação Teste3 Mai18Documento3 páginasNovo11Q Critérios Específicos Classificação Teste3 Mai18pituchaAinda não há avaliações
- Novo 11Q NL (Teste2 CC) Abr.2019Documento3 páginasNovo 11Q NL (Teste2 CC) Abr.2019Rui SantosAinda não há avaliações
- 1 AL - V de GowinDocumento1 página1 AL - V de Gowinjonysequeira99Ainda não há avaliações
- Queda PDFDocumento10 páginasQueda PDFMarco AlvesAinda não há avaliações
- 02 - Teste - Avaliacao - q10 - d2 - sd1 Ligações QuimicaDocumento5 páginas02 - Teste - Avaliacao - q10 - d2 - sd1 Ligações QuimicaElsa Viana BaptistaAinda não há avaliações
- 4teste - 11º Ano V1-1101 VFFDocumento6 páginas4teste - 11º Ano V1-1101 VFFSofia DiasAinda não há avaliações
- Teste N.º7Documento6 páginasTeste N.º7Tania FernandesAinda não há avaliações
- Aef11 Ques Aulalab 3Documento2 páginasAef11 Ques Aulalab 3Mafalda Nunes100% (1)
- Novo 11Q NL (Teste2) Maio2021Documento7 páginasNovo 11Q NL (Teste2) Maio2021Sofia CarvalhoAinda não há avaliações
- Teste Avaliacao 05Documento3 páginasTeste Avaliacao 05Rita RibeiroAinda não há avaliações
- VERSÃO 1 FICHA DE AVALIAÇÃO DE BIOLOGIA E GEOLOGIA. Ano - 11º Turma - C e D Data - 23 - 02 - 2016. Duração - 100 MINUTOS. Estruturas PedagógicasDocumento11 páginasVERSÃO 1 FICHA DE AVALIAÇÃO DE BIOLOGIA E GEOLOGIA. Ano - 11º Turma - C e D Data - 23 - 02 - 2016. Duração - 100 MINUTOS. Estruturas PedagógicasGuilherme Ramalho100% (1)
- AL - 2.1, 2.2 e 2.3 Química-2Documento3 páginasAL - 2.1, 2.2 e 2.3 Química-2joao sequeira100% (2)
- 5 - Teste Global 2 Jogo Partículas 11º AnoDocumento2 páginas5 - Teste Global 2 Jogo Partículas 11º AnoSérgio MarquesAinda não há avaliações
- Ficha de Revisões 1Documento10 páginasFicha de Revisões 1David Salpico0% (1)
- FT de Preparação Qa Abril 2021Documento22 páginasFT de Preparação Qa Abril 2021ines100% (1)
- Testes Globais Fisica e Quimica 11 PDFDocumento48 páginasTestes Globais Fisica e Quimica 11 PDFNuno TendaAinda não há avaliações
- ProvaModelo BG11Documento17 páginasProvaModelo BG11Ana Santos100% (1)
- Aspetos Quantitativos + CorreçãoDocumento13 páginasAspetos Quantitativos + CorreçãoBeatriz AmorimAinda não há avaliações
- Actividade Laboratorial 2.3Documento4 páginasActividade Laboratorial 2.3Jorge Alves CorreiaAinda não há avaliações
- Questões AlsDocumento8 páginasQuestões AlsInês DominguezAinda não há avaliações
- FT2 Revisões Exercicios Experiencias Obtenção Distribuição Da Matéria PlantasDocumento5 páginasFT2 Revisões Exercicios Experiencias Obtenção Distribuição Da Matéria PlantasPaula Lopes100% (1)
- Teste 3 (2016)Documento4 páginasTeste 3 (2016)anaAinda não há avaliações
- Relatório FQDocumento8 páginasRelatório FQInes FerreiraAinda não há avaliações
- FTUnidade5 PDFDocumento9 páginasFTUnidade5 PDFBruna Sousa100% (1)
- Ae q11 Sol TestesDocumento4 páginasAe q11 Sol TestesNuno TendaAinda não há avaliações
- Areal - Teste 11BG - MAR2022Documento12 páginasAreal - Teste 11BG - MAR2022vfr workAinda não há avaliações
- Eq12 Cad Lab Exploracao Al 1 2Documento7 páginasEq12 Cad Lab Exploracao Al 1 2Alexandra Ribeiro100% (2)
- Enunciado Provamodelo Mai2020Documento5 páginasEnunciado Provamodelo Mai2020capuchinhoguardenseAinda não há avaliações
- Ae Sec bg11 Questaoaula1 Nov2019 CCDocumento1 páginaAe Sec bg11 Questaoaula1 Nov2019 CCJANET PEREIRAAinda não há avaliações
- Ficha de Exercicios Obtenção de Matéria BiologiaDocumento4 páginasFicha de Exercicios Obtenção de Matéria BiologiaPatrícia Tomás0% (1)
- Solução Questão de AulaDocumento3 páginasSolução Questão de AulaSandra AndradeAinda não há avaliações
- Química 12º Ano Unidade 1 APL 1 - Construção de Uma Pilha Com Diferença de Potencial Determinada (1.1 V)Documento10 páginasQuímica 12º Ano Unidade 1 APL 1 - Construção de Uma Pilha Com Diferença de Potencial Determinada (1.1 V)Magda RafaelAinda não há avaliações
- Ficha Trabalho MeioseDocumento3 páginasFicha Trabalho MeioseDulce NevesAinda não há avaliações
- Edicoes ASA - 11 Ano 2019-20 - 4 Teste PDFDocumento9 páginasEdicoes ASA - 11 Ano 2019-20 - 4 Teste PDFrefúgio do saberAinda não há avaliações
- Ficha2 BG11 2122Documento4 páginasFicha2 BG11 2122Clara Gomes100% (1)
- Teste Global - FQ - 11anoDocumento11 páginasTeste Global - FQ - 11anoSandra PintoAinda não há avaliações
- 11F NL (Teste2 CC) - Nov2021Documento3 páginas11F NL (Teste2 CC) - Nov2021diana BaptistaAinda não há avaliações
- FT1 - ENERGIA e FENÓMENOS ELÉTRICOS PDFDocumento6 páginasFT1 - ENERGIA e FENÓMENOS ELÉTRICOS PDFeuniceAinda não há avaliações
- 02 Eq11 Teste Global v1Documento10 páginas02 Eq11 Teste Global v1Elsa Viana BaptistaAinda não há avaliações
- Teste Formativo 1Documento11 páginasTeste Formativo 1Mario LouroAinda não há avaliações
- Mpag11 Ficha Leitura 2Documento4 páginasMpag11 Ficha Leitura 2AntonioAinda não há avaliações
- Observação Ao Microscópio Ótico Composto de LeucócitosDocumento10 páginasObservação Ao Microscópio Ótico Composto de LeucócitosNádia VilãoAinda não há avaliações
- Ae Pal11 Leitura Gram4Documento3 páginasAe Pal11 Leitura Gram4SilviaMariaRocha100% (2)
- 3ºficha Preparação Exames - CorreçãoDocumento25 páginas3ºficha Preparação Exames - CorreçãolaraAinda não há avaliações
- Ficha 1 TeDocumento4 páginasFicha 1 Teaptgaptg100% (1)
- A.P.L. 1.6 Química 12ºDocumento6 páginasA.P.L. 1.6 Química 12ºAna FilipaAinda não há avaliações
- Anexoi Taf Questao-Aula Fotossintese v1 10actDocumento3 páginasAnexoi Taf Questao-Aula Fotossintese v1 10actisamvgm67% (3)
- Apoio Às Atividades LaboratoriaisDocumento5 páginasApoio Às Atividades Laboratoriaisanitadiogo0% (1)
- Teste 1 2019-20 EnviarDocumento8 páginasTeste 1 2019-20 EnviarDulce DiasAinda não há avaliações
- Ae Sec bg10 Teste Maio21Documento10 páginasAe Sec bg10 Teste Maio21Susana Alves100% (2)
- Ficha Formativa BiologiaDocumento6 páginasFicha Formativa BiologiaJoão FaroAinda não há avaliações
- Triplex 11ºano Quimica SolubilidadeDocumento12 páginasTriplex 11ºano Quimica Solubilidadealmeida.agostinho8406100% (1)
- Ae Pal11 Criterios Teste Form1Documento7 páginasAe Pal11 Criterios Teste Form1Nhés SilvaAinda não há avaliações
- Ae Pal11 Leitura Gram1Documento3 páginasAe Pal11 Leitura Gram1Alexandra Vieira100% (1)
- Resolução Dos Testes Sobre As ALDocumento3 páginasResolução Dos Testes Sobre As ALEdite BrandãoAinda não há avaliações
- 11oqui Mica FT Apoio No2Documento4 páginas11oqui Mica FT Apoio No2milenerato224050% (2)
- 11Q NL Teste 3 05 2023Documento4 páginas11Q NL Teste 3 05 2023Sofia OliveiraAinda não há avaliações
- Teste 2 (2017-2018)Documento4 páginasTeste 2 (2017-2018)Rúben Cristiano Teixeira da Silva (a3412)Ainda não há avaliações
- Questão de Aula 3 - Ácido-Base - Titulação e Chuvas ÁcidasDocumento3 páginasQuestão de Aula 3 - Ácido-Base - Titulação e Chuvas ÁcidasPedro CarrolaAinda não há avaliações
- Lista de Exercícios Da Recuperação Final - Professor NagibDocumento5 páginasLista de Exercícios Da Recuperação Final - Professor NagibAlysson da SilvaAinda não há avaliações
- Teste Matematica 5 Ano Tratamento de DadosDocumento3 páginasTeste Matematica 5 Ano Tratamento de DadosIsabel Vilhena FerreiraAinda não há avaliações
- Revisões de Geologia 11º AnoDocumento17 páginasRevisões de Geologia 11º AnoIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Matematica 5 Ano Estatistica2Documento3 páginasFicha Matematica 5 Ano Estatistica2Isabel Vilhena FerreiraAinda não há avaliações
- Ficha Portugues 3 Ano Interpretacao Lua e SolDocumento2 páginasFicha Portugues 3 Ano Interpretacao Lua e SolIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Portugues 3 Ano Interpretacao Queijo Da SerraDocumento2 páginasFicha Portugues 3 Ano Interpretacao Queijo Da SerraIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Geografia 7 Ano Localizacao Relativa Dos LugaresDocumento1 páginaFicha Geografia 7 Ano Localizacao Relativa Dos LugaresIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Portugues 3 Ano Interpretacao A Avo e A NetaDocumento2 páginasFicha Portugues 3 Ano Interpretacao A Avo e A NetaIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Informativa Resumo Geografia 7 Ano o Metodo GeograficoDocumento15 páginasFicha Informativa Resumo Geografia 7 Ano o Metodo GeograficoIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Informativa Resumo Geografia 7 Ano Formas de Representacao Da Terra 1 ParteDocumento8 páginasFicha Informativa Resumo Geografia 7 Ano Formas de Representacao Da Terra 1 ParteIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Informativa Resumo Geografia 7 Ano Tipos de MapasDocumento11 páginasFicha Informativa Resumo Geografia 7 Ano Tipos de MapasIsabel Vilhena FerreiraAinda não há avaliações
- Ficha Informativa Resumo Geografia 7 Ano Categorias Dos PlanetasDocumento12 páginasFicha Informativa Resumo Geografia 7 Ano Categorias Dos PlanetasIsabel Vilhena FerreiraAinda não há avaliações
- Teste HGP 5 Ano Portugal Nos Seculo XVDocumento7 páginasTeste HGP 5 Ano Portugal Nos Seculo XVIsabel Vilhena FerreiraAinda não há avaliações
- Teste Historia 5 Ano Os Romanos Na Peninsula IbericaDocumento5 páginasTeste Historia 5 Ano Os Romanos Na Peninsula IbericaIsabel Vilhena Ferreira100% (2)
- Ficha HGP 5 Ano MuçulmanosDocumento6 páginasFicha HGP 5 Ano MuçulmanosIsabel Vilhena FerreiraAinda não há avaliações
- Despacho 19-07-2022 Abre Vistas Proposta para Próximas Parcelas 0001413-79.2014.5.06.0191 AlusaDocumento4 páginasDespacho 19-07-2022 Abre Vistas Proposta para Próximas Parcelas 0001413-79.2014.5.06.0191 AlusaMarcelo AraujoAinda não há avaliações
- 2º Ano - Planos de EstudosDocumento7 páginas2º Ano - Planos de EstudosLucianeDóroAinda não há avaliações
- Entrevista: Ricardo Darín - Entrevista - PlayboyDocumento8 páginasEntrevista: Ricardo Darín - Entrevista - PlayboyClarIssaAinda não há avaliações
- Manual X Test 2Documento13 páginasManual X Test 2Edson CostaAinda não há avaliações
- Script de Vendas MVC PromotoraDocumento2 páginasScript de Vendas MVC PromotoraMatheus Pongeluppe100% (2)
- Reconstrução Do Trânsito Alimentar Pós GastrectomiaDocumento13 páginasReconstrução Do Trânsito Alimentar Pós GastrectomiaNatalia Yumi YamamotoAinda não há avaliações
- Boletim Da CMF Índice Por Assunto PDFDocumento31 páginasBoletim Da CMF Índice Por Assunto PDFLilianBritoAlvesAinda não há avaliações
- Nit Dicla 16 - 01Documento10 páginasNit Dicla 16 - 01Marcus HugenneyerAinda não há avaliações
- Cantate Domino - Santos e Devoções - 25.10.2020Documento79 páginasCantate Domino - Santos e Devoções - 25.10.2020Guthierri SoaresAinda não há avaliações
- Modelo Receituário Especial para ImpressãoDocumento1 páginaModelo Receituário Especial para ImpressãoLetícia Melo100% (1)
- Movimento Circular UniformeDocumento15 páginasMovimento Circular UniformeMJTours LdaAinda não há avaliações
- LoiyDocumento3 páginasLoiycarlos albertoAinda não há avaliações
- Cox (2009,75-90) Estudos Linguísticos MTDocumento16 páginasCox (2009,75-90) Estudos Linguísticos MTJessyca PachecoAinda não há avaliações
- Aprendendo Assertividade 2Documento2 páginasAprendendo Assertividade 2roseliverissimoAinda não há avaliações
- Apres. WAIS III Avançado CompletoDocumento397 páginasApres. WAIS III Avançado CompletoFrancieli Oratz100% (9)
- Planilha de VendasDocumento53 páginasPlanilha de VendasMateus AraujoAinda não há avaliações
- Medidas TendenciaCentral ExcelDocumento2 páginasMedidas TendenciaCentral ExcelAndré XavierAinda não há avaliações
- BOM - Roteiro 001 (Semana 29 A 05maio)Documento17 páginasBOM - Roteiro 001 (Semana 29 A 05maio)Daniel Braga100% (1)
- OsteotomiasDocumento27 páginasOsteotomiasHeliza GomesAinda não há avaliações
- A Erótica e o FemininoDocumento186 páginasA Erótica e o FemininoMatheus HenriqueAinda não há avaliações
- Itaucard - 4078 - Fatura - 2024-04Documento4 páginasItaucard - 4078 - Fatura - 2024-04EL Gráfica SolutionAinda não há avaliações
- 022 - Leucemia Mieloide Aguda e Crônica Diagnósticos e Possíveis TratamentosDocumento16 páginas022 - Leucemia Mieloide Aguda e Crônica Diagnósticos e Possíveis TratamentosManoel VieiraAinda não há avaliações
- Pavlova Tropical - PanelinhaDocumento8 páginasPavlova Tropical - PanelinhaLeandro MagesteAinda não há avaliações
- Atividades Não Presenciais 3 Ano - 1 A 5 de FevDocumento7 páginasAtividades Não Presenciais 3 Ano - 1 A 5 de FevFabiolla PiresAinda não há avaliações
- Aborto SeminárioDocumento8 páginasAborto SeminárioMikeAinda não há avaliações
- 2268 8062 1 PB PDFDocumento19 páginas2268 8062 1 PB PDFCícero FilhoAinda não há avaliações
- Plano de Curso 2018 - Matemática - Fundamental VDocumento4 páginasPlano de Curso 2018 - Matemática - Fundamental VIsrael Farraz de SouzaAinda não há avaliações
- Formulas Excel ProcvDocumento2 páginasFormulas Excel ProcvTimothy KirbyAinda não há avaliações
- Biologia ForenseDocumento9 páginasBiologia ForenseErillene FurtadoAinda não há avaliações
- Atividade Complementar - 6º Ano - 1º BimestreDocumento19 páginasAtividade Complementar - 6º Ano - 1º BimestreFernanda De Souza Alves De JesusAinda não há avaliações