Escolar Documentos
Profissional Documentos
Cultura Documentos
Módulo de Termoquímica
Enviado por
João Victor0 notas0% acharam este documento útil (0 voto)
9 visualizações2 páginasExercícios resolvidos de termoquímica.
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoExercícios resolvidos de termoquímica.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
9 visualizações2 páginasMódulo de Termoquímica
Enviado por
João VictorExercícios resolvidos de termoquímica.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
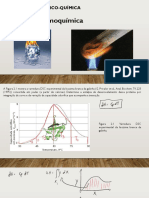
Módulo de Termoquímica 14/06/2021
Reações endotérmicas absorvem energia, enquanto as exotérmicas liberam energia
para o meio ; esse ramo da química estuda as transformações de energia química
em térmica ou vice-versa
Para que uma ligação seja quebrada, ela precisa receber energia. Dessa forma, ela
passará de uma condição de estabilidade para instabilidade após a quebra.
Entalpia nada mais é do que o estado energético de um corpo;
Em reações endotérmicas, a energia final é maior do que a energia inicial, por isso
pode-se dizer que o ∆H é positivo. Por outro lado, nas reações exotérmicas o ∆H é
negativo;
Uma forma de representar reações exotérmicas é através de um ∆H negativo, um
sinal de – ou a formação de energia no produto.
Catalisadores são substâncias que influenciam na velocidade dessas reações
químicas, pois ele ajuda a diminuir a energia necessária para que ela possa
acontecer. Ps: Catalisadores não são consumidos nas reações químicas
Todas as reações de neutralização e de combustão são exotérmicas. Importante
destacar que as reações exotérmicas são favorecidas em baixas temperaturas.
# Quais são os fatores que podem influenciar no cálculo de ∆H ?
1°: Temperatura, pois ela mede a agitação das partículas e, sendo assim, o seu
estado energético.
2°: Quantidade de regentes, pois quanto a quantidade de produtos também vai
aumentar e, consequentemente, haverá uma variação de entalpia.
3°: Estados físicos, já que cada um deles apresenta um grau de agitação diferente
nas moléculas . Do Sólido para o líquido ou do líquido para o gasoso é preciso
absorver energia;
# Como fazer o cálculo do ∆H ?
1 °: Estado alotrópico: Substâncias simples no seu estado alotrópico mais estável
têm menor energia e, por convenção, são considerados iguais a zero no cálculo de
∆H. Ps: Se não estiverem no estado específico, essa regra não pode ser aplicada.
Os mais importantes são o Carbono grafite, o oxigênio gasoso, o enxofre rômbico e
o fósforo vermelho.
2°: ∆H = H(Final) – H(Inicial)
Você também pode gostar
- Princípios da Termodinâmica e suas aplicações biológicasDocumento42 páginasPrincípios da Termodinâmica e suas aplicações biológicasDavid Cesar Rocha100% (1)
- Bioenergética e MetabolismoDocumento31 páginasBioenergética e Metabolismolucia100% (2)
- Reações químicas e equilíbrio dinâmicoDocumento40 páginasReações químicas e equilíbrio dinâmicoMargarida Silva100% (5)
- 5 Bioenergética e FosforilaçãoDocumento15 páginas5 Bioenergética e FosforilaçãoAna SilvaAinda não há avaliações
- TermoquimicaDocumento2 páginasTermoquimicaBicAinda não há avaliações
- Termoquimica: conceitos e equaçõesDocumento3 páginasTermoquimica: conceitos e equaçõeschérieAinda não há avaliações
- Super Intensivo - Química - Parte 2 - Aula 08Documento3 páginasSuper Intensivo - Química - Parte 2 - Aula 08juliasevenluAinda não há avaliações
- 5 - Bioenergética e MetabolismoDocumento5 páginas5 - Bioenergética e MetabolismoFelipe RostirollaAinda não há avaliações
- Aula 1 - ConceitosBaÌ Sicos - BioenergeÌ Tica - TermodinaÌ Mica - CMRL - 2023Documento19 páginasAula 1 - ConceitosBaÌ Sicos - BioenergeÌ Tica - TermodinaÌ Mica - CMRL - 2023xavier.phoneAinda não há avaliações
- Aula 2 - ConceitosBaÌ Sicos - BioenergeÌ Tica - TermodinaÌ Mica - CMRL - 2023Documento17 páginasAula 2 - ConceitosBaÌ Sicos - BioenergeÌ Tica - TermodinaÌ Mica - CMRL - 2023xavier.phoneAinda não há avaliações
- Capítulo 13 - Princípios de BioenergéticaDocumento3 páginasCapítulo 13 - Princípios de BioenergéticaJean Carlos Araujo BrilhanteAinda não há avaliações
- Termoquímica IntroduçãoDocumento28 páginasTermoquímica IntroduçãoleaorsAinda não há avaliações
- A VELOCIDADE DAS REAÇÕES QUÍMICAS: TEORIA DAS COLISÕES E FATORES QUE AFETAMDocumento8 páginasA VELOCIDADE DAS REAÇÕES QUÍMICAS: TEORIA DAS COLISÕES E FATORES QUE AFETAMVitória FreitasAinda não há avaliações
- Reações químicas: entalpia e diagramas de energiaDocumento21 páginasReações químicas: entalpia e diagramas de energiaAluno Ana Carolina Silva CabralAinda não há avaliações
- 1Documento13 páginas1samuelsoaresvasco2020Ainda não há avaliações
- As Transformações Físicas e As Reações Químicas Quase Sempre Estão Envolvidas em Perda Ou Ganho de CalorDocumento2 páginasAs Transformações Físicas e As Reações Químicas Quase Sempre Estão Envolvidas em Perda Ou Ganho de CalorMileny Santos LirançoAinda não há avaliações
- Instituto Federal de RondôniaDocumento7 páginasInstituto Federal de RondôniabrunaAinda não há avaliações
- Termoquímica: calor, entalpia e reações químicasDocumento45 páginasTermoquímica: calor, entalpia e reações químicascesarAinda não há avaliações
- TermoquímicaDocumento1 páginaTermoquímicaSamir LimaAinda não há avaliações
- TERMOQUÍMICADocumento2 páginasTERMOQUÍMICAWuazoAinda não há avaliações
- Termoquímica: conceitos e aplicaçõesDocumento14 páginasTermoquímica: conceitos e aplicaçõesAntonio PortelaAinda não há avaliações
- Termoquímica - Conceito de Entalpia, Calores e Reações, Lei de HessDocumento10 páginasTermoquímica - Conceito de Entalpia, Calores e Reações, Lei de HessLucas SenaAinda não há avaliações
- TermoquímicaDocumento7 páginasTermoquímicaBruno CostaAinda não há avaliações
- TermoquímicaDocumento6 páginasTermoquímicaANA PAULA SILVA DOS ANJOSAinda não há avaliações
- A Lei de Hess Consiste em Calcular As Entalpias de Reações QGDocumento7 páginasA Lei de Hess Consiste em Calcular As Entalpias de Reações QGMércio Emanuel AfonsoAinda não há avaliações
- Termoquímica (1) .PDF - 20231029 - 155415 - 0000Documento14 páginasTermoquímica (1) .PDF - 20231029 - 155415 - 0000Po RathAinda não há avaliações
- Energia Das Reações QuímicasDocumento7 páginasEnergia Das Reações QuímicasluisaAinda não há avaliações
- Aquecimento Química Termoquímica 23 11 2021Documento17 páginasAquecimento Química Termoquímica 23 11 2021Vinicius de OliveiraAinda não há avaliações
- Quím 2 AnoDocumento9 páginasQuím 2 AnoFabio FerreiraAinda não há avaliações
- Termoquímica: Estudo das trocas de calorDocumento18 páginasTermoquímica: Estudo das trocas de calorVaniely SiqueiraAinda não há avaliações
- Questions 1683920145872-TermoquimicaDocumento39 páginasQuestions 1683920145872-TermoquimicaTortruguitaah CascudaAinda não há avaliações
- Apostila de Química III 63.1072Documento45 páginasApostila de Química III 63.1072Richard De Medeiros Castro100% (1)
- Energia de ligação e reações químicasDocumento29 páginasEnergia de ligação e reações químicasAna LoretoAinda não há avaliações
- TermoquímicaDocumento7 páginasTermoquímicaArly maluleque MalulequeAinda não há avaliações
- Processos Exotérmicos e Endotérmicos - EEGuarda - Vs ImpressaoDocumento11 páginasProcessos Exotérmicos e Endotérmicos - EEGuarda - Vs ImpressaoGuaracyara Ribas AugustoAinda não há avaliações
- Aspectos cinéticos e termodinâmicos de reações químicas (ΔGDocumento15 páginasAspectos cinéticos e termodinâmicos de reações químicas (ΔGMjrsantos SantosAinda não há avaliações
- 2 - Ficha Informativa Variacao de Entalpia - Ozono Estratosferico - 10 - FSE - 21.22Documento7 páginas2 - Ficha Informativa Variacao de Entalpia - Ozono Estratosferico - 10 - FSE - 21.22Bia CostaAinda não há avaliações
- Aula 5Documento36 páginasAula 5Thauan GomesAinda não há avaliações
- Termoquímica: Estudo da Energia em ReaçõesDocumento4 páginasTermoquímica: Estudo da Energia em ReaçõesAelsonMelloAinda não há avaliações
- 10ano Q 2 3 1 Energia de Ligacao e Reacoes QuimicasDocumento17 páginas10ano Q 2 3 1 Energia de Ligacao e Reacoes QuimicasJoana SilvaAinda não há avaliações
- Entalpia 1Documento23 páginasEntalpia 1DaviAinda não há avaliações
- Bioenergética em 40Documento8 páginasBioenergética em 40Luisa SantosAinda não há avaliações
- Apostila Termoquimica I GratisDocumento7 páginasApostila Termoquimica I GratisMainara LimaAinda não há avaliações
- Reações químicas: entalpia, energia de ligação e balanço energéticoDocumento16 páginasReações químicas: entalpia, energia de ligação e balanço energéticoNeuza FonsecaAinda não há avaliações
- Av Fisico-QuimicaDocumento5 páginasAv Fisico-Quimicaweshenrik98Ainda não há avaliações
- Termodinâmica e suas leis fundamentaisDocumento12 páginasTermodinâmica e suas leis fundamentaisWaldiney SantosAinda não há avaliações
- Entropia, porque o estado natural de tudo é o caosDocumento14 páginasEntropia, porque o estado natural de tudo é o caosJoao Paulo RochaAinda não há avaliações
- QMC AP Termoquímica Introdução À TermoquímicaDocumento13 páginasQMC AP Termoquímica Introdução À TermoquímicaVitorAinda não há avaliações
- Variação de temperatura em reações químicasDocumento12 páginasVariação de temperatura em reações químicasLucas CAinda não há avaliações
- Teoria da Dissociação EletrolíticaDocumento48 páginasTeoria da Dissociação EletrolíticaThiago CordeiroAinda não há avaliações
- TermoquímicaDocumento10 páginasTermoquímicarpovilsAinda não há avaliações
- Entropia Padrão de Reação: Cálculo e InterpretaçãoDocumento3 páginasEntropia Padrão de Reação: Cálculo e InterpretaçãoLau Martins0% (1)
- Termoquà MicaDocumento42 páginasTermoquà MicaLuiz Fillipe VargasAinda não há avaliações
- 170105 Termo1 Paulo.correia SlidesDocumento28 páginas170105 Termo1 Paulo.correia Slidesranito zacariasAinda não há avaliações
- Introdução À TermoquímicaDocumento6 páginasIntrodução À TermoquímicaJoanna de Paoli100% (1)
- Enem 2018 - Ciências Da Natureza E Suas TecnologiasNo EverandEnem 2018 - Ciências Da Natureza E Suas TecnologiasAinda não há avaliações
- Biofísica para ciências biomédicas – 4ª ediçãoNo EverandBiofísica para ciências biomédicas – 4ª ediçãoAinda não há avaliações
- Tabela RevisãoDocumento3 páginasTabela RevisãoJoão VictorAinda não há avaliações
- 29 Educação FinanceiraDocumento1 página29 Educação FinanceiraJoão VictorAinda não há avaliações
- BIOLOGIADocumento1 páginaBIOLOGIAJoão VictorAinda não há avaliações
- Relatório Manutenção MecânicaDocumento3 páginasRelatório Manutenção MecânicaJoão VictorAinda não há avaliações
- Lista de Exercícios de FísicaDocumento27 páginasLista de Exercícios de FísicaJoão VictorAinda não há avaliações
- REPERTÓRIOSDocumento3 páginasREPERTÓRIOSJoão VictorAinda não há avaliações
- BIOLOGIADocumento1 páginaBIOLOGIAJoão VictorAinda não há avaliações
- Válvulas mecânicas aula 04Documento2 páginasVálvulas mecânicas aula 04João VictorAinda não há avaliações