Escolar Documentos
Profissional Documentos
Cultura Documentos
Formulario Termo Basica 21 1
Enviado por
Moises TovarTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Formulario Termo Basica 21 1
Enviado por
Moises TovarDireitos autorais:
Formatos disponíveis
lOMoARcPSD|23768960
Formulario Termo Básica 21-1
Termodinámica Básica (Instituto Politécnico Nacional)
Studocu no está patrocinado ni avalado por ningún colegio o universidad.
Descargado por Moises Tovar (moisesgabriel79@gmail.com)
lOMoARcPSD|23768960
FORMULARIO TERMO BÁSICA 21-1
𝐹 𝜌𝑥
Presión 𝑃= 𝐹 = 𝑚𝑎 𝑃 = 𝜌ℎ𝑎 𝜌1 ℎ1 = 𝜌2 ℎ2 𝜌𝑟𝑒𝑙 𝑥 =
𝐴 𝜌𝐻2𝑂
𝑉 𝑚 𝑚𝑎 𝑉 𝜋 2 𝑚
Volumen 𝑉𝑚𝑜𝑙𝑎𝑟 = 𝑛= 𝑃𝑒𝑠𝑜𝑒𝑠𝑝 = 𝑉𝑒𝑠𝑝 = 𝐴= ∅ 𝜌=
𝑛 𝑀 𝑉 𝑚 4 𝑉
𝐾
°𝐹 °𝑅 𝑇(𝐾) = (1 ) 𝑡(°𝐶) + 273.15𝐾
Temperatura 𝑡(°𝐹) = (1.8 ) 𝑡(°𝐶) + 32°𝐹 T(°𝑅) = (1.8 ) 𝑇(𝐾) °𝐶
°𝐶 𝐾 °𝑅
𝑇(°𝑅) = (1 ) 𝑡(°𝐹) + 459.67 °𝑅
°𝐹
Gases ideales 𝑃𝑉=𝑛𝑅𝑇 𝑝𝑝𝑎𝑟𝑐𝑖𝑎𝑙 = 𝑦𝑖 𝑃𝑡𝑜𝑡𝑎𝑙 𝑣𝑝𝑎𝑟𝑐𝑖𝑎𝑙 = 𝑦𝑖 𝑉𝑡𝑜𝑡𝑎𝑙
𝑃𝑉 𝑛𝑅𝑇 𝑛𝑅𝑇 𝑃𝑉
𝑛= 𝑃= 𝑉= 𝑇=
𝑅𝑇 𝑉 𝑃 𝑛𝑅
𝑃𝑡𝑜𝑡𝑎𝑙 = ∑ 𝑝𝑝𝑎𝑟𝑐𝑖𝑎𝑙 𝑉𝑡𝑜𝑡𝑎𝑙 = ∑ 𝑣𝑝𝑎𝑟𝑐𝑖𝑎𝑙
𝑓𝑟𝑎𝑐𝑣𝑜𝑙𝑢𝑚𝑒𝑛 =
𝑣𝑖 𝑛𝑖 𝑚𝑖 𝑚𝑖
𝑉𝑡𝑜𝑡𝑎𝑙 𝑦𝑖 = = 𝑓𝑟𝑎𝑐𝑣𝑜𝑙𝑢𝑚𝑒𝑛 𝑥𝑖 = % 𝑥𝑖 = × 100
𝑛𝑡 𝑚𝑡𝑜𝑡𝑎𝑙 𝑚𝑡𝑜𝑡𝑎𝑙
𝑛𝑖 𝑚𝑡𝑜𝑡𝑎𝑙
% 𝑦𝑖 = × 100 𝑀𝑝𝑟𝑜𝑚 = ∑ 𝑦𝑖 𝑀𝑖 𝑀𝑝𝑟𝑜𝑚 =
𝑛𝑡 𝑛𝑡
Primera ley
𝑄 + 𝑊 = ∆𝑈 𝐻 = 𝑈 + 𝑃𝑉(𝑓𝑐) 𝑄𝑝 = ∆𝐻 = ∫ 𝑛𝐶𝑝𝑑𝑡
𝐶𝑝
𝐶𝑝 − 𝐶𝑣 = 𝑅 =𝛾 𝑄𝑣 = ∆𝑈 = ∫ 𝑛𝐶𝑣𝑑𝑡 𝑊 = − ∫ 𝑃𝑑𝑉
𝐶𝑣
Datos PVT para 𝑃𝑖 𝑉𝑖 𝑃𝑓 𝑉𝑓 𝛿
𝑃𝑖 𝑉𝑖 = 𝑃𝑓 𝑉𝑓 𝛿
𝑉𝑓 𝛿
procesos = 𝑃𝑖 = 𝑃𝑓 ( )
𝑇𝑖 𝑇𝑓 𝑉𝑖
1
𝑉𝑓 𝛿−1
1
𝑃𝑓 𝛿 𝑇𝑖 = 𝑇𝑓 ( ) 𝑇𝑖 𝛿−1
𝑉𝑖 = 𝑉𝑓 ( ) 𝑉𝑖 𝑉𝑓 = 𝑉𝑖 ( )
𝑃𝑖 𝑇𝑓
𝛿
𝑃
1−𝛿
𝑇𝑓 1−𝛿 𝑙𝑛 ( 𝑖 )
𝑃𝑖 𝛿
𝑃𝑖 = 𝑃𝑓 ( ) 𝑃𝑓
𝑇𝑓 = 𝑇𝑖 ( ) 𝑇𝑖 𝛿= 𝑉𝑓
𝑃𝑓 𝑙𝑛 ( )
𝑉𝑖
Proceso Isobárico Isotérmico Isocórico Adiabático politrópico
𝑉𝑖 𝑉𝑓 𝑃𝑖 𝑃𝑓 𝛾 𝛾
𝑇𝑖
= 𝑐𝑡𝑒 =
𝑇𝑓
𝑃𝑖 𝑉𝑖 = 𝑐𝑡𝑒 = 𝑃𝑓 𝑉𝑓 = 𝑐𝑡𝑒 = 𝑃𝑖 𝑉𝑖 = 𝑐𝑡𝑒 = 𝑃𝑓 𝑉𝑓 𝑃𝑖 𝑉𝑖 𝛿 = 𝑐𝑡𝑒 = 𝑃𝑓 𝑉𝑓 𝛿
𝑇𝑖 𝑇𝑓
∆U 𝑛𝐶𝑣(𝑇𝑓 − 𝑇𝑖 )
𝑛𝐶𝑝(𝑇𝑓 − 𝑇𝑖 )
∆H
𝐵 𝐶 𝐷 1 1
∆𝐻 = 𝑛𝑅 [𝐴 (𝑇2 − 𝑇1 ) + (𝑇 2 − 𝑇1 2 ) + (𝑇2 3 − 𝑇1 3 ) + ( − )]
2 2 3 −1 𝑇2 𝑇1
𝑇𝑓 𝑛𝑅 𝑇𝑓
+ 𝑙𝑛 𝑛𝐶𝑣𝑙𝑛
𝑇𝑖 1 − 𝛿 𝑇𝑖
𝑇𝑓 𝑉𝑓 𝑇𝑓 𝑇𝑓 𝑉𝑓
𝑛𝐶𝑝𝑙𝑛 𝑛𝑅𝑙𝑛 𝑛𝐶𝑣𝑙𝑛 0 𝑛𝐶𝑣𝑙𝑛 + 𝑛𝑅𝑙𝑛
𝑇𝑖 𝑉𝑖 𝑇𝑖 𝑇𝑖 𝑣𝑖
∆S 𝑇𝑓 𝑃𝑖
𝑛𝐶𝑝𝑙𝑛 + 𝑛𝑅𝑙𝑛
𝑇𝑖 𝑃𝑓
𝑇2 𝐶 2 2 𝐷 1 1 𝑃𝑖
∆𝑆 = 𝑛𝑅 [𝐴 𝑙𝑛 + 𝐵 (𝑇2 − 𝑇1 ) + (𝑇2 − 𝑇1 ) + ( − )] + 𝑛𝑅𝑙𝑛
𝑇1 2 −2 𝑇22 𝑇12 𝑃𝑓
Q ∆H -W ∆𝑈 0 ∆𝑈 − 𝑊
W 𝑉𝑓 𝑛 𝑅 (𝑇𝑓 − 𝑇𝑖 )
∆𝑈 − 𝑄 −𝑛𝑅𝑇𝑙𝑛 0 ∆𝑈 −
𝑉𝑖 1−𝛿
Segunda Ley 𝛿𝑄𝑟𝑒𝑣 𝑊𝑇𝑜𝑡𝑎𝑙 𝑝𝑟𝑜𝑑𝑢𝑐𝑖𝑑𝑜 𝑄𝐵 𝑇𝐵
∆𝑆 = ∫ 𝜂 = 𝜂 = 1 − 𝜂𝑚𝑎𝑞.𝑟𝑒𝑣. = 1−
𝑇 𝑄𝑠𝑢𝑚𝑖𝑛𝑖𝑠𝑡𝑟𝑎𝑑𝑜 𝑄𝐴 𝑇𝐴
1 1
𝑄𝐴 𝑇𝐵 𝑄𝑠𝑢𝑚𝑖𝑛𝑖𝑠𝑡𝑟𝑎𝑑𝑜 𝛽 = 𝑄𝐴 𝛽𝑚𝑎𝑞.𝑟𝑒𝑣. = 𝑇𝐴
= QA= w + QB 𝛽= −1 −1
𝑄𝐵 𝑇𝐴 𝑊𝑐𝑜𝑛𝑠𝑢𝑚𝑖𝑑𝑜 𝑄𝐵 𝑇𝐵
Termoquímica
∆𝐻 0 𝑅 = ∑ ∆𝐻 0 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜𝑠 − ∑ ∆𝐻 0 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑟𝑒𝑎𝑐𝑡𝑖𝑣𝑜𝑠 ∆𝐻𝑅 = ∆𝐻𝑟𝑒𝑎𝑐𝑡𝑖𝑣𝑜𝑠 + ∆𝐻 0 𝑅 + ∆𝐻𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜𝑠
𝑇 298 𝑇𝑓𝑖𝑛𝑎𝑙
∆𝐻𝑅 = ∆𝐻 0 𝑅 + ∫ ∑ ∆𝑛 𝐶𝑝 𝑑𝑇 ∆𝐻𝑟𝑒𝑎𝑐𝑡𝑖𝑣𝑜𝑠 = ∫ 𝑛𝐶𝑝𝑑𝑇𝑟𝑒𝑎𝑐𝑡. ∆𝐻𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜𝑠 = ∫ 𝑛𝐶𝑝𝑑𝑇𝑝𝑟𝑜𝑑.
298 𝑇𝑖𝑛𝑖𝑐𝑖𝑎𝑙 298
∆𝑆 0 𝑅 = ∑ 𝑛𝑆 0 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜𝑠 − ∑ 𝑛𝑆 0 𝑟𝑒𝑎𝑐𝑡𝑖𝑣𝑜𝑠 ∆𝐺 0 = ∆𝐻 0 𝑅 − 𝑇∆𝑆 0 𝑅 ∆𝑈𝑅 = ∆𝐻 0 𝑅 − ∆𝑛𝑔 𝑅 𝑇 ∆𝑛𝑔 = ∑ 𝑛𝑔𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜𝑠 − ∑ 𝑛𝑔𝑟𝑒𝑎𝑐𝑡𝑖𝑣𝑜𝑠
Descargado por Moises Tovar (moisesgabriel79@gmail.com)
Você também pode gostar
- Formulario Termo Basica 21 1Documento2 páginasFormulario Termo Basica 21 1Daniela NajeraAinda não há avaliações
- Teste 1 12ºfísica V1 17 Out 2019Documento9 páginasTeste 1 12ºfísica V1 17 Out 2019Edite BrandãoAinda não há avaliações
- $R5IAQZBDocumento42 páginas$R5IAQZBLARISSA EVANIELE MIRANDAAinda não há avaliações
- Aula 2 - Solução Ideal e Grandezas de MisturaDocumento10 páginasAula 2 - Solução Ideal e Grandezas de MisturaLarissa MeneghiniAinda não há avaliações
- Formulas Fisica Eletrica 3Documento1 páginaFormulas Fisica Eletrica 3Black MageAinda não há avaliações
- Lista de Exercícios TermodinâmicaDocumento2 páginasLista de Exercícios TermodinâmicaLeonardoAinda não há avaliações
- Resumo 10 - AlgebraDocumento2 páginasResumo 10 - AlgebraInêsAinda não há avaliações
- Areas y VolumenesDocumento1 páginaAreas y VolumenesMARCELO BUSTILLOSAinda não há avaliações
- Aula 10 - Geometria Básica I - Professor (Respostas)Documento5 páginasAula 10 - Geometria Básica I - Professor (Respostas)Isabela BelchiolAinda não há avaliações
- Aula 2 - 17outDocumento10 páginasAula 2 - 17outLaura Cristina BairrosAinda não há avaliações
- Formulário Mecânica Dos SolosDocumento2 páginasFormulário Mecânica Dos Solosemerson senna0% (1)
- Resumo P.G.Documento1 páginaResumo P.G.Carolina RodriguesAinda não há avaliações
- FormularioDocumento2 páginasFormularioAndrew HernandezAinda não há avaliações
- Formulário EpidemiologiaDocumento2 páginasFormulário EpidemiologiaRinelly PazinatoAinda não há avaliações
- Aula05 GEO003 ExemplosIndicesfisicosDocumento15 páginasAula05 GEO003 ExemplosIndicesfisicosPedro BrandãoAinda não há avaliações
- Formulário e Tabelas - Hidráulica AplicadaDocumento6 páginasFormulário e Tabelas - Hidráulica AplicadaPaula CostaAinda não há avaliações
- Formulário TermodinâmicaDocumento2 páginasFormulário TermodinâmicaKalopsia SwevenAinda não há avaliações
- Formulário Fisica12 PDFDocumento2 páginasFormulário Fisica12 PDFRafael FariaAinda não há avaliações
- Atividade+Processual+01 - Opt01 (1) (1) (Recuperação Automática)Documento9 páginasAtividade+Processual+01 - Opt01 (1) (1) (Recuperação Automática)Gustavo MirandaAinda não há avaliações
- Formulario Física 2 DR Basurto Sin UNidadesDocumento4 páginasFormulario Física 2 DR Basurto Sin UNidadesnatalia hernandez moyaAinda não há avaliações
- ATV3Documento7 páginasATV3Izah GarciaAinda não há avaliações
- Resumo 9 Ano - TrigoDocumento1 páginaResumo 9 Ano - TrigoInêsAinda não há avaliações
- DDDDDocumento8 páginasDDDDobrasAinda não há avaliações
- TransmissaoDocumento5 páginasTransmissaoEstevao Francisco Da SilvaAinda não há avaliações
- Prova 1 - Mecânica Dos Fluidos I - 20212-1Documento3 páginasProva 1 - Mecânica Dos Fluidos I - 20212-1Josiliane OliveiraAinda não há avaliações
- Formulario FQ 10Documento2 páginasFormulario FQ 10Andrew HernandezAinda não há avaliações
- Aula 10 20 10 2021Documento20 páginasAula 10 20 10 2021DenisAlexandreAinda não há avaliações
- Formulario P2Documento1 páginaFormulario P2d2020002552Ainda não há avaliações
- Matemática 10º Ano Resumo Radicais - Prof - Mónica PintoDocumento1 páginaMatemática 10º Ano Resumo Radicais - Prof - Mónica PintoJoana santosAinda não há avaliações
- Cinemática - Velocidade MédiaDocumento1 páginaCinemática - Velocidade MédiaMauricio CebolinhaAinda não há avaliações
- Aula 23 ENG 4281 C01 - 2020.1Documento18 páginasAula 23 ENG 4281 C01 - 2020.1EmperorTwiceAinda não há avaliações
- Atividade+Processual+01 - Opt01 (1) (1) (Recuperação Automática)Documento9 páginasAtividade+Processual+01 - Opt01 (1) (1) (Recuperação Automática)Gustavo MirandaAinda não há avaliações
- Memorial de Cálculo EngrenagensDocumento18 páginasMemorial de Cálculo EngrenagenskarlloshenryqueberaldoAinda não há avaliações
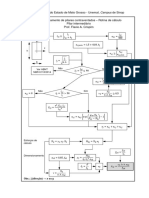
- Fluxograma - Rotina de Cálculo para Pilares ContraventadosDocumento3 páginasFluxograma - Rotina de Cálculo para Pilares ContraventadosEmília GarcezAinda não há avaliações
- UFABC - Mecânica Clássica II - Resolução de Lista de Exercícios 4Documento37 páginasUFABC - Mecânica Clássica II - Resolução de Lista de Exercícios 4xTeoxAinda não há avaliações
- Termodinâmica - Versão CompactaDocumento12 páginasTermodinâmica - Versão CompactaVictor Oliveira NunesAinda não há avaliações
- Aula 12 - Geometria AnalíticaDocumento21 páginasAula 12 - Geometria AnalíticaDavi PedradaAinda não há avaliações
- Aula 7 22 09 2021Documento29 páginasAula 7 22 09 2021DenisAlexandreAinda não há avaliações
- Lista de Exercícios 2ºsem de 2021 - Ex 04Documento2 páginasLista de Exercícios 2ºsem de 2021 - Ex 04ViníciusAinda não há avaliações
- 2 - Tábuas de ComutaçãoDocumento33 páginas2 - Tábuas de ComutaçãoRaphael TenorioAinda não há avaliações
- Formulário Exercicios 02 Maquinas IDocumento2 páginasFormulário Exercicios 02 Maquinas IChristian PaulAinda não há avaliações
- Aplicação Pratica Biomecânica - Projéteis e Aceleração UniformeDocumento13 páginasAplicação Pratica Biomecânica - Projéteis e Aceleração UniformeGabriel LopesAinda não há avaliações
- 1 Prova de Mecânica Dos Fluidos - Eng Mecânica - CE - Noite - Tipo 03Documento5 páginas1 Prova de Mecânica Dos Fluidos - Eng Mecânica - CE - Noite - Tipo 03Pct kblosoAinda não há avaliações
- Ma2020prob123 PDFDocumento138 páginasMa2020prob123 PDFTanaquil SorbitolAinda não há avaliações
- CMM Formulário 2 Teste PDFDocumento2 páginasCMM Formulário 2 Teste PDFRicardo CarvalhoAinda não há avaliações
- Motores A CombustaoDocumento6 páginasMotores A CombustaoGustavo MirandaAinda não há avaliações
- Rectificadores de Media OndaDocumento4 páginasRectificadores de Media OndaAldair BallesterosAinda não há avaliações
- Aula 24 ENG 4281 C01 - 2020.1Documento13 páginasAula 24 ENG 4281 C01 - 2020.1EmperorTwiceAinda não há avaliações
- Aula 4 01 09 21Documento28 páginasAula 4 01 09 21DenisAlexandreAinda não há avaliações
- Aula 26 ENG 4281 C01 - 2020.1Documento22 páginasAula 26 ENG 4281 C01 - 2020.1EmperorTwiceAinda não há avaliações
- MEC2240 Teoria Da Elasticidade RevAlgDocumento14 páginasMEC2240 Teoria Da Elasticidade RevAlgThiago RPGAinda não há avaliações
- Sub 2020-2Documento3 páginasSub 2020-2Eduardo OliveiraAinda não há avaliações
- Aula 02 FTEIVDocumento16 páginasAula 02 FTEIVCristiano FernandesAinda não há avaliações
- TRABALHO Máquinas de Fluxo DEPDocumento6 páginasTRABALHO Máquinas de Fluxo DEPGustavo MirandaAinda não há avaliações
- Aula 8 24 03 2021Documento35 páginasAula 8 24 03 2021DenisAlexandreAinda não há avaliações
- Geometria Analítica e Álgebra Linear - RevisãoDocumento8 páginasGeometria Analítica e Álgebra Linear - RevisãoRafael PinheiroAinda não há avaliações
- Aula 4 Titulometria de Neutralização QUI094 2012.2Documento32 páginasAula 4 Titulometria de Neutralização QUI094 2012.2NAYARA DA SILVA PANTOJAAinda não há avaliações
- Telhas 16 10 2018Documento8 páginasTelhas 16 10 2018Marcelo AlvesAinda não há avaliações
- Indicador de Degradação Do Papel Kraft de TransformadoresDocumento10 páginasIndicador de Degradação Do Papel Kraft de TransformadoresMat MaxAinda não há avaliações
- (Apostila) Tratamento de Efluentes Industriais - PUCDocumento111 páginas(Apostila) Tratamento de Efluentes Industriais - PUCEduardo BandeiraAinda não há avaliações
- UFSC - Relatório Pilhas (Turma A)Documento5 páginasUFSC - Relatório Pilhas (Turma A)Leslie WhiteAinda não há avaliações
- Manual - Química Mineral Parte 1Documento9 páginasManual - Química Mineral Parte 1Joana Isabel Xavier FerreiraAinda não há avaliações
- Refrigeracao-E Ar Condicionado CiclosDocumento79 páginasRefrigeracao-E Ar Condicionado CiclosFilho D OxossiAinda não há avaliações
- Materia Kelas 2Documento35 páginasMateria Kelas 2Jose D CostaAinda não há avaliações
- Calor e Sua PropagaçãoDocumento27 páginasCalor e Sua PropagaçãoMarcos MacedoAinda não há avaliações
- Lista 8 - Termodinamica IIDocumento2 páginasLista 8 - Termodinamica IILucas RenanAinda não há avaliações
- 02 Quimica Aula 22 04Documento6 páginas02 Quimica Aula 22 04juliocezarfranciscomartinsinfaAinda não há avaliações
- Catalogo Tratamiento Schulz C&EDocumento11 páginasCatalogo Tratamiento Schulz C&EEber.CVAinda não há avaliações
- Experiências de Física Sobre ConvecçãoDocumento4 páginasExperiências de Física Sobre Convecçãojoao gabrielAinda não há avaliações
- Prática 10Documento12 páginasPrática 10Maria Luiza de Abreu Alves100% (1)
- DesengraxanteDocumento14 páginasDesengraxanteJaqueline GontijoAinda não há avaliações
- Manual de Instalação 8890 Com PAL 3 - SSP TO - 310943901Documento8 páginasManual de Instalação 8890 Com PAL 3 - SSP TO - 310943901Pedro Fernando Veloso dos PassosAinda não há avaliações
- Secagem Aula02Documento19 páginasSecagem Aula02Elmo Sena JúniorAinda não há avaliações
- 183386transferência de Calor em Superfícies EstendidasDocumento13 páginas183386transferência de Calor em Superfícies EstendidasElimar Russi FilhoAinda não há avaliações
- Fispq346 - 000 RiodineDocumento7 páginasFispq346 - 000 RiodinemarielsonAinda não há avaliações
- Ficha de Ciencias 5º Ano Agua PDFDocumento5 páginasFicha de Ciencias 5º Ano Agua PDFAna Pires100% (1)
- Física - Óptica - IDocumento9 páginasFísica - Óptica - IFísica Caderno de ResoluçõesAinda não há avaliações
- Rev. K 12 / 2012: ProcedimentoDocumento9 páginasRev. K 12 / 2012: ProcedimentodicintraAinda não há avaliações
- Carta Psicrometrica Temp. ElevadasDocumento18 páginasCarta Psicrometrica Temp. ElevadasBernardo HuykeAinda não há avaliações
- 15 Dedini 31 PDFDocumento43 páginas15 Dedini 31 PDFMarcio SilvaAinda não há avaliações
- Simuladores HYSYS Exercícios e GuiaDocumento4 páginasSimuladores HYSYS Exercícios e GuiaLarissa PinheiroAinda não há avaliações
- Resumo Aula TeóricaDocumento6 páginasResumo Aula TeóricaPhellipe AraujoAinda não há avaliações
- Exercícios-Propriedades Gerais Da Matéria.Documento5 páginasExercícios-Propriedades Gerais Da Matéria.Luana TrevizanAinda não há avaliações
- Catalogo Parker Valvulas ExpansaoDocumento56 páginasCatalogo Parker Valvulas Expansaotdrltda0% (1)
- Isolamentos TérmicosDocumento59 páginasIsolamentos TérmicosPedro Malheiro100% (1)
- Exercícios Mecânica Dos Fluidos Com RespostasDocumento10 páginasExercícios Mecânica Dos Fluidos Com RespostasPâmela TrindadeAinda não há avaliações
- Mãos de Luz: Um Guia Para a Cura Através do Campo de Energia HumanoNo EverandMãos de Luz: Um Guia Para a Cura Através do Campo de Energia HumanoNota: 4 de 5 estrelas4/5 (5)
- Sincronicidade e entrelaçamento quântico. Campos de força. Não-localidade. Percepções extra-sensoriais. As surpreendentes propriedades da física quântica.No EverandSincronicidade e entrelaçamento quântico. Campos de força. Não-localidade. Percepções extra-sensoriais. As surpreendentes propriedades da física quântica.Nota: 5 de 5 estrelas5/5 (5)
- Introdução Às Redes De Computadores: Modelos Osi E Tcp/ipNo EverandIntrodução Às Redes De Computadores: Modelos Osi E Tcp/ipAinda não há avaliações
- Fitoenergética: A Energia das Plantas no Equilíbrio da AlmaNo EverandFitoenergética: A Energia das Plantas no Equilíbrio da AlmaNota: 5 de 5 estrelas5/5 (17)
- Segurança Da Informação DescomplicadaNo EverandSegurança Da Informação DescomplicadaAinda não há avaliações
- Raciocínio lógico e matemática para concursos: Manual completoNo EverandRaciocínio lógico e matemática para concursos: Manual completoNota: 5 de 5 estrelas5/5 (1)
- NIKOLA TESLA: Minhas Invenções - AutobiografiaNo EverandNIKOLA TESLA: Minhas Invenções - AutobiografiaNota: 4.5 de 5 estrelas4.5/5 (15)
- Como passar concursos CEBRASPE -Raciocínio Lógico, Matemática e InformáticaNo EverandComo passar concursos CEBRASPE -Raciocínio Lógico, Matemática e InformáticaAinda não há avaliações
- Simetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaNo EverandSimetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaAinda não há avaliações
- Fundamentos de Cinemática e Dinâmica de MecanismosNo EverandFundamentos de Cinemática e Dinâmica de MecanismosAinda não há avaliações
- Contabilidade Geral Para O Exame De SuficiênciaNo EverandContabilidade Geral Para O Exame De SuficiênciaAinda não há avaliações
- Redes De Computadores DescomplicadasNo EverandRedes De Computadores DescomplicadasAinda não há avaliações