Escolar Documentos
Profissional Documentos
Cultura Documentos
Resumo Completo de MRU (CSA)
Enviado por
PDR1000 0Descrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Resumo Completo de MRU (CSA)
Enviado por
PDR1000 0Direitos autorais:
Formatos disponíveis
RESOLUÇÃO COMENTADA
PROVA DE QUÍMICA - A1 15/03/2023
Professora: Luana Agostinho 3ª Série Valor: 4,0
(1,0)
01. LEIA o texto e OBSERVE a imagem a seguir:
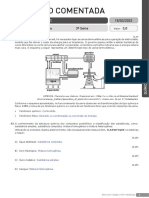
O experimento de Lavoisuer
Lavoisier aqueceu o mercúrio metálico numa retorta com a boca dentro de uma redoma contendo ar e mergulhada
numa cuba com mercúrio. Depois do aquecimento, o volume do ar na retorta diminuiu, pois o volume do mercúrio
na cuba subiu pela redoma. Isso significa que o mercúrio reagiu com “algo” no ar, que hoje sabemos que é o
oxigênio. O produto formado foi o óxido de mercúrio II, um pó vermelho que aderiu às paredes da retorta.
QUÍMICA
Sabendo-se que 20 g de mercúrio necessitam de 1,6 g de gás oxigênio para formar óxido de mercúrio, ao usar
10 g de mercúrio e 1,0 g de gás oxigênio, após a reação tem-se qual massa de óxido de mercúrio?
10,8 g.
(1,0)
02. Muitos fenômenos podem ser explicados por um ou mais modelos atômicos. Porém, determinado modelo é
sempre o primeiro a explicar este ou aquele fenômeno.
Considere os seguintes fenômenos:
I. A existência de carga positiva e massa no núcleo atômico dos átomos.
II. A combinação entre átomos de diferentes elementos, formando compostos.
III. O fato de tomar choque ao se colocar o dedo numa tomada em funcionamento.
IV. A mudança de cor da chama no teste de chama.
INDIQUE o modelo – Dalton, Thomson, Rutherford ou Bohr – que primeiro explicou cada fenômeno.
I. Rutherford.
II. Dalton.
III. Thomson.
IV. Bohr.
Bernoulli Colégio e Pré-Vestibular 1
3ª Série Química
(1,0)
03. Em 1911, o químico e físico neozelandês Ernest Rutherford realizou uma experiência para verificar se os
átomos eram maciços, bombardeando uma fina lâmina de ouro com pequenas partículas de carga positivas,
denominadas partículas alfa, emitidas por um material radioativo proveniente do polônio.
Ele observou que a maior parte dessas partículas atravessava a lâmina, algumas retrocediam e outras eram desviadas.
DESCREVA as conclusões de Rutherford a respeito dos resultados da experiência.
O átomo possui imenso espaço vazio, e a sua massa e carga positiva estão concentradas numa pequena
região chamada núcleo.
(1,0)
04. São dadas as seguintes informações relativas aos átomos hipotéticos X, Y e W:
• O átomo Y tem número atômico 46, número de massa 127 e é isótono de W.
• O átomo X é isótopo de W e possui número de massa igual a 130.
• O número de massa de W é 128.
DETERMINE o número atômico de X.
47.
2 Bernoulli Colégio e Pré-Vestibular
Você também pode gostar
- Análise Gravimétrica de NíquelDocumento5 páginasAnálise Gravimétrica de NíquelAssíria MariaAinda não há avaliações
- Atividade Prática - Química Geral UninterDocumento6 páginasAtividade Prática - Química Geral UninterAna Leticya Gomes100% (1)
- Relatório I, Teste Da Chama PDFDocumento4 páginasRelatório I, Teste Da Chama PDFAlex CarvalhoAinda não há avaliações
- Banco de Questoes. 06Documento9 páginasBanco de Questoes. 06Mundo_da_QuimicaAinda não há avaliações
- 1° Lista Química GeralDocumento4 páginas1° Lista Química GeralDara SavioAinda não há avaliações
- Modelos AtômicosDocumento40 páginasModelos Atômicosluccasgabriel087Ainda não há avaliações
- Livro Didático 1 Física em RadiologiaDocumento30 páginasLivro Didático 1 Física em Radiologia「Derik」 AMVAinda não há avaliações
- Lista 1 Ano PDFDocumento3 páginasLista 1 Ano PDFVitoria De Oliveira Do Nascimento GoncalvesAinda não há avaliações
- Estutura Atmica Parte 1 PDFDocumento32 páginasEstutura Atmica Parte 1 PDFJoão LucasAinda não há avaliações
- Estrutura AtômicaDocumento42 páginasEstrutura Atômicasz.kayooAinda não há avaliações
- Resumo Modelo AtômicoDocumento4 páginasResumo Modelo AtômicoGustavo DalPaiAinda não há avaliações
- Quim01 Livro PropostosDocumento136 páginasQuim01 Livro PropostosRamalde SantanaAinda não há avaliações
- PECN - Modelos AtômicosDocumento2 páginasPECN - Modelos AtômicosTamiris AssisAinda não há avaliações
- Trabalho de QuímicaDocumento8 páginasTrabalho de QuímicaMário Gabriel fausto100% (1)
- Quim01 Livro PropostosDocumento136 páginasQuim01 Livro PropostosValdeir AntonioAinda não há avaliações
- Quim01 Livro PropostosDocumento136 páginasQuim01 Livro PropostosbeatrizaraujoriAinda não há avaliações
- Trabalho de Ciências - CópiaDocumento6 páginasTrabalho de Ciências - CópiaGabriel PrataAinda não há avaliações
- Lista 2 - Teoria Atômica Quimica GeralDocumento3 páginasLista 2 - Teoria Atômica Quimica GeralGláucia GuimaraesAinda não há avaliações
- 01 20atom C3 ADstica 20 - 20modelos 20at C3 B4micos 20VDocumento31 páginas01 20atom C3 ADstica 20 - 20modelos 20at C3 B4micos 20VALEXANDRE ALMEIDAAinda não há avaliações
- Diversos Tipos de Modelo Atomico e Modelo Atomico AtualDocumento9 páginasDiversos Tipos de Modelo Atomico e Modelo Atomico AtualThaís RúbioAinda não há avaliações
- Qu Imica: Exerc Icios - Atom Istica: Modelos at Omicos e RadioatividadeDocumento3 páginasQu Imica: Exerc Icios - Atom Istica: Modelos at Omicos e Radioatividadeyngrid santosAinda não há avaliações
- Livro 1Documento21 páginasLivro 1Quézia Soares de PaulaAinda não há avaliações
- Aula 4Documento22 páginasAula 4ronneiafonsoAinda não há avaliações
- 201802estrutura Atc3b4mica 1 PDFDocumento23 páginas201802estrutura Atc3b4mica 1 PDFIsa Na medicinaAinda não há avaliações
- Evolução Dos Modelos Atômicos (PDF - Io)Documento12 páginasEvolução Dos Modelos Atômicos (PDF - Io)Eduarda De Oliveira MorenoAinda não há avaliações
- Trabalho de QuimicaDocumento11 páginasTrabalho de QuimicaMarli EngsterAinda não há avaliações
- Química para Ingresso Nas EngenhariasDocumento32 páginasQuímica para Ingresso Nas EngenhariasManecos JúniorAinda não há avaliações
- Quimica GeralDocumento69 páginasQuimica GeralCarolina BragaAinda não há avaliações
- Desvendando o Átomo - IfbaDocumento51 páginasDesvendando o Átomo - IfbaClaudio SergioAinda não há avaliações
- Lista de Soluções 1º Ano Ita - 01Documento5 páginasLista de Soluções 1º Ano Ita - 01Ana Ester CavalcanteAinda não há avaliações
- Apostila Química 14 19 PDFDocumento6 páginasApostila Química 14 19 PDFPablo FirminoAinda não há avaliações
- Aula 13 - MatériaDocumento23 páginasAula 13 - MatériaCarlos SchirmerAinda não há avaliações
- Modelos Atômicos II - Rutherford e BohrDocumento6 páginasModelos Atômicos II - Rutherford e BohrPipoca GrandeAinda não há avaliações
- Apostila Inorganica I 2012 2 UFESDocumento140 páginasApostila Inorganica I 2012 2 UFESZenith26Ainda não há avaliações
- Aula 01 - Teoria Atômica ReformuladoDocumento79 páginasAula 01 - Teoria Atômica ReformuladoPhablo JuniorAinda não há avaliações
- Evolução Modelo Atômico para Os PadawansDocumento27 páginasEvolução Modelo Atômico para Os Padawansconta.2.pek3noAinda não há avaliações
- Lista de Exercícios - Ciências Da NaturezaDocumento3 páginasLista de Exercícios - Ciências Da NaturezaCAÇADOR DE MENDIGOS TOME CUIDADOAinda não há avaliações
- A Descoberta Do EletronDocumento7 páginasA Descoberta Do EletronSyara SantsAinda não há avaliações
- Ciências Aplicadas - Química Dos MateriaisDocumento114 páginasCiências Aplicadas - Química Dos MateriaisAlfredo Nunes da SilvaAinda não há avaliações
- As Leis Ponderais e Estrutura AtômicaDocumento8 páginasAs Leis Ponderais e Estrutura AtômicavasconcelosjAinda não há avaliações
- Estrutura Atômica - Modelos Atômicos.Documento3 páginasEstrutura Atômica - Modelos Atômicos.ingridlira1406Ainda não há avaliações
- Atomistica Resumo e Exercicios Com GabaritoDocumento13 páginasAtomistica Resumo e Exercicios Com GabaritoRomeuComastriAbdalaAinda não há avaliações
- Extensivoenem Química Evolução Dos Modelos Atômicos 22-02-2019Documento12 páginasExtensivoenem Química Evolução Dos Modelos Atômicos 22-02-2019eng civil Paulo Vitor MedeirosAinda não há avaliações
- 564 Farias Brito Quimica Sergio Matos Estrutura AtomicaDocumento35 páginas564 Farias Brito Quimica Sergio Matos Estrutura AtomicaNízia RodriguesAinda não há avaliações
- Questao Atdq Lista 06Documento17 páginasQuestao Atdq Lista 06Emanuelle Vincenzi CamattiAinda não há avaliações
- Modelo Atómico de RutherfordDocumento4 páginasModelo Atómico de RutherfordMesach GilAinda não há avaliações
- Trabalho Atomística - Alunas - Andressa Luíza Ratajk (21103299) e Gabrielli Bilck (21100922) - Turma - 01753Documento5 páginasTrabalho Atomística - Alunas - Andressa Luíza Ratajk (21103299) e Gabrielli Bilck (21100922) - Turma - 01753Andressa RatajkAinda não há avaliações
- O Átomo e Os Modelos Atômicos: Ciências - Prof Gerlânea SilvaDocumento53 páginasO Átomo e Os Modelos Atômicos: Ciências - Prof Gerlânea SilvaKaua molAinda não há avaliações
- Atomística 1Documento3 páginasAtomística 1Bia CabralAinda não há avaliações
- MEDICINADocumento4 páginasMEDICINAMatheus LeãoAinda não há avaliações
- Cap.2 - FA - 2022.2 - Estrutura Atômica - Propriedades PeriódicasDocumento79 páginasCap.2 - FA - 2022.2 - Estrutura Atômica - Propriedades PeriódicasBalafharAinda não há avaliações
- Série Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosNo EverandSérie Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- Newtonianos no mercado: dos primeiros professores universitários aos professores independentes e/ou itinerantes de filosofia natural e experimental na Inglaterra do século XVIIINo EverandNewtonianos no mercado: dos primeiros professores universitários aos professores independentes e/ou itinerantes de filosofia natural e experimental na Inglaterra do século XVIIIAinda não há avaliações
- Resumo Completo de ESTRUTURA ATÔMICA (CSADocumento7 páginasResumo Completo de ESTRUTURA ATÔMICA (CSAPDR1000 0Ainda não há avaliações
- Resumo Completo de Tecidos (CSA)Documento4 páginasResumo Completo de Tecidos (CSA)PDR1000 0Ainda não há avaliações
- Resumo Completo de Carboidratos (CSA)Documento2 páginasResumo Completo de Carboidratos (CSA)PDR1000 0Ainda não há avaliações
- Resumo Lipídios (CSA)Documento3 páginasResumo Lipídios (CSA)PDR1000 0Ainda não há avaliações
- 53c6d016ber VISTO 01 - Reacoes-2Documento3 páginas53c6d016ber VISTO 01 - Reacoes-2Thiago SoaresAinda não há avaliações
- Exercícios de Ligações Químicas e Suas PropriedadesDocumento3 páginasExercícios de Ligações Químicas e Suas PropriedadesMIRIAM FEITOSAAinda não há avaliações
- Ácido BaseDocumento18 páginasÁcido Basecristinajlopes100% (1)
- Exercício - Estrutura AtômicaDocumento2 páginasExercício - Estrutura AtômicaLucas Matheus LessaAinda não há avaliações
- Água DuraDocumento4 páginasÁgua DuravanS2tutyAinda não há avaliações
- Tabela PeriódicaDocumento109 páginasTabela PeriódicawarleyAinda não há avaliações
- Exercícioquimica - Reagente LimitanteDocumento2 páginasExercícioquimica - Reagente LimitanteLaura OliveiraAinda não há avaliações
- Tabela de Densidade Dos MateriaisDocumento1 páginaTabela de Densidade Dos MateriaisEdimilson AlvesAinda não há avaliações
- Lista 1 PDFDocumento1 páginaLista 1 PDFJamileAinda não há avaliações
- Avaliação Da Eficiência Da Lixiviação de Metais Preciosos Das Placas de Circuito Impreso Com Utilização de Lixiviantes Alternativo Ao CianetoDocumento0 páginaAvaliação Da Eficiência Da Lixiviação de Metais Preciosos Das Placas de Circuito Impreso Com Utilização de Lixiviantes Alternativo Ao CianetostudwesleyAinda não há avaliações
- Lista 01 Radioatividade 2c2b0 Em1Documento5 páginasLista 01 Radioatividade 2c2b0 Em1deisifabiAinda não há avaliações
- MilleritaDocumento1 páginaMilleritaMenderson MirandaAinda não há avaliações
- Caracterização Microestrutural de Solda Dissimilar Aisi 304 e Inconel 625Documento5 páginasCaracterização Microestrutural de Solda Dissimilar Aisi 304 e Inconel 625Moito CarvalhoAinda não há avaliações
- Aplicação Dos Elementos QuimicosDocumento7 páginasAplicação Dos Elementos QuimicosAvelino AugustoAinda não há avaliações
- Periodic Table Large-Pt BRDocumento1 páginaPeriodic Table Large-Pt BRcapitalistaestrelaswarAinda não há avaliações
- Lista de Exercicios - QuímicaDocumento3 páginasLista de Exercicios - QuímicaAna SalmontAinda não há avaliações
- Lista de Exercícios 2º BimestreDocumento2 páginasLista de Exercícios 2º BimestreMARIAH ALVARES MOREIRAAinda não há avaliações
- 9ANO - 07 - TABELAPERIODICA - CertoDocumento20 páginas9ANO - 07 - TABELAPERIODICA - CertoNatália NunesAinda não há avaliações
- Exercícios de Propriedades PeriódicasDocumento8 páginasExercícios de Propriedades PeriódicasyagoAinda não há avaliações
- Obtencao Do Oxigenio - LaboratorioDocumento11 páginasObtencao Do Oxigenio - LaboratorioEmidioMafastela100% (1)
- fq9 - Teste 5 - Enunciado 3 Periodo PDFDocumento5 páginasfq9 - Teste 5 - Enunciado 3 Periodo PDFzxx100% (1)
- Divulgação de DadosDocumento769 páginasDivulgação de DadosPedro SousaAinda não há avaliações
- Relatório - Reatividade Química Dos Metais. Síntese Do Gás Hidrogenio - Mariana AlmeidaDocumento9 páginasRelatório - Reatividade Química Dos Metais. Síntese Do Gás Hidrogenio - Mariana AlmeidaMariana AlmeidaAinda não há avaliações
- Número de Oxidação (Nox)Documento16 páginasNúmero de Oxidação (Nox)Octavio Augustto Santana DouradoAinda não há avaliações
- Apresentação QuímicaDocumento40 páginasApresentação QuímicaJoão EwertonAinda não há avaliações
- Níveis de Potássio em Pastagens de Panicum Maximum Cv. CentenárioDocumento3 páginasNíveis de Potássio em Pastagens de Panicum Maximum Cv. CentenárioNewton de Lucena CostaAinda não há avaliações
- Poster Caracterização Geoquimica Mulala III CIBAP vf-1 PDFDocumento1 páginaPoster Caracterização Geoquimica Mulala III CIBAP vf-1 PDFJeane Cristine MenesesAinda não há avaliações