Escolar Documentos
Profissional Documentos
Cultura Documentos
Lista 2 - Fisico Quimica
Enviado por
faculdade arquivosTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Lista 2 - Fisico Quimica
Enviado por
faculdade arquivosDireitos autorais:
Formatos disponíveis
IC-395 / IC-603 2020.
1
Segunda Lista de Exercícios
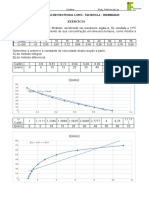
1a Questão. Considere os dados de concentração em função do tempo para o reagente A da reação:
2A + B → P.
[B]0 (mol dm-3) 1,0 1,5 2,0 a) Calcule o valor da constante de velocidade (adote as
mesmas unidades usadas na tabela ao lado para
t [A] [A] [A] expressar a unidade da constante de velocidade).
(h) (mol dm-3) (mol dm-3) (mol dm-3)
0,00 1,00E-02 1,00E-02 1,00E-02
0,01 9,83E-03 9,75E-03 9,67E-03
0,02 9,67E-03 9,50E-03 9,34E-03
0,05 9,19E-03 8,80E-03 8,44E-03
b) Considere o experimento realizado com
0,08 8,73E-03 8,16E-03 7,62E-03 concentrações iniciais [A]0 = 0,40 mol dm-3 e
0,10 8,44E-03 7,75E-03 7,12E-03 [B]0 = 0,18 mol dm-3.
0,20 7,12E-03 6,01E-03 5,07E-03
0,30 6,01E-03 4,66E-03 3,61E-03 Qual o tempo necessário para que [A]=[A]0/2 ?
0,40 5,07E-03 3,61E-03 2,57E-03
0,50 4,28E-03 2,80E-03 1,83E-03
0,60 3,61E-03 2,17E-03 1,30E-03
0,80 2,57E-03 1,31E-03 6,62E-04
1,20 1,31E-03 4,72E-04 1,70E-04
2a Questão. A velocidade de bromação da acetona (CH3COCH3 + Br2 → CH3COCH2Br + H+ + Br-) foi medida
em experimentos com diferentes condições iniciais.
Velocidade [CH3COCH3] [Br2] [H+]
(mol L-1s-1) (molL-1) (molL-1) (molL-1)
5,79x10-5 0,30 0,050 0,050
1,16x10-4 0,30 0,100 0,100
3,08x10-4 0,40 0,050 0,200
7,72x10-5 0,40 0,050 0,050
Qual a lei de velocidade? Qual o valor da constante de velocidade?
3a Questão. Os valores de coeficientes de velocidade de uma reação de primeira ordem são informados na
tabela abaixo.
k (s-1) 1,738E+00 1,415E+01 7,144E+02 1,536E+04
T (K) 1200 1300 1540 1800
Obtenha os parâmetros da equação de Arrhenius.
4a Questão. Considere o mecanismo proposto para a reação 2 F2O → 2 F2 + O2:
2 F2O → F + OF + F2O k1
F + F2O → F2 + OF k2
2 OF → O2 + 2 F k3
2 F + F2O → F2 + F2O k4
d [F 2 O]
Mostre que a lei de velocidade é expressa por: =k I [ F2 O]2 + k II [F 2 O]3 / 2
dt
Você também pode gostar
- Cinética Química: exercícios sobre leis de velocidade e fatores que influenciam reaçõesDocumento10 páginasCinética Química: exercícios sobre leis de velocidade e fatores que influenciam reaçõesFabiane De Oliveira Cantão FonsecaAinda não há avaliações
- Reações Químicas UFMADocumento5 páginasReações Químicas UFMADaniel ArrudaAinda não há avaliações
- Lista II - CINÉTICA QUÍMICA.Documento16 páginasLista II - CINÉTICA QUÍMICA.Vanessa MarcelliAinda não há avaliações
- QG1 Terceiro Exercício Gabarito 2016.2Documento4 páginasQG1 Terceiro Exercício Gabarito 2016.2IsabellaAinda não há avaliações
- LISTA 06-Cinética QuímicaDocumento4 páginasLISTA 06-Cinética QuímicaBreno RochaAinda não há avaliações
- Exercícios de Físico-químicaDocumento5 páginasExercícios de Físico-químicaLisiane AliesAinda não há avaliações
- ListacineticaDocumento2 páginasListacineticaSARAHAinda não há avaliações
- Cinética Química - Velocidades de ReaçãoDocumento3 páginasCinética Química - Velocidades de Reaçãogivaldo_antonio47050% (1)
- Lista de ExercíciosDocumento3 páginasLista de ExercíciosSamira Aguiar PedrosaAinda não há avaliações
- Cinética Química - ExercíciosDocumento6 páginasCinética Química - ExercíciosRafael AldreemAinda não há avaliações
- LISTA 05-Cinética QuímicaDocumento4 páginasLISTA 05-Cinética QuímicaMarcsAinda não há avaliações
- Apresentação Lab.1Documento23 páginasApresentação Lab.1Joel PintoAinda não há avaliações
- Exercício Cinética QuímicaDocumento6 páginasExercício Cinética QuímicaLucas BentesAinda não há avaliações
- Lista 6 - Cinetica Quimica - Quimica 2 PDFDocumento15 páginasLista 6 - Cinetica Quimica - Quimica 2 PDFArthur GarciaAinda não há avaliações
- Físico-Química II - Lista de Exercícios Cinética QuímicaDocumento3 páginasFísico-Química II - Lista de Exercícios Cinética QuímicaLucas CamargoAinda não há avaliações
- Folha 2 de Cinética Química-IME-ITADocumento3 páginasFolha 2 de Cinética Química-IME-ITAHelton MoreiraAinda não há avaliações
- Determinação da ordem e constante de velocidade de reações químicasDocumento7 páginasDeterminação da ordem e constante de velocidade de reações químicasRodrigo BertaciniAinda não há avaliações
- Cinética Química ExercíciosDocumento23 páginasCinética Química ExercíciosmatBarreto e transferidor o nome do objeto.Ainda não há avaliações
- LISTADocumento5 páginasLISTAAcássio PaivaAinda não há avaliações
- Lista de exercícios cinéticaDocumento4 páginasLista de exercícios cinéticaJeferson ThomazAinda não há avaliações
- 3a Lista de Exercicios - CineticaDocumento3 páginas3a Lista de Exercicios - CineticaTércia AragãoAinda não há avaliações
- Lista de Exercicios 1Documento4 páginasLista de Exercicios 1Mariana MartinsAinda não há avaliações
- Correção em PDF - QuímicaDocumento13 páginasCorreção em PDF - QuímicaMarcelo TrindadeAinda não há avaliações
- Reações químicas resolvidasDocumento20 páginasReações químicas resolvidasmuralha17Ainda não há avaliações
- Viscosidade de fluidos: análise experimentalDocumento7 páginasViscosidade de fluidos: análise experimentalVictor GomesAinda não há avaliações
- Cinética Química - Lista de exercícios UFTMDocumento1 páginaCinética Química - Lista de exercícios UFTMLetícia Mesquita GodoiAinda não há avaliações
- Eng. Materiais - 4 Unid.Documento12 páginasEng. Materiais - 4 Unid.Henrique MagalhaesAinda não há avaliações
- Lista de ExercíciosDocumento2 páginasLista de Exercícioswh42m9m9c9Ainda não há avaliações
- Cinética Química UFCEDocumento3 páginasCinética Química UFCEPaulo GonçalvesAinda não há avaliações
- Lista de Exercícios de Química Geral com Reações de VelocidadeDocumento2 páginasLista de Exercícios de Química Geral com Reações de VelocidadePedro MarizAinda não há avaliações
- 7 Lista QGE2001 CineticaDocumento5 páginas7 Lista QGE2001 CineticaWashington RamosAinda não há avaliações
- Aula09ExercciosdeCinticadaReao_20240416145414Documento21 páginasAula09ExercciosdeCinticadaReao_20240416145414Júlio VianaAinda não há avaliações
- Exercícios Revisão CinéticaDocumento20 páginasExercícios Revisão CinéticaIara DaherAinda não há avaliações
- Aula 14 - Revisão e Lista de ExercíciosDocumento4 páginasAula 14 - Revisão e Lista de ExercíciosLílian Barreto GonçalvesAinda não há avaliações
- Determinação de Ordem de Reação Entre Violeta Cristal e Hidróxido de SódioDocumento6 páginasDeterminação de Ordem de Reação Entre Violeta Cristal e Hidróxido de SódioAna Flávia Caldeira MachadoAinda não há avaliações
- Folha2 Calc ElementaresDocumento2 páginasFolha2 Calc ElementaresAna CarolinaAinda não há avaliações
- Físico-Química III – Cinética QuímicaDocumento2 páginasFísico-Química III – Cinética QuímicaodnumiarAinda não há avaliações
- Exercicio Físico Química 2 2017 1Documento5 páginasExercicio Físico Química 2 2017 1Vitor LimaAinda não há avaliações
- 2021.2 Cinetica Quimica 1a Lista de ExerciciosDocumento2 páginas2021.2 Cinetica Quimica 1a Lista de ExerciciosDanielle SylvaAinda não há avaliações
- Selecao 2018.2 DR GabaritoDocumento17 páginasSelecao 2018.2 DR GabaritoWilkins BarrosAinda não há avaliações
- Ficha Cinetica LEF LEBM 2022 23Documento3 páginasFicha Cinetica LEF LEBM 2022 23Gabriel PereiraAinda não há avaliações
- Exame.N - EE - Uni - Apol 2022.3Documento1 páginaExame.N - EE - Uni - Apol 2022.3Jonas ValenteAinda não há avaliações
- Lista 05Documento4 páginasLista 05Nicole PacíficoAinda não há avaliações
- Trabalho Otimização - Parte2Documento9 páginasTrabalho Otimização - Parte2IvanAinda não há avaliações
- Exame de Capacidade IQ-USP - Prova de QuímicaDocumento8 páginasExame de Capacidade IQ-USP - Prova de QuímicaFábio HenriqueAinda não há avaliações
- Coletânea de Provas - IME/QuímicaDocumento40 páginasColetânea de Provas - IME/QuímicaFelipe MonteAinda não há avaliações
- Lista de Exerccios Cintica - 32 Horas - SDocumento3 páginasLista de Exerccios Cintica - 32 Horas - SJoyce OliverAinda não há avaliações
- Cinética química: Teoria das colisões e lei cinéticaDocumento6 páginasCinética química: Teoria das colisões e lei cinéticaAnica GabrielliAinda não há avaliações
- Recuperação Paralela 2º AnosDocumento2 páginasRecuperação Paralela 2º AnoskhaiuktAinda não há avaliações
- Atividade Cinética Química FEITADocumento2 páginasAtividade Cinética Química FEITAnathaliafanaia19Ainda não há avaliações
- PG Selecao20191 Mestrado GabaritoDocumento9 páginasPG Selecao20191 Mestrado GabaritoWilkins BarrosAinda não há avaliações
- Química: Raio atômico, reatividade e pares galvânicosDocumento9 páginasQuímica: Raio atômico, reatividade e pares galvânicosKelita CoimbraAinda não há avaliações
- Reações Químicas e EletroquímicaDocumento3 páginasReações Químicas e EletroquímicaLeo CrozAinda não há avaliações
- Lista 6 ECE GabDocumento8 páginasLista 6 ECE Gabvinivcius da silva barbosaAinda não há avaliações
- Olimpíada Brasileira de Física 2006 - 3a faseDocumento6 páginasOlimpíada Brasileira de Física 2006 - 3a faseLuisAinda não há avaliações
- Cinética Química Lista 1Documento3 páginasCinética Química Lista 1Maria TargaryenAinda não há avaliações
- Ficha V - Cinetica QuimicaDocumento3 páginasFicha V - Cinetica QuimicaAngelique ViannyAinda não há avaliações
- CINÉTICA - Lista de ExeríciosDocumento3 páginasCINÉTICA - Lista de ExeríciosrobsonAinda não há avaliações
- Média Aritmética Simples Ponderada Harmonica GeometricaDocumento4 páginasMédia Aritmética Simples Ponderada Harmonica GeometricaEduardo GuimarãesAinda não há avaliações
- Modulo Economia AmbientalDocumento87 páginasModulo Economia AmbientalSérgio SaguarAinda não há avaliações
- Moisés e a jornada de Israel pelo desertoDocumento44 páginasMoisés e a jornada de Israel pelo desertoCarolina MarinhoAinda não há avaliações
- Manual Marca BBDocumento3 páginasManual Marca BBrdogoncalvesAinda não há avaliações
- Exercícios A Nova IndustrializaçãoDocumento6 páginasExercícios A Nova Industrializaçãosantiagoal1914Ainda não há avaliações
- MAN-002 - Manutenção de Máquinas e Equipamentos de Produção Rev 12 19-03-2013Documento6 páginasMAN-002 - Manutenção de Máquinas e Equipamentos de Produção Rev 12 19-03-2013Jefferson MoraesAinda não há avaliações
- A Caixa de Ferramentas de DeusDocumento4 páginasA Caixa de Ferramentas de Deuswalter_pacheco_1Ainda não há avaliações
- Cadeias, Pirâmides e Teias Alimentares - BiologiaDocumento1 páginaCadeias, Pirâmides e Teias Alimentares - BiologiaThaís LoiolaAinda não há avaliações
- Porta VillartaDocumento45 páginasPorta VillartaAngelo TeixeiraAinda não há avaliações
- Patologia Veterinária Geral: Causas, Sinais e TratamentosDocumento15 páginasPatologia Veterinária Geral: Causas, Sinais e TratamentosMilenaAinda não há avaliações
- Fundações profundas: tipos de estacasDocumento16 páginasFundações profundas: tipos de estacasd23m89Ainda não há avaliações
- Modelos de Introdução para Redação 6 Exemplos de Como Iniciar Seu TextoDocumento1 páginaModelos de Introdução para Redação 6 Exemplos de Como Iniciar Seu TextoVictor ZanardiAinda não há avaliações
- Termostato 40Documento49 páginasTermostato 40Carlos MachadoAinda não há avaliações
- Aposentadoria por invalidez - laudo pericialDocumento13 páginasAposentadoria por invalidez - laudo pericialcarlos henrique nunes pintoAinda não há avaliações
- Aloe Vera Emfal FispqDocumento3 páginasAloe Vera Emfal FispqcelmorcelliAinda não há avaliações
- Uso Excessivo Das Redes Sociais e Seus ReflexosDocumento2 páginasUso Excessivo Das Redes Sociais e Seus ReflexosGraziella SouzaAinda não há avaliações
- Catalogo Voltimetro Digital BHS Bdi Rev. 15Documento7 páginasCatalogo Voltimetro Digital BHS Bdi Rev. 15hchico2010Ainda não há avaliações
- Modelo Banner Evento Cascavel ProntoDocumento1 páginaModelo Banner Evento Cascavel ProntoRafael Gil FerquesAinda não há avaliações
- Prova Clinica CirurgicaDocumento4 páginasProva Clinica CirurgicaEuAinda não há avaliações
- Regulamento CONCREBOL CEENC 2013Documento5 páginasRegulamento CONCREBOL CEENC 2013Magno BernardoAinda não há avaliações
- Manual de Normas e Rotinas Da Unidade Materno Infantil (UMI) - Clínica ObstétricaDocumento25 páginasManual de Normas e Rotinas Da Unidade Materno Infantil (UMI) - Clínica ObstétricaLauraTechy100% (1)
- Avaliação Serviço Eletricidade NR10Documento12 páginasAvaliação Serviço Eletricidade NR10Murilo SantosAinda não há avaliações
- VOLEIBOLDocumento3 páginasVOLEIBOLCleidiane Ferreira50% (2)
- Aula 05 - Hidatidose e Fasciolose PDFDocumento26 páginasAula 05 - Hidatidose e Fasciolose PDFKaroline RaianeAinda não há avaliações
- Classe III PDFDocumento34 páginasClasse III PDFGabriela RodriguesAinda não há avaliações
- Curso - Análise Da InformaçãoDocumento12 páginasCurso - Análise Da InformaçãoCESAR HENRIQUE PIGNATON RAVANIAinda não há avaliações
- Teste o TesouroDocumento7 páginasTeste o TesouroSusana Rodrigues100% (1)
- Método para Cálculo Do Gasto Calórico Nas Atividades de Vida DiáriaDocumento7 páginasMétodo para Cálculo Do Gasto Calórico Nas Atividades de Vida DiáriaCENTRO UNIVERSITÁRIO CORPORATIVO100% (3)
- Atividade 1.1 - Exercício de FixaçãoDocumento4 páginasAtividade 1.1 - Exercício de FixaçãoLorráynny GuimarãesAinda não há avaliações
- Provas de Física e Matemática abordam conceitos sobre ondas eletromagnéticas, afastamento da Lua e capacitoresDocumento85 páginasProvas de Física e Matemática abordam conceitos sobre ondas eletromagnéticas, afastamento da Lua e capacitoresrenaneves_95100% (2)