Escolar Documentos
Profissional Documentos
Cultura Documentos
Atividade Cinética Química FEITA
Enviado por
nathaliafanaia19Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Atividade Cinética Química FEITA
Enviado por
nathaliafanaia19Direitos autorais:
Formatos disponíveis
Cinética Química- Química Geral II
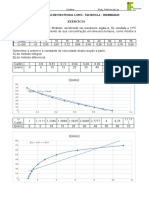
1) Um frasco que contêm 0,100mol de A é deixado reagir para formar B de acordo com a
reaçã o hipotética A(g) 2B(g). Os seguintes dados foram coletados:
Tempo (s) 0 40 80 120 160
Quantidade de matéria (mols) 0,100 0,067 0,045 0,030 0,020
a) Calcule a quantidade de B em cada tempo da tabela.
b) Calcule a velocidade média de desaparecimento de A para cada intervalo de 40 segundos.
Vm= 0,067-0,100/40-0= 0,033/40= -8,25x10-4
Vm= 0,045-0,067/80-40= -5,5x10-4
Vm= 0,030-0,045/120-80= 3,75x10-4
Vm= 0,020-0,030/160-120= 2,5x10-4
c) Qual a velocidade instantâ nea a 80 segundos?
Vi= 0,045/ 80= 5,625x10-4
2) Para a reaçã o foram realizados três experimentos conforme a tabela abaixo:
[A] mol/L [B] mol/L Velocidade de reaçã o mol/(L.min)
0,1 0,1 2,0 x 10-3
0,2 0,2 8,0 x 10-3
0,1 0,2 4,0 x 10-3
Determine:
a) A lei da velocidade da reaçã o acima
b) A constante da velocidade
c) A velocidade de formaçã o de C quando as concentraçõ es de A e B forem ambas 0,5 mol/L
Ra= 0,1/0,2= 0,5 Rva= 4,0x10-3/8,0x10-3= 0,5 0,5n = 0,5 N=1
Rb= 0,2/0,1=1 Rvb= 4,0x10-3/2,0x10-3=2 1n=2 N=1????
C)???
3) Os seguintes dados foram obtidos para a reaçã o A+ B+ C produtos
Experimento Concentraçã o inicial (mmol/L Velocidade
[A] [B] [C] mmol/Ls
1 1,25 1,25 1,25 8,7
2 2,5 1,25 1,25 17,4
3 1,25 3,02 1,25 50,8
4 1,25 3,02 3,75 457
5 3,01 1,00 1,15 ?
a) Escreva a lei de velocidade da reaçã o?
V=K [A]a x [B]bx [C]c
b) Qual a ordem da reaçã o?
Ordem 2
c) Determine a partir dos dados a constante de velocidade.
A=1 B=2 C=2
Tem que dividir pela 1 e 2 linha onde a é diferente de c e b e assim por diante, mesmo esquema
da questã o anterior
d) Use os dados para predizer a velocidade de reaçã o do experimento 5.
???
Você também pode gostar
- Lista de ExercíciosDocumento3 páginasLista de ExercíciosSamira Aguiar PedrosaAinda não há avaliações
- ListacineticaDocumento2 páginasListacineticaSARAHAinda não há avaliações
- Cinetica PDFDocumento10 páginasCinetica PDFFabiane De Oliveira Cantão FonsecaAinda não há avaliações
- Exercicios Reações Químicas Cinética Parte 1Documento5 páginasExercicios Reações Químicas Cinética Parte 1Daniel ArrudaAinda não há avaliações
- Lista CineticaDocumento1 páginaLista CineticaLetícia Mesquita GodoiAinda não há avaliações
- Lista de Exercicios - Cinetica - Quimica GeralDocumento1 páginaLista de Exercicios - Cinetica - Quimica GeralBruno Leandro VieiraAinda não há avaliações
- Lista Área II Química FundamentalDocumento20 páginasLista Área II Química FundamentalGuillaume HaddadAinda não há avaliações
- Lista Exercícios 03 CinéticaDocumento3 páginasLista Exercícios 03 CinéticaBeatriz FerreiraAinda não há avaliações
- Desafio IDocumento7 páginasDesafio IVictoria VitalAinda não há avaliações
- Lista de Exercicios Prova IIIDocumento6 páginasLista de Exercicios Prova IIIGABRIEL LORENCONI FASSARELLAAinda não há avaliações
- Lista Cinética 5 - Método Do Tempo de Meia-VidaDocumento3 páginasLista Cinética 5 - Método Do Tempo de Meia-VidaFabio ReisAinda não há avaliações
- LISTADocumento5 páginasLISTAAcássio PaivaAinda não há avaliações
- Lista de Exercícios - Mecanismos de Catálise HeterogêneaDocumento3 páginasLista de Exercícios - Mecanismos de Catálise HeterogêneaLucas da silvaAinda não há avaliações
- QUI116 - T - Avaliaà à o 3 - 2022-2-1 Prova Eleroquimica UfopDocumento2 páginasQUI116 - T - Avaliaà à o 3 - 2022-2-1 Prova Eleroquimica Ufopthaismarianacvo96Ainda não há avaliações
- QG1 Terceiro Exercício Gabarito 2016.2Documento4 páginasQG1 Terceiro Exercício Gabarito 2016.2IsabellaAinda não há avaliações
- Exercicios Cinetica - Parte 1Documento6 páginasExercicios Cinetica - Parte 1Rafael AldreemAinda não há avaliações
- SSA - Ficha de QuimicaDocumento19 páginasSSA - Ficha de Quimica010260100% (1)
- Lista 2 - Fisico QuimicaDocumento1 páginaLista 2 - Fisico Quimicafaculdade arquivosAinda não há avaliações
- Cinetica ResolucaoDocumento51 páginasCinetica ResolucaoCarlos Henrique0% (1)
- 1listadeexerciciosdecinetica 2010Documento3 páginas1listadeexerciciosdecinetica 2010givaldo_antonio47050% (1)
- Lista 05Documento4 páginasLista 05Nicole PacíficoAinda não há avaliações
- Lista 2. CinéticaDocumento2 páginasLista 2. CinéticaodnumiarAinda não há avaliações
- Lista II - CINÉTICA QUÍMICA.Documento16 páginasLista II - CINÉTICA QUÍMICA.Vanessa MarcelliAinda não há avaliações
- CDocumento8 páginasCprincipiaAinda não há avaliações
- DF Quimica Ita 5e8df32448beeDocumento6 páginasDF Quimica Ita 5e8df32448beeAnica GabrielliAinda não há avaliações
- Exercício Cinética QuímicaDocumento6 páginasExercício Cinética QuímicaLucas BentesAinda não há avaliações
- Ficha V - Cinetica QuimicaDocumento3 páginasFicha V - Cinetica QuimicaAngelique ViannyAinda não há avaliações
- CQ091 ListaExercicios L3 L4 L5Documento3 páginasCQ091 ListaExercicios L3 L4 L5Leo CrozAinda não há avaliações
- Lista de Exercícios - Cinética EnzimáticaDocumento4 páginasLista de Exercícios - Cinética EnzimáticaKetllin SimonettiAinda não há avaliações
- Selecao 2018.2 DR GabaritoDocumento17 páginasSelecao 2018.2 DR GabaritoWilkins BarrosAinda não há avaliações
- Lista de Cinética 1Documento3 páginasLista de Cinética 1Lucas CamargoAinda não há avaliações
- Exercicios de Apliacaã Ã o de ReactoresDocumento5 páginasExercicios de Apliacaã Ã o de ReactoresMariana CunhaAinda não há avaliações
- Lista 1 ps5Documento3 páginasLista 1 ps5TlalocAinda não há avaliações
- Lista de Exercício CINETICA (Corrigida)Documento4 páginasLista de Exercício CINETICA (Corrigida)Lael EduardoAinda não há avaliações
- Exercicios Absorcao e Emissao AtomicaDocumento2 páginasExercicios Absorcao e Emissao AtomicaMarli EmilianoAinda não há avaliações
- Folha 2 de Cinética Química-IME-ITADocumento3 páginasFolha 2 de Cinética Química-IME-ITAHelton MoreiraAinda não há avaliações
- Aula 4Documento14 páginasAula 4AUGUSTO GABRIELAinda não há avaliações
- Estudo DirigidoDocumento3 páginasEstudo Dirigidojuliana duarteAinda não há avaliações
- Coletania Livro IME QuímicaDocumento40 páginasColetania Livro IME QuímicaFelipe MonteAinda não há avaliações
- Lista de Exercicios Cinetica Quimica EQM061Documento13 páginasLista de Exercicios Cinetica Quimica EQM061Mariana DomicianoAinda não há avaliações
- 3a Lista de Exercicios - CineticaDocumento3 páginas3a Lista de Exercicios - CineticaTércia AragãoAinda não há avaliações
- Folha2 Calc ElementaresDocumento2 páginasFolha2 Calc ElementaresAna CarolinaAinda não há avaliações
- Gabarito 2022 2f QuimicaDocumento14 páginasGabarito 2022 2f QuimicaFelipe CostaAinda não há avaliações
- Lista QuímicaDocumento2 páginasLista QuímicaPedro MarizAinda não há avaliações
- 5a Lista de Exercicios de Fisico Quimica11Documento5 páginas5a Lista de Exercicios de Fisico Quimica11Lisiane AliesAinda não há avaliações
- Avaliação BioquímicaDocumento3 páginasAvaliação Bioquímicajuliana duarteAinda não há avaliações
- Lista Cintica - QumicaDocumento3 páginasLista Cintica - QumicaMaria TargaryenAinda não há avaliações
- Unidade Curricular:: Modelagem e Simulação Do Mundo Físico Químico Profa. DanielaDocumento21 páginasUnidade Curricular:: Modelagem e Simulação Do Mundo Físico Químico Profa. DanielaJúlio VianaAinda não há avaliações
- P2 - AsfDocumento24 páginasP2 - Asfluiz franciscoAinda não há avaliações
- 1 Lista de Exercícios - Análise Instrumental - Ciência Da InstrumentaçãoDocumento4 páginas1 Lista de Exercícios - Análise Instrumental - Ciência Da InstrumentaçãoDanny CiciliotteAinda não há avaliações
- Exercícios de Cinética QuímicaDocumento6 páginasExercícios de Cinética QuímicaVinicyus MartinsAinda não há avaliações
- Exercícios Resolvidos - Cinética QuímicaDocumento4 páginasExercícios Resolvidos - Cinética QuímicaSapatonaamazonia100% (1)
- 7 Lista QGE2001 CineticaDocumento5 páginas7 Lista QGE2001 CineticaWashington RamosAinda não há avaliações
- Curva de Solubilidade para Um Sistema Ternário: Labo3 2021/2022Documento9 páginasCurva de Solubilidade para Um Sistema Ternário: Labo3 2021/2022Cris OliveiraAinda não há avaliações
- Lista Exercícios CinéticaB - 23Documento8 páginasLista Exercícios CinéticaB - 23isamatias01Ainda não há avaliações
- Eng. Químico - Casa Da MoedaDocumento5 páginasEng. Químico - Casa Da MoedaprincipiaAinda não há avaliações
- Apresentação Lab.1Documento23 páginasApresentação Lab.1Joel PintoAinda não há avaliações
- Mec Lista2Documento2 páginasMec Lista2bernardo.marinho2010Ainda não há avaliações
- Check-List NP en ISO 9001-2015Documento54 páginasCheck-List NP en ISO 9001-2015Anonymous 3sOtS4Uvqm86% (7)
- Manual Aps Aluno SPP Unip - 2014 - 2Documento11 páginasManual Aps Aluno SPP Unip - 2014 - 2Barão BaronesAinda não há avaliações
- TCC FinalizadoDocumento40 páginasTCC FinalizadoLindolfoOliveiraAinda não há avaliações
- Acerto de Contas - Celia WaldenDocumento326 páginasAcerto de Contas - Celia Waldenjosue.calazans07Ainda não há avaliações
- Tarefa 6 - Desenvolvimento Cognitivo (Palavras Cruzadas) - SoluçãoDocumento1 páginaTarefa 6 - Desenvolvimento Cognitivo (Palavras Cruzadas) - SoluçãoAna GonçalvesAinda não há avaliações
- A Arte Da MassagemDocumento16 páginasA Arte Da MassagemAlexandra AzevedoAinda não há avaliações
- Atividade 2 - TQ 26Documento6 páginasAtividade 2 - TQ 26LidiaAinda não há avaliações
- Saber e Fazer Agroecologico Páginas 1,3 4,11 15,17 29Documento21 páginasSaber e Fazer Agroecologico Páginas 1,3 4,11 15,17 29Thauy Cabral100% (1)
- 08-Projeto de MolasDocumento50 páginas08-Projeto de MolasFelipe Frizon100% (1)
- Hibridacao 3cerao FMMDocumento6 páginasHibridacao 3cerao FMMifbenjitrueloginAinda não há avaliações
- Características GeraisDocumento13 páginasCaracterísticas Geraisrui19932009476Ainda não há avaliações
- ITATIAIA - CATALOGO - PRODUTOS AÇO 2019 - 30x21cmDocumento66 páginasITATIAIA - CATALOGO - PRODUTOS AÇO 2019 - 30x21cmWil SanAinda não há avaliações
- Do 20032020 1532Documento3 páginasDo 20032020 1532Benedicta SodréAinda não há avaliações
- Biodiversida de Marinha Da Ilha Do MaranhaoDocumento210 páginasBiodiversida de Marinha Da Ilha Do MaranhaoCarolinaAinda não há avaliações
- Passos para Escrever Um DocumentárioDocumento6 páginasPassos para Escrever Um DocumentárioSilas LimaAinda não há avaliações
- Bomba de Seringa BSS 200 BiosensorDocumento28 páginasBomba de Seringa BSS 200 BiosensorRafael AlbuquerqueAinda não há avaliações
- Cana de Açúcar - FermentaçãoDocumento2 páginasCana de Açúcar - FermentaçãoRobson RodriguesAinda não há avaliações
- Questões para o SimuladoDocumento13 páginasQuestões para o SimuladoCarlos BraynerAinda não há avaliações
- AULA 26 - Números Complexos - Frente 1 - Versao 1Documento19 páginasAULA 26 - Números Complexos - Frente 1 - Versao 1Joao MoneziAinda não há avaliações
- Concurso Público: EDITAL #005/2010Documento53 páginasConcurso Público: EDITAL #005/2010b4t3dorAinda não há avaliações
- PPC Mecânico de Manutenção de Máquinas FlorestaisDocumento199 páginasPPC Mecânico de Manutenção de Máquinas Florestaisarlindo assisAinda não há avaliações
- Química e Materiais - Lista 3Documento12 páginasQuímica e Materiais - Lista 3Gabriela Fontes Deiró FerreiraAinda não há avaliações
- Relatório Final Do Estagio I PDFDocumento11 páginasRelatório Final Do Estagio I PDFGessicaAinda não há avaliações
- 2021 - Cartilha Vamos Falar Sobre AnsiedadeDocumento19 páginas2021 - Cartilha Vamos Falar Sobre AnsiedadeJade FalcãoAinda não há avaliações
- Catalogo Linha Industrial 2016 WebDocumento40 páginasCatalogo Linha Industrial 2016 WebJéssica NunesAinda não há avaliações
- Cintura PelvicaDocumento3 páginasCintura PelvicaTaynara BissAinda não há avaliações
- ArquivoDocumento1 páginaArquivoCharlim SabaraAinda não há avaliações
- Exercicio Avaliativo 1 AnoDocumento4 páginasExercicio Avaliativo 1 AnoDan AlexAinda não há avaliações
- 3 Exercícios Sobre Movimento Uniformemente VariadoDocumento28 páginas3 Exercícios Sobre Movimento Uniformemente VariadoReginaldo CoelhoAinda não há avaliações