Escolar Documentos
Profissional Documentos
Cultura Documentos
Tema2 Ligacoes Quimicas
Enviado por
Fazisvaldo Pimentão0 notas0% acharam este documento útil (0 voto)
0 visualizações3 páginasTítulo original
tema2_ligacoes_quimicas
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
0 visualizações3 páginasTema2 Ligacoes Quimicas
Enviado por
Fazisvaldo PimentãoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 3
LIGAÇÕES QUÍMICAS
Ligações Químicas: Ligação Iônica, Covalente e Metálica
1. O que é ligação química?
2. O que é potencial de ionização e afinidade eletrônica?
3. Observe os valores de potencial de ionização e afinidade eletrônica dos elementos da família dos
halogênios (7A ou 18) e dos metais alcalinos (1A ou 1) apresentados nas Tabelas 1 e 2 a seguir. De
acordo com o texto, qual o elemento tem maior tendência em receber elétrons? Qual elemento tem
menor tendência em doar elétrons? Explique a sua resposta.
Tabela 1. Afinidade eletrônica em eV.
Tabela 2. Potencial de Ionização em kJ/mol.
4. O que são cátions? O que são ânions?
5. Quais são os tipos de ligação química
6. O que é energia de rede?
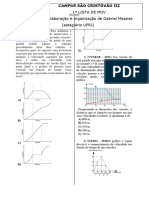
7. Explique o gráfico apresentado na figura2. Por que o sistema não entra em colapso quando r tende a
zero?
8. O que é a força de repulsão?
9. O que descreve a equação 9? Explique.
10. A tabela 3 mostra que a Equação 10 explica cerca de 98% da energia de rede de sistemas
considerados iônicos. E os outros 2% que faltam, se deve a que tipo de interação?
11. O que é eletronegatividade?
12. Quando podemos tratar o sistema como sendo uma interação entre íons?
13. O que é a ligação iônica?
14. Como a Química Quântica mostra a distribuição da função de onda dos elétrons?
15. Quantos elétrons serão compartilhados pelos átomos?
16. O que é a regra do octeto?
17. Como a equação de Schrodinger pode ser resolvida?
18. Em que consiste a função de onda Ψ2?
19. O que é o princípio de exclusão de Pauli?
20. Como podemos descrever os orbitais moleculares pela Teoria do Orbital Molecular (TOM)?
21. Explique a figura 3.
22. Por que a molécula de He2 não é formada?
23. O que são cálculos ab initio? E os métodos semiempíricos?
24. Como a Teoria da Ligação de Valência (TLV) explica a ligação química?
25. Qual o ponto fraco da TLV comparada com a TOM?
26. O que são orbitais híbridos?
27. Como a TLV racionaliza a formação da ligação BeH2? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
28. Como a TLV racionaliza a formação da ligação BF3? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
29. Como a TLV racionaliza a formação da ligação CH4? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
30. Como a TLV racionaliza a formação da ligação H2O? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
31. Como a TLV racionaliza a formação da ligação NH3? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
32. Como a TLV racionaliza a formação da ligação PCl5? Quais os orbitais híbridos formados? Qual a
geometria da molécula?
33. Como a TOM descreve a ligação metálica
34. O que é banda s? O que é banda d?
A Química Quântica Na Compreensão De Teorias De Química Orgânica
1. O que é ligação covalente?
2. O que é eletronegatividade?
3. O que é ligação polar? De um exemplo.
4. O que é ligação apolar? Dê um exemplo.
5. O que são orbitais moleculares?
6. O que são orbitais moleculares ligantes?
7. O que são orbitais moleculares anti-ligantes?
8. O que são orbitais moleculares não-ligantes?
9. Qual a hibridização do carbono quando envolvida em: ligação simples; ligação dupla; ligação tripla?
Coloque em ordem crescente de comprimento de ligação e força de ligação.
Exercícios:
1. Identifique a hibridização dos carbonos nas moléculas abaixo:
2. Considerando a Teoria da Ligação de Valência, desenhe as estruturas em linhas para as moléculas
abaixo e indique a hibridização do carbono das moléculas abaixo. Use o exercício anterior como
exemplo.
a) Propano (CH3CH2CH3)
b) Propeno (CH2=CHCH3)
c) Propino (CH≡CCH3)
d) Diclorometano (CH2Cl2)
e) Metilamina (CH3NH2)
f) N-metiletanimina (CH3CH=NCH3)
g) Acetonitrila (CH3C≡N)
h) Propanol (CH3CH2CH2OH)
i) Éter etílico e metílico (CH3OCH2CH3)
j) Propanona ou Acetona (CH3COCH3)
Você também pode gostar
- Lista de Exercícios - P1Documento7 páginasLista de Exercícios - P1malhenasmAinda não há avaliações
- Fundamentos de Química: Física Quântica e EletromagnetismoNo EverandFundamentos de Química: Física Quântica e EletromagnetismoAinda não há avaliações
- Permissão de TrabalhoDocumento5 páginasPermissão de TrabalhoFRANCISCO PEREIRAAinda não há avaliações
- Compostos ComplexosDocumento14 páginasCompostos ComplexosAlbino José JoaquimAinda não há avaliações
- Estrutura Molecular - Daniel e LeonardoDocumento16 páginasEstrutura Molecular - Daniel e LeonardoGloria DiasAinda não há avaliações
- Lista de Sobre Teoria Atómica e Estrutura Da Materia, Ligação Química e Termodinâmica QuímicaDocumento6 páginasLista de Sobre Teoria Atómica e Estrutura Da Materia, Ligação Química e Termodinâmica QuímicaRafael faruqueAinda não há avaliações
- Lista de Exercícios 01 - Introdução À Química OrgânicaDocumento2 páginasLista de Exercícios 01 - Introdução À Química OrgânicaLyndonJohnson0% (1)
- Lista de Exercicios - Ligacao QuimicaDocumento4 páginasLista de Exercicios - Ligacao QuimicaGabriel Cristofoletti DiorioAinda não há avaliações
- Lista de Química 1Documento3 páginasLista de Química 1Joao NetoAinda não há avaliações
- Exercícios Da Teoria Do OrbitalDocumento5 páginasExercícios Da Teoria Do OrbitalPaulo Henrique Barcellos França100% (1)
- Lista 3 Hibridização PDFDocumento1 páginaLista 3 Hibridização PDFVictor EduardoAinda não há avaliações
- Geometria Molecular ResumoDocumento10 páginasGeometria Molecular ResumoPedro Ricardo BessowAinda não há avaliações
- Estudo Dirigido 02 PDFDocumento2 páginasEstudo Dirigido 02 PDFEroaldo Da Silva AlvesAinda não há avaliações
- Lista 11Documento3 páginasLista 11santosbrizielle6Ainda não há avaliações
- Capitulo II - Teoria de Orbitais MolecularesDocumento15 páginasCapitulo II - Teoria de Orbitais MolecularesZuleca Sara PedroAinda não há avaliações
- Turma Enem-IFPI-Geometria-Polaridade-Ligações Intermoleculares.Documento18 páginasTurma Enem-IFPI-Geometria-Polaridade-Ligações Intermoleculares.Janielson VianaAinda não há avaliações
- Lista 2 PDFDocumento4 páginasLista 2 PDFJoaog123Ainda não há avaliações
- QG1P2Documento15 páginasQG1P2João Pedro MaiaAinda não há avaliações
- Introdução-Química Orgânica e Ligações Químicas 2018Documento52 páginasIntrodução-Química Orgânica e Ligações Químicas 2018vizjerei-brAinda não há avaliações
- Aula - Ligações Covalentes - Profº - Diego RobsonDocumento4 páginasAula - Ligações Covalentes - Profº - Diego RobsonDiego RobsonAinda não há avaliações
- Ligações QuímicasDocumento63 páginasLigações QuímicaswilliamAinda não há avaliações
- Ligações QuímicasDocumento20 páginasLigações QuímicasRobaoufgAinda não há avaliações
- Lista de Exercicios - P2-2011 Atualizada Com Gabarito-1Documento8 páginasLista de Exercicios - P2-2011 Atualizada Com Gabarito-1Joece SamotAinda não há avaliações
- Teoria Da Ligação de Valência (RPECV)Documento16 páginasTeoria Da Ligação de Valência (RPECV)TatianyAinda não há avaliações
- Lista 02 - CA PDFDocumento3 páginasLista 02 - CA PDFVictoria Lopes (Vick)Ainda não há avaliações
- Estudo Dirigido de Química - 1º Ano - 2º BIM..Docx AngloDocumento4 páginasEstudo Dirigido de Química - 1º Ano - 2º BIM..Docx AngloPeterson FaconiAinda não há avaliações
- Ficha Formativa3 Ligacao QuimicaDocumento2 páginasFicha Formativa3 Ligacao QuimicaMarwan GhunimAinda não há avaliações
- Compostos ComplexosDocumento9 páginasCompostos ComplexosAlbino José JoaquimAinda não há avaliações
- Lista de ExercíciosDocumento1 páginaLista de ExercíciosMatias SoaresAinda não há avaliações
- Aula 8 - Geometria MolecularDocumento32 páginasAula 8 - Geometria MolecularCliciane PeixotoAinda não há avaliações
- Exercicios P2 - Com Algumas RespostasDocumento10 páginasExercicios P2 - Com Algumas RespostasCaroline CarvalhoAinda não há avaliações
- FTQ10-D2 SD1 Paenac 2021-2022Documento6 páginasFTQ10-D2 SD1 Paenac 2021-2022Francisca CamachoAinda não há avaliações
- Lista U1Documento3 páginasLista U1Lucas AndradeAinda não há avaliações
- Química Inorgânica 1Documento43 páginasQuímica Inorgânica 1Daniele ZafraAinda não há avaliações
- Ligação Covalente Parte I PDFDocumento92 páginasLigação Covalente Parte I PDFigor santosAinda não há avaliações
- Aula 3 - F.M. - Quimica - Roberto Mazzei - Ligacoes InteratomicasDocumento13 páginasAula 3 - F.M. - Quimica - Roberto Mazzei - Ligacoes InteratomicasThiago SantosAinda não há avaliações
- 365 Reações Orgânicas 2007Documento136 páginas365 Reações Orgânicas 2007rbeckert100% (4)
- Domínio 2Documento4 páginasDomínio 2Marília PachecoAinda não há avaliações
- Lista de Exercícios 9Documento11 páginasLista de Exercícios 9Miguel Amorim FaulhaberAinda não há avaliações
- Cap 3Documento15 páginasCap 3Bruna FariasAinda não há avaliações
- TOM Aula Formulas Funcao OndaDocumento11 páginasTOM Aula Formulas Funcao OndaLUIZA NAZARETHAinda não há avaliações
- Aula 2 Ligações QuimicasDocumento16 páginasAula 2 Ligações QuimicasJanaina Rigotti KubiszeskiAinda não há avaliações
- FT 7 RespostasDocumento5 páginasFT 7 RespostasptpbzpwtqdAinda não há avaliações
- Lista ExerciciosDocumento4 páginasLista Exerciciosaliceac100% (1)
- Lista de Quã - Mica Geral (Ligaã - Ã - Es Quã - Micas) - 230316 - 150242Documento2 páginasLista de Quã - Mica Geral (Ligaã - Ã - Es Quã - Micas) - 230316 - 150242Maria GabrielaAinda não há avaliações
- 2 - Ligação Covalente (Lewis e Propriedades Das Ligações) PDFDocumento30 páginas2 - Ligação Covalente (Lewis e Propriedades Das Ligações) PDFJullyAinda não há avaliações
- Avaliação RespondidaDocumento4 páginasAvaliação Respondidanatalia LinsAinda não há avaliações
- Exercicio Ligacao 2012Documento3 páginasExercicio Ligacao 2012Cristiano Silva100% (1)
- Aula+6+-+Ligações+Quimicas Fabiana+AlmeidaDocumento49 páginasAula+6+-+Ligações+Quimicas Fabiana+AlmeidaBené JúniorAinda não há avaliações
- Ligacao CovalenteDocumento12 páginasLigacao CovalenterodrigomenegazgoularAinda não há avaliações
- Ligações QuímicasDocumento19 páginasLigações QuímicasTatianyAinda não há avaliações
- Estrutura MolecularDocumento65 páginasEstrutura MolecularStefanie MarinhoAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Simetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaNo EverandSimetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaAinda não há avaliações
- Série Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosNo EverandSérie Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosAinda não há avaliações
- CQ - Aula 2bDocumento28 páginasCQ - Aula 2bFazisvaldo PimentãoAinda não há avaliações
- FQAnalitica Aula2Documento15 páginasFQAnalitica Aula2Marck Kahvencíý VoltæireAinda não há avaliações
- Prova 1 2018 - UNBDocumento10 páginasProva 1 2018 - UNBFazisvaldo PimentãoAinda não há avaliações
- Universidade Federal de Viçosa Centro de Ciências Exatas E Tecnológicas Departamento de Engenharia Elétrica Curso de Engenharia ElétricaDocumento27 páginasUniversidade Federal de Viçosa Centro de Ciências Exatas E Tecnológicas Departamento de Engenharia Elétrica Curso de Engenharia ElétricaFazisvaldo PimentãoAinda não há avaliações
- Ocbio Mercado de Carbono 1Documento17 páginasOcbio Mercado de Carbono 1Avelino PereiraAinda não há avaliações
- Etapas Do Projeto de PesquisaDocumento2 páginasEtapas Do Projeto de Pesquisajoao vitorAinda não há avaliações
- Gestão Tributaria Da Cadeia de Suprimentos - 2013 - Cap - 6Documento2 páginasGestão Tributaria Da Cadeia de Suprimentos - 2013 - Cap - 6hawks 5.0Ainda não há avaliações
- Sas2018 4Documento17 páginasSas2018 4jgabrielcdaviAinda não há avaliações
- Apostila Projeção Da Consciência - Waldo VieiraDocumento12 páginasApostila Projeção Da Consciência - Waldo VieiraRanilson Angelo100% (1)
- QuestionarioDocumento3 páginasQuestionarioDhandara LucymillaAinda não há avaliações
- 10 FLUXO CORTE LASER - Revisado 21-07-2020Documento1 página10 FLUXO CORTE LASER - Revisado 21-07-2020Rafael PassarelliAinda não há avaliações
- Esquema Geral Cursos EfaDocumento50 páginasEsquema Geral Cursos EfaJose GalasAinda não há avaliações
- AutoP03158216425 PDFDocumento1 páginaAutoP03158216425 PDFwitalo taveiraAinda não há avaliações
- Termodinâmica - 3Documento46 páginasTermodinâmica - 3moises20caAinda não há avaliações
- Vasos de BarroDocumento5 páginasVasos de BarroDaniel Sipriano NetoAinda não há avaliações
- Estrutura Remuneratoria Senai (74131)Documento7 páginasEstrutura Remuneratoria Senai (74131)Lucimari SuzukiAinda não há avaliações
- Trabalho de TGA - Handy, Fayol e FordDocumento9 páginasTrabalho de TGA - Handy, Fayol e FordMarcos Roberto RosaAinda não há avaliações
- ANIM-012 - Manual Tosa Cocker SpanielDocumento15 páginasANIM-012 - Manual Tosa Cocker SpanielMarcos CelestinoAinda não há avaliações
- Registro Na Jucesp de Armazém GeralDocumento3 páginasRegistro Na Jucesp de Armazém Geralabertura de empresaAinda não há avaliações
- Óquio: Istema Etro ErroviárioDocumento96 páginasÓquio: Istema Etro ErroviárioJLAinda não há avaliações
- Cartilha FNS - Acesso A Recursos Da Saúde 2022Documento166 páginasCartilha FNS - Acesso A Recursos Da Saúde 2022vieiraianaAinda não há avaliações
- Prova Teorica NR 06Documento2 páginasProva Teorica NR 06Lih AssisAinda não há avaliações
- Desenvolvimento Da Radiologia IntervencionistaDocumento3 páginasDesenvolvimento Da Radiologia IntervencionistaProf-Alexsandro FerreiraAinda não há avaliações
- Lista 1 MruvDocumento5 páginasLista 1 MruvCamilla BuçardAinda não há avaliações
- BudaKamakura PDFDocumento16 páginasBudaKamakura PDFjuniorterapiaAinda não há avaliações
- Poemas - Pablo NerudaDocumento2 páginasPoemas - Pablo NerudaDenise SiqueiraAinda não há avaliações
- Guia de Identificação Das Pastagens Nativas Do Pantanal (2019)Documento223 páginasGuia de Identificação Das Pastagens Nativas Do Pantanal (2019)Andreia CostaAinda não há avaliações
- Aula 6 - Recursos CinesioterapêuticosDocumento9 páginasAula 6 - Recursos CinesioterapêuticosVeronica luz anselmoAinda não há avaliações
- Extensao Counitaria IDocumento17 páginasExtensao Counitaria Idércio nevesAinda não há avaliações
- 2017 - Producao Textual-6oAno - Etapa02 Fábulas, Apólogos, Contos Maravilhosos Prova e GabaritoDocumento8 páginas2017 - Producao Textual-6oAno - Etapa02 Fábulas, Apólogos, Contos Maravilhosos Prova e GabaritoRosimere BritoAinda não há avaliações
- Noção Intuitiva de LimitesDocumento14 páginasNoção Intuitiva de LimitesThayla CastroAinda não há avaliações
- Yago CastroDocumento21 páginasYago CastroYago CastroAinda não há avaliações
- Geometria ÁtomoDocumento4 páginasGeometria Átomoemarchesi2012Ainda não há avaliações
- Classificacao Geral Vestibular UeaDocumento991 páginasClassificacao Geral Vestibular UeamartinselanildaAinda não há avaliações