Escolar Documentos
Profissional Documentos
Cultura Documentos
Lista de Exercícios Exa416 2020.1
Enviado por
Laryssa NascimentoTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Lista de Exercícios Exa416 2020.1
Enviado por
Laryssa NascimentoDireitos autorais:
Formatos disponíveis
UEFS - DEXA
EXA416 – Lista de exercícios 2020.1
Prof. Alanjone Azevêdo Nascimento
Profa. Olívia Maria Bastos Costa
Estudante:_____________________________________________________________________________________________
1) A termoquímica estuda as energias envolvidas nas reações. Através dos seguintes parâmetros
termodinâmicos: variações de padrão de entalpia (H°), entropia (S°) e energia livre de Gibbs (G°) é
possível compreender ou fazer previsões sobre o estado de um sistema ou processo físico químico.
Sabendo disso, IDENTIFIQUE qual destes parâmetros é utilizado em cada uma das situações abaixo. Em cada
situação, EXEMPLIFIQUE com dados da literatura e gráficos.
a) Como avaliar a estabilidade de um sistema?
b) Como avaliar o calor envolvido numa reação?
c) Como avaliar a energia dissipada numa dada temperatura no sistema que não pode mais ser
convertida em trabalho?
d) Como prever se uma reação ocorre ou não em condições específicas?
e) Como avaliar a força relativa das ligações químicas entre reagentes e produtos?
2) Sobre Catalisadores é INCORRETO dizer:
a) Participa da reação formando uma espécie intermediária, mas não é nem reagente e nem produto;
b) Atuam muitas vezes enfraquecendo as ligações químicas e assim diminuindo a energia de ativação;
c) Não altera a diferença de entalpia entre reagente e produto, portanto, não altera a Hreação°;
d) Pode ser recuperado praticamente 100% ao final da reação química;
e) Pode ser substância, mistura, calor ou luz.
3) A constante de equilíbrio de solubilidade em água de um dado sólido M +X- é 0,002. Com base neste
dado, responda:
a) Este sólido é muito solúvel ou pouco solúvel em água? JUSTIFIQUE
b) Para remover o cátion M+ da água, é adicionado um sólido muito solúvel A+X-. Por que isso é possível?
4) Mencione os fatores (condições experimentais) que podem alterar a velocidade de uma reação
química. E com base na Teoria das Colisões, explique como um desses fatores atua modificando a
velocidade. Use como exemplo a reação de síntese da amônia.
5) Verdadeiro ou Falso? “O aumento da temperatura sempre torna a reação química mais rápida e mais
espontânea (∆G < 0)”. Justifique sua resposta.
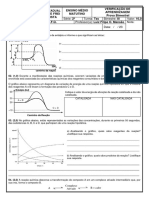
6) A decomposição do petóxido de dinitrogênio (N2O5) dissolvido em tetracloreto de carbono está
representada na equação a seguir: 2N2O5 (g) ⇌ 4NO2(g) + O2(g)
Assumindo-se que esta reação ocorre num sistema fechado e está em equilíbrio, responda:
a) Para que sentido (direto ou inverso) o equilíbrio será deslocado se ao sistema reacional for adicionado
mais gás oxigênio (O2)? Justifique sua resposta.
b) Após estabelecido a nova condição de equilíbrio, as concentrações de N 2O5 e NO2 serão maiores ou
menores que aquelas da condição de equilíbrio inicial? Justifique sua resposta.
Prof. Alanjone Azevêdo Nascimento UEFS - DEXA
Você também pode gostar
- Q4 - G1 - Guia de Estudos Da Unidade 1Documento4 páginasQ4 - G1 - Guia de Estudos Da Unidade 1Everson AlmeidaAinda não há avaliações
- Lista de Cinética Sem RespostaDocumento13 páginasLista de Cinética Sem RespostaLuiz Filipe Oliveira Mansão LuizAinda não há avaliações
- Lista de Exercícios QuímicaDocumento6 páginasLista de Exercícios QuímicaJulia MargrafAinda não há avaliações
- Avaliação bimestral de química sobre equilíbrio químico e velocidade de reaçõesDocumento4 páginasAvaliação bimestral de química sobre equilíbrio químico e velocidade de reaçõesRuan PabloAinda não há avaliações
- Avaliação de Química sobre Cinética QuímicaDocumento4 páginasAvaliação de Química sobre Cinética QuímicaMateus MenegassiAinda não há avaliações
- Cinetica 1Documento8 páginasCinetica 1Nanda OdebrechtAinda não há avaliações
- Cinética química: decomposição de N2O5Documento3 páginasCinética química: decomposição de N2O5RiaAinda não há avaliações
- Estudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .Documento4 páginasEstudo Dirigido de Química - Ceja - Fascículo 5 (Unidades 11, 12 e 13) .falecomarilsonAinda não há avaliações
- Curso 246253 Aula 11 241e SimplificadoDocumento23 páginasCurso 246253 Aula 11 241e Simplificadoisabelle's UniverseAinda não há avaliações
- 20 - 21 - Cinetica QuimicaDocumento10 páginas20 - 21 - Cinetica QuimicaGustavo MoraisAinda não há avaliações
- Lei de Hess - Exercícios de Revisão PDFDocumento7 páginasLei de Hess - Exercícios de Revisão PDFGeliane RochaAinda não há avaliações
- Equilíbrio e CinéticaDocumento7 páginasEquilíbrio e CinéticaHidro Solo - Departamento TécnicoAinda não há avaliações
- FichatrabeqquímicoDocumento3 páginasFichatrabeqquímicoAndrei GalanAinda não há avaliações
- 11FQA Ficha Formativa Q1.2Documento3 páginas11FQA Ficha Formativa Q1.2Andrei GalanAinda não há avaliações
- CAPÍTULO XII - EQUILÍBRIO QUÍMICODocumento8 páginasCAPÍTULO XII - EQUILÍBRIO QUÍMICOryan ferreiraAinda não há avaliações
- AULA PRÁTICA Nº02 - Entalpia Da Reacção-3Documento5 páginasAULA PRÁTICA Nº02 - Entalpia Da Reacção-3Patrício Zua Correia ZuaAinda não há avaliações
- Cinética Química: Ano Letivo 2023 4º Corte TemporalDocumento2 páginasCinética Química: Ano Letivo 2023 4º Corte Temporalleozinhocr5Ainda não há avaliações
- Prova de Física e Química do Ensino SecundárioDocumento12 páginasProva de Física e Química do Ensino SecundárioMariana JesusAinda não há avaliações
- Trabalho de Recuperacao Quimica 3 Ano And7131244Documento7 páginasTrabalho de Recuperacao Quimica 3 Ano And7131244Hilda maria rodrigues bragaAinda não há avaliações
- Química Pet 1Documento6 páginasQuímica Pet 1Isa SantosAinda não há avaliações
- Aula Cinética QuímicaDocumento33 páginasAula Cinética QuímicaBixoFelipeGomesAinda não há avaliações
- 3º Ano - 3º Trim - Sem 31 - Exercícios de Fixação de Química para o TC2Documento5 páginas3º Ano - 3º Trim - Sem 31 - Exercícios de Fixação de Química para o TC2Henrique AraujoAinda não há avaliações
- ArtigoDocumento9 páginasArtigoJean MacariAinda não há avaliações
- Trabalho 2º AnoDocumento1 páginaTrabalho 2º Anoh7mbwzyz76Ainda não há avaliações
- Velocidade de reações químicasDocumento6 páginasVelocidade de reações químicasKayron Willis100% (1)
- Roteiro Experimental de Química Computacional - Físico-QuímicaDocumento3 páginasRoteiro Experimental de Química Computacional - Físico-Químicageovanapicolo2020Ainda não há avaliações
- Quimica Aula 14 Cinetica QuimicaDocumento9 páginasQuimica Aula 14 Cinetica QuimicaNatany AssaiAinda não há avaliações
- Determinação Da Energia de Ativação de Uma Reação Iônica em Meio AquosoDocumento10 páginasDeterminação Da Energia de Ativação de Uma Reação Iônica em Meio AquosoAlexsander LopesAinda não há avaliações
- Lista 04Documento3 páginasLista 04Bárbara YasminAinda não há avaliações
- Química 1Documento14 páginasQuímica 1Maria Vitoria Moreira DantasAinda não há avaliações
- Determinacao Da Ordem de Reacao QuimicaDocumento11 páginasDeterminacao Da Ordem de Reacao Quimicatrigono_metriaAinda não há avaliações
- Equilíbrio Químico ListaDocumento8 páginasEquilíbrio Químico ListamateusAinda não há avaliações
- Cinetica CompletaDocumento5 páginasCinetica CompletaConta ReservaAinda não há avaliações
- ExerciciosDocumento3 páginasExerciciosrailson oliveiraAinda não há avaliações
- Termodinâmica e equilíbrio químicoDocumento15 páginasTermodinâmica e equilíbrio químicoCinara PavesiAinda não há avaliações
- LISTADocumento5 páginasLISTAAcássio PaivaAinda não há avaliações
- Teste de Quimica 3 Unidade 2023 (2 Ano)Documento3 páginasTeste de Quimica 3 Unidade 2023 (2 Ano)dasilvadeivilinAinda não há avaliações
- 2ª série - Física, Roteiro de EstudosDocumento16 páginas2ª série - Física, Roteiro de Estudosadna.quimicaAinda não há avaliações
- Fatores que influenciam a cinética químicaDocumento4 páginasFatores que influenciam a cinética químicaAndreia AnnaAinda não há avaliações
- Cinética química: influência da concentração e temperaturaDocumento10 páginasCinética química: influência da concentração e temperaturaRafa CossulAinda não há avaliações
- Determinação da Energia de Ativação de Reação QuímicaDocumento15 páginasDeterminação da Energia de Ativação de Reação QuímicaPdb1 NTCAinda não há avaliações
- Cine TicaDocumento7 páginasCine TicaLarissa LimaAinda não há avaliações
- Balanceamento de reações químicasDocumento67 páginasBalanceamento de reações químicasEdson JoseAinda não há avaliações
- Prof. Rafa - Química - Cinética Química - Prova P2 - 1 BimDocumento3 páginasProf. Rafa - Química - Cinética Química - Prova P2 - 1 BimRafael VaristeloAinda não há avaliações
- Prova - 3 Bimestre - ApfqDocumento2 páginasProva - 3 Bimestre - ApfqLuiz Filipe Oliveira Mansão LuizAinda não há avaliações
- Reação catalisadaDocumento2 páginasReação catalisadaElysangela RavaniAinda não há avaliações
- Qui MicaDocumento8 páginasQui Micamaria.hsvh0Ainda não há avaliações
- Cinetqui 001Documento31 páginasCinetqui 001Anonymous QMpWb7Vc3XAinda não há avaliações
- Cinética química e efeito da temperaturaDocumento6 páginasCinética química e efeito da temperaturaJoão Paulo EmrichAinda não há avaliações
- Lei de Arrhenius na reação de redução do persulfato de potássioDocumento7 páginasLei de Arrhenius na reação de redução do persulfato de potássioHaniel HonoratoAinda não há avaliações
- FT10 - Domínio 2 - Transformações QuímicasDocumento13 páginasFT10 - Domínio 2 - Transformações QuímicasLuciana SilvaAinda não há avaliações
- AULA 5-Atividade de Sistematização-Catalisadores-AlunosDocumento7 páginasAULA 5-Atividade de Sistematização-Catalisadores-AlunosCarlos AlcantaraAinda não há avaliações
- FQ Cap3Documento6 páginasFQ Cap3filipelima.graveAinda não há avaliações
- MM - FQ - KC IntroDocumento6 páginasMM - FQ - KC IntroPetrus NegreiroAinda não há avaliações
- Apostila de Cinetica e Reatores (Grad.) Revisada PDFDocumento53 páginasApostila de Cinetica e Reatores (Grad.) Revisada PDFLorenzo MatteoAinda não há avaliações
- Análise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018No EverandAnálise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018Ainda não há avaliações
- Biofísica para ciências biomédicas – 4ª ediçãoNo EverandBiofísica para ciências biomédicas – 4ª ediçãoAinda não há avaliações
- Operações Unitárias na Indústria de Alimentos e QuímicaNo EverandOperações Unitárias na Indústria de Alimentos e QuímicaAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Suvinil Látex Maxx Branco NeveDocumento9 páginasSuvinil Látex Maxx Branco NevethiagoAinda não há avaliações
- Exercícios de Termometria e Dilatação TérmicaDocumento3 páginasExercícios de Termometria e Dilatação TérmicaFagner TallesAinda não há avaliações
- Introdução À Automação, Autores: Schneck e SpinolaDocumento337 páginasIntrodução À Automação, Autores: Schneck e SpinolaGleison Elias Silva100% (3)
- Produção de água quente por termoacumulador e perigo da LegionellaDocumento16 páginasProdução de água quente por termoacumulador e perigo da Legionellabacuri7992Ainda não há avaliações
- Filtro de mangas - Fatores químicosDocumento13 páginasFiltro de mangas - Fatores químicosEdson BAinda não há avaliações
- Lista de verificação de boas práticas de fabricação de geladosDocumento17 páginasLista de verificação de boas práticas de fabricação de geladosrcrondon0% (1)
- Lista 02 2º AnoDocumento3 páginasLista 02 2º AnoAdriano MedeirosAinda não há avaliações
- Lista de exercícios de gases perfeitos da UFCEDocumento3 páginasLista de exercícios de gases perfeitos da UFCEHiêldoAinda não há avaliações
- Manual de Instrução Caldeira Aalborg 3 Pass Alfa Laval AalborgDocumento168 páginasManual de Instrução Caldeira Aalborg 3 Pass Alfa Laval Aalborgmarcoscesarfernandes100% (2)
- Engates Rápidos - Balflex PDFDocumento20 páginasEngates Rápidos - Balflex PDFFredericoFerrazAinda não há avaliações
- Relatório Estágio MecânicaDocumento27 páginasRelatório Estágio MecânicaIsmael Rodrigues PereiraAinda não há avaliações
- Boas Práticas Refrigeração ComercialDocumento41 páginasBoas Práticas Refrigeração ComercialCarlos SilvaAinda não há avaliações
- Lasanha Segura: Pontos de Atenção no PreparoDocumento1 páginaLasanha Segura: Pontos de Atenção no PreparoSivonildoAinda não há avaliações
- Manual Usuário BRASTEMP BMK38Documento2 páginasManual Usuário BRASTEMP BMK38LHMFAinda não há avaliações
- Mecânica Estatística 2Documento19 páginasMecânica Estatística 2Polliane de SousaAinda não há avaliações
- Manual técnico do Diesel S-10: propriedades e cuidados para transferênciaDocumento14 páginasManual técnico do Diesel S-10: propriedades e cuidados para transferênciaWellington MouraAinda não há avaliações
- Manual Luva BioclipDocumento18 páginasManual Luva BioclipAndre AzeredoAinda não há avaliações
- Resoluções Das Fichas FormativasDocumento22 páginasResoluções Das Fichas FormativasPaula FernandesAinda não há avaliações
- Física e Química A – 10o - Ficha de Trabalho 11Documento8 páginasFísica e Química A – 10o - Ficha de Trabalho 11Carlos Eduardo FukudaAinda não há avaliações
- Manual de Uso Do DensímetroDocumento2 páginasManual de Uso Do DensímetroDaniel Goldenberg0% (1)
- Calor específico experimentoDocumento11 páginasCalor específico experimentoCamila PachecoAinda não há avaliações
- Fispq - Emulsão Asfáltica para Pavimentação Tipo RR 2C e - Rev00 - VS00 PDFDocumento10 páginasFispq - Emulsão Asfáltica para Pavimentação Tipo RR 2C e - Rev00 - VS00 PDFVictor ChavesAinda não há avaliações
- Energia Solar Fotovoltaica-1911Documento16 páginasEnergia Solar Fotovoltaica-1911Franciwily donatoAinda não há avaliações
- Naufrágio de Navios Por Uso de Material Inadequado de RebitesDocumento1 páginaNaufrágio de Navios Por Uso de Material Inadequado de RebitesPablo Virgolino FreitasAinda não há avaliações
- Transferência de calor em paredes compostas e coeficientes de convecçãoDocumento4 páginasTransferência de calor em paredes compostas e coeficientes de convecçãoValdeirM.deSouzaAinda não há avaliações
- Introdução Aos Automatismos IndustriaisDocumento8 páginasIntrodução Aos Automatismos IndustriaisAntónio HenriquesAinda não há avaliações
- KANTHAL - Monografia (School Work)Documento18 páginasKANTHAL - Monografia (School Work)João RibeiroAinda não há avaliações
- Análisis del calor y transferencia de masa durante el tostado de café en loteDocumento8 páginasAnálisis del calor y transferencia de masa durante el tostado de café en loteLaís NorcinoAinda não há avaliações
- Update N 03 - Vazao Variavel No Primario e Economia de Energia YorkDocumento4 páginasUpdate N 03 - Vazao Variavel No Primario e Economia de Energia YorkMauro S Cabral100% (1)
- Manual Emprego de Pontes de MadeiraDocumento150 páginasManual Emprego de Pontes de MadeiraDarlan Felipe GomesAinda não há avaliações