Escolar Documentos
Profissional Documentos
Cultura Documentos
2 Série - Exercícios - QUÍMICA - 11-03
Enviado por
Alana WolfTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
2 Série - Exercícios - QUÍMICA - 11-03
Enviado por
Alana WolfDireitos autorais:
Formatos disponíveis
REVISANDO – 2º ANO- QUIMICA – EVI WEBER – 11/03/23
1. Na formação das moléculas de ácido clorídrico, ácido hipocloroso, ácido clórico e de ácido
perclórico podem participar os isótopos de 1H, 2H, 3H, 160, 17O, 180, 35Cl e 37Cl. Com relação às
massas moleculares das moléculas formadas, assinale o que for correto:
01. A menor massa molecular é 36 u e a maior massa molecular é 112 u.
02. A massa molecular do ácido hipocloroso pode variar entre 52 u e 58 u.
04. As moléculas de 2H35Cl17O e 1H37Cl160 apresentam número de nêutrons totais diferente.
08. O número de prótons em moléculas de ácido perclórico com diferentes massas moleculares
é o mesmo.
16. Compostos de mesma fórmula molecular, mas com massa molecular diferente, apresentam
o mesmo número de elétrons e número de nêutrons diferente.
Dê como resposta a soma dos números associados às proposições verdadeiras.
2. (UEM) Em física e química é essencial que aqueles que realizam medições adotem padrões
aceitos por todos para representar os resultados dessas medições, de modo que tais resultados
possam ser transmitidos de um laboratório para outro e verificados em qualquer lugar do
mundo. Sobre o padrão de massa é correto afirmar que:
01) O padrão de massa do Sistema Internacional de Unidades (SI) é um cilindro de platina-
irídio, cuja massa, atribuída em acordo internacional, é de 1 kg (um quilograma).
02) Na escala atômica existe um segundo padrão de massa, baseado no átomo 1H.
04) A unidade de massa atômica (u), definida por um acordo internacional, corresponde a um
décimo da massa do 12C.
08) O mol é uma unidade do SI que mede a quantidade de uma substância, sendo que um mol
de uma dada substância contém aproximadamente 6,02 1023 entidades elementares.
16) Um segundo padrão de massa é necessário visto que é possível comparar massas atômicas
entre si com uma precisão superior à que atualmente se consegue comparando-as com o
quilograma padrão
3. Um mol de um determinado composto contém 72 g de carbono (C), 12 mols de hidrogênio
(H) e 12.1023 ´ átomos de oxigênio (O). Constante de Avogadro = 6,0 1023. ´ Sobre o
composto, assinale o que for correto. Dados: C 12 g mol; H 1g mol; O 16 g mol
01) A fórmula mínima do composto é C3H3O6.
02) A massa molar do composto é 116 g mol.
04) 2,0 mols do composto possuem 3,6 1024 átomos de carbono.
08) 58 g do composto possuem 2 mols de oxigênio.
4. Assinale o que for correto.
01) A unidade de massa atômica, cujo símbolo é u, é definida como sendo igual a 1/12 da
massa de um átomo do isótopo 12C.
02) A massa atômica e o número de massa são grandezas idênticas.
04) A massa molar do CO2 é 44 u e a massa molecular do CO é 28 g/mol.
08) Um recipiente contendo 180 g de glicose possui o mesmo número de moléculas (porém
distintas) que um recipiente contendo 1 mol de água.
16) A fórmula mínima da sacarose é C6H12O6
5. Um lingote de massa 10 kg é constituído de uma liga metálica contendo prata, ouro e platina,
de composição Ag2Au3Pt5. Assinale a(s) alternativa(s) que descreve(m) corretamente esse
material.
01. O lingote de Ag2Au3Pt5 apresenta aproximadamente 1212 g de prata.
02. O lingote de Ag2Au3Pt5 apresenta aproximadamente 16,8 mols de ouro.
04. O lingote de Ag2Au3Pt5 apresenta aproximadamente 3,38 1025 átomos.
08. O lingote de Ag2Au3Pt5 apresenta uma razão de 10 átomos de platina para cada átomo de
prata.
16. O lingote de Ag2Au3Pt5 apresenta as mesmas propriedades físicas e químicas de um lingote
de Ag1Au3Pt6, pois ambos são compostos exclusivamente de prata, ouro e platina.
6. A solubilidade do nitrato de potássio em água, em função da temperatura, é dada na tabela
abaixo. Considerando-se soluções de KNO3 em 100g de água, assinale o que for correto:
Temperatura (ºC)--------------------- 0 20 40 60 100
Solubilidade KNO3g/100g de água-- 13.3 31.6 63.9 110 246
01) A 20ºC, uma solução com 40g está saturada.
REVISANDO – 2º ANO- QUIMICA – EVI WEBER – 11/03/23
02) A0ºC, uma solução com 10g está insaturada.
04) a 40ºC, uma solução com 120g está supersaturada.
08) A 100ºC, uma solução com 120g está saturada.
7. Preparou-se uma solução saturada de nitrato de potássio (KNO3), adicionando-se o sal a 50
g de água, à temperatura de 80°C. A seguir, a solução foi resfriada a 40°C. Qual a massa, em
gramas, do precipitado formado?
Dados: T = 80°C S = 180 g de KNO3/100g de H2O
T = 40°C S = 60 g de KNO3/100g de H2O
8. Analise os dados de solubilidade do KCℓ e do Li2CO3 contidos na tabela a seguir, na pressão
constante, em várias temperaturas e assinale o que for correto.
(01) Quando se adiciona 40g de KCℓ a 100g de água, a 20ºC, ocorre formação de precipitado, que
se dissolve com aquecimento a 40°C.
(02) Quando se adiciona 0,154g de Li2CO3 a 100g de água, a 50°C, forma-se uma solução
insaturada.
(04) O resfriamento favorece a solubilização do KCℓ, cuja dissolução é exotérmica.
(08) Quando se adiciona 37g de KCℓ a 100g de H2O, a 30°C, forma-se uma solução saturada.
(16) A dissolução do Li2CO3 é endotérmica e favorecida com o aumento de temperatura.
9. As concentrações de cátions e ânions em uma solução 0,2M de sulfato de potássio são,
respectivamente:
a) 0,2M e 0,2M b) 0,3M e 0,3M c) 0,3M e 0,4M
d) 0,4M e 0,2M e) 0,4M e 0,30
10. Sabe-se que uma solução de cloreto férrico em água contém 0,60 mol/litro de íons cloreto. A
molaridade da solução em relação ao FeCl3 é:
a) 0,20 molar b) 1,20 molar c) 0,60 molar d) 1,80 molar e) 0,80 molar
11. Um litro de uma solução contém 0,1 mol de NaCl e 0,2 mol de CaCl2. A molaridade dos íons
Na+, Ca2+ e Cl1- será, respectivamente, igual a:
a) 0,01M; 0,02M; 0,05M. b) 0,01M; 0,02M; 0,04M. c) 0,1 M; 0,2M; 0,4M.
d) 0,1M; 0,2M; 0,5M. e) 0,2M; 0,4M; 0,4M.
12. Um determinado gás poluente apresenta tolerância máxima de 2,0 ⋅ 10–5 mol/L em relação
ao ar. Uma sala fechada de dimensões 4m × 5m × 3m contém 6mol daquele gás. A tolerância foi
ultrapassada?
13. Um técnico pesou uma amostra de sulfato de cobre II pentahidratado (CuSO4 ⋅ 5H2O) e
encontrou o valor de 49,9g. A amostra foi colocada em um balão volumétrico. Em seguida, o
técnico adicionou água destilada até a marca do balão, correspondente a 250mL. Determine a
concentração em mol/L da solução. (Cu = 63,5 , S = 32, O = 16, H = 1)
14. Em uma emergência, um técnico de hospital preparou soro glicosado, dissolvendo 108g de
glicose em água suficiente para 2,0 litros de solução. Determine a concentração em mol/L de
glicose no soro obtido. (Glicose = 180 g/mol)
15. Em um balão volumétrico de 500 mL colocaram-se 9,5g de cloreto de magnésio e completou-
se o volume com água destilada. Sabendo-se que o cloreto de magnésio foi totalmente dissolvido,
assinale a concentração aproximada do íon magnésio nessa solução: Dados: Mg = 24; Cl = 35,5
REVISANDO – 2º ANO- QUIMICA – EVI WEBER – 11/03/23
a) 0,05 mol/L. b) 0,1 mol/L. c) 0,2 mol/L. d) 0,4 mol/L.
16. Foi preparada uma solução de 1000 mL com 148g de carbonato de lítio. A molaridade (mol/L)
dessa solução é: Dados: Li = 7 g/mol; C = 12 g/mol; 16 g/mol.
a) 0,002 mol/L. b) 0,2 mol/L. c) 2 mol/L. d) 5 mol/L. e) 20 mol/L.
17. Prepara-se uma solução, dissolvendo 16,4g de acetato de sódio (CH3COONa) em água e
elevando o volume para 500 mL. A molaridade da solução obtida é: Dados: H = 1 u; C = 12 u;
Na = 23 u; O = 16 u.
a) 0,2 mol/L. b) 0,4 mol/L. c) 0,8 mol/L. d) 1,6 mol/L. e) 2,0 mol/L.
18. Um químico preparou uma solução de carbonato de sódio (Na2CO3) pesando 53g do sal,
dissolvendo e completando o volume para 2 litros. A molaridade da solução preparada foi de:
Dados: C = 12 u; O = 16 u; Na = 23 u
a) 1,00 mol/L. b) 0,50 mol/L. c) 0,25 mol/L. d) 0,125 mol/L. e) 0,0625 mol/L.
19. São dissolvidos 19,6g de H2SO4 em água suficiente para 800 mL de solução. Qual é a
molaridade dessa solução? Dados: H = 1 u; O = 16 u; S = 32 u
a) 0,25 mol / L. b) 2,5 mol / L. c) 0,025 mol / L. d) 0,50 mol / L. e) 5,0 mol / L.
Gabarito
1. 27
2. 25
3. 03
4. 09
5. 07
6. 06
7. 60
8. 09
9. C
10. C
11. C
12. SIM 1.10-4
13. 0,8M
14. 0,3M
15. C
16. C
17. B
18. C
19. A
Você também pode gostar
- Engenharia Mecânica Química ExercíciosDocumento4 páginasEngenharia Mecânica Química ExercíciosPedro FerreiraAinda não há avaliações
- Aula Pratica 3Documento5 páginasAula Pratica 3Zeferino ReisAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Exerc Cálc Quím2009Documento4 páginasExerc Cálc Quím2009lurianmcAinda não há avaliações
- Introducao AQuantitativos - 094338Documento2 páginasIntroducao AQuantitativos - 094338Francisco silva cossaAinda não há avaliações
- Tratamento de Lodos de Estações de Tratamento de ÁguaNo EverandTratamento de Lodos de Estações de Tratamento de ÁguaAinda não há avaliações
- Teoria atômico-molecularDocumento4 páginasTeoria atômico-molecularmeninoAinda não há avaliações
- Potenciometria: aspectos teóricos e práticosNo EverandPotenciometria: aspectos teóricos e práticosAinda não há avaliações
- Lista de Exercícios IIDocumento6 páginasLista de Exercícios IIIgor Ferreira da SilvaAinda não há avaliações
- Calculo Estequiometrico ExcessoDocumento16 páginasCalculo Estequiometrico ExcessoJorge Henrique DiasAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- Lista 1 Leis PonderaisDocumento3 páginasLista 1 Leis PonderaisJoão Vitor Lanzarini0% (1)
- Lista de exercícios de química com equilíbrio químico, ácido-base e eletroquímicaDocumento3 páginasLista de exercícios de química com equilíbrio químico, ácido-base e eletroquímicaAlmeida Malembe100% (1)
- Exercícios de Cálculos Químicos e TermodinâmicaDocumento6 páginasExercícios de Cálculos Químicos e TermodinâmicaFernanda Abbate dos SantosAinda não há avaliações
- Avaliação Quimica 160623Documento7 páginasAvaliação Quimica 160623LMM LMMAinda não há avaliações
- Estequiometria - Exercícios BásicosDocumento7 páginasEstequiometria - Exercícios BásicosisadorarochamirandaAinda não há avaliações
- 686131-TD 3 - Unidade 3 e 4 - Estequiometria e Gases Ideais PDFDocumento3 páginas686131-TD 3 - Unidade 3 e 4 - Estequiometria e Gases Ideais PDFOcaras PitombeiraAinda não há avaliações
- Jan2024 - Apostila de Exercícios QuímicaDocumento4 páginasJan2024 - Apostila de Exercícios Químicagabrieleduardo20066Ainda não há avaliações
- 2a Lista de ExercíciosDocumento6 páginas2a Lista de Exercíciosramon7789Ainda não há avaliações
- Exercicios 2012 Aulas1a5Documento6 páginasExercicios 2012 Aulas1a5Filipe GrahlAinda não há avaliações
- Estequiometria-Exerc CiosDocumento8 páginasEstequiometria-Exerc CiosViriato Ricardo AzevedoAinda não há avaliações
- 1.1 - Cálculos Estequimétricos PDFDocumento5 páginas1.1 - Cálculos Estequimétricos PDFPedro SilvaAinda não há avaliações
- EstequiometriaDocumento4 páginasEstequiometriaBeatriz LimaAinda não há avaliações
- 3 Lista Exercicios 2020 (Solidos e Solucoes) V 03Documento4 páginas3 Lista Exercicios 2020 (Solidos e Solucoes) V 03Guilherme BarbosaAinda não há avaliações
- 1 EstequiometriaDocumento9 páginas1 EstequiometriaCarlos Ramon Andrade de OliveiraAinda não há avaliações
- Átomos, moléculas e o mol: uma introduçãoDocumento98 páginasÁtomos, moléculas e o mol: uma introduçãoJanaina Rigotti KubiszeskiAinda não há avaliações
- Cálculos químicos e reações de decomposição térmicaDocumento2 páginasCálculos químicos e reações de decomposição térmicaJackson Monteiro de BarrosAinda não há avaliações
- UFCG - CES - UAE Química Geral e InorgânicaDocumento6 páginasUFCG - CES - UAE Química Geral e InorgânicaArthurGrafdeSousaAinda não há avaliações
- Quimica AnaliicaDocumento8 páginasQuimica AnaliicaCamila MoreiraAinda não há avaliações
- Lista de Exercícios de Química GeralDocumento5 páginasLista de Exercícios de Química GeralLeonardo CarneiroAinda não há avaliações
- Gama - Módulo 16Documento23 páginasGama - Módulo 16lucas2308Ainda não há avaliações
- 2 A Listade Exercicios Quimica Geral 2014Documento2 páginas2 A Listade Exercicios Quimica Geral 2014Viviane CamargoAinda não há avaliações
- Lista 10 Geral 2023-2Documento6 páginasLista 10 Geral 2023-2yjb46zys2hAinda não há avaliações
- ESTEQUIOMETRIA E TERMOQUÍMICADocumento13 páginasESTEQUIOMETRIA E TERMOQUÍMICARafaela De Lima FrançaAinda não há avaliações
- Lista GasesDocumento3 páginasLista GasesEmannuel SousaAinda não há avaliações
- A) 35 B) 34 C) 33 D) 32 E) 31: Atividade de Química 2 1º TRIMESTRE/2023Documento5 páginasA) 35 B) 34 C) 33 D) 32 E) 31: Atividade de Química 2 1º TRIMESTRE/2023Ágata Ferreira S.1.T.10Ainda não há avaliações
- Lista Química 2º (A, B, C e D)Documento4 páginasLista Química 2º (A, B, C e D)wwwisaque18Ainda não há avaliações
- Lista de Exercícios 1 - QuímicaDocumento15 páginasLista de Exercícios 1 - QuímicaDianderson ChristianoAinda não há avaliações
- Lista 2 - Cálculo EstequiométricoDocumento17 páginasLista 2 - Cálculo EstequiométricomarinaandthediamondsAinda não há avaliações
- Exercicios Sobre EstequeometriaDocumento18 páginasExercicios Sobre EstequeometriaRicardo BrunoAinda não há avaliações
- Lista de Exerccio 4 - 2VADocumento3 páginasLista de Exerccio 4 - 2VAmonyyyeAinda não há avaliações
- Gases 2015Documento9 páginasGases 2015Welff JuniorAinda não há avaliações
- Exercícios de Estequiometria e RendimentoDocumento1 páginaExercícios de Estequiometria e RendimentoRoberto Almeida FerreiraAinda não há avaliações
- Lista 2 ANO1 BIDocumento1 páginaLista 2 ANO1 BIgabicrisos2501Ainda não há avaliações
- Exercicios Gases TermoquimicaDocumento4 páginasExercicios Gases TermoquimicaDaniel ArrudaAinda não há avaliações
- 1 Lista de Exercícios - Estequiometria - IQG114Documento4 páginas1 Lista de Exercícios - Estequiometria - IQG114Sonya KarlaAinda não há avaliações
- Exerc Equil-Analitica222Documento4 páginasExerc Equil-Analitica222JefferoiAinda não há avaliações
- Rendimento, Pureza e ReagentesDocumento15 páginasRendimento, Pureza e ReagentesJoana FerreiraAinda não há avaliações
- Ensino Médio - Exercícios de QuímicaDocumento6 páginasEnsino Médio - Exercícios de QuímicaBarbara Chagas0% (1)
- Lista de Exercícios Equlíbrio QuímicoDocumento2 páginasLista de Exercícios Equlíbrio QuímicoBrandie ThompsonAinda não há avaliações
- Lista de Exercícios GasesDocumento2 páginasLista de Exercícios GasesalvaroAinda não há avaliações
- Lista de Exercícios 2 - EstequiometriaDocumento5 páginasLista de Exercícios 2 - EstequiometriaKeveny SouzaAinda não há avaliações
- Lista 04Documento3 páginasLista 04Nicole PacíficoAinda não há avaliações
- Revisão 2 Bimestral Química IiDocumento6 páginasRevisão 2 Bimestral Química IiCanal Da MusicaAinda não há avaliações
- Equilíbrios químicos e iônicosDocumento4 páginasEquilíbrios químicos e iônicosmailas33Ainda não há avaliações
- Exercícios Cálculo Estequiométrico 2014Documento24 páginasExercícios Cálculo Estequiométrico 2014João Ribeiro Franco Neto0% (1)
- Anexo II - Relação de ConvidadosDocumento1 páginaAnexo II - Relação de ConvidadosAlana WolfAinda não há avaliações
- Anexo I - Orçamento 062024 (A 34) - Termo de RefêrenciaDocumento17 páginasAnexo I - Orçamento 062024 (A 34) - Termo de RefêrenciaAlana WolfAinda não há avaliações
- EXTENSIVO - SEMI - Tema 13-2023 - Resumo - PL Das Fake NewsDocumento2 páginasEXTENSIVO - SEMI - Tema 13-2023 - Resumo - PL Das Fake NewsAlana WolfAinda não há avaliações
- Estrutura Da RedaçãoDocumento1 páginaEstrutura Da RedaçãoAlana WolfAinda não há avaliações
- Tema IaDocumento1 páginaTema IaAlana WolfAinda não há avaliações
- Guia Do Aluno Alfa 2024 Ensino Médio 3 ANODocumento12 páginasGuia Do Aluno Alfa 2024 Ensino Médio 3 ANOAlana WolfAinda não há avaliações
- Procura-Se Um Namorado (Alexis Hall)Documento482 páginasProcura-Se Um Namorado (Alexis Hall)Maria Clara Morais Brito100% (2)
- Social InvestigativoDocumento22 páginasSocial InvestigativoCamilly PascoalAinda não há avaliações
- Guia Do Aluno Alfa 2024 Ensino Médio 3 ANODocumento12 páginasGuia Do Aluno Alfa 2024 Ensino Médio 3 ANOAlana WolfAinda não há avaliações
- Organic - Química Orgânica II - 2005 - Constantino PDFDocumento558 páginasOrganic - Química Orgânica II - 2005 - Constantino PDFÉrik Eduardo Pereira de OliveiraAinda não há avaliações
- Estudo Dirigido Cálculo NuméricoDocumento3 páginasEstudo Dirigido Cálculo NuméricoRogerio SantosAinda não há avaliações
- Anuario 2012Documento260 páginasAnuario 2012Geny Kucher100% (1)
- Aula - Cultura Do Milho (Cont.)Documento32 páginasAula - Cultura Do Milho (Cont.)Ricardo SaydAinda não há avaliações
- AULA 1 Historia e Evolucao e Princípios Da HomeopatiaDocumento30 páginasAULA 1 Historia e Evolucao e Princípios Da HomeopatiaJacqueline MarconatoAinda não há avaliações
- Estágio na Educação InfantilDocumento5 páginasEstágio na Educação InfantilFERNANDA COSTAAinda não há avaliações
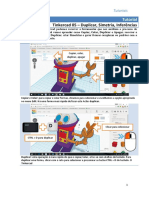
- Tinkercad 05 – Copiar, duplicar, simetria, inferênciasDocumento5 páginasTinkercad 05 – Copiar, duplicar, simetria, inferênciasEdson Pires da SilvaAinda não há avaliações
- Leis Fundamentais de Reações QuímicasDocumento6 páginasLeis Fundamentais de Reações QuímicasNicolas Diderot Fontenele BeanAinda não há avaliações
- Ensinar compartilhando sonhosDocumento228 páginasEnsinar compartilhando sonhosAna Paula da Cunha GóesAinda não há avaliações
- Artigo Kwon and Wertz, 2015 2Documento18 páginasArtigo Kwon and Wertz, 2015 2cleverton limaAinda não há avaliações
- EBF MOB Roteiros para As LiçõesDocumento17 páginasEBF MOB Roteiros para As LiçõesGabryelle MayaraAinda não há avaliações
- Teorias da ComunicaçãoDocumento25 páginasTeorias da ComunicaçãoMiguel MorgadoAinda não há avaliações
- Propriedades minerais na Sesmaria da Câmara Municipal de Ouro PretoDocumento12 páginasPropriedades minerais na Sesmaria da Câmara Municipal de Ouro PretoGABRIEL LUZ DE OLIVEIRAAinda não há avaliações
- Aol 1 Tec MedDocumento11 páginasAol 1 Tec MedBrunellesche100% (3)
- Proteção em máquinas e equipamentosDocumento47 páginasProteção em máquinas e equipamentosDiico MarcondesAinda não há avaliações
- Teorias e concepções de currículoDocumento21 páginasTeorias e concepções de currículoKaIque Stefanno100% (2)
- ApostilajurossimplesDocumento16 páginasApostilajurossimplesJamilsonMedeirosAinda não há avaliações
- Bypass de Células Carga-FibrasDocumento5 páginasBypass de Células Carga-FibrasJoão VictorAinda não há avaliações
- Sistema para Livraria ResolveDocumento2 páginasSistema para Livraria ResolveNatália LavraAinda não há avaliações
- Niquice - Testes de HipoteseDocumento14 páginasNiquice - Testes de Hipoteseluis cassimooAinda não há avaliações
- Cartas de Instrumentos da Aeronáutica BrasileiraDocumento92 páginasCartas de Instrumentos da Aeronáutica Brasileiraomulato010% (1)
- Discente David Bizarro - Atividade Contextualizada AV1Documento5 páginasDiscente David Bizarro - Atividade Contextualizada AV1David Salomão Pinto Castanho BizarroAinda não há avaliações
- Frigelar - Orçamento 30642191-1Documento3 páginasFrigelar - Orçamento 30642191-1joserosineiassisdasilvaAinda não há avaliações
- Jessica Trapp - Mestre Da SeduçãoDocumento248 páginasJessica Trapp - Mestre Da SeduçãoHelton Mabote100% (1)
- Representações históricas do Egito Antigo: influências midiáticas e transformações escolaresDocumento142 páginasRepresentações históricas do Egito Antigo: influências midiáticas e transformações escolaresDaniel NunesAinda não há avaliações
- Radiação Térmica - Fundamentos Da Transferência de CalorDocumento35 páginasRadiação Térmica - Fundamentos Da Transferência de CalorOsvaldo Damazio NetoAinda não há avaliações
- Aula - 05 Ética e Reprodução AssistidaDocumento29 páginasAula - 05 Ética e Reprodução AssistidaDinisAinda não há avaliações
- A Autora Anna Augusta de Almeida NovvaDocumento1 páginaA Autora Anna Augusta de Almeida NovvaMaria Candida100% (1)
- 2 Atividades Do Capítulo 3Documento7 páginas2 Atividades Do Capítulo 3Jackelini Muzy VazAinda não há avaliações
- Manual Basico Construcao CasasDocumento30 páginasManual Basico Construcao Casasapi-3709444100% (11)
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- Biomecânica Básica dos Exercícios: Membros InferioresNo EverandBiomecânica Básica dos Exercícios: Membros InferioresNota: 3.5 de 5 estrelas3.5/5 (8)
- Inteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNo EverandInteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNota: 5 de 5 estrelas5/5 (3)
- 365 Ideias De Posts Para Ter Um Instagram De Sucesso!No Everand365 Ideias De Posts Para Ter Um Instagram De Sucesso!Ainda não há avaliações
- Dieta Anti-inflamatória EstratégicaNo EverandDieta Anti-inflamatória EstratégicaNota: 5 de 5 estrelas5/5 (2)
- Ser bom não é ser bonzinho: Como a comunicação não violenta e a arte do palhaço podem te ajudar a identificar e expressar as suas necessidades de maneira clara e autêntica – e evitar julgamentos, como o deste títuloNo EverandSer bom não é ser bonzinho: Como a comunicação não violenta e a arte do palhaço podem te ajudar a identificar e expressar as suas necessidades de maneira clara e autêntica – e evitar julgamentos, como o deste títuloNota: 5 de 5 estrelas5/5 (12)
- Uma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNo EverandUma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNota: 4 de 5 estrelas4/5 (13)
- Hormonios E Fisiculturismo - Uso De Substâncias Para Aumento De PerformanceNo EverandHormonios E Fisiculturismo - Uso De Substâncias Para Aumento De PerformanceAinda não há avaliações
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- Raciocínio lógico e matemática para concursos: Manual completoNo EverandRaciocínio lógico e matemática para concursos: Manual completoNota: 5 de 5 estrelas5/5 (1)