Escolar Documentos
Profissional Documentos
Cultura Documentos
100 Questoes de Calculo Estequiometrico PDF
100 Questoes de Calculo Estequiometrico PDF
Enviado por
Shi NaneTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
100 Questoes de Calculo Estequiometrico PDF
100 Questoes de Calculo Estequiometrico PDF
Enviado por
Shi NaneDireitos autorais:
Formatos disponíveis
100 questes de calculo estequiomtrico
TEXTO PARA A PRXIMA QUESTO
(Uerj) O cloro uma substncia simples e de grande importncia industrial. utilizado como desinfetante,
alvejante e na produo de inmeros compostos qumicos. Um deles, por exemplo, o 1,2 - dicloro etano,
obtido pela reao do cloro com o eteno.
A reao do dixido de mangans com cido clordrico um dos processos mais antigos para obteno de
cloro que, nas condies ambientes, um gs. Assim, os anncios de cloro lquido, que vemos freqentemente,
vendem, na realidade, uma soluo de hipoclorito de sdio.
1. Escreva a equao qumica correspondente obteno do 1,2 - dicloro etano e indique o tipo de mecanismo
da reao em funo da partcula reagente.
TEXTO PARA A PRXIMA QUESTO
(Ufrj) Na busca por combustveis mais "limpos", o hidrognio tem-se mostrado uma alternativa muito
promissora, pois sua utilizao no gera emisses poluentes. O esquema a seguir mostra a utilizao do
hidrognio em uma pilha eletroqumica, fornecendo energia eltrica a um motor.
2.
Um prottipo de carro movido a hidrognio foi submetido a um teste em uma pista de provas. Sabe-se que o
prottipo tem um tanque de combustvel (H) com capacidade igual a 164 litros e percorre 22 metros para cada
mol de H consumido. No incio do teste, a presso no tanque era de 600 atm e a temperatura, igual a 300 K.
Sabendo que, no final do teste, a presso no tanque era de 150 atm e a temperatura, igual a 300 K, calcule a
distncia, em km, percorrida pelo prottipo.
pag.1
100 questes de calculo estequiomtrico
TEXTO PARA AS PRXIMAS 2 QUESTES.
(Unicamp)
Vestibular, tempo de tenses, de alegrias, de surpresas... Nan e Chu formam um casal de
namorados. Eles esto prestando o Vestibular da Unicamp 2001. J passaram pela primeira fase e agora se
preparam para a etapa seguinte. Hoje resolveram rever a matria de Qumica. Arrumaram o material sobre a
mesa da sala e iniciaram o estudo:
- Ser que estamos preparados para esta prova? - pergunta Nan.
- Acho que sim! - responde Chu. - O fato de j sabermos que Qumica no se resume regra de trs e
decorao de frmulas nos d uma certa tranqilidade.
- Em grande parte graas nossa professora - observa Nan.
- Bem, vamos ao estudo!
3.
- Voc se lembra daquela questo da primeira fase, sobre a camada de cido orgnico que formava um
crculo sobre a gua? - diz Chu.
- Se lembro! - responde Nan. - Ns a resolvemos com certa facilidade pois conseguimos visualizar a
camada de molculas, usando a imaginao. E se a banca resolvesse continuar com esse tema na segunda
fase? - sugere Chu.
- Ser? - pergunta Nan.
- Bem, j que estamos estudando, vamos imaginar perguntas e depois respond-las.
- Por exemplo, na experincia relatada, formava-se uma nica camada do cido orgnico sobre a gua.
Hoje sabemos que se trata do cido olico, que tem uma dupla ligao na cadeia
(CH(CH)CH=CH(CH)COH, ou simplesmente R-COH).
Massas molares (g/mol): I = 253,8
a) Na experincia foram usados 1,410g de cido, que correspondem a aproximadamente 310 molculas.
Se essa quantidade de cido reagisse completamente com iodo, quantos gramas de iodo seriam gastos?
- Esta tranqila - vibra Chu! - Basta saber como o iodo reage com a molcula do cido olico e fazer
um clculo muito simples. Vamos ver uma outra questo que no envolva clculo!
b) Como ocorre a interao das molculas do cido olico com as da gua, na superfcie deste lquido?
pag.2
100 questes de calculo estequiomtrico
4.
- Que moleza! Est pensando o qu? Pergunta a que vou lhe fazer agora! - vibra Nan. - Vamos falar
um pouco de respirao.
- Respirao? - pergunta Chu. - Mas estamos estudando Qumica ou Biologia?
- Pois , mas os tomos e as molculas no sabem disso, e as reaes qumicas continuam ocorrendo
em todos os seres vivos - emenda Nan, continuando: - No corpo humano, por exemplo, o CO dos tecidos vai
para o sangue e o O do sangue vai para os tecidos. Quando o sangue alcana os pulmes, d-se a troca
inversa. O sangue contm, tambm, substncias que impedem a variao do pH, o que seria fatal ao indivduo.
Mesmo assim, pode ser observada pequena diferena de pH (da ordem de 0,04) entre o sangue arterial e o
venoso.
a) Utilizando equaes qumicas explique onde se pode esperar que o pH seja um pouco mais baixo: no sangue
arterial ou no venoso?
- Puxa! Nessa voc me pegou. Mas vou resolver - diz Chu.
Nan, porm, logo continua: - Quando em "repouso", liberamos nos pulmes, por minuto, cerca de
200mL de dixido de carbono oriundo do metabolismo, medida esta feita a temperatura ambiente (25C). Voc
est comendo po que podemos considerar, numa simplificao, como sendo apenas um polmero de glicose
(CHO). A massa dessa fatia de aproximadamente 18 gramas.
Massa molar (g/mol): CHO = 180
b) Seguindo esse raciocnio e admitindo, ainda, que a fatia se transforme em CO e gua, sendo o dixido de
carbono eliminado totalmente pela respirao, quantos minutos sero necessrios para que ela seja "queimada"
no organismo?
5. (Uff) Por muitos anos, os aborgenes da Austrlia usaram folhas de eucalipto para combater dores, em
particular, a de garganta. O componente ativo dessas folhas foi identificado como EUCALIPTOL, cuja massa
molar 154,0 g.
Ao se analisar uma amostra de eucaliptol com 3,16 g, encontrou-se o seguinte resultado: C=2,46g; H=0,37g;
O=0,33 g.
Considere essas informaes e determine:
a) a frmula molecular do eucaliptol;
b) a massa, em grama, de HO produzida na combusto completa da amostra.
6. (Uflavras) Um caminho-tanque derramou 4,9 toneladas de cido sulfrico numa estrada. Para que esse
cido no atinja uma lagoa prxima ao local do acidente e para amenizar os danos ecolgicos, jogou-se barrilha
(50%) sobre o cido sulfrico derramado (barrilha=NaCO).
a) Classifique a reao que ocorre entre o cido sulfrico e a barrilha, mostrando a equao qumica.
b) Qual a massa de barrilha (50%) necessria para neutralizar todo o cido derramado?
Massas molares (g/mol): HSO=98; NaCO=106.
pag.3
100 questes de calculo estequiomtrico
7. (Ufv) A reduo de permanganato (MnO), em meio cido, resulta em ons mangans(II). A equao no
balanceada da reao :
KMnO+Fe+HSOFeSO+MnSO+KSO+HO
a) Escreva a equao da reao devidamente BALANCEADA.
b) A quantidade de ferro metlico necessria para reduzir totalmente 0,2 mol de permanganato de potssio
_______ mol.
c) A quantidade de sulfato de mangans(II) obtida a partir de 0,2 mol de permanganato de potssio _______
mol.
8. (Fuvest) O equipamento de proteo conhecido como "air bag" usado em automveis, contm substncias
que se transformam, em determinadas condies, liberando N que infla um recipiente de plstico. As equaes
das reaes envolvidas no processo so:
2 NaN 2Na + 3N
10Na + 2KNO KO + 5NaO + N
a) Considerando que N gerado nas duas reaes, calcule a massa de azoteto de sdio (NaN) necessria
para que sejam gerados 80L de nitrognio, nas condies ambiente.
b) Os xidos formados, em contato com a pele, podem provocar queimaduras. Escreva a equao da reao de
um desses xidos com a gua contida na pele.
Dados: Volume molar de gs nas condies ambiente: 25 L/mol
massa molar do NaN: 65 g/mol
9. (Fuvest) ma jovem senhora, no querendo revelar sua idade, a no ser s suas melhores amigas, convidouas para a festa de aniversrio, no sto de sua casa, que mede 3,0 m x 2,0 m x 2,0 m. O bolo de aniversrio
tinha velas em nmero igual idade da jovem senhora, cada uma com 1,55 g de parafina. As velas foram
queimadas inteiramente, numa reao de combusto completa. Aps a queima, a porcentagem de gs
carbnico, em volume, no sto, medido nas condies-ambiente, aumentou de 0,88 %. Considere que esse
aumento resultou, exclusivamente, da combusto das velas.
Dados:
massa molar da parafina, CH:310 g mol; volume molar dos gases nas condies-ambiente de presso e
temperatura: 24 L mol.
a) Escreva a equao de combusto completa da parafina.
b) Calcule a quantidade de gs carbnico, em mols, no sto, aps a queima das velas.
c) Qual a idade da jovem senhora? Mostre os clculos.
pag.4
100 questes de calculo estequiomtrico
10. (Uerj) Uma das principais causas da poluio atmosfrica a queima de leos e carvo, que libera para o
ambiente gases sulfurados. A seqncia reacional abaixo demonstra um procedimento moderno de eliminao
de anidrido sulfuroso, que consiste em sua converso a gesso.
Calcule a massa de gesso, em gramas, que pode ser obtida a partir de 192g de anidrido sulfuroso,
considerando um rendimento de 100% no processo de converso.
11. (Uerj) O cido nicotnico e sua amida, a nicotinamida, so os componentes da vitamina B, fundamental no
metabolismo de glicdios. A frmula estrutural dessa amida pode ser obtida substituindo o grupo CH da posio
3 do anel benznico da fenil-metanamida por um tomo de nitrognio.
(Dados: C = 12; N = 14; H = 1; O = 16).
a) Apresente a frmula estrutural da nicotinamida.
b) Calcule o nmero de pessoas que, a partir de um mol de cido nicotnico, CHNO, podem receber uma
dose de 15 mg desse cido.
pag.5
100 questes de calculo estequiomtrico
12. (Ufal) A transformao de enxofre em trixido de enxofre se d em duas etapas:
Dados:
Massas moleculares (g/mol):
Enxofre ... 32
Oxignio ... 16
Calcule a massa de SO que pode ser obtida a partir de 64g de enxofre sabendo que a 1 reao representada
total e a 2 reao tem um rendimento de 50%, em mols, em relao ao SO.
13. (Ufes) A uma velocidade constante de 50km/h, um automvel faz cerca de 10km por litro de etanol
(CHOH). Considerando a queima total do combustvel, qual deve ser o volume de gs carbnico (CO) em
metros cbicos, lanado na atmosfera pelo automvel, aps 2 horas de viagem?
Considere:
densidade do lcool = 0,8 kg/L
massa molar do etanol = 46 g/mol
volume molar do CO = 25 L/mol
1 dm = 1L
14. (Uff) Sabe-se que a pureza do nitrato de amnio (NHNO) pode ser determinada por meio da reao entre
uma soluo do sal e uma soluo de NaOH. Assim, realizou-se um experimento com uma amostra do nitrato
preparado industrialmente. Verificou-se que 0,2041g do sal foram neutralizados com 24,42mL de uma soluo
de NaOH 0,1023 M.
Com base nestas informaes, calcule o percentual da pureza da amostra.
pag.6
100 questes de calculo estequiomtrico
15. (Uff) Um produto secundrio de um processo industrial consiste em uma mistura de sulfato de sdio
(NaSO) e hidrogenocarbonato de sdio (NaHCO).
Para determinar a composio da mistura, uma amostra de 8.00 g foi aquecida at que se alcanasse massa
constante. A reao durante o aquecimento foi completa. Nessas condies, o hidrogenocarbonato de sdio
sofre decomposio de acordo com a reao
2NaHCO(s) NaCO(s) + CO(g) + HO(g)
e o sulfato de sdio permanece inalterado. A massa da amostra aps o aquecimento foi 6,02 g.
Informe por meio de clculos:
a) o percentual de CO na mistura dos produtos gasosos
b) a massa de CO existente no item anterior
c) a massa de NaHCO que sofreu decomposio
d) a percentagem de NaHCO, na amostra
16. (Uflavras) A produo de gs amnia (NH) foi realizada em uma fbrica, reagindo-se 280kg de gs
nitrognio (N) e 60kg de gs hidrognio (H). Na presena de catalisador em condies adequadas, a reao
foi completa, sendo os reagentes totalmente convertidos no produto.
Pergunta-se:
a) Qual a equao balanceada que representa a reao entre os gases nitrognio e hidrognio, formando como
produto o gs amnia?
b) Qual seria o volume de gs amnia obtido nas CNTP (Condies Normais de Temperatura e Presso), se as
massas de reagentes e as condies de reao fossem as acima indicadas, porm com o gs nitrognio
possuindo 80% de pureza, considerando-se que a reao foi completa?
Massas molares (g/mol): N = 28,0; H = 2,0.
pag.7
100 questes de calculo estequiomtrico
17. (Ufrj) Um dos processos mais usados para purificar ouro consiste no borbulhamento de cloro gasoso
atravs de ouro impuro fundido. O ouro no reage com o cloro, enquanto os contaminantes so removidos na
forma de cloretos.
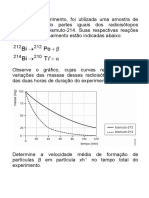
O grfico a seguir apresenta os dados de um processo de refino de uma liga de ouro que contm 8% em massa
de prata e 2% em massa de cobre, e relaciona o decaimento da quantidade dos contaminantes com o tempo de
reao.
Deseja-se refinar 1 kg dessa liga.
Calcule a massa de prata e de cobre metlicos presentes quando o processo atingir o tempo de meia-vida da
prata na reao de clorao.
18. (Ufrrj) Para plantar uma determinada cultura tem-se que acertar a quantidade de ons H do solo,
acrescentando-se uma quantidade de carbonato de clcio.
a) Qual a massa de carbonato de clcio necessria para a obteno de 168g de xido de clcio, a fim de fazer
o acerto da concentrao de H do solo ?
b) Qual o volume de CO obtido nas CNTP?
Dados:
Massas molares (g/mol): C = 12; O = 16; Ca = 40
19. (Ufsc) Para se determinar o contedo de cido acetilsaliclico (AAS) (CHO) num comprimido isento de
outras substncias cidas, 1,0 g do comprimido foi dissolvido numa mistura de etanol e gua. Essa soluo
consumiu 15 mL de soluo aquosa de NaOH, de concentrao 0,20 mol.L, para reao completa.
Ocorreu a seguinte transformao qumica:
CHO(aq) + NaOH(aq) CHONa(aq) + HO
Sabendo que a massa molar do cido acetilsaliclico (AAS) 180 g.mol, calcule a porcentagem (%) em massa
de AAS no comprimido.
pag.8
100 questes de calculo estequiomtrico
20. (Ufv) A benzamida pode ser preparada pela reao entre amnia e cloreto de benzola:
NH(aq)+CHOC() CHON(s)+HC(aq)
A 50mL de soluo de amnia concentrada (6,0mol.L) foram adicionados 14,05g de cloreto de benzola. A
benzamida produzida foi filtrada, lavada com gua fria e secada ao ar.
a) A quantidade de amnia presente nos 50mL da soluo anteriormente descrita ______ mol.
b) Nos 50mL de soluo de amnia h _________ molculas de amnia.
c) A massa molar do cloreto de benzola __________g.mol.
d) Em 14,05g de cloreto de benzola h __________mol de cloreto de benzola.
e) A massa molar da benzamida ______ g.mol.
f) Considerando 100% de rendimento, foram obtidos __________ g de benzamida.
pag.9
100 questes de calculo estequiomtrico
21. (Ufv) Na revista "Journal of Chemical Education" (maio de 2000) foi descrita uma experincia interessante e
de fcil execuo para a obteno da substncia iodeto de sdio, a partir de sdio metlico e iodo. Um tubo de
ensaio pequeno contendo iodo pendurado dentro de um tubo maior que contm o sdio metlico, conforme
ilustrado pela figura adiante.
Aquecendo-se o sistema, o sdio metlico se funde formando sdio lquido (e tambm vapor de sdio). O iodo,
por sua vez, se vaporiza e se desloca na direo do fundo do tubo maior.
No encontro das duas substncias ocorre vigorosa reao qumica, com emisso de luz e calor. O iodeto de
sdio slido se deposita nas paredes do tubo.
a) Escreva a equao balanceada para a reao qumica descrita anteriormente:
b) O tipo de ligao qumica existente entre os tomos de iodo no I __________.
c) O tipo de ligao qumica existente entre os tomos de sdio no cubo de Na __________.
d) O tipo de ligao qumica existente entre os tomos de sdio e iodo no iodeto de sdio __________.
e) Supondo que o sdio seja 90% puro e que a massa do cubinho de sdio seja igual a 2,60g, havendo iodo em
excesso, sero obtidos __________g de iodeto de sdio.
f) Conforme descrito no item anterior, o iodo estava presente em excesso. Foram consumidos _________g de
iodo.
pag.10
100 questes de calculo estequiomtrico
22. (Unesp) A "gua de lavadeira" uma soluo aquosa diluda de NaCO. Quando esta soluo tratada
com excesso de ons I em meio cido, os ons CO so reduzidos a C e os ons I so inicialmente oxidados
a I. O I formado reage imediatamente com o excesso de I presente, formando I. Nestas condies, a
equao global da reao, no balanceada, :
CO + I + H C + I + HO
a) Balanceie a equao, indicando os menores coeficientes estequiomtricos.
b) So necessrios 40,0 ml de soluo aquosa de KI de concentrao 2,50 mol/L, para reagir completamente
com 50,0g de gua de lavadeira, segundo a equao anterior. Calcule a porcentagem em massa de NaCO na
"gua de lavadeira".
(Massa molar de NaCO = 74,5 g/mol)
23. (Unesp) Hidreto de ltio pode ser preparado segundo a reao expressada pela equao qumica:
2Li(s) + H(g) 2LiH(s)
Admitindo que o volume de hidrognio medido nas condies normais de temperatura e presso (CNTP),
calcule:
a) a massa de hidreto de ltio que pode ser produzida na reao de 13,8g de ltio com 11,2L de hidrognio;
b) o rendimento (em porcentagem) da reao se, com as quantidades de reagentes acima indicadas, ocorrer a
formao de 6,32g de LiH.
Volume molar dos gases(CNTP) = 22,4L
Massas molares (g/mol): Li = 6,90; H = 1,00.
24. (Unesp) Estima-se que a quantidade de metanol capaz de provocar a morte de um ser humano adulto de
cerca de 48 g. O adoante aspartame (M[aspartame] = 294 gmol) pode, sob certas condies, reagir
produzindo metanol (M[metanol] = 32 gmol), cido asprtico (M[cido asprtico] = 133 gmol) e
fenilalanina, segundo a equao apresentada a seguir:
CHON + 2X
CHOH + CHON + CHON
a) Identifique o reagente X na equao qumica apresentada e calcule a massa molar da fenilalanina. (Dadas as
massas molares, em gmol: H = 1; C = 12; N = 14; O = 16.)
b) Havendo cerca de 200 mg de aspartame em uma lata de refrigerante light, calcule a quantidade mnima de
latas desse refrigerante necessria para colocar em risco a vida de um ser humano adulto. (Suponha que todo o
aspartame contido no refrigerante ser decomposto para a produo do metanol.)
pag.11
100 questes de calculo estequiomtrico
25. (Unesp) O carbeto de clcio (massa molar = 64 g.mol) - tambm conhecido como carbureto - pode ser
obtido aquecendo-se uma mistura de cal (CaO, massas molares Ca = 40 g.mol e O = 16 g.mol) e carvo (C,
massa molar = 12 g.mol) a uma temperatura de aproximadamente 3 000C, gerando um subproduto gasoso
com massa molar igual a 28 g.mol. O carbeto de clcio pode reagir com gua, produzindo acetileno (massa
molar = 26 g.mol) e hidrxido de clcio, sendo de uso comum nas carbureteiras, nas quais o gs que sai do
recipiente queimado para fins de iluminao, especialmente em cavernas.
a) Escreva a equao qumica que representa a reao de obteno do carbeto de clcio.
b) Que massa de carbeto de clcio necessria para a obteno de 13 g de acetileno?
26. (Unicamp) Em alguns fogos de artifcio, alumnio metlico em p queimado, libertando luz e calor. Este
fenmeno pode ser representado como:
2A(s)+(3/2)O(g)AO(s);
H= -1653kJ/mol
a) Qual o volume de O nas condies normais de temperatura e presso, necessrio para reagir com 1,0g do
metal?
b) Qual a quantidade de calor presso constante desprendida na reao de1,0g de alumnio?
Volume molar do gs ideal nas condies normais de temperatura e presso = 22,4 litros.
Massa atmica relativa do alumnio = 27
27. (Unicamp) A obteno de etanol, a partir de sacarose (acar) por fermentao, pode ser representada pela
seguinte equao:
CHO + HO 4CHOH + 4CO
Admitindo-se que o processo tenha rendimento de 100% e que o etanol seja anidro (puro), calcule a massa (em
kg) de acar necessria para produzir um volume de 50 litros de etanol, suficiente para encher um tanque de
um automvel.
Densidade do etanol = 0,8 g/cm
Massa molar da sacarose = 342 g/mol
Massa molar do etanol = 46 g/mol
28. (Unicamp) Duas amostras de carbono, C, de massas iguais, foram totalmente queimadas separadamente,
empregando-se oxignio, O, num dos casos, e oznio, O, no outro. Houve sempre combusto completa,
produzindo somente CO.
a) A massa de dixido de carbono, CO, que se forma, a mesma nos dois casos? Justifique sua resposta.
b) So iguais as quantidades, em moles, de O e de O consumidas nas duas reaes? Justifique sua resposta.
pag.12
100 questes de calculo estequiomtrico
29. (Unicamp) Determinar a poca em que o ser humano surgiu na Terra um assunto ainda bastante
polmico. No entanto, alguns acontecimentos importantes de sua existncia j esto bem estabelecidos, dentre
eles, o domnio do fogo e a descoberta e o uso dos metais.
J na pr-histria, o homem descobriu como trabalhar metais. Inicialmente o cobre, depois o estanho, o bronze
e o ouro. Por volta de 1500a.C., ele j trabalhava com o ferro. bem provvel que este metal tenha sido
encontrado nas cinzas de uma fogueira feita sobre algum minrio de ferro, possivelmente xidos de ferro (II) e
ferro (III). Estes xidos teriam sido quimicamente reduzidos a ferro metlico pelo monxido de carbono
originado na combusto parcial do carvo na chama da fogueira. Esse um processo bastante semelhante ao
que hoje se usa nos fornos das mais modernas indstrias siderrgicas.
a) Cite uma propriedade que possa ter levado o homem daquela poca a pensar que "aquilo diferente" junto s
cinzas da fogueira era um metal.
b) Suponha duas amostras de rochas, de mesma massa, reagindo com monxido de carbono, uma contendo
exclusivamente xido de ferro (II) e outra contendo exclusivamente xido de ferro (III). Qual delas possibilitaria a
obteno de mais ferro metlico ao final do processo? Justifique.
c) No caso do item b, escreva a frmula estrutural do principal subproduto do processo de produo do ferro
metlico.
30. (Unirio) A hidrazina, NH, e o perxido de hidrognio, HO, tm sido usados como combustveis de
foguetes. Eles reagem de acordo com a equao:
7HO + NH 2HNO + 8HO
A reao de hidrazina com 75% de pureza com perxido de hidrognio suficiente produziu 3,78kg de cido
ntrico, com rendimento de 80%.
(Dados: Massas atmicas: H=1u, O=16u; N=14u)
a) Determine a massa, em gramas, de hidrazina impura utilizada
b) Determine a massa, em gramas, de gua formada.
pag.13
100 questes de calculo estequiomtrico
31. (Unicamp) Com a inteno de proteger o motorista e o passageiro de leses corporais mais graves, em
muitos pases j obrigatrio, em automveis, o dispositivo chamado de "air bag". Em caso de acidente um
microprocessador desencadeia uma srie de reaes qumicas que liberam uma certa quantidade de
nitrognio, N(g), que infla rapidamente um balo plstico situado frente dos ocupantes do automvel. As
reaes qumicas que ocorrem nesse processo esto representadas pelas seguintes equaes:
Equao 1
2NaN(s) = 2Na(s) + 3N(g)
Equao 2
10Na(s) + 2KNO(s) = 5NaO(s) + KO(s) + N(g)
Equao 3
KO(s) + NaO(s) + SiO(s) = silicato alcalino
(vidro)
No caso de acionamento do sistema de segurana descrito, supondo que o volume do saco plstico, quando
totalmente inflado, seja de 70 litros e que, inicialmente, houvesse 2,0 moles de NaN e 2,0 moles de KNO.
a) Qual ser a presso do gs (em kPa), dentro do balo, quando este estiver totalmente inflado? Considere a
temperatura como sendo 27C.
Dado: R = 8,3 kPa L mol K; kPa = quilopascal
b) Supondo-se que o processo envolvesse apenas as reaes representadas pelas equaes 1 e 2, qual seria a
massa total de substncias slidas restantes no sistema?
Dados: Massas molares
KNO = 101,1 g.mol
NaO = 62 g.mol
KO = 94,2 g.mol
pag.14
100 questes de calculo estequiomtrico
32. (Unesp) Um estudante quer obter no laboratrio exatamente 14,9 g de cloreto de potssio slido. Ele tem,
sua disposio, trs solues de concentrao 0,500 mol/L, dos seguintes compostos:
I. carbonato de potssio,
II. hidrxido de potssio,
III. cido clordrico.
Escolha duas dessas solues, que permitam obter o composto desejado.
a) Escreva a equao qumica da reao correspondente.
b) Calcule as quantidades necessrias de cada soluo escolhida, em mL, para se obter a massa requerida de
KC, supondo rendimento de 100%.
Dado: Massa molar do KC = 74,5 g/mol.
33. (Ufrj) As regies mais favorveis para a obteno de cloreto de sdio a partir da gua do mar so as que
apresentam grande intensidade de insolao e ventos permanentes. Por esse motivo, a Regio dos Lagos do
Estado do Rio de Janeiro uma grande produtora de sal de cozinha.
a) Considerando que a concentrao de NaC na gua do mar 0,5M, determine quantos quilogramas de
NaC, no mximo, podem ser obtidos a partir de 6000L de gua do mar.
b) Alm de sua utilizao como sal de cozinha, o cloreto de sdio tambm empregado como matria-prima
para a produo, por eletrlise, de hidrxido de sdio e gs cloro, segundo a reao:
Determine, em quilogramas, a massa de gs cloro produzida a partir de 11,7kg de cloreto de sdio.
Dados: Na = 23 u; C = 35,5 u; O = 16 u; H = 1 u
pag.15
100 questes de calculo estequiomtrico
34. (Puc-rio) O processo de Haber para a sntese da amnia foi um grande avano em relao fixao de
nitrognio atmosfrico. No processo Haber, a sntese realizada em temperatura de 400 a 500C e presso de
200 a 600atm, utilizando um catalisador apropriado. A reao que ocorre :
N(g) + 3H (g) 2NH (g)
a) Calcule a constante de equilbrio para esta reao, sabendo que as concentraes dos reagentes e produto,
no equilbrio, foram medidas como sendo:
[N(g)]=0,15M; [H(g)]=1,00M; [NH(g)]=0,15M.
b) Supondo um rendimento de 100% para a reao, calcule a quantidade em gramas de amnia produzida,
partindo-se de 28g de N(g) e de um excesso de H(g).
Dados:
Massas molares
N = 28 g/mol
NH = 17 g/mol
TEXTO PARA A PRXIMA QUESTO
(Unirio) "O vazamento do produto MTBE (ter metil terc-butlico), ocorrido em uma tubulao da Petrobrs em
Guarajuba, distrito de Paracambi, na Baixada Fluminense, pode ter atingido o lenol fretico da regio. (...).
Segundo a Petrobrs, o vazamento que ocorreu est entre 100 e 1.000 litros. (...) O MTBE proibido no Brasil.
Toda a produo brasileira exportada para os Estados Unidos, onde empregado como aditivo na gasolina".
(JB, 2000)
Na verdade, a notcia nos remete a uma significativa preocupao ambiental e nesse sentido importante que
voc considere a reao de sntese a seguir.
CHOK + CHI CHO + KI
Partindo-se de 560 gramas de t-butxido de potssio e de 750 gramas de iodeto de metila.
H = 1u; C = 12u; O = 16u; K = 39u; I = 127u;
considerar dMTBE = 0,8 g/mL
35. Determine volume, em litros, de MTBE formado.
TEXTO PARA A PRXIMA QUESTO
(Enem) Na investigao forense, utiliza-se luminol, uma substncia que reage com o ferro presente na
hemoglobina do sangue, produzindo luz que permite visualizar locais contaminados com pequenas quantidades
de sangue, mesmo superfcies lavadas.
proposto que, na reao do luminol (I) em meio alcalino, na presena de perxido de hidrognio (II) e de um
metal de transio (M(n)), forma-se o composto 3-aminoftalato (III) que sofre uma relaxao dando origem ao
produto final da reao (IV), com liberao de energia (hv) e de gs nitrognio (N).
(Adaptado. "Qumica Nova", 25, n 6, 2002. pp. 1003-10)
pag.16
100 questes de calculo estequiomtrico
Dados: pesos moleculares:
Luminol = 177
3-aminoftalato = 164
36.
Na anlise de uma amostra biolgica para anlise forense, utilizou-se 54 g de luminol e perxido de hidrognio
em excesso, obtendo-se um rendimento final de 70 %.
Sendo assim, a quantidade do produto final (IV) formada na reao foi de
a) 123,9.
b) 114,8.
c) 86,0.
d) 35,0.
e) 16,2.
pag.17
100 questes de calculo estequiomtrico
TEXTO PARA A PRXIMA QUESTO
(Ufrs) SE NECESSRIO, ADOTE g = 10 m/s.
37. A combusto completa da glicose, CHO, responsvel pelo fornecimento de energia ao organismo
humano. Na combusto de 1,0 mol de glicose, o nmero de gramas de gua formado igual a
a) 6.
b) 12.
c) 18.
d) 108.
e) 180.
Dados: H = 1; O = 16; C = 12.
TEXTO PARA A PRXIMA QUESTO
(Puccamp)
Ao distncia, velocidade, comunicao, linha de montagem, triunfo das massas,
Holocausto: atravs das metforas e das realidades que marcaram esses cem ltimos anos, aparece a
verdadeira doena do progresso...
O sculo que chega ao fim o que presenciou o Holocausto, Hiroshima, os regimes dos Grandes
Irmos e dos Pequenos Pais, os massacres do Camboja e assim por diante. No um balano tranqilizador.
Mas o horror desses acontecimentos no reside apenas na quantidade, que, certamente, assustadora.
Nosso sculo o da acelerao tecnolgica e cientfica, que se operou e continua a se operar em
ritmos antes inconcebveis. Foram necessrios milhares de anos para passar do barco a remo caravela ou da
energia elica ao motor de exploso; e em algumas dcadas se passou do dirigvel ao avio, da hlice ao
turborreator e da ao foguete interplanetrio. Em algumas dezenas de anos, assistiu-se ao triunfo das teorias
revolucionrias de Einstein e a seu questionamento. O custo dessa acelerao da descoberta a
hiperespecializao. Estamos em via de viver a tragdia dos saberes separados: quanto mais os separamos,
tanto mais fcil submeter a cincia aos clculos do poder. Esse fenmeno est intimamente ligado ao fato de ter
sido neste sculo que os homens colocaram mais diretamente em questo a sobrevivncia do planeta. Um
excelente qumico pode imaginar um excelente desodorante, mas no possui mais o saber que lhe permitiria
dar-se conta de que seu produto ir provocar um buraco na camada de oznio.
O equivalente tecnolgico da separao dos saberes foi a linha de montagem. Nesta, cada um conhece
apenas uma fase do trabalho. Privado da satisfao de ver o produto acabado, cada um tambm liberado de
qualquer responsabilidade. Poderia produzir venenos sem que o soubesse - e isso ocorre com freqncia. Mas
a linha de montagem permite tambm fabricar aspirina em quantidade para o mundo todo. E rpido. Tudo se
passa num ritmo acelerado, desconhecido dos sculos anteriores. Sem essa acelerao, o Muro de Berlim
poderia ter durado milnios, como a Grande Muralha da China. bom que tudo se tenha resolvido no espao
de trinta anos, mas pagamos o preo dessa rapidez. Poderamos destruir o planeta num dia.
Nosso sculo foi o da comunicao instantnea, presenciou o triunfo da ao distncia. Hoje, apertase um boto e entra-se em comunicao com Pequim. Aperta-se um boto e um pas inteiro explode. Aperta-se
um boto e um foguete lanado a Marte. A ao distncia salva numerosas vidas, mas irresponsabiliza o
crime.
Cincia, tecnologia, comunicao, ao distncia, princpio da linha de montagem: tudo isso tornou
possvel o Holocausto. A perseguio racial e o genocdio no foram uma inveno de nosso sculo; herdamos
do passado o hbito de brandir a ameaa de um compl judeu para desviar o descontentamento dos
explorados. Mas o que torna to terrvel o genocdio nazista que foi rpido, tecnologicamente eficaz e buscou
pag.18
100 questes de calculo estequiomtrico
o consenso servindo-se das comunicaes de massa e do prestgio da cincia.
Foi fcil fazer passar por cincia uma teoria pseudocientfica porque, num regime de separao dos
saberes, o qumico que aplicava os gases asfixiantes no julgava necessrio ter opinies sobre a antropologia
fsica. O Holocausto foi possvel porque se podia aceit-lo e justific-lo sem ver seus resultados. Alm de um
nmero, afinal restrito, de pessoas responsveis e de executantes diretos (sdicos e loucos), milhes de outros
puderam colaborar distncia, realizando cada qual um gesto que nada tinha de aterrador.
Assim, este sculo soube fazer do melhor de si o pior de si. Tudo o que aconteceu de terrvel a seguir
no foi se no repetio, sem grande inovao.
O sculo do triunfo tecnolgico foi tambm o da descoberta da fragilidade. Um moinho de vento podia
ser reparado, mas o sistema do computador no tem defesa diante da m inteno de um garoto precoce. O
sculo est estressado porque no sabe de quem se deve defender, nem como: somos demasiado poderosos
para poder evitar nossos inimigos. Encontramos o meio de eliminar a sujeira, mas no o de eliminar os
resduos. Porque a sujeira nascia da indigncia, que podia ser reduzida, ao passo que os resduos (inclusive os
radioativos) nascem do bem-estar que ningum quer mais perder. Eis porque nosso sculo foi o da angstia e
da utopia de cur-la.
Espao, tempo, informao, crime, castigo, arrependimento, absolvio, indignao, esquecimento,
descoberta, crtica, nascimento, vida mais longa, morte... tudo em altssima velocidade. A um ritmo de STRESS.
Nosso sculo o do enfarte.
(Adaptado de Umberto Eco, Rpida Utopia. VEJA, 25 anos, Reflexes para o futuro. So Paulo, 1993).
38. Segundo determinados autores, a bomba atmica causadora da catstrofe em Hiroshima utilizou a fisso do
istopo U. A abundncia deste istopo no elemento urnio natural de apenas 0,7% contra 99,3% do istopo
U, que no fssil (% em tomos). Para a separao deles, primeiramente obtido o gs UF a partir de UO
slido, o que se d pelas transformaes:
UO(s) + 4HF(g) UF(s) + 2HO(g)
UF(s) + F(g) UF(g)
Sendo assim, cada mol de molculas UF obtido dessa forma poder originar por separao isotpica total,
uma quantidade do U igual a
a) 7 x 10 mol
b) 7 x 10 mol
c) 7 x 10 mol
d) 7 x 10 mol
e) 7 x 10 mol
TEXTO PARA A PRXIMA QUESTO
(Ufrn) Num balo de vidro, com dois litros de capacidade e hermeticamente fechado, encontra-se uma mistura
gasosa constituda por hidrognio (H), hlio (He) e oxignio (O), na qual existe 0,32 g de cada gs
componente, nas condies ambientais de temperatura e presso. A reao de formao de gua iniciada por
meio de uma fasca eltrica produzida no interior do balo.
pag.19
100 questes de calculo estequiomtrico
39. Na reao de formao de gua (HO), houve um excesso de reagente igual a
a) 0,02 mol de H.
b) 0,14 mol de H.
c) 0,08 mol de O.
d) 0,15 mol de O.
40. (Unirio) A seqncia de reaes adiante mostra a formao do cloreto de polivinila (PVC):
Supondo que a etapa de polimerao ocorra com rendimento de 100% e as demais, com rendimento de 50%, a
massa em gramas de PVC que se forma a partir de 11,20g de CaO, aproximadamente de:
Dados: MA (Ca=40 ; O=16 ; C=12 ; C=35,5 ; H=1)
a) 0,390 g.
b) 0,781 g.
c) 1,562 g.
d) 3,125 g.
e) 6,250 g.
41. (Cesgranrio) O HS reage com o SO segundo a reao:
2 HS + SO 3 S + 2 HO.
Assinale, entre as opes abaixo, aquela que indica o nmero mximo de mols de S que pode ser formado
quando se faz reagir 5 moles de HS com 2 mols de SO:
a) 3
b) 4
c) 6
d) 7,5
e) 15
pag.20
100 questes de calculo estequiomtrico
42. (Cesgranrio) O lcool etlico, CHOH, usado como combustvel, pode ser obtido industrialmente pela
fermentao da sacarose, representada simplificadamente pelas equaes:
CHO + HO 2CHO
2CHO 2CHOH + 2CO
Partindo-se de uma quantidade de caldo de cana, que contenha 500 kg de sacarose, e admitindo-se um
rendimento de 68,4%, a massa de lcool obtida em kg ser:
Dados:
C = 12
H=1
O = 16
a) 44
b) 46
c) 92
d) 107
e) 342
43. (Cesgranrio) Tem-se 200 litros de um gs natural composto por 95% de Metano e 5% de Etano.
Considerando o teor de Oxignio no ar igual a 20%, o volume de ar necessrio para queimar completamente a
mistura gasosa ser de:
a) 83 litros
b) 380 litros
c) 415 litros
d) 1660 litros
e) 2075 litros
44. (Cesgranrio) Uma pesquisa revelou que as indstrias do Rio Grande do Sul despejam, em conjunto, mais de
500.000 toneladas de poluentes atmosfricos por ano, obrigando cada um dos 9 milhes de habitantes daquele
estado a respirar, em mdia, alm do oxignio, 3kg de CO, 9kg de hidrocarbonetos, 13kg de xidos de
nitrognio, 12kg de derivados de enxofre e 14kg de poeira. Some-se a isso que os xidos de nitrognio e de
enxofre originam as chamadas chuvas cidas.
Se considerarmos que a queima de 1 tonelada de carvo libera enxofre suficiente para produzir na atmosfera
16kg de anidrido sulfrico, est correto afirmar que, numa reao completa dessa quantidade de SO com
gua, haver, no mximo, formao da seguinte massa, em kg, de HSO:
Dados:
Massas Molares (g/mol): H = 1,0, O = 16, S = 32
a) 28,7
b) 19,6
c) 15,5
d) 12,8
e) 10,4
pag.21
100 questes de calculo estequiomtrico
45. (Enem) O ferro pode ser obtido a partir da hematita, minrio rico em xido de ferro, pela reao com carvo
e oxignio. A tabela a seguir apresenta dados da anlise de minrio de ferro (hematita) obtido de vrias regies
da Serra de Carajs.
No processo de produo do ferro, a slica removida do minrio por reao com calcrio (CaCO). Sabe-se,
teoricamente (clculo estequiomtrico), que so necessrios 100g de calcrio para reagir com 60g de slica.
Dessa forma, pode-se prever que, para a remoo de toda a slica presente em 200 toneladas do minrio na
regio 1, a massa de calcrio necessria , aproximadamente, em toneladas, igual a:
a) 1,9.
b) 3,2.
c) 5,1.
d) 6,4.
e) 8,0.
46. (Enem) Para se obter 1,5 kg do dixido de urnio puro, matria-prima para a produo de combustvel
nuclear, necessrio extrair-se e tratar-se 1,0 tonelada de minrio. Assim, o rendimento (dado em % em
massa) do tratamento do minrio at chegar ao dixido de urnio puro de
a) 0,10 %.
b) 0,15 %.
c) 0,20 %.
d) 1,5 %.
e) 2,0 %.
pag.22
100 questes de calculo estequiomtrico
47. (Fatec) O carbeto de clcio pode ser empregado como gerador de gs acetileno ao reagir com gua. A
equao da reao :
CaC + 2HO CH + Ca(OH)
A quantidade mnima de carbeto de clcio, em gramas, necessria para produzir 5,6 metros cbicos de gs
acetileno, medidos nas condies normais de temperatura e presso (CNTP), :
Dados: Volume molar (nas CNTP) = 22,4dm/mol
Massas molares (em g/mol):
Ca = 40,0; O = 16,0; H = 1,0; C = 12,0
a) 1600
b) 3200
c) 6400
d) 16000
e) 32000
48. (Fatec) Uma das etapas do ciclo do nitrognio consiste na "nitrificao", isto , ons amnio NH presentes
na gua contida no solo so oxidados por certas bactrias, formando ons NO, que, por sua vez, se oxidam
facilmente a NO.
As equaes no balanceadas que representam essas transformaes so:
NH(aq) + O NO(aq) + H(aq) + HO
NO(aq) + O NO(aq)
Para que ocorra a formao de um mol de ons NO(aq), a partir dos ons NH(aq), a quantidade mnima
necessria, em mol, de oxignio de
a) 4
b) 2
c) 3/2
d) 1
e) 1/2
pag.23
100 questes de calculo estequiomtrico
49. (Fatec) Metanol um excelente combustvel que pode ser preparado pela reao entre monxido de
carbono e hidrognio, conforme a equao qumica
CO(g) + 2H(g) CHOH()
Supondo rendimento de 100% para a reao, quando se adicionam 336g de monxido de carbono a 60g de
hidrognio, devemos afirmar que o reagente em excesso e a massa mxima, em gramas, de metanol formada
so, respectivamente,
Dados:
massas molares g/mol: CO: 28; H: 2; CHOH:32
a) CO, 384.
b) CO, 396.
c) CO, 480.
d) H, 384.
e) H, 480.
50. (Fgv) Balanceando-se a reao
A (SO)+3 Ca(OH) y A(OH)+z CaSO
corretamente, obtm-se os valores de y e z.
Qual a massa necessria de Ca(OH) para reagir completamente com w quilogramas de A (SO)?
Dados:
Massas Molares de A(SO)=342g.mol ; Ca(OH)=74g.mol w=y+z
a) 3,25 quilogramas
b) 5,40 quilogramas
c) 4,62 quilogramas
d) 1,08 quilogramas
e) 67,57 gramas
51. (Fuvest) Nas estaes de tratamento de gua, eliminam-se as impurezas slidas em suspenso atravs do
arraste por flculos de hidrxido de alumnio, produzidos na reao representada por
A(SO) + 3Ca(OH) 2 A(OH) + 3CaSO
Para tratar 1,0x10m de gua foram adicionadas 17 toneladas de A(SO). Qual a massa de Ca(OH)
necessria para reagir completamente com esse sal?
a) 150 quilogramas.
b) 300 quilogramas.
c) 1,0 tonelada.
d) 11 toneladas.
e) 30 toneladas.Dados: massas molares
A(SO)= 342 g/mol
Ca(OH)= 74 g/mol
pag.24
100 questes de calculo estequiomtrico
52. (Fuvest) Um composto submetido decomposio produziu hidrognio (H) e silcio (Si) na proporo,
respectivamente, de 3,0g para 28,0g. No composto original, quantos tomos de hidrognio esto combinados
com um tomo de silcio?
Massas molares:
H = 2,0 g/mol
Si = 28,0 g/mol
a) 1
b) 2
c) 3
d) 4
e) 6
53. (Fuvest) Nas condies ambiente, foram realizados trs experimentos, com aparelhagem idntica, nos quais
se juntou NaCO slido, contido em uma bexiga murcha, a uma soluo aquosa de HC contida em um
erlenmeyer. As quantidades adicionadas foram:
Dado:
Massa molar do NaCO=106g/mol
Ao final dos experimentos, comparando-se os volumes das bexigas, observa-se que
a) a bexiga de E1 a mais cheia.
b) a bexiga de E2 a mais cheia.
c) a bexiga de E3 a mais cheia.
d) a bexiga de E1 a menos cheia.
e) as trs bexigas esto igualmente cheias.
pag.25
100 questes de calculo estequiomtrico
54. (Fuvest) Uma instalao petrolfera produz 12,8kg de SO por hora. A liberao desse gs poluente pode
ser evitada usando-se calcrio, o qual por decomposio fornece cal, que reage com o SO formando CaSO,
de acordo com as equaes:
CaCO(s) CaO(s) + CO(g)
CaO(s) + SO(g) CaSO(s)
Qual a massa mnima de calcrio (em kg), por dia, necessria para eliminar todo SO formado?
Suponha 100% de rendimento para as reaes.
Massas molares (g/mol)
CaCO.....100
SO..........64
a) 128
b) 240
c) 480
d) 720
e) 1200
55. (Fuvest) O tanque externo do nibus espacial Discovery carrega, separados, 1,20 10 L de hidrognio
lquido a - 253C e 0,55 10 L de oxignio lquido a - 183C. Nessas temperaturas, a densidade do hidrognio
34 mol/L (equivalente a 0,068 g/mL) e a do oxignio 37 mol/L (equivalente a 1,18 g/mL).
Considerando o uso que ser feito desses dois lquidos, suas quantidades (em mols), no tanque, so tais que
h
a) 100% de excesso de hidrognio.
b) 50% de excesso de hidrognio.
c) proporo estequiomtrica entre os dois.
d) 25% de excesso de oxignio.
e) 75% de excesso de oxignio.
Massa molar (g/mol)
H .......... 1,0
O ...........16
pag.26
100 questes de calculo estequiomtrico
56. (Fuvest-gv) O magnsio obtido da gua do mar por um processo que se inicia pela reao dos ons Mg
com xido de clcio, conforme:
Mg(aq)+CaO(s)+HO()Mg(OH)(s)+Ca(aq)
Sabendo-se que a concentrao de Mg no mar 0,054 mol/litro, a massa de CaO necessria para precipitar o
magnsio contido em 1,0 litro de gua do mar :
a) 3,0g
b) 40g
c) 56g
d) 2,1g
e) 0,24gDados: massas atmicas: H=1,0; O=16; Mg=24; Ca=40.
57. (G1) O anticido sal de frutas contm, dentre outros, bicarbonato de sdio que, em contato com a gua, se
decompe conforme a reao representada pela equao:
2 NaHCO NaO + 2 CO(g) + HO
H = + 32,8 kcal
De acordo com a reao correto afirmar que, na decomposio de 0,10 mol desse sal, ocorrer:
a) produo de 0,10 mol de xido de sdio.
b) formao de 6,02 10 molculas de gua.
c) liberao de 2,24 litros de gs carbnico nas CNTP.
d) liberao de 32,8 quilocalorias.
58. (Ita) Fazendo-se borbulhar gs cloro atravs de 1,0 litro de uma soluo de hidrxido de sdio, verificou-se
ao final do experimento que todo hidrxido de sdio foi consumido, e que na soluo resultante foram formados
2,5 mol de cloreto de sdio. Considerando que o volume da soluo no foi alterado durante todo o processo, e
que na temperatura em questo tenha ocorrido apenas a reao correspondente seguinte equao qumica,
no balanceada,
OH(aq) + C(g) C(aq) + CO(aq) + HO(),
qual deve ser a concentrao inicial do hidrxido de sdio?
a) 6,0 mol/L
b) 5,0 mol/L
c) 3,0 mol/L
d) 2,5 mol/L
e) 2,0 mol/L
pag.27
100 questes de calculo estequiomtrico
59. (Ita) Um estudante preparou uma MISTURA A, constituda dos seguintes slidos: cloreto de sdio, cloreto
de potssio e cloreto de brio. Numa primeira experincia, foi preparada uma soluo aquosa pela total
dissoluo de 34,10g da MISTURA A em gua destilada, a 25C, qual foi adicionada, a seguir, uma soluo
aquosa de nitrato de prata em excesso, obtendo-se 57,40g de um certo precipitado. Num segundo experimento,
foi preparada uma soluo aquosa pela total dissoluo de 6,82g da MISTURA A em gua destilada, a 25C,
qual foi adicionada, a seguir, uma soluo aquosa de sulfato de sdio em excesso, obtendo-se 4,66g de um
outro precipitado. Qual das opes a seguir apresenta o valor CORRETO da composio percentual, em
massa, da MISTURA A?
Massas molares (g/mol):
Na = 22,90; C = 35,45; K = 39,10
Ba = 137,33; S = 32,60; 0 = 16,00
Ag = 107,87
a) 17,2% de NaC, 21,8% de KC e 61,0% de BaC.
b) 21,8% de NaC, 17,2% de KC e 61,0% de BaC.
c) 61,0% de NaC, 21,8% de KC e 17,2% de BaC.
d) 21,8% de NaC, 61,0% de KC e 17,2% de BaC.
e) 61,0% de NaC, 17,2% de KC e 21,8% de BaC.
60. (Mackenzie) No ataque a 1,25g de calcrio (CaCO impuro), so consumidos 100ml de cido sulfrico
0,1mol/L. O nmero de mols de cido que reagem, a massa de sal que reage e a pureza do calcrio so,
respectivamente, iguais a:
(Massas Molares: HSO=98g/mol e CaCO=100g/mol)
a) 0,01 mol, 1,125 g e 90%
b) 0,1 mol, 0,025 g e 20%
c) 0,01 mol, 1,0 g e 80%
d) 0,1 mol, 1,25 g e 100 %
e) 0,1 mol, 0,125 g e 80%
61. (Puc-rio) Assinale a alternativa que indica a quantidade de N(g) produzida quando dois moles de NH()
so consumidos segundo a reao a seguir:
2NH() + NO () 3N (g) + 4HO ()
Dado: massa molar do N = 28 g/mol
a) 84 g.
b) 56 g.
c) 42 g.
d) 28 g.
e) 3 g.
pag.28
100 questes de calculo estequiomtrico
62. (Puc-rio) A combusto do etano ocorre segundo a reao a seguir:
CH (g) + 7/2 O (g) 2 CO (g) + 3 HO (g).
Quantos kg de CO so liberados a partir de 30kg de CH?
a) 22 kg.
b) 44 kg.
c) 60 kg.
d) 88 kg.
e) 120 kg.
63. (Puc-rio) Um dos gases responsveis pelo aquecimento da Terra o CO(g), presente na atmosfera.
Atendendo ao Protocolo de Kioto, uma das tecnologias empregadas na reduo dos teores deste gs est
baseada na seguinte reao:
CaO(s) + CO(g) Ca CO(s)
Se um determinado dispositivo contm 560 g de CaO(s), a massa de CO(g) que pode ser removida atravs
deste dispositivo :
a) 44g.
b) 100g.
c) 440g.
d) 560g.
e) 1.120g.Dentre as opes acima, qual apresenta o valor correto?Dados: Ca = 40; C = 12; O = 16.
64. (Puccamp) Carbonato de sdio reage com gua de cal formando carbonato de clcio, material pouco
solvel em gua. Na reao de 106kg de carbonato de sdio com excesso de gua de cal a massa de
carbonato de clcio produzida igual a:
Massas molares (g/mol)
H = 1; O = 16; Na = 23; C = 12; Ca = 40
a) 50,0 kg
b) 100 kg
c) 150 kg
d) 500 kg
e) 1000 kg
pag.29
100 questes de calculo estequiomtrico
65. (Pucmg) Sob condies apropriadas, gs acetileno (CH) e cido clordrico reagem para formar cloreto de
vinila, CHC. Essa substncia usada para produzir policloreto de vinila (P.V.C) plstico e foi considerada
recentemente carcinognica. A reao na formao do CHC pode ser representada pela equao:
CH + HC CHC
Quando se obtm 2 mols de cloreto de vinila, o volume de gs acetileno consumido, nas CNTP, igual a:
a) 11,2 L
b) 22,4 L
c) 33,6 L
d) 44,8 L
e) 89,2 L
66. (Pucmg) Um mtodo usado para obter o oxignio em laboratrio a decomposio trmica do cloreto de
potssio. Essa reao pode ser representada pela equao:
2KCO(s) 2KC(s) + 3O(g)
Com relao decomposio completa de 2mols de cloreto de potssio, CORRETO afirmar que:
a) as quantidades, em mol, de cada um dos produtos so iguais.
b) a massa de KCO(s) decomposta de 122,5g.
c) a massa de KC(s) obtida de 149,0 g.
d) a quantidade de O(g) produzida de 33,6 L nas CNTP.
e) a massa de O(g) produzida de 48 g.
67. (Pucmg) A gua oxigenada, usada para desinfeco e para clarear cabelos, decompe-se segundo a
equao:
HO HO + 1/2 O
Considerando a decomposio completa de 500mL de HO e 3,4% p/v, o volume de gs oxignio, em litros,
produzido nas CNTP, igual a:
a) 1,12
b) 2,24
c) 5,60
d) 22,40
e) 112,0
pag.30
100 questes de calculo estequiomtrico
68. (Pucmg) A uria - CO(NH) - uma substncia utilizada como fertilizante e obtida pela reao entre o gs
carbnico e amnia, conforme a equao:
CO(g) + 2 NH(g) CO(NH)(s) + HO(g)
Sabendo-se que 89,6 litros de gs amnia reagem completamente no processo com o gs carbnico, nas
CNTP, a massa de uria, obtida em gramas, igual a:
a) 240,0
b) 180,0
c) 120,0
d) 60,0
Dados: C= 12; N = 14; O = 16; H = 1.
69. (Pucmg) A fluoretao de guas utilizada para diminuir a incidncia de cries na populao. Um dos
compostos utilizados para esse fim o fluoreto de sdio (NaF). Sabe-se que a gua para consumo apresenta,
aproximadamente, uma concentrao de on fluoreto igual a 1 mg/L. Assinale a massa, em gramas, de fluoreto
de sdio necessria para fluoretar 38.000 litros de gua para consumo.
a) 8,4
b) 16,8
c) 84,0
d) 168,0
Dados: Na = 23; F = 19.
70. (Pucmg) Nas usinas siderrgicas, a obteno do ferro metlico, Fe (MM = 56 g.mol), a partir da hematita,
FeO (MM = 160 g.mol), envolve a seguinte equao, no balanceada:
FeO(s) + CO(g) Fe(s) +CO(g)
Assinale a massa de ferro metlico, em gramas, obtida quando se faz reagir 200 kg de hematita, que apresenta
20 % de impurezas.
a) 5,60 10
b) 1,12 10
c) 5,60 10
d) 1,12 10
pag.31
100 questes de calculo estequiomtrico
71. (Pucpr) Dados:
M(Na) = 23,00 g/mol M(S) = 32,00 g/mol
M(O) = 16,00 g/mol M(H) = 1,00 g/mol
As quantidades de hidrxido de sdio e cido sulfrico necessrias para a obteno de 72,5 g de sulfato de
sdio so, respectivamente:
a) 38,7 g e 33,8 g
b) 40,8 g e 50,0 g
c) 20,4 g e 60,0 g
d) 36,2 g e 54,0 g
e) 30,0 g e 42,5 g
72. (Pucsp) A reao entre o gs nitrognio (N) e o gs hidrognio (H) produz o gs amnia (NH). Em um
recipiente fechado de 10L, a 800K, foram colocados 5mol de N e 20mol de H. Considerando que o rendimento
dessa reao nessas condies de 40% e que no houve variao de temperatura, a relao entre a presso
final e inicial do sistema
a) Pf = 0,84 Pi
b) Pf = Pi
c) Pf = 1,19 Pi
d) Pf = 0,4 Pi
e) Pf = 0,6 Pi
73. (Pucsp) A aluminotermia um processo para se obter metais a partir dos seus xidos. Ao reagirmos xido
de zinco (ZnO) com alumnio metlico (A), obtemos xido de alumnio (AO) e Zn metlico segundo a
equao:
3ZnO(s) + 2A(s) AO(s) + 3Zn(s)
A proporo entre as massas dos reagentes melhor representada pelo grfico
pag.32
100 questes de calculo estequiomtrico
74. (Uece) A massa de carbonato de clcio formado ao reagirmos completamente 14,8 g de hidrxido de clcio
aquoso com gs carbnico ser de:
Dados:
Ca = 40
C = 12
O = 16
H=1
a) 33,6 g
b) 74,0 g
c) 20,0 g
d) 100,0 g
75. (Uel) Que quantidade de NaOH, em mols, necessrio para neutralizar 15,0g de cido actico?
(Dado: massa molar do cido actico = 60g/mol)
a) 0,25
b) 0,30
c) 0,35
d) 0,40
e) 0,45
76. (Uel) Mg (s) + 2Ag (aq) Mg (aq) + 2Ag (s)
Que quantidade de Mg(s), em mols, reage com 4,0mols de Ag(aq)?
a) 1,0
b) 2,0
c) 3,0
d) 4,0
e) 8,0
77. (Uel) A oxidao, pela ao do oxignio do ar, de minrio de zinco contendo 95,5% de ZnS produz xido de
zinco. A reduo deste xido, pelo carvo, produz o metal livre. Dessa maneira, admitindo um processo de
obteno de zinco com rendimento total, que massa desse metal obtida a partir de 100kg desse minrio?
Dados:
Massa atmicas (g/mol)
zinco .......... 63,5
enxofre ....... 32,0
a) 95,5 kg
b) 63,5 kg
c) 52,5 kg
d) 40,0 kg
e) 32,0 kg
pag.33
100 questes de calculo estequiomtrico
78. (Uel) O rendimento do processo de obteno do formaldedo (constituinte da soluo aquosa conhecida
como formol) a partir do metanol, por reao com O em presena de prata como catalisador da ordem de
90%, em massa. Sendo assim, a massa do aldedo obtida pela oxidao de 3,2kg de metanol
Dados:
O outro produto da oxidao do metanol gua.
Massas molares (g/mol)
H = 1,0; C = 12,0; O = 16,0
a) 0,90 kg
b) 1,2 kg
c) 2,4 kg
d) 2,7 kg
e) 3,2 kg
79. (Uerj) - Uma rea agrcola, prxima a um lago, precisa ser adubada antes do incio do plantio de hortalias.
- O esquema da figura 1 indica as medidas do terreno a ser plantado. Os dois lados paralelos distam 10 km e os
trs ngulos obtusos indicados so congruentes.
- Para corrigir a elevada acidez do solo, o produto recomendado foi o calcrio (CaCO), na dosagem de 5 g/m
de solo.
- Para a adubao do terreno, emprega-se um pulverizador com 40 m de comprimento, abastecido por um
reservatrio de volume igual a 2,16 m, que libera o adubo vazo constante de 1.200 cm/s. Esse conjunto,
rebocado por um trator que se desloca velocidade constante de 1 m/s, est representado na figura 2.
- A partir do incio da adubao, a qualidade da gua do lago passou a ser avaliada com regularidade.
Para corrigir a acidez do solo, a quantidade de matria necessria, em mol de CaCO, por km de rea a ser
plantada, corresponde a:
a) 4,0 10
b) 5,0 10
c) 1,5 10
d) 2,5 10
pag.34
100 questes de calculo estequiomtrico
80. (Ufc) Quando o dixido de enxofre reage com cloro (ambos gasosos), originam-se dois produtos: o cloreto
de tionila (SOC) e o monxido de cloro (OC). Com relao a essa reao, correto afirmar que:
a) o SOC possui geometria molecular em gangorra.
b) um cido de Bronsted reage com uma base de Bronsted.
c) o oxignio possui maior raio atmico entre os elementos presentes.
d) o enxofre varia seu estado de oxidao de -4 nos reagentes para +4 nos produtos.
e) o cloro o reagente limitante quando 12,8 g de dixido de enxofre reagem com 14,2 g de cloro com 100 %
de rendimento.
81. (Ufes) A reao entre o cido actico e o lcool etlico na presena de cido sulfrico (catalisador) produz
gua e o acetato de etila, solvente muito utilizado na indstria de tintas. Sabendo-se que essa reao tem um
rendimento de 70%, a massa de lcool necessria para se produzir 440g do acetato ser aproximadamente
Massas molares (g/mol): H=1,0; C=12,0; O=16,0
a) 230 g
b) 237 g
c) 327 g
d) 440 g
e) 628 g
82. (Uff) Para produzir 4,48 L de CO nas CNTP, conforme a reao
CaCO CaO + CO
a quantidade necessria, em gramas, de CaCO :
Dado:
Massa molar CaCO = 100 g/mol
a) 20,0
b) 10,0
c) 100,0
d) 200,0
e) 18,3
83. (Ufla) Uma clula de combustvel (hidrognio-oxignio) tem as funes de fornecer eletricidade e gua
potvel em um nibus espacial. Os projetistas da misso sabem quanto de gua formada quando certa
quantidade de O reage com o H.
A equao qumica para a reao
2H(g) + O(g) 2HO() + Energia
Quando 0,25 mol de O reage com H, a quantidade de gua formada
a) 18,0 g
b) 36,0 g
c) 4,5 g
d) 9,0 g
e) 2,0 g
pag.35
100 questes de calculo estequiomtrico
84. (Ufpe) Um pedao de ferro pesando 5,60 gramas sofreu corroso quando exposto ao ar mido por um
perodo prolongado. A camada de ferrugem formada foi removida e pesada, tendo sido encontrado o valor de
1,60 gramas. Sabendo-se que a ferrugem tem a composio FeO, quantos gramas de ferro no corrodo
ainda restaram? Considere Fe=56,0g/mol e FeO=160,0g/mol
a) 2,40 g
b) 4,48 g
c) 5,32 g
d) 5,04 g
e) 4,00 g
85. (Ufpe) Nas usinas siderrgicas, a obteno de ferro metlico a partir da hematita envolve a seguinte reao
(no balanceada):
FeO(s) + CO(g) Fe(s) + CO(g)
Percebe-se desta reao que o CO liberado para a atmosfera, podendo ter um impacto ambiental grave
relacionado com o efeito estufa. Qual o nmero de molculas de CO liberadas na atmosfera, quando um mol
de xido de ferro (III) consumido na reao? Considere: nmero de Avogadro igual a 6 10 mol.
a) 6 10
b) 24 10
c) 12 10
d) 36 10
e) 18 10
86. (Ufrn) O bicarbonato de sdio (NaHCO) utilizado na fabricao do extintor de incndio que produz
espuma. Nesse extintor, existe bicarbonato de sdio slido e uma soluo de cido sulfrico, em
compartimentos separados. Quando o extintor acionado, o bicarbonato de sdio e o cido sulfrico se
misturam e reagem segundo a equao:
2NaHCO + HSO NaSO + 2CO + 2HO
Se 196g de HSO reagem em soluo, com suficiente NaHCO, o volume de CO gasoso liberado (em litros),
nas CNTP, de:
DADO: Massa Molar do HSO = 98 g/mol
a) 4,48 L
b) 8,96 L
c) 44,8 L
d) 89,6 L
pag.36
100 questes de calculo estequiomtrico
87. (Ufrrj) O xido de alumnio (AO) utilizado como anticido.
Sabendo-se que a reao que ocorre no estmago 1AO+6HC2AC+3HO, a massa desse xido que
reage com 0,25 mol de cido ser
a) 3,25g.
b) 4,25g.
c) 5,35g.
d) 6,55g.
e) 7,45g.
88. (Ufrs) Um vazamento de gs de cozinha pode provocar srios acidentes. O gs de cozinha, quando
presente no ar em concentrao adequada, pode ter sua combusto provocada por uma simples fasca
proveniente de um interruptor de luz ou de um motor de geladeira. Essas exploses so, muitas vezes,
divulgadas erroneamente como exploses do botijo de gs. A reao de combusto completa de um dos
componentes do gs de cozinha apresentada a seguir:
CH + 5O 3CO + 4HO
A partir da equao anterior, qual a massa de oxignio necessria para produzir a combusto completa de 224
litros de propano nas CNTP?
Dado: O = 16 u
a) 32 g
b) 160 g
c) 320 g
d) 1600 g
e) 3200 g
pag.37
100 questes de calculo estequiomtrico
89. (Ufrs) Num processo de produo de cido actico, borbulha-se oxignio no acetaldedo (CHCHO), a 60C,
na presena de acetato de mangans (II) como catalisador:
2 CHCHO() + 0(g) 2 CHCOOH()
Num ensaio de laboratrio para esta reao, opera-se no vaso de reao com 22,0 gramas de CHCHO e 16,0
gramas de O. Quantos gramas de cido actico so obtidos nesta reao a partir destas massas de reagentes
e qual o reagente limitante, ou seja, o reagente que completamente consumido?
90. (Ufsm) O ferro obtido pela reduo de seus minrios, em temperaturas muito elevadas, em altos fornos,
na presena de coque, conforme a equao global
FeO + 3C 2Fe + 3CO
Obtm-se, assim, o ferro-gusa, que contm muitas impurezas.
Quantos gramas de coque (C) so necessrios para converter totalmente 319,2g de FeO em ferro-gusa?
a) 24
b) 72
c) 108
d) 180
e) 360
pag.38
100 questes de calculo estequiomtrico
91. (Ufv) Aquecendo-se 2,443g de cloreto de brio hidratado (BaC.nHO) at a completa desidratao do sal,
obtm-se 2,083g do sal anidro (BaC). O valor do coeficiente n na frmula do sal hidratado :
Dados:
Ba = 137,3
C = 35,5
H = 1,0
O = 16,0
a) 1
b) 2
c) 3
d) 4
e) 5
92. (Ufv) H analgsicos que apresentam como um de seus constituintes a aspirina, que pode ser sintetizada
atravs da reao representada pela equao a seguir:
2 CHO + CHO 2 CHO + HO
cido
anidrido
aspirina
saliclico
actico
Se misturarmos 1,38 g de cido saliclico com excesso de anidrido actico, a massa de aspirina obtida, em
gramas, ser:
Dados:
Massas molares (g/mol)- C = 12; H = 1; O = 16
a) 1,38
b) 3,60
c) 3,18
d) 0,90
e) 1,80
93. (Unesp) So colocadas para reagir entre si as massas de 1,00g de sdio metlico e 1,00g de cloro gasoso.
Considere que o rendimento da reao 100%. So dadas as massas molares, em g/mol: Na=23,0 e C=35,5.
A afirmao correta :
a) h excesso de 0,153 g de sdio metlico.
b) h excesso de 0,352 g de sdio metlico.
c) h excesso de 0,282 g de cloro gasoso.
d) h excesso de 0,153 g de cloro gasoso.
e) nenhum dos dois elementos est em excesso.
pag.39
100 questes de calculo estequiomtrico
94. (Unifesp) O gs sulfeto de hidrognio uma substncia que d aos ovos podres o nauseabundo odor que
exalam. Esse gs formado na reao de um cido forte, como o cido clordrico, HC(aq), com sulfeto de
sdio, NaS. Considerando que a reao qumica se processa at consumir todo o reagente limitante, quando
so transferidos para um recipiente 195 g de sulfeto de sdio, 584 g de cido clordrico a 25 % em massa e
gua destilada, a quantidade produzida de sulfeto de hidrognio, em gramas, igual a
a) 779.
b) 683.
c) 234.
d) 85.
e) 68.
95. (Unirio) xido de clcio, xido de potssio e xido de sdio reagem separadamente, consumindo 18g de
HO em cada reao. Considere:
m massa de hidrxido de clcio formado;
m massa de hidrxido de potssio formado;
m massa de hidrxido de sdio formado.
Assim, podemos afirmar que:
Dados:
Massas molares H=1,0g/mol; O=16g/mol; Ca=40g/mol; K=39g/mol; Na=23g/mol
a) m > m > m
b) m > m > m
c) m > m > m
d) m > m > m
e) m > m > m
96. (Unirio) Jacques A. C. Charles, qumico famoso por seus experimentos com bales, foi o responsvel pelo
segundo vo tripulado. Para gerar o gs hidrognio, com o qual o balo foi enchido, ele utilizou ferro metlico e
cido, conforme a seguinte reao:
Fe(s) + HSO(aq) FeSO(aq) + H(g)
Supondo-se que tenham sido utilizados 448 kg de ferro metlico, o volume, em litros, de gs hidrognio obtido
nas C.N.T.P. foi de:
(Massa Atmicas: H = 1u; Fe = 56u)
a) 89,6
b) 179,2
c) 268,8
d) 89.600
e) 179.200
pag.40
100 questes de calculo estequiomtrico
97. (Unirio) Solues de amnia so utilizadas com freqncia em produtos de limpeza domsticas. A amnia
pode ser preparada por inmeras formas. Dentre elas:
CaO(s) + 2NHC(s)
2NH(g) + HO(g) + CaC(s)
Partindo-se de 224g de CaO, obtiveram-se 102g de NH. O rendimento percentual da reao foi de:
(H = 1; N = 14; O = 16, C = 35,5; Ca = 40)
a) 100
b) 90
c) 80
d) 75
e) 70
98. (Fuvest) Um slido S decomposto por aquecimento e o produto slido obtido, ao reagir com gua, forma
hidrxido de clcio. Este reage com carbonato de sdio produzindo soda custica (NaOH) e regenerando o
slido S que reciclado. Qual a frmula de S e sua respectiva massa necessria para iniciar um ciclo de
produo de soda custica a partir de 1,06 toneladas de carbonato de sdio ?
massas molares (g/mol)
C...........12
O...........16
Na......... 23
Ca......... 40
Admita em todas as etapas um rendimento de 100%.
a) CaO e 0,56t
b) CaO e 1,12t
c) Ca(OH) e 1,06t
d) CaCO e 1,00t
e) CaCO e 2,00t
99. (Fuvest) Tanto gs natural como leo diesel so utilizados como combustvel em transportes urbanos. A
combusto completa do gs natural e do leo diesel liberam, respectivamente, 910kJ e 910kJ por mol de
hidrocarboneto. A queima desses combustveis contribui para o efeito estufa. Para igual energia liberada,
quantas vezes a contribuio do leo diesel maior que a do gs natural?
(Considere gs natural = CH, leo diesel = CH)
a) 1,1.
b) 1,2.
c) 1,4.
d) 1,6.
e) 1,8.
pag.41
100 questes de calculo estequiomtrico
100. (Ufsm) O pequeno produtor, ao transportar seus produtos para as feiras, pode utilizar o etanol como
combustvel no seu veculo.
A cana-de-acar uma fonte de sacarose, matria-prima para a obteno industrial desse combustvel. A
reao de fermentao da sacarose para a obteno do lcool etlico pode ser representada pela equao:
Partindo-se de uma quantidade de caldo de cana que contenha 684 g de sacarose e admitindo-se um
rendimento de 80 %, calcule, em kJ, a energia liberada na combusto do lcool etlico formado na reao,
sendo o seu calor de combusto -1.230 kJ mol.
a) - 9.840
b) + 9.840
c) - 2.460
d) - 7.872
e) + 7.872
pag.42
100 questes de calculo estequiomtrico
GABARITO
1. Observe a equao qumica a seguir:
O mecanismo utilizado da adio eletroflica.
2. Distncia = 66 km.
3. a) x = 126,9 . 10 g de I
b) A parte da molcula do cido olico que interage com a gua a sua parte polar, que est representada pela
figura 1.
Essa interao pode ser representada da seguinte forma:
4. a) De maneira geral, a presso parcial do CO no sangue venoso maior que a do sangue arterial, isto , a
concentrao em quantidade de mol de CO dissolvido maior; logo, o sangue venoso deve apresentar um
carter cido mais acentuado, ou seja, um menor pH.
CO(g) + HO() HCO(aq) + H(aq)
b) 72 min.
pag.43
100 questes de calculo estequiomtrico
5. a) CHO
b) 3,32 g de HO
6. a) HSO + NaCO HCO + NaSO
(dupla troca)
b) 10,6 toneladas
7. a) 2 KMnO + 5 Fe + 8 HSO
5 FeSO + 2 MnSO + 1 KSO + 8 HO
b) 0,5 mol
c) 0,2 mol
8. a) 130 g
b) NaO(s) + HO () 2 NaOH (aq)
KO(s) + HO () 2 KOH (aq)
9. a) CH + (67/2)O 22CO + 23HO
b) 4,4 mols.
c) 1 mol (parafina) _____ 22 mols (CO)
310 g _____ 22 mols
x g _____ 4,4 mols
x = 62 g.
Como uma vela equivale a um ano, temos:
1 ano (1 vela) _____ 1,55 g
t _____ 62 g
t = 40 anos.
10. x = 516 g
11.
pag.44
100 questes de calculo estequiomtrico
b) 1 mol (cico nicotnico) = 123 g
1 pessoa ------- 15 x 10g
x
-------- 123 g
x = 8200 pessoas.
12. 320 g
13. 8,7 m
14. 97,92%
15. a) [(44gCO)/(44gCO + 11gHO)]100 71,0 %
b) Sabendo-se que: 8,00 g - 6,02 g = 1,98 g representa a massa da mistura gasosa liberada, temos
100 g mistura __________ 71,0 g CO
1,98 g ________________
y
y 1,41 g CO.
c) 2 NaHCO __________ 44g CO
z' _______________ 1,41 g
z' = 5,38 g
d) 100% ______________ 8,00 g
y _______________ 5,38 g
y 67,30%.
16. a) N + 3 H 2 NH
b) 358,4 m
17. Em 1 kg da liga (Au + Ag + Cu), teremos:
2 % de cobre = 0,02 kg.
8 % de prata = 0,08 kg.
pag.45
100 questes de calculo estequiomtrico
90 % de ouro = 0,90 kg.
De acordo com o grfico, a meia vida do contaminante Ag (prata) de 15 minutos e aps este tempo teremos
50 % de Ag e 40 % de Cu (contaminantes).
100 % Ag ---------- 0,08 kg (na liga)
50 % Ag ---------x
x = 0,04 kg de prata.
100 % Cu ---------- 0,02 kg (na liga)
40 % Cu ---------y
y = 0,008 kg de cobre.
18. a) 300g CaCO
b) 67,2 L CO
19. 0,20 mol NaOH ----- 1000mL
n mol NaOH ----- 15 mL
n = 0,003 mol de NaOH
De acordo com a equao:
180 g AAS ----- 1 mol NaOH
p x 1 g AAS ----- 0,003 mol NaOH
p = 0,54 = 54 %
20. a) 0,3 mol
b) 1,8 10
c) 140,5 g.mol
d) 0,1 mol
e) 121 g.mol
f) 12,1 g
21. a) Na + 1/2 I NaI
b) ligao covalente apolar
c) ligao metlica
d) ligao inica
e) 15,26 g
f) 12,92 g
pag.46
100 questes de calculo estequiomtrico
22. a) 1 CO + 3 I + 2 H 1 C + 1 I + 1 HO
b) % em massa = 4,96 %
23. a) Massa do LiH = 7,90 g
b) rendimento = 80 %
24. (a) CHON + 2X CHOH + CHON + CHON
294 g + 2X
= 32 g + 133 g + 165 g
2X = 36; X = 18 g. Logo, X = HO.
(b) CHON + 2X CHOH + CHON + CHON
294 g --------------------- 32 g
200x10 g --------------------- m
m = 0,02177 g -------- 1 lata de refrigerante
48 g -------n
n = 2204,87 = 2205 latas de refrigerante.
25. a) CaC(s) + 3C(s) CO(g) + CaC(s)
b) CaC(s) +2HO() Ca(OH)(aq) + CH(g)
64 g ------------------------------------------ 26 g
m ------------------------------------------ 13 g
m = 32 g de carbeto de clcio.
26. a) V = 0,62
b) Q = 30,6 kJ
27. 74,3 kg de C H O
28. a) Sim, pois foram queimadas massas iguais de carbono.
b) No, a quantidade em mols de O consumida maior.
29. a) Brilho metlico e a maleabilidade do material.
b) Supondo-se inicialmente uma rocha que contenha exclusivamente xido de ferro II, FeO:
FeO + CO Fe + CO
1 mol
1 mol
72g
56g
Admitindo a mesma massa (72g), porm de xido de ferro III, podemos calcular a massa de ferro obtido:
FeO + 3 CO 2 Fe + 3 CO
1 mol
2 mol
160g
112g
pag.47
100 questes de calculo estequiomtrico
72g
x = 50,4 g
Logo, a amostra de xido de ferro II (FeO) possibilitaria a obteno de maior quantidade de ferro metlico.
c) O = C = O
30. a) 1600 g
b) 4320 g
31. a) 113,83 kPa
b) 242,6 g
32. a) Opo (A)
KOH(aq) + HC(aq) KC(aq) + HO ()
ou
Opo (B)
KCO(aq)+2HC(aq)2KC(aq)+CO(g)+HO()
b) Opo (A) 400 mL de KOH(aq)
ou
Opo (B) 200 mL de KCO(aq)
33. a) 175,5 kg de NaC
b) 7,1 kg de C
34. a) K = 0,15
b) 34 g
35. 0,55 L
36. [D]
37. [D]
38. [C]
39. [B]
40. [C]
41. [C]
pag.48
100 questes de calculo estequiomtrico
42. [C]
43. [E]
44. [B]
45. [B]
46. [B]
47. [D]
48. [B]
49. [D]
50. [A]
51. [D]
52. [C]
53. [E]
54. [C]
55. [C]
56. [A]
57. [C]
58. [C]
59. [A]
60. [C]
61. [A]
62. [D]
63. [C]
64. [B]
pag.49
100 questes de calculo estequiomtrico
65. [D]
66. [C]
67. [C]
68. [C]
69. [C]
70. [B]
71. [B]
72. [A]
73. [D]
74. [C]
75. [A]
76. [B]
77. [B]
78. [D]
79. [B]
80. [E]
81. [C]
82. [A]
83. [D]
84. [B]
85. [E]
86. [D]
87. [B]
pag.50
100 questes de calculo estequiomtrico
88. [D]
89. [C]
90. [B]
91. [B]
92. [E]
93. [B]
94. [E]
95. [C]
96. [E]
97. [D]
98. [D]
99. [C]
100. [D]
pag.51
Você também pode gostar
- 1000 Questões de Vestibular Quimica Com GabaritoDocumento15 páginas1000 Questões de Vestibular Quimica Com GabaritoRosana Galev Oliveira80% (5)
- Resumo de Quimica OrganicaDocumento12 páginasResumo de Quimica OrganicaEmerson Jair Machava100% (2)
- Equilíbrio iônico: aplicações em química analíticaNo EverandEquilíbrio iônico: aplicações em química analíticaAinda não há avaliações
- Física com aplicação tecnológica: Oscilações, ondas, fluidos e termodinâmicaNo EverandFísica com aplicação tecnológica: Oscilações, ondas, fluidos e termodinâmicaAinda não há avaliações
- Eletrólitos e Não PDFDocumento23 páginasEletrólitos e Não PDFRayanne FernandesAinda não há avaliações
- ELETROQUÍMICA Teoria e Exercícios PDFDocumento9 páginasELETROQUÍMICA Teoria e Exercícios PDFEraclitoSL100% (1)
- ELETROQUÍMICA Teoria e Exercícios PDFDocumento9 páginasELETROQUÍMICA Teoria e Exercícios PDFEraclitoSL100% (1)
- Atomos PolieletrônicosDocumento8 páginasAtomos PolieletrônicosEraclitoSL100% (1)
- Exercicios SolucoesDocumento12 páginasExercicios SolucoesEraclitoSL91% (11)
- Físico-Química - Termoquímica (30 Questões)Documento10 páginasFísico-Química - Termoquímica (30 Questões)Ciencias PPT100% (1)
- Exercícios Resolvidos de QuímicaDocumento140 páginasExercícios Resolvidos de QuímicaTiago Bruno Valandro50% (16)
- Termoquímica 2011 Resumo260511Documento4 páginasTermoquímica 2011 Resumo260511Jefferson PinheiroAinda não há avaliações
- Química Orgânica - CASD - Aula06a08 Funções Orgânicas Oxigenadas IDocumento4 páginasQuímica Orgânica - CASD - Aula06a08 Funções Orgânicas Oxigenadas IQuímica Caderno de Resoluções100% (3)
- Física - Exercícios Com Gabarito - Queda LivreDocumento2 páginasFísica - Exercícios Com Gabarito - Queda LivreFísica Concurso Vestibular88% (8)
- Físico-Química - Equilíbrio Iônico (30 Questões)Documento10 páginasFísico-Química - Equilíbrio Iônico (30 Questões)Ciencias PPT100% (2)
- Tabela Periódica SlidesDocumento27 páginasTabela Periódica SlidesIgor AparecidoAinda não há avaliações
- 100 Questões de Conc de SoluçõesDocumento42 páginas100 Questões de Conc de SoluçõesEraclitoSL100% (5)
- Apostila Curso de Física 3ano Módulo 01 EletrostáticaDocumento19 páginasApostila Curso de Física 3ano Módulo 01 EletrostáticaFísica Concurso Vestibular88% (8)
- Ime-Ita Apostila Quimica Vol 3 PDFDocumento100 páginasIme-Ita Apostila Quimica Vol 3 PDFCarlos Vane50% (2)
- Calculo EstequiometricoDocumento8 páginasCalculo EstequiometricoEraclitoSL100% (21)
- Ligações Químicas - Profº Agamenon RobertoDocumento14 páginasLigações Químicas - Profº Agamenon Robertocb_penatrujillo0% (1)
- Física - Resumos Vestibular1 - MRUVDocumento12 páginasFísica - Resumos Vestibular1 - MRUVFísica Concurso Vestibular100% (4)
- Química PPT - Introdução A QuímicaDocumento61 páginasQuímica PPT - Introdução A QuímicaQuímica PPT83% (6)
- Aula Soluções (PH e pOH) ..EXCELENTE - Professor Rikardo CoimbraDocumento3 páginasAula Soluções (PH e pOH) ..EXCELENTE - Professor Rikardo CoimbraRicardo Coimbra100% (2)
- Atividade - Mapa Mental - QuímicaDocumento2 páginasAtividade - Mapa Mental - QuímicaCamilly Rodrigues100% (1)
- Apostila Quimica OrganicaDocumento66 páginasApostila Quimica OrganicaHenrique Silveira83% (6)
- Aula Cinetica QuimicaDocumento57 páginasAula Cinetica QuimicaMussageAinda não há avaliações
- Química CesupaDocumento3 páginasQuímica CesupaEditora100% (2)
- Funções OrgânicasDocumento1 páginaFunções OrgânicasJeanAinda não há avaliações
- Química - Pré-Vestibular Impacto - Ácidos - Classificação IIIDocumento2 páginasQuímica - Pré-Vestibular Impacto - Ácidos - Classificação IIIQuímica Qui100% (1)
- 28 20estequiometria 20II 20 C C3 A1lculo 20estequiom C3 A9tricoDocumento11 páginas28 20estequiometria 20II 20 C C3 A1lculo 20estequiom C3 A9tricoJoão MiguelAinda não há avaliações
- Lista 2 - Cálculo EstequiométricoDocumento17 páginasLista 2 - Cálculo EstequiométricomarinaandthediamondsAinda não há avaliações
- Ceja Quimica Unidade 9 ExerciciosDocumento6 páginasCeja Quimica Unidade 9 ExerciciosRe-I MayerAinda não há avaliações
- Aula 2 - 2 Ano - EstequiometriaDocumento4 páginasAula 2 - 2 Ano - EstequiometriaLúcio BarbozaAinda não há avaliações
- Trabalho de Recuperacao Final Quimica 3 Ano10115910Documento6 páginasTrabalho de Recuperacao Final Quimica 3 Ano10115910Vitória BarrosAinda não há avaliações
- 2009 FinalDocumento6 páginas2009 FinaliolaAinda não há avaliações
- Fase 3 Lista 2 CinéticaDocumento2 páginasFase 3 Lista 2 CinéticaventiladoramoebaAinda não há avaliações
- Quimica Termoquimica ExerciciffosDocumento47 páginasQuimica Termoquimica ExerciciffosFernando RaposoAinda não há avaliações
- Cinetica Quimica Questoes SubjetivasDocumento18 páginasCinetica Quimica Questoes SubjetivasJosue Dos Santos NascimentoAinda não há avaliações
- Exerc Cinetica Termoquimica SolucoesDocumento17 páginasExerc Cinetica Termoquimica SolucoeseuAinda não há avaliações
- EstequiometriaDocumento4 páginasEstequiometriaBeatriz LimaAinda não há avaliações
- Exercícios Cinética Química LivretoDocumento8 páginasExercícios Cinética Química LivretoJoão Ribeiro Franco NetoAinda não há avaliações
- Juvencio DocumentsDocumento10 páginasJuvencio DocumentsAnastacio Augusto Mucupela Augusto MucupelaAinda não há avaliações
- Tecnologia 506Documento2 páginasTecnologia 506Renata Alves De Oliveira FernandesAinda não há avaliações
- Lista 2Documento5 páginasLista 2Bruno EduardoAinda não há avaliações
- 3 Lista de Exercicios EEMADocumento6 páginas3 Lista de Exercicios EEMALaysa BebezinhaAinda não há avaliações
- TEORIAATo MICOMOLECULARDocumento4 páginasTEORIAATo MICOMOLECULARmeninoAinda não há avaliações
- Revisão Unesp 2021Documento7 páginasRevisão Unesp 2021ALLANA OLIVEIRAAinda não há avaliações
- Lista CinéticaDocumento18 páginasLista Cinéticamoitinhamhsp2Ainda não há avaliações
- Exerc Cálc Quím2009Documento4 páginasExerc Cálc Quím2009lurianmcAinda não há avaliações
- Tarefa 09-08 - 220814 - 105102Documento4 páginasTarefa 09-08 - 220814 - 105102Steffany NicoliAinda não há avaliações
- 2000 FinalDocumento6 páginas2000 FinaliolaAinda não há avaliações
- Prova-Modelo (2018) FQADocumento11 páginasProva-Modelo (2018) FQALeonor SantosAinda não há avaliações
- Lista 10 Geral 2023-2Documento6 páginasLista 10 Geral 2023-2yjb46zys2hAinda não há avaliações
- Lista de Exercícios - RevisãoDocumento5 páginasLista de Exercícios - Revisãofilha01Ainda não há avaliações
- 3 Módulo C - QuimicaDocumento16 páginas3 Módulo C - QuimicaMarilene MateusAinda não há avaliações
- 112160-Capítulo 19 Cultura e IdeologiaDocumento7 páginas112160-Capítulo 19 Cultura e IdeologiaOlavo ConceiçãoAinda não há avaliações
- Quimica 4Documento4 páginasQuimica 4João PedroAinda não há avaliações
- ESTEQUIOMETRIA ExercíciosDocumento26 páginasESTEQUIOMETRIA ExercíciosRafaela De Lima FrançaAinda não há avaliações
- Correção Comentada 3º DiaDocumento26 páginasCorreção Comentada 3º DiaMafezinha PirolaAinda não há avaliações
- Bi Po Bi T β α Documento3 páginasBi Po Bi T β α EraclitoSLAinda não há avaliações
- Divisão 2 Série 6 de NovembroDocumento6 páginasDivisão 2 Série 6 de NovembroEraclitoSLAinda não há avaliações
- RESULTADO OPQ - 2021 - MODALIDADE EM1 - OkDocumento5 páginasRESULTADO OPQ - 2021 - MODALIDADE EM1 - OkEraclitoSLAinda não há avaliações
- Resultado Opq - 2021 - Modalidade Em2 - OkDocumento3 páginasResultado Opq - 2021 - Modalidade Em2 - OkEraclitoSLAinda não há avaliações
- Simulado EnemDocumento3 páginasSimulado EnemEraclitoSLAinda não há avaliações
- Lista SolucoesDocumento5 páginasLista SolucoesEraclitoSL100% (1)
- Revisao FuvestDocumento2 páginasRevisao FuvestEraclitoSLAinda não há avaliações
- Revisao FacidDocumento2 páginasRevisao FacidEraclitoSLAinda não há avaliações
- Questões de Balanceamento Com GabaritoDocumento2 páginasQuestões de Balanceamento Com Gabaritodesinhalove100% (5)
- ProvaFacid-2016 1Documento16 páginasProvaFacid-2016 1EraclitoSL86% (14)
- Balanceamento1EspLETT PROVEST 18 09 2012Documento6 páginasBalanceamento1EspLETT PROVEST 18 09 2012EraclitoSLAinda não há avaliações
- 100 Questões de Conc de SoluçõesDocumento42 páginas100 Questões de Conc de SoluçõesEraclitoSL100% (5)
- 126 ArquivoDocumento2 páginas126 ArquivoEraclitoSLAinda não há avaliações
- Exercicios Calculo Esteq.Documento4 páginasExercicios Calculo Esteq.EraclitoSL100% (4)
- Revisão de Reforço Equilíbrio Quimica 1Documento2 páginasRevisão de Reforço Equilíbrio Quimica 1EraclitoSLAinda não há avaliações
- Os Primeiros Modelos AtômicosDocumento5 páginasOs Primeiros Modelos AtômicosEraclitoSL100% (3)
- Vitamina C em Suco de Caju e CajuínaDocumento6 páginasVitamina C em Suco de Caju e CajuínaEraclitoSL100% (2)
- Olimpiada de Quimica CearáDocumento16 páginasOlimpiada de Quimica CearáEraclitoSL100% (9)
- Apoio - Calculo EstequiometricoDocumento3 páginasApoio - Calculo EstequiometricoEraclitoSL100% (6)
- Exercicios de Reações OrganicaDocumento23 páginasExercicios de Reações OrganicaEraclitoSL92% (12)
- Exercicios RadioatividadeDocumento3 páginasExercicios RadioatividadeEraclitoSL100% (2)
- Exercicios SolucoesDocumento12 páginasExercicios SolucoesEraclitoSL91% (11)
- Reações OrganicasDocumento55 páginasReações OrganicasEraclitoSL100% (11)
- Estrutura AtomicaDocumento18 páginasEstrutura AtomicaEraclitoSL100% (1)
- Lei de HessDocumento3 páginasLei de HessEraclitoSL100% (5)
- Calculo EstequiometricoDocumento8 páginasCalculo EstequiometricoEraclitoSL100% (21)
- Atendimento A Emergências QuímicasDocumento71 páginasAtendimento A Emergências QuímicasMaria SilvaneideAinda não há avaliações
- Geração de Energia ElectricaDocumento21 páginasGeração de Energia ElectricaSuper ScottfwAinda não há avaliações
- Adsil - Sílica Ativa em SuspensãoDocumento3 páginasAdsil - Sílica Ativa em SuspensãoJeovane VasconcelosAinda não há avaliações
- Ficha Seguranca de Gas Natural PTDocumento11 páginasFicha Seguranca de Gas Natural PTFabio RubinAinda não há avaliações
- Cidadania e Transito PDFDocumento40 páginasCidadania e Transito PDFEmília QuerinoAinda não há avaliações
- 126 Quimica ITA 89Documento10 páginas126 Quimica ITA 89jbmccavalcantiAinda não há avaliações
- Diluente Especial Pu BT038 5L SikkensDocumento18 páginasDiluente Especial Pu BT038 5L SikkensIzabelAinda não há avaliações
- Manuseios de Solo, Segurança e Equipamentos deDocumento315 páginasManuseios de Solo, Segurança e Equipamentos deMauricio Togo ImamuraAinda não há avaliações
- Fispq - Grapax Chassis 2Documento9 páginasFispq - Grapax Chassis 2julioebc2014Ainda não há avaliações
- Apostila de CarburadoresDocumento52 páginasApostila de CarburadoresFábioAinda não há avaliações
- Seleção de Secadores-FluxogramaDocumento24 páginasSeleção de Secadores-FluxogramadfiorilloAinda não há avaliações
- Teste 2 8 Ano Reacoes QuimicasDocumento4 páginasTeste 2 8 Ano Reacoes QuimicasMena DamilAinda não há avaliações
- Manual de Higiene e Segurança No AmbienteDocumento30 páginasManual de Higiene e Segurança No AmbienteMário Domingos Tchipenda100% (1)
- FT Alsan Flashing r00 B - 20230314193600Eud21CpldIDocumento2 páginasFT Alsan Flashing r00 B - 20230314193600Eud21CpldIThiago De Lima RamosAinda não há avaliações
- Teor de Álcool em GasolinaDocumento3 páginasTeor de Álcool em GasolinaGlorifique O CriadorAinda não há avaliações
- 01 Noções Básicas de Perícia de Incêndio PDFDocumento76 páginas01 Noções Básicas de Perícia de Incêndio PDFJose Wilton Sousa Nunes100% (1)
- Fisp - Chapa PPDocumento3 páginasFisp - Chapa PPAndersonAinda não há avaliações
- 2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoDocumento3 páginas2º Ano - Avaliação - Quimica - 08-07-2021 - JulhoSelma Eliane Quatroque TavaresAinda não há avaliações
- 6 Ano Agosto Aula Semana 2 e 3 PDFDocumento9 páginas6 Ano Agosto Aula Semana 2 e 3 PDFRochedao RogAinda não há avaliações
- Lista de Exercicios EstequiometriaDocumento5 páginasLista de Exercicios Estequiometriamariana rubiaAinda não há avaliações
- Acessórios de IniciaçãoDocumento8 páginasAcessórios de IniciaçãoBruna GonçalvesAinda não há avaliações
- SULGÁS - RIP-2020 - 6-Instalacao - Aparelhos - A - GasDocumento26 páginasSULGÁS - RIP-2020 - 6-Instalacao - Aparelhos - A - GasMário PorralAinda não há avaliações
- Temperatura AdiabáticaDocumento7 páginasTemperatura AdiabáticaWillie Victor FerreiraAinda não há avaliações
- Turbinas A GasDocumento37 páginasTurbinas A GaswiredrawingAinda não há avaliações
- FISPQ CloroDocumento12 páginasFISPQ Clororicardo_potascheffAinda não há avaliações
- Provbim1ºano3 Etcmm 22Documento5 páginasProvbim1ºano3 Etcmm 22Daniel SousaAinda não há avaliações
- Questões Enem CalorimetriaDocumento5 páginasQuestões Enem Calorimetriaerymaxiimus8113Ainda não há avaliações
- EstequiometriaDocumento4 páginasEstequiometriaTelmo CarmoAinda não há avaliações
- MSDS CuprexDocumento1 páginaMSDS Cuprexobed2028Ainda não há avaliações
- Conceitos Básicos - Modulo 2Documento16 páginasConceitos Básicos - Modulo 2neyzanata5043Ainda não há avaliações