Escolar Documentos
Profissional Documentos
Cultura Documentos
Aula 6 - Quimica Pre-Tecnico
Enviado por
Beatriz EstudosTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Aula 6 - Quimica Pre-Tecnico
Enviado por
Beatriz EstudosDireitos autorais:
Formatos disponíveis
Preparatório municipal de Nova Iguaçu
Pré Técnico/Professora: Beatriz Andrade
Disciplina: Química
Aula 6
Tópicos:
1. Exercicios de revisão: Processos de separação de misturas
2. Explicando a materia e as suas transformações:
2.2 Lei de Lavoisier
2.3 Lei de Proust
2.4 A HIPÓTESE DE DALTON
Exercicios de revisão: Processos de separação de misturas
1 - (Mackenzie-SP) Ao se preparar o tradicional cafezinho, executam-se dois processos físicos que são,
respectivamente:
a) extração e filtração
b) decantação e destilação
c) evaporação e filtração
d) filtração e liqüefação
e) dissolução e liqüefação
2 - (UFPE) Leia as atividades do cotidiano, abaixo, e as técnicas de laboratório apresentadas a seguir:
A. Preparação de cafezinho de café solúvel 1. Filtração
B. Preparação de chá de saquinho 2. Solubilização
C. Coar um suco de laranja 3. Extração
4. Destilação
A associação correta entre ambas é:
a) A2, B3 e C1
b) A4, B2 e C3
c) A3, B4 e C1
d) A1, B3 e C2
e) A2, B2 e C4
3 - (UFR-RJ) Com a adição de uma solução aquosa de açúcar a uma mistura contendo querosene e
areia, são vistas claramente três fases. Para separar cada componente da mistura final, a melhor
seqüência é:
a) destilação, filtração e decantação
b) cristalização, decantação e destilação
c) filtração, cristalização e destilação
d) filtração, decantação e destilação
e) centrifugação, filtração e decantação
Explicando a materia e as suas transformações
A lei de Lavoisier
No final do século XVIII, o cientista Antoine Lavoisier realizou uma série de experiências em recipientes
fechados (para que não entrasse nem escapasse nada do sistema em estudo) e, efetuando pesagens
com balanças mais precisas do que as dos cientistas anteriores, concluiu:
No interior de um recipiente fechado, a massa total não varia, quaisquer que sejam as
transformações que venham a ocorrer.
Tal afirmativa é uma lei da Natureza, descoberta por Lavoisier e que, por esse motivo, ficou conhecida
como lei de Lavoisier (ou lei da conservação da massa, ou lei da conservação da matéria).
Por exemplo: verifica-se que 3 gramas de carbono reagem com 8 gramas de oxigênio, produzindo 11
gramas de gás carbônico.
Como 3 g + 8 g = 11 g, conclui-se que nada se perdeu.
A lei de Lavoisier, portanto, pode ser enunciada também da seguinte maneira:
A soma das massas antes da reação é igual à soma das massas após a reação.
Ou ainda:
Na natureza, nada se perde, nada se cria; a matéria apenas se transforma.
A lei de Proust
Quase na mesma época de Lavoisier, Joseph Louis Proust, efetuando também uma grande série de
pesagens em inúmeras experiências, chegou à seguinte conclusão:
Uma determinada substância composta é formada por substâncias mais simples, unidas
sempre na mesma proporção em massa.
Por exemplo, observa-se que o gás carbônico é sempre formado por carbono e oxigênio, e verificase
também que:
1º experiência: 3 g de carbono (C) se unem a 8 g de oxigênio (O2), produzindo 11 g de gás carbônico
(CO2)
2 º experiência: 6 g de carbono (C) se unem a 16 g de oxigênio (O2), produzindo 22 g de gás
carbônico (CO2)
Veja que, na 1º experiência, a proporção entre as massas é de 3 : 8 : 11.
Na 2 º experiência, é de 6 : 16 : 22.
Nesta última, os números mudaram, mas obedecendo à relação: 6 é o dobro de 3; 16 é o
dobro de 8; e 22 é o dobro de 11.
Enfim, os números mudaram, mas a proporção é a mesma, como se diz em Matemática.
Essa conclusão é chamada de lei de Proust ou lei das proporções constantes (ou fixas ou definidas).
As duas leis enunciadas — a de Lavoisier e a de Proust — são denominadas leis ponderais, porque
falam em massa das substâncias envolvidas. São leis importantíssimas, pois marcam o início
(nascimento) da Química como ciência.
A HIPÓTESE DE DALTON
Para explicar os fatos experimentais observados nas duas leis ponderais vistas anteriormente, o
cientista inglês John Dalton imaginou a seguinte hipótese:
Todo e qualquer tipo de matéria é formado por partículas indivisíveis, chamadas átomos.
Para entendermos a relação entre essa hipotese e as leis ponderais imagine o átomo de carbono
representado por (e considere sua massa estabelecida arbitrariamente neste exemplo, em 3
g), e o átomo de oxigênio representado por (com massa também arbitrária de 4 g).
A lei de Lavoisier seria explicada do seguinte modo:
A lei de Proust seria explicada da seguinte maneira:
Da 1a experiência para a 2a, a quantidade de átomos dobrou; como conseqüência, todas as
massas duplicaram. Atualmente, com técnicas avançadíssimas, já é possível ter uma visão do átomo.
Desde o século 19, muitas experiências confirmam a existência do átomo.
Podemos também dizer que Dalton criou um modelo para o átomo, hoje chamado de modelo
atômico de Dalton.
Você também pode gostar
- Leis das reações químicas e teoria atômica clássicaDocumento2 páginasLeis das reações químicas e teoria atômica clássicaCarlos NeyAinda não há avaliações
- Química - Lei Das Combinações Químicas (Cristiane Santos)Documento23 páginasQuímica - Lei Das Combinações Químicas (Cristiane Santos)Marianne CammarotaAinda não há avaliações
- QUÍMICA GERALDocumento3 páginasQUÍMICA GERALMatheus De Araujo SilvaAinda não há avaliações
- Série Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosNo EverandSérie Didática para o Apoio à Formação de Professores de Química – Volume 1 – ÁtomosAinda não há avaliações
- Lei de LavoisierDocumento4 páginasLei de LavoisierIsabelle CristinaAinda não há avaliações
- Enem 2018 - Ciências Da Natureza E Suas TecnologiasNo EverandEnem 2018 - Ciências Da Natureza E Suas TecnologiasAinda não há avaliações
- Apostila de Modelos AtômicosDocumento24 páginasApostila de Modelos AtômicosSara Chaves.NAinda não há avaliações
- Biofísica para ciências biomédicas – 4ª ediçãoNo EverandBiofísica para ciências biomédicas – 4ª ediçãoAinda não há avaliações
- Lista 1 - Química BrunaDocumento5 páginasLista 1 - Química BrunaBruna AlvarengaAinda não há avaliações
- Docsity Relatorio Conservacao Da MassaDocumento8 páginasDocsity Relatorio Conservacao Da MassaLuciana BonfimAinda não há avaliações
- Plano de Ensino de Química II sobre EstequiometriaDocumento7 páginasPlano de Ensino de Química II sobre EstequiometriaSamara FernandesAinda não há avaliações
- FÍSICADocumento88 páginasFÍSICAisraelarmindo7Ainda não há avaliações
- Pet 02 - 1º emDocumento25 páginasPet 02 - 1º emAna Elisa Teixeira AlcobaAinda não há avaliações
- Água - Aula 2Documento7 páginasÁgua - Aula 2lucasmanjosAinda não há avaliações
- Semana 03 Quimica Inorgância Leis de Lavoisier e ProustDocumento5 páginasSemana 03 Quimica Inorgância Leis de Lavoisier e ProustFerreira HerculesAinda não há avaliações
- Leis de conservação da massa e proporções constantes em reações químicasDocumento5 páginasLeis de conservação da massa e proporções constantes em reações químicasCarlos augusto cumbiAinda não há avaliações
- Antoine Lavoisier - Pai Da QuímicaDocumento11 páginasAntoine Lavoisier - Pai Da QuímicalojaserafimoficialAinda não há avaliações
- Reações químicas pré-testeDocumento4 páginasReações químicas pré-testeOlavo DuarteAinda não há avaliações
- Conservação Matéria LeisDocumento4 páginasConservação Matéria LeisSthefanie de CarvalhoAinda não há avaliações
- Lei de LavoisierDocumento3 páginasLei de LavoisierGETULIO VICENTE VIEIRA MENEZES100% (1)
- Trabalho LavíniaDocumento6 páginasTrabalho Lavíniainfoservicos9Ainda não há avaliações
- Relatório de Reações QuímicasDocumento19 páginasRelatório de Reações QuímicasEdu NevesAinda não há avaliações
- Leis Das Reações QuímicasDocumento4 páginasLeis Das Reações QuímicasizaaknewtonAinda não há avaliações
- As leis das combinações químicasDocumento5 páginasAs leis das combinações químicassamuel souzaAinda não há avaliações
- Apqg02. o Átomo PDFDocumento19 páginasApqg02. o Átomo PDFErica SilvaAinda não há avaliações
- Quimica Pre-TecnicoDocumento4 páginasQuimica Pre-TecnicoBeatriz EstudosAinda não há avaliações
- Química estequiométrica fundamentosDocumento4 páginasQuímica estequiométrica fundamentosLucas BernalAinda não há avaliações
- Modelos atômicos e leis químicas fundamentaisDocumento25 páginasModelos atômicos e leis químicas fundamentaisPlantão MatemáticoAinda não há avaliações
- Relatório Pratica - Lab. Quimica GeralDocumento14 páginasRelatório Pratica - Lab. Quimica GeralMEILANGY IRIS FERREIRA DE OLIVEIRAAinda não há avaliações
- 2021 - Química - 2 Série - Slides - Aula 1Documento21 páginas2021 - Química - 2 Série - Slides - Aula 1ADRIANA DE LIMA ALVESAinda não há avaliações
- Apostila 2ºanoDocumento11 páginasApostila 2ºanoAdriana JesusAinda não há avaliações
- Leis PonderaisDocumento2 páginasLeis PonderaisjorgeAinda não há avaliações
- 1° AnoDocumento81 páginas1° Anoantonio220Ainda não há avaliações
- Atividade final de química sobre leis ponderaisDocumento3 páginasAtividade final de química sobre leis ponderaisTallys Santos MendesAinda não há avaliações
- Conservação da massa comprovada em experimentoDocumento7 páginasConservação da massa comprovada em experimentoCarlos HenriqueAinda não há avaliações
- Química I - Cálculos Químicos e Leis das ReaçõesDocumento7 páginasQuímica I - Cálculos Químicos e Leis das ReaçõesVanessa Vieira100% (1)
- 06 - Equilíbrio QuímicoDocumento3 páginas06 - Equilíbrio Químicocleyton_775918781Ainda não há avaliações
- Conservação Da MassaDocumento8 páginasConservação Da MassaCarlos HenriqueAinda não há avaliações
- Química Geral I - Aula 3 - Terceira Lista de ExercíciosDocumento3 páginasQuímica Geral I - Aula 3 - Terceira Lista de ExercíciosKauane SilvaAinda não há avaliações
- Turmadefevereiro-Química-Leis Ponderais e Cálculo de Fórmulas-25!04!2023Documento15 páginasTurmadefevereiro-Química-Leis Ponderais e Cálculo de Fórmulas-25!04!2023LaurenAinda não há avaliações
- Atividade 1ano Reserva 2bimDocumento5 páginasAtividade 1ano Reserva 2bimmilaelaAinda não há avaliações
- Leis Ponderais Reações QuímicasDocumento3 páginasLeis Ponderais Reações QuímicasLucasHenriqueAinda não há avaliações
- EstequiometriaDocumento17 páginasEstequiometriaMaria BiaAinda não há avaliações
- Leis das Reações QuímicasDocumento9 páginasLeis das Reações QuímicasTayna ChagasAinda não há avaliações
- Reações Químicas - LeisDocumento6 páginasReações Químicas - LeisAlessandro FreitasAinda não há avaliações
- Lei Da Conservacao Das Massas - LavoisierDocumento2 páginasLei Da Conservacao Das Massas - LavoisierMariana MendesAinda não há avaliações
- 3 - Propriedades e Transformações Da Matéria e Leis Ponderais Da QuímicaDocumento3 páginas3 - Propriedades e Transformações Da Matéria e Leis Ponderais Da QuímicaCyele MouraAinda não há avaliações
- Lei da Conservação de LavoisierDocumento3 páginasLei da Conservação de LavoisierrmcafonsoAinda não há avaliações
- 1 Estequiometria Iqg 114Documento23 páginas1 Estequiometria Iqg 114Tatiane MorenoAinda não há avaliações
- Leis ponderais químicasDocumento13 páginasLeis ponderais químicasgenesis sala10Ainda não há avaliações
- 04 - Relatorio Fisico-QuimicaDocumento8 páginas04 - Relatorio Fisico-QuimicaLuan ModestoAinda não há avaliações
- A Matéria e Suas TransformaçõesDocumento9 páginasA Matéria e Suas TransformaçõescosmowalkerAinda não há avaliações
- Aula 2 - Leis PonderaisDocumento17 páginasAula 2 - Leis PonderaisMARILIA RONSSENAinda não há avaliações
- Equilíbrio químico e solubilidade de solutosDocumento4 páginasEquilíbrio químico e solubilidade de solutosCarlos Frederico Santos MartinsAinda não há avaliações
- Relatório Laboratório de QuímicaDocumento6 páginasRelatório Laboratório de QuímicaLudmilla FernandesAinda não há avaliações
- Leis Fundamentais de Reações QuímicasDocumento6 páginasLeis Fundamentais de Reações QuímicasNicolas Diderot Fontenele BeanAinda não há avaliações
- 2° Ano-Leis Ponderais-10Documento2 páginas2° Ano-Leis Ponderais-10Vinicio ElétricaAinda não há avaliações
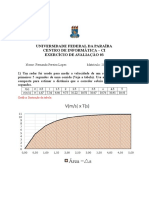
- Estimando distância com regra de SimpsonDocumento5 páginasEstimando distância com regra de SimpsonFernanda LopesAinda não há avaliações
- Centro Baiano de Computação de Alto DesempenhoDocumento70 páginasCentro Baiano de Computação de Alto DesempenhoGeronimo AmaralAinda não há avaliações
- Catálogo de Peças Agrale MarruáDocumento109 páginasCatálogo de Peças Agrale Marruágumarango100% (2)
- Como Fazer Queijo GorgonzolaDocumento4 páginasComo Fazer Queijo GorgonzolaRoberta SabinoAinda não há avaliações
- Pirólise de PequiDocumento72 páginasPirólise de PequiIara SilveiraAinda não há avaliações
- Manual do DesenvolvedorDocumento52 páginasManual do DesenvolvedorDihego CostaAinda não há avaliações
- O Conflito Como SociaçãoDocumento7 páginasO Conflito Como SociaçãoLarissa GuimarãesAinda não há avaliações
- Método de Custo MínimoDocumento12 páginasMétodo de Custo MínimoEdson Arlindo Nhatuve100% (1)
- Arquitetura e Organização de ComputadoresDocumento52 páginasArquitetura e Organização de ComputadoresBruno AraújoAinda não há avaliações
- Medições elétricas: projetos de instrumentosDocumento7 páginasMedições elétricas: projetos de instrumentosMarcelo José CividiniAinda não há avaliações
- Isomeria Química FundamentosDocumento65 páginasIsomeria Química FundamentosDaniel SantanaAinda não há avaliações
- Estudos clínicos de não-inferioridadeDocumento7 páginasEstudos clínicos de não-inferioridadeRoberto DiasAinda não há avaliações
- Modelo de Avaliação BimestralDocumento1 páginaModelo de Avaliação BimestralLucas MarcelinoAinda não há avaliações
- Trabalho Avaliativo - Hidrostática - PressãoDocumento2 páginasTrabalho Avaliativo - Hidrostática - PressãoCarla Cristina Alves da SilvaAinda não há avaliações
- Cálculos estequiométricos para reações químicasDocumento4 páginasCálculos estequiométricos para reações químicasTelmo CarmoAinda não há avaliações
- Sistema de Injeção Rochester EFI MULTEC 700Documento7 páginasSistema de Injeção Rochester EFI MULTEC 700silvio ortizAinda não há avaliações
- Aula sobre Juros CompostosDocumento91 páginasAula sobre Juros CompostosMariana SouzaAinda não há avaliações
- Manual de Piloto PrivadoDocumento106 páginasManual de Piloto PrivadoRodrigo Cesar RighiAinda não há avaliações
- PROPOSTA GERAÇÃO DE 3000 KWH MesDocumento9 páginasPROPOSTA GERAÇÃO DE 3000 KWH MesFilipe LopesAinda não há avaliações
- B1 90 TB1000 01 02 PortugueseDocumento11 páginasB1 90 TB1000 01 02 PortugueseEMT EBRAinda não há avaliações
- Gabarito - Aulas5 6 8Documento50 páginasGabarito - Aulas5 6 8Tarso RezendeAinda não há avaliações
- Relatório 6Documento12 páginasRelatório 6Felipe SouzaAinda não há avaliações
- Joins Banco DadosDocumento2 páginasJoins Banco DadostcriccoAinda não há avaliações
- Frases de Céticos e AteusDocumento20 páginasFrases de Céticos e AteusPaulo AcostaAinda não há avaliações
- Cap 08 - FloculaçãoDocumento52 páginasCap 08 - FloculaçãoPaulo FreitasAinda não há avaliações
- Tensão - ExercíciosDocumento97 páginasTensão - ExercíciosFireX JyuoiAinda não há avaliações
- Mã -  Dulo 04 Matemà - ¡tica1Documento31 páginasMã -  Dulo 04 Matemà - ¡tica1Roni ItamarAinda não há avaliações
- 03 Apostila Versao Digital Raciocinio Logico Atualizada 002.575.571!48!1645656821Documento134 páginas03 Apostila Versao Digital Raciocinio Logico Atualizada 002.575.571!48!1645656821jucilene DantasAinda não há avaliações
- CT-0460 - SRP 4075E Flex - 2021-08 - (Trilingue) - REV.004Documento24 páginasCT-0460 - SRP 4075E Flex - 2021-08 - (Trilingue) - REV.004André DavidAinda não há avaliações
- Artigo 433Documento10 páginasArtigo 433AnnaAinda não há avaliações
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- Inteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNo EverandInteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNota: 5 de 5 estrelas5/5 (3)
- Instalações elétricas e o projeto de arquiteturaNo EverandInstalações elétricas e o projeto de arquiteturaAinda não há avaliações
- O Que Todo Atirador Precisa Saber Sobre BalísticaNo EverandO Que Todo Atirador Precisa Saber Sobre BalísticaNota: 5 de 5 estrelas5/5 (1)
- Biomecânica Básica dos Exercícios: Membros InferioresNo EverandBiomecânica Básica dos Exercícios: Membros InferioresNota: 3.5 de 5 estrelas3.5/5 (8)
- Exclusão e abraço: Uma reflexão teológica sobre identidade, alteridade e reconciliaçãoNo EverandExclusão e abraço: Uma reflexão teológica sobre identidade, alteridade e reconciliaçãoAinda não há avaliações
- Educação ambiental: A formação do sujeito ecológicoNo EverandEducação ambiental: A formação do sujeito ecológicoAinda não há avaliações
- Eletricista Residencial E PredialNo EverandEletricista Residencial E PredialNota: 3 de 5 estrelas3/5 (1)
- Dimensionamento e Planejamento de Máquinas e Implementos AgrícolasNo EverandDimensionamento e Planejamento de Máquinas e Implementos AgrícolasNota: 1 de 5 estrelas1/5 (2)
- Estratégias E Macetes Matemáticos Para ConcurseirosNo EverandEstratégias E Macetes Matemáticos Para ConcurseirosAinda não há avaliações
- Motores automotivos: evolução, manutenção e tendênciasNo EverandMotores automotivos: evolução, manutenção e tendênciasNota: 5 de 5 estrelas5/5 (1)
- Cartas xamânicas: A descoberta do poder através da energia dos animaisNo EverandCartas xamânicas: A descoberta do poder através da energia dos animaisNota: 4 de 5 estrelas4/5 (10)
- Uma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNo EverandUma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNota: 4 de 5 estrelas4/5 (13)