Escolar Documentos
Profissional Documentos
Cultura Documentos
Gerador SenTiva™ M1000
Enviado por
amarco.music7Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Gerador SenTiva™ M1000
Enviado por
amarco.music7Direitos autorais:
Formatos disponíveis
Gerador SenTiva™ M1000
Gerador SenTiva™ M1000
O Modelo 1000 é um gerador de pulso implantável e programável para o tratamento de epilepsia refratária. O Modelo 1000
fornece estimulação em resposta a aumentos rápidos da frequência cardíaca, que podem estar associados a crises, permite
programação dia-noite, programação programada e registro de baixa frequência cardíaca e posição prona.
O modelo 1000 é compatível com estes componentes do sistema:
COMPONENTE MODELO
COMPATIBILIDADE
Eletrodo 302, 303, 304
Dispositivo tipo Wand M2000
Software Tablet M3000 (todas as versões)
Tunelizador 402
Pacote de acessórios 502
Ímãs 220
Parâmetros de Estimulação Configurações de Parâmetros Disponíveis
Corrente de saída (0-2,0 mA em etapas de 0,125 mA)(2,0-3,5 mA em etapas de 0,250 mA)(+0,1 mA ou +10%; o que for maior)
Frequência do sinal 1, 2, 5, 10, 15, 20, 25, 30 Hz ±6%
Largura de pulso 130, 250, 500, 750, 1000 µseg ±10%
Sinal LIGADO (Modo normal: 7, 14, 21, 30, 60 s)(Modo ímã: 7, 14, 21, 30, 60 se)(Modo AutoStim: 30, 60 s)
Sinal DESLIGADO (0,2, 0,3, 0,5, 0,8, 1,1, 1,8, 3 min, e 5 a 180 min )(5 a 60 em etapas de 5-min; 60 a 180 em etapas de 30-min)(+4,4 s ou +/-1%, o que for maior)
Ativação do ímã Fornecida pela aplicação do ímã (corrente de saída, largura de pulso e tempo de sinal ligado podem ser programados independentemente para esse fim)
AutoStim Resposta automática de taquicardia (corrente de saída, largura de pulso e tempo de sinal ligado podem ser programados independentemente para esse fim)
Além disso, a detecção de crises, a sensibilidade aos batimentos cardíacos e o limiar para AutoStim podem ser programados independentemente para esse fim.
Programação Dia/Noite Ativada ou Desativada; Quando ativado, permite que os usuários programem o gerador e forneçam 2 conjuntos independentes de parâmetros de
estimulação em momentos diferentes durante um período de 24 horas.
Programação Agendada Ativada ou Desativada; Quando habilitado permite que o usuário agende aumentos na corrente de saída usando um protocolo de até 7 etapas.
Baixa frequência cardíaca (LHR) Permite que um médico defina um limiar de detecção de 30 a 60 bpm em incrementos de 10 bpm. Os eventos de LHR são armazenados na memória dos
ESPECIFICAÇÕES DO GERADOR
geradores e visíveis durante as visitas de acompanhamento do paciente através do programador.
Posição prona Uma vez calibrados, os eventos de posição prona são armazenados na memória dos geradores e visíveis durante as visitas de acompanhamento do
paciente através do programador.
Os eventos de Frequência Cardíaca Baixa e Posição Prona são apenas para fins informativos.
Relatórios de Telemetria Fonte de Alimentação
Relatório de histórico do dispositivo ID do paciente, data do implante, número do Química Monofluoreto de carbono de lítio
modelo, número de série, Tensão 3.3 V, circuito aberto
Ativações magnéticas, tempo total ON, tempo total de
Capacidade nominal 1,7 Amp-hora
operação e data de fabricação
Relatório de diagnóstico do dispositivo ID do paciente, ID do modelo, número de série, data do Taxa da auto-descarga <1% por ano
implante,
status de comunicação, status da corrente de Medições (Típicas)
saída, corrente medida entregue, impedância de
Receptáculo do eletrodo 0,126 pol (3,2 mm) nominal
eletrodo e indicadores de status da bateria (IFI, N
EOS, EOS) Dimensões 1.pol x 1.pol x 0.pol
(45mm x 32mm x 6,9mm)
Características Físicas - Materiais Peso 0,56 ox (16g)
Caixa Titânio, hermeticamente selada
Cabeçote Poliuretano — Tecothane TT-1075D-M
Força de retenção do conector
Blocos de conector de eletrodo Aço inoxidável Com Eletrodo de Terapia VNS >10N
Plug do parafuso de fixação Nenhum componente do Sistema de Terapia VNS é feito
com látex de borracha natural.
Consulte os Manuais do Médico de Terapia Terapia para obter informações completas sobre a programação e diagnósticos. Para
prescrição completa e informações de segurança importantes, visite www.vnstherapy.co.uk/safety-information, pergunte ao seu
representante da Terapia VNS Therapy ou ligue para os Serviços Técnicos Clínicos em 1-866-882-8804
Este dispositivo é aprovado pela marca CE.
Breve Resumo1 das Informações de Segurança para o Sistema de Terapia VNS™
[Indicação de epilepsia] (fevereiro de 2021)
1. USO PRETENDIDO/ INDICAÇÕES A segurança e eficácia do Sistema de Terapia VNS não foram estabelecidas para uso durante a gravidez. A VNS
Epilepsia (Não EUA)- O Sistema de Terapia VNS é indicado para uso como terapia adjuvante na redução da deve ser usada durante a gravidez apenas se for claramente necessário.
frequência de crises em pacientes cujo distúrbio epiléptico é dominado por crises parciais (com ou sem O Sistema de Terapia VNS é indicado para uso apenas na estimulação do nervo vago esquerdo na área do pescoço
generalização secundária) ou crises generalizadas refratárias a medicamentos para crises. AspireSR™, SenTiva™ e dentro da bainha carotídea. O Sistema de Terapia VNS é indicado para uso apenas na estimulação do nervo vago
SenTiva DUO™ apresentam um Modo de Estimulação Automática que se destina a pacientes que sofrem crises esquerdo abaixo, onde os ramos cardíacos cervicais superiores e inferiores se separam do nervo vago. É
importante seguir os procedimentos de controle de infecção. Infecções relacionadas a qualquer dispositivo
associadas a aumentos do ritmo cardíaco conhecidos como implantado são
taquicardia ictal. difíceis de tratar e podem exigir que o dispositivo seja explantado. O paciente deve receber antibióticos no pré-
2. CONTRAINDICAÇÕES operatório. O cirurgião deve garantir que todos os instrumentos estejam estéreis antes do procedimento.
Vagotomia - O Sistema de Terapia VNS não pode ser usado em pacientes após uma vagotomia Crianças (<12 anos de idade) podem ter maior risco de infecção quando comparadas a pacientes adolescentes e
cervical bilateral ou esquerda. adultos (≥ 12 anos). Deve ser salientada a monitorização cuidadosa da infeção no local, bem como a prevenção da
Diatermia - Não usar diatermia de ondas curtas, diatermia de micro-ondas ou diatermia de ultrassom manipulação do local cirúrgico após o implante em crianças.
terapêutico em pacientes implantados com um Sistema de Terapia VNS. O ultrassom diagnóstico não está O Sistema de Terapia VNS pode afetar a operação de outros dispositivos implantados, como marcapassos
incluído nesta contraindicação. cardíacos e desfibriladores implantados. Possíveis efeitos incluem problemas de detecção e respostas inadequadas
3. ADVERTÊNCIAS — GERAL do dispositivo. Se o paciente precisar de marcapasso implantável concomitante, terapia desfibriladora
Os médicos devem informar os pacientes sobre todos os riscos potenciais e eventos adversos discutidos ou outros tipos de estimuladores, pode ser necessária uma programação cuidadosa de cada sistema para
nos manuais do médico. Este documento não se destina a substituir os manuais médicos completos. otimizar o benefício do paciente em cada dispositivo.
A segurança e eficácia do Sistema de Terapia VNS não foram estabelecidas para usos fora do capítulo “Uso A reversão da polaridade do eletrodo foi associada a um aumento da chance de bradicardia em estudos em
Pretendido/Indicações” dos manuais do médico. animais. É importante que os eletrodos estejam ligados ao nervo vago esquerdo na orientação correta. Também é
A segurança e eficácia do Sistema de Terapia VNS em pacientes com disfunção predisposta de sistemas de importante certificar-se de que os cabos com pinos de conector duplo estão inseridos corretamente (banda de
condução cardíaca (via de reentrada) não foram estabelecidas. Se clinicamente indicado, recomenda-se a marcador branco para + conexão) nos receptáculos de cabo do gerador.
realização de eletrocardiogramas pós-implante e monitorização com Holter. O paciente pode usar um colar cervical durante a primeira semana para ajudar a garantir a estabilização adequada do
Bradicardia pós-operatória pode ocorrer entre pacientes com certas arritmias cardíacas subjacentes. eletrodo.
É importante seguir os procedimentos de implantação recomendados e os testes intraoperatórios do produto Não programe o Sistema de Terapia VNS para um tratamento "ligado" ou de estimulação periódica por pelo
descritos no capítulo Procedimento de Implantação do manual do médico. Durante o Diagnóstico do Sistema menos 14 dias após o implante inicial ou de substituição.
intraoperatório (Teste de Eletrodo), ocorreram incidentes pouco frequentes de bradicardia e/ou assistolia. Para os Modelos 100, 101, 102 e 102R, não use frequências de 5 Hz ou abaixo para estimulação de longo prazo.
Se houver assistolia, bradicardia grave (frequência cardíaca < 40 bpm) ou uma alteração clinicamente Reiniciar o gerador de pulsos desliga o dispositivo (corrente de saída = 0 mA). Para os modelos 100, 101, 102 e
significativa na frequência cardíaca durante um Diagnóstico do Sistema (Teste de Eletrodo) ou durante o início da 102R, a reinicialização do gerador de pulsos resultará na perda do histórico do dispositivo.
estimulação, os médicos devem estar preparados para seguir as diretrizes consistentes com Suporte Avançado Pacientes que fumam podem ter um risco aumentado de irritação laríngea.
de Vida Cardíaca (ACLS).
Geradores apenas com AutoStim — Para dispositivos que detectam mudanças na frequência cardíaca, a detecção
Dificuldade de deglutição (disfagia) pode ocorrer com estimulação ativa, e a aspiração pode resultar do aumento de falsos positivos pode causar estimulação não intencional. Exemplos de casos em que a frequência cardíaca
das dificuldades de deglutição. Os pacientes com dificuldades de deglutição pré-existentes correm maior risco de pode aumentar incluem exercício, atividade física e alterações autonômicas normais na frequência cardíaca, tanto
aspiração. acordados quanto dormindo, etc.
Pode ocorrer dispneia (falta de ar) com a Terapia VNS ativa. Qualquer paciente com doença pulmonar subjacente Geradores apenas com AutoStim — Para o recurso AutoStim, a localização física do dispositivo afeta criticamente
ou insuficiência, como doença pulmonar obstrutiva crônica ou asma, pode estar em risco aumentado de sua capacidade de sentir adequadamente os batimentos cardíacos. Portanto, deve-se tomar cuidado para seguir o
dispneia. processo de seleção do local do implante descrito no Procedimento de Implantação. Observe que este
Pacientes com apneia obstrutiva do sono (SAOS) podem ter um aumento nos eventos apneicos durante a procedimento de seleção do local do implante pode ser realizado no pré-operatório como parte do exame
estimulação. Reduzir a frequência do estímulo ou prolongar o tempo de "desligamento" pode prevenir a cirúrgico do paciente.
exacerbação da SAOS. A estimulação do nervo vago também pode causar apneia do sono de novo início em Somente M1000/1000-D — Como o recurso de Programação Programada permite que o gerador aplique aumentos
pacientes que não foram previamente diagnosticados com esse distúrbio. de terapia em intervalos programados, pode não ser apropriado para uso em pacientes não verbais ou
O mau funcionamento do dispositivo pode causar estimulação dolorosa ou estimulação por corrente contínua. incapazes de usar o ímã do paciente para interromper a estimulação indesejada. Da mesma forma, tenha cuidado
Qualquer um dos eventos pode causar danos nos nervos. Os pacientes devem ser instruídos a usar o ímã para para o uso deste recurso em pacientes com histórico de apneia obstrutiva do sono, falta de ar, tosse, dificuldades
interromper a estimulação se suspeitarem de um mau funcionamento e, em seguida, entrar em contato com de deglutição ou aspiração.
seu médico imediatamente para avaliação posterior. 6. PERIGOS AMBIENTAIS E DE TERAPIA MÉDICA
Os pacientes com o Sistema de Terapia VNS ou qualquer parte do Sistema de Terapia VNS implantado devem Os pacientes devem ter cuidado razoável ao evitar dispositivos que gerem um forte campo elétrico ou magnético.
ter procedimentos de ressonância magnética realizados apenas conforme descrito na ressonância magnética Se um gerador interromper a operação enquanto na presença de interferência eletromagnética (EMI), afastar-se
com as instruções de uso do Sistema de Terapia VNS. Em alguns casos, a cirurgia será necessária para remover da fonte pode permitir que ele retorne ao seu modo normal de operação.
o Sistema de Terapia VNS se for necessária uma leitura usando uma bobina corporal de RF de transmissão. A operação do Sistema de Terapia VNS deve sempre ser verificada realizando o diagnóstico do dispositivo após
A estimulação excessiva em um ciclo de trabalho em excesso (isto é, um que ocorre quando o tempo "LIGADO" é qualquer um dos procedimentos mencionados nos manuais do médico.
maior do que o tempo "DESLIGADO") e a estimulação de alta frequência (isto é, estimulação a ≥50 Hz) resultou em Para imagens claras, as pacientes podem precisar ser posicionadas especialmente para procedimentos de
danos degenerativos nos nervos em animais de laboratório. mamografia, devido à localização do gerador no tórax.
Pacientes que manipulam o gerador e o eletrodo através da pele (Síndrome de Twiddler) podem danificar ou A radiação terapêutica pode danificar os circuitos do gerador. Fontes de tal radiação incluem radiação terapêutica,
desconectar o eletrodo do gerador e/ou possivelmente causar danos ao nervo vago. máquinas de cobalto e aceleradores lineares. O efeito da radiação é cumulativo, com a dosagem total
O leitor, o programador e o ímã do paciente são dispositivos não seguros para RM. Esses dispositivos são riscos de determinando a extensão do dano. Os efeitos da exposição a essa radiação podem variar de uma perturbação
projéteis e não devem ser trazidos para a sala do scanner de RM. temporária a danos permanentes e podem não ser detectáveis imediatamente.
Geradores apenas com AutoStim — O recurso Modo AutoStim não deve ser usado em pacientes com A desfibrilação externa pode danificar o gerador.
arritmias clinicamente significativas ou que estejam usando tratamentos que interfiram nas respostas O uso de eletrocirurgia [eletrocautério ou dispositivos de ablação por radiofrequência (RF)] pode
intrínsecas normais da frequência cardíaca (por exemplo, dependência de marcapasso, desfibrilador danificar o gerador.
implantável, medicamentos bloqueadores A ressonância magnética (MRI) não deve ser realizada usando uma bobina corporal de RF de transmissão para
beta adrenérgicos). Os doentes também não devem ter antecedentes de incompetência cronotrópica certas configurações de dispositivos de terapia VNS ou sob determinadas condições específicas. Em alguns
[frequentemente observada em doentes com bradicardia sustentada (frequência cardíaca < 50 bpm)]. casos, o aquecimento do eletrodo causado pela bobina do corpo de RF de transmissão durante a ressonância
4. ADVERTÊNCIAS — EPILEPSIA magnética pode resultar em ferimentos graves. Campos eletromagnéticos estáticos, gradientes e de
O Sistema de Terapia VNS só deve ser prescrito e monitorado por médicos que tenham treinamento e radiofrequência (RF) associados à ressonância magnética podem alterar as configurações do gerador (ou seja,
experiência específicos no gerenciamento de crises e no uso deste dispositivo. Deve ser implantado apenas por reiniciar parâmetros) ou ativar o dispositivo VNS se a saída do Modo Magnético permanecer "ligada". Observe
médicos treinados em cirurgia da bainha carotídea e que tenham recebido treinamento específico na que certas bobinas de cabeçote do sistema de ressonância magnética (MR) operam no modo somente recepção
implantação deste dispositivo. e requerem o uso da bobina do corpo de RF de transmissão. Outros sistemas de RM usam uma bobina de
O Sistema de Terapia VNS não é terapêutico. Os médicos devem alertar os pacientes que o Sistema de Terapia cabeçote de RF de transmissão/recepção. As bobinas locais ou de superfície também podem ser bobinas de RF
VNS não é uma cura para a epilepsia e que, como as crises podem ocorrer inesperadamente, os pacientes devem apenas de recepção que requerem a bobina do corpo de RF de transmissão para MRI. O uso de uma bobina
consultar um médico antes de se envolver em atividades não supervisionadas, como dirigir, nadar e tomar de RF de recepção não altera os riscos da bobina de corpo de RF de transmissão A exposição do Sistema de Terapia VNS a
banho, e em esportes cansativos que podem prejudicá-los ou a outros. qualquer
bobina de RF de transmissão deve ser evitada. Não realize exames de ressonância magnética usando qualquer
Morte súbita inesperada na epilepsia (SUDEP): Até agosto de 1996, 10 mortes súbitas e inesperadas (definitivas,
bobina de RF de transmissão nas zonas de exclusão definidas. Consulte a ressonância magnética com as instruções
prováveis e possíveis) foram registradas entre os 1.000 pacientes implantados e tratados
de uso do Sistema de Terapia VNS para obter detalhes ou instruções adicionais para casos especiais, como quebras
Com o dispositivo Terapia VNS. Durante esse período, esses pacientes acumularam 2.017 pacientes-ano de de eletrodo ou sistemas de Terapia VNS parcialmente explantados.
exposição. Algumas dessas mortes poderiam representar mortes relacionadas a crises em que a crise não foi
observada, por exemplo, à noite. Esse número representa uma incidência de 5,0 óbitos definitivo, provável e A litotripsia por ondas de choque extracorpóreas pode danificar o gerador. Se a terapia de ultrassom
possível SUDEP por 1.000 pacientes-ano. Embora essa taxa exceda a esperada em uma população saudável (não terapêutica for necessária, evite posicionar a área do corpo onde o gerador está implantado no banho-maria
ou em qualquer outra posição que o exponha à terapia de ultrassom. Se esse posicionamento não puder ser
epiléptica) pareada por idade e sexo, está dentro da faixa de estimativas para pacientes com epilepsia que não
evitado,
recebem estimulação do nervo vago, variando de 1,3 mortes por SUDEP para
programe a saída do gerador para 0 mA para o tratamento e, após a terapia, reprograme o gerador para os
a população geral de pacientes com epilepsia, a 3,5 (para definitivo e provável) para uma população de ensaios
parâmetros originais.
clínicos de drogas antiepilépticas (AED) recentemente estudada semelhante à coorte clínica do Sistema de Terapia
VNS, a 9,3 para pacientes com epilepsia medicamente intratável que eram candidatos à cirurgia de epilepsia. Se o paciente receber tratamento médico para o qual a corrente elétrica é passada através do corpo (como de
uma unidade de DEZENAS), o gerador deve ser ajustado para 0 mA ou a função do gerador deve ser monitorada
5. PRECAUÇÕES — GERAL durante os estágios iniciais do tratamento.
Os médicos devem informar os pacientes sobre todos os riscos potenciais e eventos adversos discutidos O ultrassom terapêutico de rotina pode danificar o gerador e pode ser inadvertidamente concentrado pelo
nos manuais do médico da VNS Therapy. dispositivo, causando danos ao paciente.
Os médicos prescritores devem ter experiência no diagnóstico e tratamento da depressão ou epilepsia e devem Para obter informações completas relacionadas a ambientes ocupacionais domésticos, telefones celulares,
estar familiarizados com a programação e uso do Sistema de Terapia VNS. outros riscos ambientais, outros dispositivos e monitores de ECG, consulte os manuais do médico.
Os médicos que implantam o Sistema de Terapia VNS devem ter experiência na realização de cirurgia na bainha
carotídea e devem ser treinados na técnica cirúrgica relacionada à implantação do 7.EVENTOS ADVERSOS — EPILEPSIA
Os eventos adversos relatados durante os estudos clínicos como estatisticamente significativos estão listados
Sistema de Terapia VNS.
abaixo em ordem alfabética: ataxia (perda da capacidade de coordenar o movimento muscular); dispepsia
(indigestão); dispneia (dificuldade em respirar, falta de ar); hipoestesia (sensação de tato prejudicada); aumento
da tosse; infecção; insônia (incapacidade de dormir); laringismo (garganta, espasmos laríngeos); náuseas; dor;
parestesia (picadas na pele); faringite (inflamação da faringe, garganta); alteração da voz (rouquidão); vômitos. Os
eventos adversos relatados na investigação clínica do recurso AutoStim foram comparáveis.
26-0009-0100/6 (OUS) — 1
LIVANOVA USA, INC. LIVANOVA BÉLGICA NV 1 As informações contidas neste Breve Resumo para Médicos representam trechos parciais de
100 Cyberonics Boulevard Ikaroslaan 83 informações importantes de prescrição retiradas dos manuais do médico. (Cópias dos manuais do
Houston, Texas 77058 , EUA B -1930 Zaventem, médico e do paciente da Terapia VNS são publicadas em www.livanova.com) As informações não se
Tel: +1 (281) 228-7200 / Bélgica destinam a servir como um substituto para uma compreensão completa e completa do material
+1 (800) 332-1375 Tel: +3227209593 apresentado em todos os manuais do médico para o Sistema de Terapia VNS e suas partes
componentes, nem essas informações representam a divulgação completa de todas as informações
Fax: +1 (281) 218-9332 Fax: +3227206053 pertinentes sobre o uso deste produto, possíveis complicações de segurança ou resultados de eficácia.
www.livanova.com
Todas as marcas e nomes comerciais são propriedade da LivaNova ou propriedade das subsidiárias consolidadas da LivaNova e estão protegidos pelas leis de propriedade
intelectual aplicáveis. Apenas por conveniência, as marcas e nomes comerciais da LivaNova podem aparecer sem os símbolos ® ou TM, mas tais referências não se
destinam a indicar de forma alguma que a LivaNova não afirmará, em toda a extensão sob a lei aplicável, os direitos da LivaNova a essas marcas e nomes comerciais. A
permissão prévia da Livanova é necessária para o uso ou reprodução de tais direitos de propriedade intelectual. IM-7600688-EPI-BR
Você também pode gostar
- Monitor Multiparâmetros C80 - Descrição para CotaçãoDocumento7 páginasMonitor Multiparâmetros C80 - Descrição para CotaçãoDaniel BauerAinda não há avaliações
- Monitores de Paciente Infinity Delta e Delta XLDocumento8 páginasMonitores de Paciente Infinity Delta e Delta XLdiegolimanaAinda não há avaliações
- 3instrumentacao e Dispositivos Medicos Unidade IIIDocumento33 páginas3instrumentacao e Dispositivos Medicos Unidade IIIAndré PhelpsAinda não há avaliações
- PQ 600 PDFDocumento3 páginasPQ 600 PDFDenisson VargasAinda não há avaliações
- CE7012 Mala de Testes Compacta para Subestacoes Testes Primarios e SecundariosDocumento11 páginasCE7012 Mala de Testes Compacta para Subestacoes Testes Primarios e SecundariosconproveAinda não há avaliações
- Informações Gerais OSCILOSCOPIO DSO3D12 3 em 1Documento3 páginasInformações Gerais OSCILOSCOPIO DSO3D12 3 em 1Zeferino OlivAinda não há avaliações
- PQ 700Documento3 páginasPQ 700Kenner MartinsAinda não há avaliações
- Manual Do Módulo de Análise de Arritmia e STDocumento11 páginasManual Do Módulo de Análise de Arritmia e STVinicius BardellaAinda não há avaliações
- Manual de Operação Tan Delta 10 KV MinipaDocumento17 páginasManual de Operação Tan Delta 10 KV Minipachevette dl100% (1)
- Catálogo BM5Documento2 páginasCatálogo BM5Luan AlvesAinda não há avaliações
- MAR722Documento2 páginasMAR722David Vichi de BritoAinda não há avaliações
- Datasheet UC30-21416A 6054710 PTDocumento7 páginasDatasheet UC30-21416A 6054710 PTElian SilvaAinda não há avaliações
- 57521C55-1F35-4F89-BFDD-75A38DC54363 (1)Documento2 páginas57521C55-1F35-4F89-BFDD-75A38DC54363 (1)solomagoAinda não há avaliações
- Relatório Da OS7Documento1 páginaRelatório Da OS7TOmei tapaAinda não há avaliações
- Gerador SinalDocumento5 páginasGerador SinalMárcio SpezaniAinda não há avaliações
- Manual Ms 8000Documento8 páginasManual Ms 8000Paulo Sergio GarciaAinda não há avaliações
- Aplicações Do CI de Alarme MC14600 (ART1162) PDFDocumento7 páginasAplicações Do CI de Alarme MC14600 (ART1162) PDFSabrynna SilvaAinda não há avaliações
- WEG SMW Catalogo 50115363 PTDocumento12 páginasWEG SMW Catalogo 50115363 PTAdilson Leite ProençaAinda não há avaliações
- Catalogo PowerNET P600 G4Documento4 páginasCatalogo PowerNET P600 G4Danilovsk1Ainda não há avaliações
- TR 949GLDocumento13 páginasTR 949GLDenis BrussaAinda não há avaliações
- Variador de Frequência VS Mini J7Documento20 páginasVariador de Frequência VS Mini J7marcof91Ainda não há avaliações
- Multimedidor de Energia Multifunção PL MPDocumento24 páginasMultimedidor de Energia Multifunção PL MPWesley pereira de paulaAinda não há avaliações
- LR-X100 DatasheetDocumento3 páginasLR-X100 DatasheetTassio PetryAinda não há avaliações
- Temporizador Coel HWKT e LWKTDocumento12 páginasTemporizador Coel HWKT e LWKTmestre_giovasAinda não há avaliações
- PowerPad 8336Documento2 páginasPowerPad 8336Marcelo LacerdaAinda não há avaliações
- Manual de Instruções HWKT LWKT Rev.4Documento12 páginasManual de Instruções HWKT LWKT Rev.4ynoueAinda não há avaliações
- Temporizador Contador CoelDocumento12 páginasTemporizador Contador CoelAGNALDOJULIOAinda não há avaliações
- Mutimedidor Digita HD194I - Manual BRDocumento5 páginasMutimedidor Digita HD194I - Manual BRAlex FermianoAinda não há avaliações
- Instramed - Cardiomax - Especificações GeraisDocumento2 páginasInstramed - Cardiomax - Especificações GeraisPatricia SouzaAinda não há avaliações
- WEG Motor Scan 50078032 Catalogo PT PDFDocumento8 páginasWEG Motor Scan 50078032 Catalogo PT PDFbrunofp17Ainda não há avaliações
- LR-X50 DatasheetDocumento3 páginasLR-X50 DatasheetTassio PetryAinda não há avaliações
- Manual BJ 750Documento17 páginasManual BJ 750Isaias Weiber100% (1)
- Manual de Procedimentos Dosímetro Kr130Documento12 páginasManual de Procedimentos Dosímetro Kr130alexmeioambienteAinda não há avaliações
- Nj6005 (Modulo Misto 6 Ea 4 Sa Tensao Corrente)Documento16 páginasNj6005 (Modulo Misto 6 Ea 4 Sa Tensao Corrente)Joao RochaAinda não há avaliações
- CCD-818, TRV58, TRV98 BR Ver.1.4Documento214 páginasCCD-818, TRV58, TRV98 BR Ver.1.4Anonymous Lfgk6vygAinda não há avaliações
- Et 2907 PDFDocumento98 páginasEt 2907 PDFtiago_bergonse100% (1)
- ITMRT200Documento2 páginasITMRT200arthurvalinhoAinda não há avaliações
- Manual Medidor de VibraçãoDocumento8 páginasManual Medidor de Vibraçãoemamoraes12Ainda não há avaliações
- FT-50AWP DatasheetDocumento2 páginasFT-50AWP DatasheetMarcos BalbinoAinda não há avaliações
- Tec2Plus PortuguesDocumento6 páginasTec2Plus PortuguesVanderMucioAinda não há avaliações
- Gefran 1600V 1800VDocumento21 páginasGefran 1600V 1800VMarcelo da Mota CorreaAinda não há avaliações
- Gefran 2300Documento16 páginasGefran 2300Diogo GonçalvesAinda não há avaliações
- Et 4080 1100 BR PDFDocumento33 páginasEt 4080 1100 BR PDFUlisses RodriguesAinda não há avaliações
- Cat Desfibrilador - Phase 3 - PORTDocumento2 páginasCat Desfibrilador - Phase 3 - PORTPedro HenriqueAinda não há avaliações
- Nj6000 Modulo 8 Ea Tensao CorrenteDocumento14 páginasNj6000 Modulo 8 Ea Tensao CorrenteWanderson Luiz AzevedoAinda não há avaliações
- Contador Digital Programável Microprocessado: Introdução Série: CDFM-03Documento8 páginasContador Digital Programável Microprocessado: Introdução Série: CDFM-03Rufino PereiraAinda não há avaliações
- Manual Dual 8,2 MHZDocumento16 páginasManual Dual 8,2 MHZAlexandre Camargo67% (3)
- Guia Do Gerador de Formas de Onda e Funções Arbitrárias - B&K PrecisionDocumento32 páginasGuia Do Gerador de Formas de Onda e Funções Arbitrárias - B&K Precisionapocalipc100% (1)
- Gefran 1600Documento20 páginasGefran 1600Oleoplan NordesteAinda não há avaliações
- Manual 600Documento30 páginasManual 600raphael diniz de almeidaAinda não há avaliações
- Medidas e ErrosDocumento12 páginasMedidas e ErrosVivi Tabchoury VieiraAinda não há avaliações
- Manual Multimetro Et-3910Documento21 páginasManual Multimetro Et-3910Paulo PeruchinAinda não há avaliações
- Manual DEC-6000Documento53 páginasManual DEC-6000Gilberto MarcelinoAinda não há avaliações
- ITVB100 - VIbraçãoDocumento3 páginasITVB100 - VIbraçãoestluisgustavoAinda não há avaliações
- Desfibrilador Cardiolife TEC-5600Documento4 páginasDesfibrilador Cardiolife TEC-5600Marcos Ulysses VoltarelliAinda não há avaliações
- Prolife - Catalogo p15 p12 p10Documento4 páginasProlife - Catalogo p15 p12 p10Pedro Andre Rodrigues NetoAinda não há avaliações
- CLPT CLPT 2f CLPF W CLPW PTDocumento4 páginasCLPT CLPT 2f CLPF W CLPW PTMauricio RodriguesAinda não há avaliações
- InteliLite NT AMF25 - Treinamento 2017Documento188 páginasInteliLite NT AMF25 - Treinamento 2017Vinícius de Paula100% (2)
- 59953-347104texto 7 Politica Gestao UnimedDocumento14 páginas59953-347104texto 7 Politica Gestao UnimedAugusto CésarAinda não há avaliações
- NR11 - Procedimento para Uso de Ponte Rolante - 2023Documento5 páginasNR11 - Procedimento para Uso de Ponte Rolante - 2023João MouraAinda não há avaliações
- Estrela Et Al, 2014.en - PTDocumento9 páginasEstrela Et Al, 2014.en - PTAndré VictorAinda não há avaliações
- Vestibulopatias TentandoDocumento21 páginasVestibulopatias TentandoMarcos Paulo SalesAinda não há avaliações
- Sidney Silva de Assis R.a.1888786-5Documento6 páginasSidney Silva de Assis R.a.1888786-5Marielen MartinsAinda não há avaliações
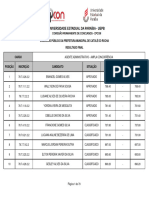
- Resultado Final Catole Do RochaDocumento79 páginasResultado Final Catole Do RochadgvcxfAinda não há avaliações
- CaninosDocumento5 páginasCaninosLuis Filipi RodriguesAinda não há avaliações
- Análise Do Comportamento Aplicada Ao Autismo e Atuação Socialmente Responsável No BrasilDocumento16 páginasAnálise Do Comportamento Aplicada Ao Autismo e Atuação Socialmente Responsável No Brasilraphael guilherme costaAinda não há avaliações
- Referencias Do TCCDocumento12 páginasReferencias Do TCCdaniel andradeAinda não há avaliações
- AULA 6 - Atuação Do Farmacêutico Na Dispensação de Antimicrobianos Com Foco Na Resistência BacterianaDocumento11 páginasAULA 6 - Atuação Do Farmacêutico Na Dispensação de Antimicrobianos Com Foco Na Resistência BacterianaEdmilson FariasAinda não há avaliações
- Classificação Das Gengivites e Periodontites Segundo As Normas IIDocumento61 páginasClassificação Das Gengivites e Periodontites Segundo As Normas IIGiovana CabralAinda não há avaliações
- Farmacologia On Line - Farmacologia I - 2Documento4 páginasFarmacologia On Line - Farmacologia I - 2Dr. CARLOS CUNHAAinda não há avaliações
- Escalas de AvaliaçãoDocumento28 páginasEscalas de AvaliaçãoGabriela100% (1)
- Manual de Normas, Rotinas e POP - S de Enfermaem Do CAPSi RECRIAR (09.12) .19Documento185 páginasManual de Normas, Rotinas e POP - S de Enfermaem Do CAPSi RECRIAR (09.12) .19Maria Fernanda Alencar100% (1)
- Cvi Argentina 3145965Documento4 páginasCvi Argentina 3145965ivo Machado SilvaAinda não há avaliações
- Avaliação Psicológica Pré-Cirurgia Bariátrica - A Experiência Dos PacientesDocumento9 páginasAvaliação Psicológica Pré-Cirurgia Bariátrica - A Experiência Dos PacientesMaria Gorete Arruda Oliveira PSICOLOGIAAinda não há avaliações
- Ficha de Preparação Final - Trabalho III - Solução de Cloridrato de PropranololDocumento3 páginasFicha de Preparação Final - Trabalho III - Solução de Cloridrato de PropranololLuísa SilvaAinda não há avaliações
- Fispq Agua Sanitaria YpeDocumento16 páginasFispq Agua Sanitaria YpeDiego Cavaglieri100% (1)
- Pop Lab Hem - 002 Confeccionar Esfregaco Sanguineo Manual202111111111111Documento7 páginasPop Lab Hem - 002 Confeccionar Esfregaco Sanguineo Manual202111111111111Maisa Santana PereiraAinda não há avaliações
- Inter Ven Cao em Psicologia Clinic ADocumento35 páginasInter Ven Cao em Psicologia Clinic ARosaAinda não há avaliações
- Os - MotoristaDocumento2 páginasOs - MotoristaThaina ManvailerAinda não há avaliações
- A Importância Das Bactérias para A HumanidadeDocumento2 páginasA Importância Das Bactérias para A HumanidadeElisabeth TölkeAinda não há avaliações
- Apostila Visão e AudiçãoDocumento2 páginasApostila Visão e AudiçãocamilaAinda não há avaliações
- Atividade Presencial para ConsultaDocumento9 páginasAtividade Presencial para ConsultaNatreFe50% (2)
- Conceitos Mobilização e Manipulação Articular:: Professor Dr. Elias PortoDocumento36 páginasConceitos Mobilização e Manipulação Articular:: Professor Dr. Elias PortoRicardo PontesAinda não há avaliações
- Ibfc 2020 Ebserh Arquiteto ProvaDocumento12 páginasIbfc 2020 Ebserh Arquiteto ProvaJéssica LacerdaAinda não há avaliações
- 1654709458481ebook #10 - FIV e FELV Tudo o Que Você Precisa SaberDocumento20 páginas1654709458481ebook #10 - FIV e FELV Tudo o Que Você Precisa SaberimaraguimaraesAinda não há avaliações
- CHECCHIA. SOUZA JR. LIMA. (Orgs.) Por Uma Psicanálise Revolucionária. Otto GrossDocumento271 páginasCHECCHIA. SOUZA JR. LIMA. (Orgs.) Por Uma Psicanálise Revolucionária. Otto GrossFelipe Araujo67% (3)
- Relacao Entre A Etica e Outras CienciasDocumento26 páginasRelacao Entre A Etica e Outras CienciasEduardo Raul88% (8)
- AULA PR TICA 01 - Imunologia CL Nica 27-09-2023Documento4 páginasAULA PR TICA 01 - Imunologia CL Nica 27-09-2023Thamires GabrielaAinda não há avaliações