Escolar Documentos
Profissional Documentos
Cultura Documentos
Laudo - para - Testes - Rapidos UPA E HMS
Laudo - para - Testes - Rapidos UPA E HMS
Enviado por
MARIA APARECIDA MOTA SOARESTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Laudo - para - Testes - Rapidos UPA E HMS
Laudo - para - Testes - Rapidos UPA E HMS
Enviado por
MARIA APARECIDA MOTA SOARESDireitos autorais:
Formatos disponíveis
Prefeitura de Santarém/Secretaria Municipal De SAÚDE
LAUDO PARA TESTE RÁPIDO
IDENTIFICAÇÃO DA UNIDADE DE SAÚDE
Unidade de Saúde: _____________________________________________
Endereço: _____________________________________________________ Telefone: ____________________
IDENTIFICAÇÃO DO USUÁRIO
Nome do Usuário (sem abreviatura): ___________________________________________________ Sexo:
Nome Social: ______________________________________________________________________ ( )F ( )M
Data de Nascimento: _____/_____/______
Data da realização dos exames:
Método: Imunocromatografia Amostra: Sangue Total
_____/_____/______
TESTE RÁPIDO PARA DETECÇÃO DE ANTICORPOS ANTI-HIV
TESTE 1 - HIV: Nome do Produto/Fabricante: ____________________ Lote: _____________ Val:_____________
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
TESTE 2 - HIV: Nome do Produto/Fabricante: ____________________ Lote: _____________ Val: _____________
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
INTERPRETAÇÃO DO RESULTADO FINAL – HIV
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
TESTE RÁPIDO PARA DETECÇÃO DA SÍFILIS
Nome do Produto/Fabricante: ______________________ Lote: _______________________Val: ______________
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
TESTE RÁPIDO PARA DETECÇÃO DE ANTICORPOS PARA HEPATITE C (Anti-HCV)
Nome do Produto/Fabricante: ______________________ Lote: _______________________ Val: _____________
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
TESTE RÁPIDO PARA DETECÇÃO DE ANTÍGENOS PARA HEPATITE B (HBsAg)
Nome do Produto/Fabricante: ______________________ Lote: _______________________ Val: ______________
( ) REAGENTE ( ) NÃO REAGENTE ( ) NÃO REALIZADO
RESPONSABILIDADE PELA EXECUÇÃO DOS TESTES RÁPIDOS
Responsável pela Execução do Teste: _____________________________________________________
(Assinatura e Carimbo)
Responsável pelo Laudo: _______________________________________________________________
(Assinatura e Carimbo)
ATENÇÃO - TESTE RÁPIDO - HIV:
1) Resultado definido com o Fluxograma 1, conforme estabelecido pela Portaria nº 29 de 17 de dezembro de 2013;
2) Realizar aconselhamento pré e pós-teste independentemente do resultado;
3) Em caso de Amostra Reagente para HIV realizar imediatamente CD4 e a Carga Viral (CV);
4) Em caso de resultado não reagente e permanecendo a suspeita de infecção pelo HIV, o TR deverá ser repetido
após 30 dias;
A amostra com resultados discordantes entre TR1 e TR2 não terá seu resultado definido. Nesse caso, deve-se repetir o
fluxograma; persistindo a discordância dos resultados, uma nova amostra deverá ser coletada por punção venosa e
encaminhada para o laboratório para ser testada com um dos fluxogramas definidos pelo Ministério da Saúde
ATENÇÃO - TESTE RÁPIDO - SÍFILIS:
Resultado definido pelo Fluxograma 3, conforme estabelecido no Manual Técnico para Diagnóstico da Sífilis – 2016.
1) O teste rápido para detecção da Sífilis é um TESTE TREPONÊMICO.
2) Em caso de resultado não reagente e permanecendo a suspeita de infecção pela Sífilis, o TR deverá ser repetido
após 30 dias;
3) A situação clínica e epidemiológica do paciente deverá ser observada;
No caso de resultado reagente no teste rápido para Sífilis: coletar amostra por punção venosa para realizar teste não
treponêmico quantitativo.
ATENÇÃO - TESTE RÁPIDO - ANTI-HCV:
1) Amostra não reagente para o anticorpo contra o vírus da hepatite C (anti-HCV): Em caso de suspeita de infecção
pelo HCV, uma nova amostra deverá ser coletada 30 dias após a data da coleta desta amostra para a realização de
um novo teste.
2) Amostra reagente para o anticorpo contra o vírus da hepatite C (anti-HCV): “Realizar confirmação do diagnóstico
da infecção pelo HCV utilizando um teste de detecção direta do vírus (HCV-RNA).
(http://www.aids.gov.br/ptbr/pub/2015/manual-tecnico-para-o-diagnostico-das-hepatites-virais).
3) “A vacina contra a hepatite A faz parte do calendário de vacinação do SUS para crianças de 15 meses até 4 anos
de idade (http://portalarquivos.saude. gov.br/campanhas/pni/). Além disso, ela está disponível nos Crie, sendo
indicada para as situações previstas no Manual dos Centros de Referência para Imunobiológicos Especiais”.
4) “A vacina contra a hepatite B faz parte do calendário de
vacinação da criança
(http://portalarquivos.saude.gov.br/campanhas/pni/). Além disso, ela está disponível nas salas de vacina do
Sistema Único de Saúde (SUS) para todas as pessoas, independentemente de idade e/ou condições de
vulnerabilidade, e para as situações previstas no Manual dos Centros de Referência para Imunobiológicos
Especiais”
ATENÇÃO - TESTE RÁPIDO - HBsAg:
1) Amostra não reagente para antígeno de superfície do vírus da Hepatite B (HBsAg): em caso de suspeita de
infecção pelo HBV, uma nova amostra deverá ser coletada 30 dias após a data da coleta desta amostra e
submetido a novo teste.
2) Amostra reagente para antígeno de superfície do vírus da Hepatite B (HBsAg): uma nova amostra deverá ser
coletada por punção venosa para a realização do momento do diagnóstico e encaminhamento oportuno ao
Serviço de Referência para Hepatite B, conforme o momento da infecção. (Manual Técnico para Diagnóstico das
hepatitesVirais:http://www.aids.gov.br/pt-br/pub/2015/manual-tecnico-para-o-diagnostico-das-hepatites-virais).
3) “A vacina contra a hepatite A faz parte do calendário de vacinação do SUS para crianças de 15 meses até 4 anos
de idade (http://portalarquivos.saude. gov.br/campanhas/pni/). Além disso, ela está disponível nos Crie, sendo
indicada para as situações previstas no Manual dos Centros de Referência para Imunobiológicos Especiais”.
4) “A vacina contra a hepatite B faz parte do calendário de vacinação da criança
http://portalarquivos.saude.gov.br/campanhas/pni/). Além disso, ela está disponível nas salas de vacina do
Sistema Único de Saúde (SUS) para todas as pessoas, independentemente de idade e/ou condições de
vulnerabilidade, e para as situações previstas no Manual dos Centros de Referência para Imunobiológicos
Especiais”
Você também pode gostar
- LTRD Alice AmandaDocumento1 páginaLTRD Alice AmandaAlice Amanda100% (1)
- Laudo para Testes RapidosDocumento1 páginaLaudo para Testes Rapidosp9012wqAinda não há avaliações
- Laudo para Testes RapidosDocumento2 páginasLaudo para Testes RapidosMoisa Santos100% (2)
- Laudo Teste Swab CovidDocumento1 páginaLaudo Teste Swab CovidIthalo BoenosAinda não há avaliações
- Anexo IIDocumento1 páginaAnexo IINati Nati NatosaAinda não há avaliações
- Casos M4 TorchsDocumento8 páginasCasos M4 TorchsRaíla Soares100% (1)
- Como Não Morrer O Livro de Receitas (Portuguese Edition) (Michael Greger, Gene Stone e Robin Robertson)Documento272 páginasComo Não Morrer O Livro de Receitas (Portuguese Edition) (Michael Greger, Gene Stone e Robin Robertson)Lady_Anne_of_Avalon100% (2)
- Laudo Do Resultado Teste Rápido de GravidezDocumento1 páginaLaudo Do Resultado Teste Rápido de GravidezBardock CodmAinda não há avaliações
- For - Multi.052 - V1 Realização de Teste Rápido Covid 19Documento1 páginaFor - Multi.052 - V1 Realização de Teste Rápido Covid 19Carlos LemesAinda não há avaliações
- Check List de Segurança em CirurgiaDocumento2 páginasCheck List de Segurança em CirurgiaSuel Costa100% (2)
- Teste Rapido Sifilis, HivDocumento1 páginaTeste Rapido Sifilis, HivJeanEscobarAinda não há avaliações
- Modelo Teste Rapido Hiv EtcDocumento1 páginaModelo Teste Rapido Hiv EtcLaísZapeliniDeBonaAinda não há avaliações
- LAUDO PARA HIV TESTE 1 E 2 E HEPATITE C - UNIDADES TÉCNICO - Doc NOVODocumento2 páginasLAUDO PARA HIV TESTE 1 E 2 E HEPATITE C - UNIDADES TÉCNICO - Doc NOVOBoa USAFAAinda não há avaliações
- Anexo IIDocumento1 páginaAnexo IINati Nati NatosaAinda não há avaliações
- Anexo IIDocumento1 páginaAnexo IINati Nati NatosaAinda não há avaliações
- Teste Rapido FormularioDocumento5 páginasTeste Rapido FormulariotesteAinda não há avaliações
- Hepatite B Anti HbsDocumento3 páginasHepatite B Anti HbsannacarolinessantosAinda não há avaliações
- Nome: Miria Rosa FerreiraDocumento2 páginasNome: Miria Rosa FerreiraMauricio Mendonça NunezAinda não há avaliações
- Termo de ConsentimentoDocumento4 páginasTermo de ConsentimentoernandocastroAinda não há avaliações
- Laudo Teste Rapido CovidDocumento1 páginaLaudo Teste Rapido CovidEnfermagem UBS VILA RIOAinda não há avaliações
- Modelos Laudos HIV Positivo (HIV Tipo 2)Documento2 páginasModelos Laudos HIV Positivo (HIV Tipo 2)Laboratório Jofre CohenAinda não há avaliações
- Anamnese Obstétrica: Lavínia Gonçalves - 4º SemestreDocumento11 páginasAnamnese Obstétrica: Lavínia Gonçalves - 4º SemestreGabrielle LucianoAinda não há avaliações
- Laudo 1-350798Documento3 páginasLaudo 1-350798vinicius.vmalufAinda não há avaliações
- HIV ExameDocumento1 páginaHIV Exameayalagisele95Ainda não há avaliações
- 66556.51250.92178.1500788 PDFDocumento1 página66556.51250.92178.1500788 PDFVinicius RicardoAinda não há avaliações
- Questões Gabarito para SiteDocumento4 páginasQuestões Gabarito para Sitedasilva903Ainda não há avaliações
- Pop - Segurança Na Realização Do TesteDocumento18 páginasPop - Segurança Na Realização Do Testegislayneoliveira.farmaAinda não há avaliações
- RDC - 48 - 2000 - Roteiro de Inspeção Do Programa de Controle de InfecçãoDocumento13 páginasRDC - 48 - 2000 - Roteiro de Inspeção Do Programa de Controle de Infecçãocassia.limaAinda não há avaliações
- Pop Testes RápidoDocumento16 páginasPop Testes RápidoJuvile Tavares100% (1)
- Portaria151 2009Documento10 páginasPortaria151 2009ronertlAinda não há avaliações
- Imprimir 34Documento1 páginaImprimir 34marcelo mendesAinda não há avaliações
- 03 Ficha Retorno Mensal PrEPDocumento2 páginas03 Ficha Retorno Mensal PrEPMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Avaliação Do Desempenho De Quatro Conjuntos Diagnósticos (elisa) Para Triagem Sorológica Do HivNo EverandAvaliação Do Desempenho De Quatro Conjuntos Diagnósticos (elisa) Para Triagem Sorológica Do HivAinda não há avaliações
- GABARITODocumento13 páginasGABARITOSophia DiasAinda não há avaliações
- REQ09619 - Formulário para Pedido de Exames de Patologia e TCLE - ÁlvaroDocumento2 páginasREQ09619 - Formulário para Pedido de Exames de Patologia e TCLE - ÁlvarodiagnosesantamariaAinda não há avaliações
- Nota Informativa Hepatites ViraisDocumento4 páginasNota Informativa Hepatites ViraisvictoryavarelaAinda não há avaliações
- GabaritoDocumento10 páginasGabaritoGutierre SilvaAinda não há avaliações
- Resultados On Lineprint23287download 1&v 1623363465185Documento1 páginaResultados On Lineprint23287download 1&v 1623363465185Elisandra CargninAinda não há avaliações
- Controle de RacDocumento1 páginaControle de RacDayane FerreiraAinda não há avaliações
- Nota Tecnica Teste Rapido de Hanseniase Revkkc - PPTX 1Documento15 páginasNota Tecnica Teste Rapido de Hanseniase Revkkc - PPTX 1Jaime Emanuel Brito AraujoAinda não há avaliações
- Formulário para Pedido de Exames de Patologia: Antonia Das Graças Marques Aguiar Rocha 19 10 1960 X 09 08 2023 9361Documento2 páginasFormulário para Pedido de Exames de Patologia: Antonia Das Graças Marques Aguiar Rocha 19 10 1960 X 09 08 2023 9361diagnosesantamariaAinda não há avaliações
- Diagnostico Molecular Coronavirus Covid-19Documento1 páginaDiagnostico Molecular Coronavirus Covid-19Jhonata AlvesAinda não há avaliações
- QUESTIONÁRIO Ressonância MagnéticaDocumento3 páginasQUESTIONÁRIO Ressonância MagnéticaAlexandre SennaAinda não há avaliações
- Formulario Requisicao Exame UnicoDocumento2 páginasFormulario Requisicao Exame UnicoNilo Lacerda Jr.50% (2)
- Fluxograma de Acidente BiologicoDocumento7 páginasFluxograma de Acidente BiologicoResidência Médica FOCOAinda não há avaliações
- Laudo Do Resultado Teste Rã Pido de Gravidez 2Documento1 páginaLaudo Do Resultado Teste Rã Pido de Gravidez 2Heloisa XavierAinda não há avaliações
- 16 - Testes Sorológicos de Triagem para Doenças Infecciosas em Doadores de SangueDocumento16 páginas16 - Testes Sorológicos de Triagem para Doenças Infecciosas em Doadores de SanguePaula NovaisAinda não há avaliações
- Formulário para Pedido de Exames de Patologia e TcleDocumento2 páginasFormulário para Pedido de Exames de Patologia e TcleLucas EmmanoelAinda não há avaliações
- Imprimir 12Documento1 páginaImprimir 12marcelo mendesAinda não há avaliações
- PCR para Coronavirus COVID-19: Reginaldo Da Silva VanderleyDocumento1 páginaPCR para Coronavirus COVID-19: Reginaldo Da Silva VanderleyRVAinda não há avaliações
- Testes para Triagem Do Sangue (Banco de Sangue)Documento23 páginasTestes para Triagem Do Sangue (Banco de Sangue)Aylton Vadner SitoeAinda não há avaliações
- Hepatite B Laudo Positivo PDF 17921Documento1 páginaHepatite B Laudo Positivo PDF 17921esfcentral1100% (1)
- Nota Tecnica 32023 HanseniaseDocumento9 páginasNota Tecnica 32023 HanseniaseGeralmente EuAinda não há avaliações
- LaudoAntigeno 2A5MontadosNoA4 Janeiro2022 20220207Documento1 páginaLaudoAntigeno 2A5MontadosNoA4 Janeiro2022 20220207Edmar PereiraAinda não há avaliações
- Instrumento de Consulta de Enfermagem Pré NatalDocumento4 páginasInstrumento de Consulta de Enfermagem Pré NatalSandra BarbosaAinda não há avaliações
- Teste Rapido para Covid-19Documento1 páginaTeste Rapido para Covid-19Gilvana SiqueiraAinda não há avaliações
- Nota Técnica Nº 15 SES SUBVS SVE DVAT CI 2020Documento6 páginasNota Técnica Nº 15 SES SUBVS SVE DVAT CI 2020Eduardo LopesAinda não há avaliações
- Casos Clà NicosDocumento3 páginasCasos Clà NicosLaura Beatriz RittAinda não há avaliações
- Laudo de Resultados de Testes RápidoDocumento1 páginaLaudo de Resultados de Testes RápidoLucas SantosAinda não há avaliações
- Manual HBsAg - Bioclin (2018)Documento9 páginasManual HBsAg - Bioclin (2018)ARMANDOAinda não há avaliações
- ARQUIVO 7 ANVERSO Formulário de ResultadosDocumento2 páginasARQUIVO 7 ANVERSO Formulário de ResultadosBrunna RodriguesAinda não há avaliações
- Avaliação Neurologica em HanseniaseDocumento9 páginasAvaliação Neurologica em HanseniaseEnfa Ana Paula Candido USF Alto das PombasAinda não há avaliações
- EXERCICIOS Relacionamento Interpessoal ColetivoDocumento2 páginasEXERCICIOS Relacionamento Interpessoal ColetivoMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Afe - Concessão - Farmácias e DrogariasDocumento4 páginasAfe - Concessão - Farmácias e DrogariasMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Crfpa - Rcontrato de TrabalhoDocumento1 páginaCrfpa - Rcontrato de TrabalhoMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Fluxo Carga Viral ATUALIZADODocumento2 páginasFluxo Carga Viral ATUALIZADOMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Coleta HTLVDocumento1 páginaColeta HTLVMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Crfpa - Termo de Compromisso Da EmpresaDocumento1 páginaCrfpa - Termo de Compromisso Da EmpresaMARIA APARECIDA MOTA SOARESAinda não há avaliações
- CRFPA - Requerimento Pessoa JuridicaDocumento1 páginaCRFPA - Requerimento Pessoa JuridicaMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Crfpa - Solicitação de Responsabilidade TécnicaDocumento1 páginaCrfpa - Solicitação de Responsabilidade TécnicaMARIA APARECIDA MOTA SOARESAinda não há avaliações
- POP - Dispensa de HIVDocumento13 páginasPOP - Dispensa de HIVMARIA APARECIDA MOTA SOARESAinda não há avaliações
- Formulário de Peticionamento RecursoDocumento3 páginasFormulário de Peticionamento RecursoMARIA APARECIDA MOTA SOARESAinda não há avaliações
- História Da AuriculoterapiaDocumento13 páginasHistória Da AuriculoterapiaGenesys Construções FinanceiroAinda não há avaliações
- Unidade 3Documento42 páginasUnidade 3Geovanna KeyllaAinda não há avaliações
- Trabalho Slide ProntoDocumento11 páginasTrabalho Slide ProntoDiego LadwigAinda não há avaliações
- Uso de Rede Mosquiteira em MocambiqueDocumento9 páginasUso de Rede Mosquiteira em Mocambiqueivandra Ilda100% (5)
- Lista de Perguntas - REVALIDA 2010-2015 :)Documento22 páginasLista de Perguntas - REVALIDA 2010-2015 :)Lohana VidaurreAinda não há avaliações
- BalantidíaseDocumento9 páginasBalantidíaseDayane AndradeAinda não há avaliações
- MCC - Cristina Ribeiro Fernandes - Filipa Cabral Tavares de Lima - Maria Francisca Duarte Dias S - de MirandaDocumento7 páginasMCC - Cristina Ribeiro Fernandes - Filipa Cabral Tavares de Lima - Maria Francisca Duarte Dias S - de MirandaPedro BorgesAinda não há avaliações
- CoxsackiosesDocumento56 páginasCoxsackiosesLucas Leite100% (1)
- Ficha de Avaliação Fisioterápica em UroginecologiaDocumento4 páginasFicha de Avaliação Fisioterápica em UroginecologiaJéssica Juliana FisioterapeutaAinda não há avaliações
- Terapia de Reidratação Oral PDFDocumento17 páginasTerapia de Reidratação Oral PDFsuporte telessaudeAinda não há avaliações
- Plano de Trabalho Brasil OrienteDocumento9 páginasPlano de Trabalho Brasil OrienteAndersonAnaniasAinda não há avaliações
- Fisioterapia Na Dor LombarDocumento72 páginasFisioterapia Na Dor LombarThales Wallison Ferreira89% (9)
- Material UroDocumento2 páginasMaterial UroAna Carolina OliveiraAinda não há avaliações
- Patogenias HumanasDocumento22 páginasPatogenias HumanasIrisdalva OliveiraAinda não há avaliações
- Ficha de Trabalho DSTDocumento1 páginaFicha de Trabalho DSTmarisafAinda não há avaliações
- 8 Aula IRCDocumento12 páginas8 Aula IRCThuany VattimoAinda não há avaliações
- Apresentação e Informações Dra Camila VilelaDocumento7 páginasApresentação e Informações Dra Camila VilelaCássia LázaroAinda não há avaliações
- Ficha de Avaliação de EstriaDocumento2 páginasFicha de Avaliação de EstriaCamila SousaAinda não há avaliações
- 11-PROGRAMA DE CONTROLE DA TUBERCULOSE (Modo de Compatibilidade)Documento37 páginas11-PROGRAMA DE CONTROLE DA TUBERCULOSE (Modo de Compatibilidade)Laura SantoroAinda não há avaliações
- Biologia 2 Ano ABC Grupos SanguineosDocumento2 páginasBiologia 2 Ano ABC Grupos SanguineosClaudio NeriAinda não há avaliações
- Casos Clínicos SífilismDocumento44 páginasCasos Clínicos SífilismFabio Souza100% (1)
- Sinais Alerta Na Avaliação NeurológicaDocumento30 páginasSinais Alerta Na Avaliação NeurológicaJULIANO CHAVES COTRIM DE SOUZAAinda não há avaliações
- Doenças No Baralho CiganoDocumento2 páginasDoenças No Baralho CiganoAnne RodriguesAinda não há avaliações
- POP de APH AL SGT FaldinDocumento5 páginasPOP de APH AL SGT FaldinvaldemarAinda não há avaliações
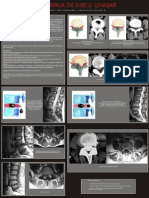
- Hérnia de Disco LombarDocumento1 páginaHérnia de Disco LombarJulio CesarAinda não há avaliações
- Doenças OrificiaisDocumento33 páginasDoenças OrificiaisLuiz Augusto0% (1)
- Colestase NeonatalDocumento5 páginasColestase NeonatalSamir NozawaAinda não há avaliações
- Ficha Botox e Mapa de AplicaçãoDocumento5 páginasFicha Botox e Mapa de AplicaçãoMaressa ChavesAinda não há avaliações