Escolar Documentos
Profissional Documentos
Cultura Documentos
Ligações Químicas - 20240305 - 231531 - 0000
Enviado por
lidy1038teen0 notas0% acharam este documento útil (0 voto)
3 visualizações1 páginaTítulo original
Ligações Químicas_20240305_231531_0000
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
3 visualizações1 páginaLigações Químicas - 20240305 - 231531 - 0000
Enviado por
lidy1038teenDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 1
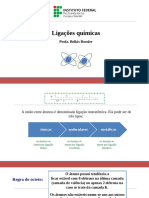
Ligações Químicas
Ligações interatômicas:
São ligações realizadas entre átomos com o intuito de ficar o mais estável possível.
Ligação iônica: transferência definitiva de elétrons de um átomo para outro, resultando na
formação de cátions e aníons. para ocorrer, a diferença de eletronegatividade deve ser grande.
características dos compostos iônicos:
Apresentam PF e PE altos
São maus condutores no estado solido
Ótimos condutores em solução aquasa ou fundidos
Ligação metálica ligação entre metais, que liberam seus elétrons periféricos formando uma
nuvem de elétrons que circula pelo reticulo cristalino (onde tem afins metálicos). Propriedades:
Alto PF e PE
Alta condutividade térmica e elétrica
Maleabilidade (moldar em lâminas) e ductibilidade (fios)
Ligação covalente ou molecular:
Essa ligação e caracterizada pelo compartilhamento de elétrons e ocorre quando há pouca
diferença de eletronegatividade entre os átomos
Simples apolar ocorre entre átomos iguais ou que apresentam a mesmo valor de
eletronegatividade, pais, nesses casos, não haverá formação de polos.
simples polar quando os átomos ligantes apresentam diferença de eletronegatividade, a
ligação possuirá um polo negativo e um polo positivo
Covalente dupla e tripla:
dupla dois pares eletrônicos compartilhados
tripla três pares compartilhados
Você também pode gostar
- Aula 06 - Ligacoes QuimicasDocumento15 páginasAula 06 - Ligacoes QuimicasMel ValdicleideAinda não há avaliações
- Aula 2 - Ciência Dos MateriasDocumento22 páginasAula 2 - Ciência Dos MateriasViniciosAinda não há avaliações
- MOD2 - UA5 - Ciência Dos MateriaisDocumento15 páginasMOD2 - UA5 - Ciência Dos Materiaiswandersonmendes508Ainda não há avaliações
- Ligações PrimáriasDocumento50 páginasLigações PrimáriasHenry MorenoAinda não há avaliações
- Ligações QuímicasDocumento30 páginasLigações QuímicasAnimes BackupAinda não há avaliações
- Ligações Iônicas Ou EletrovalentesDocumento4 páginasLigações Iônicas Ou EletrovalentesThais CerqueiraAinda não há avaliações
- Temperatura de Fusao e Ligação QuimicaDocumento44 páginasTemperatura de Fusao e Ligação QuimicaDanielle FernandesAinda não há avaliações
- Lista 2Documento8 páginasLista 2ThallesAlmeidaAinda não há avaliações
- Desafio Atrações InteratômicasDocumento2 páginasDesafio Atrações Interatômicassalomao lucio dos santosAinda não há avaliações
- Ciencias Dos Materiais - Cap II-ligações Químicas SlidesDocumento14 páginasCiencias Dos Materiais - Cap II-ligações Químicas SlidesLeonardo SilveiraAinda não há avaliações
- CAP II-LIGAÇÕES QUÍMICAS SlidesDocumento14 páginasCAP II-LIGAÇÕES QUÍMICAS SlidesMario GomesAinda não há avaliações
- Aula 3.3 Propriedades Químicas Dos MineraisDocumento13 páginasAula 3.3 Propriedades Químicas Dos Mineraisdionar.miguel30Ainda não há avaliações
- Ligações Químicas (Iônica)Documento5 páginasLigações Químicas (Iônica)Stefany CamiloAinda não há avaliações
- Cap3 Elem Quim CristalinaDocumento15 páginasCap3 Elem Quim CristalinaDercioAinda não há avaliações
- Correlação Química e Propriedade Dos MateriaisDocumento18 páginasCorrelação Química e Propriedade Dos MateriaisjorrriqueAinda não há avaliações
- Ligações QuímicasDocumento2 páginasLigações QuímicasMathias SchumannAinda não há avaliações
- Ligações Interatômicas - Aula 03Documento24 páginasLigações Interatômicas - Aula 03Mateus GarciaAinda não há avaliações
- Aula 4 - Ligao CovalenteDocumento13 páginasAula 4 - Ligao CovalenteLucas AndradeAinda não há avaliações
- Ligações QuímicasDocumento7 páginasLigações QuímicasDomingos MbanaAinda não há avaliações
- Atividade 2Documento2 páginasAtividade 2Karinne RodriguesAinda não há avaliações
- Ligações Químicas, Polaridade, ReaçõesDocumento20 páginasLigações Químicas, Polaridade, ReaçõesAlineCristineAinda não há avaliações
- Ligações Químicas - Iônica e CovalenteDocumento3 páginasLigações Químicas - Iônica e CovalenteJerusa FreitasAinda não há avaliações
- Ligações Químicas PrimáriasDocumento18 páginasLigações Químicas PrimáriasRenatoAinda não há avaliações
- Eletrônica Fundamental - UNIDADE 1Documento52 páginasEletrônica Fundamental - UNIDADE 1Ramseis RibeiroAinda não há avaliações
- 3 Ligação Interatômica v12.03.2015Documento21 páginas3 Ligação Interatômica v12.03.2015pereiramcfAinda não há avaliações
- Aula 3 - Ligações InteratômicasDocumento38 páginasAula 3 - Ligações InteratômicasThadilla SouzaAinda não há avaliações
- LigaCao Quimica 9a ClasseDocumento9 páginasLigaCao Quimica 9a ClasseNélio MachadoAinda não há avaliações
- Ligacoes Quimicas Aula 1 e 2Documento22 páginasLigacoes Quimicas Aula 1 e 2thamilisqmcAinda não há avaliações
- Aula Ligação QuímicaDocumento18 páginasAula Ligação QuímicaJoel SáAinda não há avaliações
- Ligações Químicas22Documento14 páginasLigações Químicas22renatamarques93fourAinda não há avaliações
- Ligacoes QuimicasDocumento121 páginasLigacoes QuimicasmanudaoAinda não há avaliações
- Ligações InteratomicasDocumento1 páginaLigações InteratomicasRenata BudelAinda não há avaliações
- 3 - Estrutura Atomica PDFDocumento26 páginas3 - Estrutura Atomica PDFrenanAinda não há avaliações
- Ligações QuímicasDocumento6 páginasLigações QuímicasWuazoAinda não há avaliações
- Esc Est Técnica José CanellasDocumento4 páginasEsc Est Técnica José CanellasguilhermekwacheleskiAinda não há avaliações
- Ligações QuímicasDocumento3 páginasLigações Químicasaugustorodrigo995Ainda não há avaliações
- Enlace Químico - Cepre Uni - Rev2Documento4 páginasEnlace Químico - Cepre Uni - Rev2Jean PaúlAinda não há avaliações
- Apostila 7 - Subst Ncias MolecularesDocumento24 páginasApostila 7 - Subst Ncias MolecularesPaulo SérgioAinda não há avaliações
- Ligações IntramolecularesDocumento4 páginasLigações IntramolecularesAnaAinda não há avaliações
- Aula 3 - Ligacao QuimicaDocumento34 páginasAula 3 - Ligacao QuimicaJúnior AlbuquerqueAinda não há avaliações
- Ligacoes QuimicasDocumento17 páginasLigacoes Quimicasvaldo pondecaAinda não há avaliações
- Ligações QuímicasDocumento16 páginasLigações QuímicasAmandaAinda não há avaliações
- Força e Comprimentos Das LigaçõesDocumento7 páginasForça e Comprimentos Das LigaçõesRansMilerDantasAinda não há avaliações
- Quimica LaSalle Ligacoes Quimicas ResumoDocumento5 páginasQuimica LaSalle Ligacoes Quimicas ResumoJoão Paulo MouraAinda não há avaliações
- Capitulo 2 Lista de ExerciciosDocumento8 páginasCapitulo 2 Lista de ExerciciosMaykon TuraAinda não há avaliações
- Ligações Quimicas SlidesDocumento30 páginasLigações Quimicas SlidesjuliaAinda não há avaliações
- Apostila 7 - Substâncias MolecularesDocumento36 páginasApostila 7 - Substâncias MolecularesGustavo MarinhoAinda não há avaliações
- Trabalho de Química PDFDocumento18 páginasTrabalho de Química PDFLetício FranciscoAinda não há avaliações
- INTRODUÇAODocumento75 páginasINTRODUÇAODanielly Gripa de PaulaAinda não há avaliações
- Des e Aplicações Dos Metais e LigasDocumento42 páginasDes e Aplicações Dos Metais e Ligassocramsilva100% (10)
- Introd. A Ciencias Dos MateriaisDocumento4 páginasIntrod. A Ciencias Dos MateriaisElam Gomes de LimaAinda não há avaliações
- Ligações Químicas 02-1Documento53 páginasLigações Químicas 02-1Rauan BrendonAinda não há avaliações
- Ligações InteratômicasDocumento12 páginasLigações InteratômicasCarina SiqueiraAinda não há avaliações
- Ligações Químicas - Teoria Do Octeto, Ligação Iônica, Ligação Metálica e CovalenteDocumento15 páginasLigações Químicas - Teoria Do Octeto, Ligação Iônica, Ligação Metálica e CovalentePedroAinda não há avaliações
- Aula 01B - Materiais SemicondutoresDocumento30 páginasAula 01B - Materiais Semicondutoresandre28polvinhoAinda não há avaliações
- 1 Estudo Dirigido Cap 1 e 2 PauloAndreDocumento4 páginas1 Estudo Dirigido Cap 1 e 2 PauloAndreYabuki ShingoAinda não há avaliações
- Aula 6 - QuímicaDocumento30 páginasAula 6 - QuímicaBeatriz MenezesAinda não há avaliações