Escolar Documentos
Profissional Documentos
Cultura Documentos
Exercicios Gravimetria
Enviado por
Lange De SouzaTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Exercicios Gravimetria
Enviado por
Lange De SouzaDireitos autorais:
Formatos disponíveis
Universidade Federal do Pará
Serviço público federal
Faculdade de Química
Professor: Dr. Heronides Adonias Dantas Filho
Tutor: Isaque Gemaque Medeiros
Disciplina: Química Analítica Teórica
EXERCICIO DE ANALITICA TEORICA GRAVIMETRIA
Entrega ate as 23:59 horas do dia 02/01/2021
INSTRUÇÕES
O aluno deve posta os exercícios resolvidos juntamente com os cálculos de cada
questão, não e necessário transcrever o comando de cada questão, mas e importante que
o aluno seja organizado, enumere cada resposta.
Sobre nem uma situação será aceito atividades fora da data de entrega, salve as
situações previstas em lei.
A plataforma suporta o tamanho máximo 50 MB.
Um único envio por aluno, por isso ao transforma seu exercício respondido em PDF,
salve em um único arquivo em PDF ou você estará se prejudicando.
Todas as atividades devem ser enviadas no próximo encontro, até as 23:59:59hs do
sábado, o envio e somente na plataforma.
A atividade deve ser manuscrita (escrita a mão). Não será aceito trabalhos digitados.
envie a atividade no formato PDF, para isso use um scanner para converte o
manuscrito em PDF ou o aplicativos de celular do tipo Tap Scanner e salve em PDF.
1) Um volume de 25 ml de solução fisiológica vendida no comércio farmacêutico, que
segundo a informação do fabricante apresenta uma concentração de 0,9%, foi tratada com
um excesso de solução precipitante de AgNO3 a 1N, formando um precipitado de cloreto
de prata (AgCl), cujo seu peso após realizadas todas as etapas gravimétricas, foi de
0,430g de AgCl.
a) Qual a quantidade em gramas de cloretos presentes na amostra
b) Qual o seu teor percentual na amostra ?
Dados: Ag Cl = 143,32 ; Cl = 35,5.
Ag+ + Cl- AgCl
2) O cálcio presente em uma amostra de 200,0 ml de uma água natural, foi determinada
pela precipitação do cátion na forma de Oxalato de Cálcio (CaC2O4) (PM= 96,070) pouco
solúvel, com o reagente precipitante ácido oxálico (H2C2O4). O oxalato de cálcio formado,
coletado em papel de filtro foi posteriormente convertido em Oxido de calcio CaO
(eliminação de CO2 e H2O pela ação oxidante do ar atmosférico), após a realização de
todas as etapas gravimétricas (precipitação, filtração, secagem). No processo gravimétrico
o cadinho tinha uma massa de 26,6002 g quando vazio. A massa do cadinho mais o CaO
(mol=56,077) obtida foi de 26,7134 g. Determine a quantidade e a concentração percentual
de Ca (P.M.= 40,078) na amostra analisada?
Ca + H2C2O4 CaC2O4
3) Determinar a quantidade e a concentração percentual de chumbo Pb presente em 100
ml de solução contida em um balão volumétrico. Desta solução foi tomada uma amostra de
25 ml e em seguida acrescentado 20 ml de solução de nitrato de crômio e 20 ml de
solução de bromato de potássio até a formação de precipitado de cromato de chumbo
PbCrO4. Após toda as etapas gravimétricas o precipitado final de PbCrO4 Formado pesou
0,800 gramas. Qual a quantidade e o valor percentual de Pb na amostra analisada.
Dados Pb = 207,19; PbCrO4 = 323,19
Pb + CrO4 PbCrO4
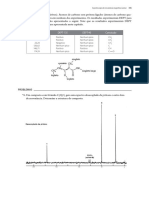
4) O teor em alumínio numa amostra pode ser determinado por precipitação como uma
base e calcinação a Al2O3, que é pesado. Qual a massa de alumínio numa amostra com
0,2365 g de precipitado calcinado?
5) O conteúdo em cálcio numa amostra de urina pode ser determinado pelo seguinte
procedimento:
1º – Precipitação do Ca2+, em meio alcalino, sob a forma de oxalato de cálcio (CaC2O4)
2º – Após lavagem do precipitado com água fria para remoção do oxalato livre, o sólido é
dissolvido em ácido, formando-se Ca2+ e H2C2O4.
3º – O ácido oxálico dissolvido é aquecido a 60 ºC e titulado com uma solução padrão de
permanganato de potássio até viragem para cor violeta (ponto final).
Supondo que na titulação de 5,00 mL de uma amostra de urina sujeita a este tratamento se
gastou 16,17 mL da solução padrão de permanganato, calcule a concentração de cálcio na
amostra de urina.
Dados: Para determinar a concentração rigorosa de permanganato de potássio procedeu-
se do seguinte modo: dissolveram-se 0,3562 g de Na2C2O4 num balão volumétrico de
250,00 mL, e titulou-se 10 mL desta solução com a solução de KMnO4, tendo-se gasto um
volume de 48,36 mL.
Você também pode gostar
- 1525096859PraConstruir - Ebook Laje PDFDocumento42 páginas1525096859PraConstruir - Ebook Laje PDFLuciana Lugon100% (1)
- Calculo EstequiometricoDocumento8 páginasCalculo EstequiometricoEraclitoSL100% (21)
- Volumetria IIDocumento45 páginasVolumetria IIAgar Abel MatsinheAinda não há avaliações
- Segunda Prova de QG - Gabarito - Versão FinalDocumento3 páginasSegunda Prova de QG - Gabarito - Versão FinalThomas JacobsenAinda não há avaliações
- Lista de Exercícios 4 - Equilíbrio Químico e Produto de SolubilidadeDocumento5 páginasLista de Exercícios 4 - Equilíbrio Químico e Produto de SolubilidadeNáthaly CoelhoAinda não há avaliações
- Gabarito - Lista de Exercícios - Verificação de Métodos AnalíticosDocumento12 páginasGabarito - Lista de Exercícios - Verificação de Métodos AnalíticosPamella RobertaAinda não há avaliações
- Extensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Documento9 páginasExtensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Pedro ManoelAinda não há avaliações
- 2a Lista de Exercícios 22015 2Documento6 páginas2a Lista de Exercícios 22015 2SheilaTardellyAinda não há avaliações
- Orientacoes para Projeto de CoquilhaDocumento74 páginasOrientacoes para Projeto de Coquilhagiokniess100% (2)
- Teste Espectrofotometria 2020.1Documento2 páginasTeste Espectrofotometria 2020.1René Villas Bôas Dos Santos100% (1)
- Lista CromatografiaDocumento3 páginasLista CromatografiaMayara LemosAinda não há avaliações
- Exercicios Absorcao e Emissao MolecularDocumento3 páginasExercicios Absorcao e Emissao MolecularCayo FariasAinda não há avaliações
- Espectrometria de Absorcao Molecular - Exercicios PDFDocumento6 páginasEspectrometria de Absorcao Molecular - Exercicios PDFccq256867Ainda não há avaliações
- Espectrometria de Absorcao Molecular - ExerciciosDocumento6 páginasEspectrometria de Absorcao Molecular - ExerciciosDébora AlvimAinda não há avaliações
- Resumo Farmacologia Do SNCDocumento2 páginasResumo Farmacologia Do SNCDébora MartinsAinda não há avaliações
- 6º Ano CiênciasDocumento2 páginas6º Ano CiênciasHeriberto Mota90% (39)
- Resumo Prática Gnosia IDocumento13 páginasResumo Prática Gnosia IJOYCE FAZOLLO FERRAZAinda não há avaliações
- Aula 2 - Erros e Tratamentos Dos Dados AnalíticosDocumento24 páginasAula 2 - Erros e Tratamentos Dos Dados AnalíticosVinícius Pianta100% (1)
- Balanceamento Químico - Explicação, Exemplos e Exercícios ResolvidosDocumento7 páginasBalanceamento Químico - Explicação, Exemplos e Exercícios ResolvidosGuaracyara Ribas AugustoAinda não há avaliações
- Exercicios - Resolvidos - Quimica - IV Substt PDFDocumento9 páginasExercicios - Resolvidos - Quimica - IV Substt PDFmarcellepratesAinda não há avaliações
- Medicina Legal - MergedDocumento18 páginasMedicina Legal - MergedRegiane PereiraAinda não há avaliações
- Relatório 1 - Química Analítica ExperimentalDocumento5 páginasRelatório 1 - Química Analítica ExperimentalMatheus RezendeAinda não há avaliações
- Resumo de ToxicologiaDocumento6 páginasResumo de ToxicologiaGiulia EstudosAinda não há avaliações
- Apostila Teórica Química Analítica EngenhariaDocumento42 páginasApostila Teórica Química Analítica EngenhariadanieleAinda não há avaliações
- Volumetria de PrecipitaçãoDocumento21 páginasVolumetria de Precipitaçãoana_s_freire100% (1)
- Exercicicos - CorrDocumento3 páginasExercicicos - CorrJoão Paulo Sousa100% (1)
- Espectofotometria IFRJDocumento36 páginasEspectofotometria IFRJMarlon FariaAinda não há avaliações
- Espectrometria de Absorcao Molecular - Exercicios PDFDocumento6 páginasEspectrometria de Absorcao Molecular - Exercicios PDFThiago RodriguesAinda não há avaliações
- Aula 02 - Avaliação de Dados Experimentais em Química AnalíticaDocumento45 páginasAula 02 - Avaliação de Dados Experimentais em Química AnalíticaMauricio Menezes100% (1)
- Química Analítica, Quantitativa - GravimetriaDocumento13 páginasQuímica Analítica, Quantitativa - GravimetriaRogério de SouzaAinda não há avaliações
- Apostila QualitativaDocumento45 páginasApostila Qualitativabruno100% (1)
- Resumo Farmacognosia IIDocumento2 páginasResumo Farmacognosia IIDogaaa100% (1)
- Exercicios Capitulo6Documento9 páginasExercicios Capitulo6Karine LeilaAinda não há avaliações
- Lista de Exercício Química Geral - ResoluçãoDocumento4 páginasLista de Exercício Química Geral - ResoluçãoLuana Bahls BittencourtAinda não há avaliações
- Quimica Analítica 2Documento145 páginasQuimica Analítica 2Chadrekzy January PungosAinda não há avaliações
- Exercícios - Aula 8 - Espectroscopia RamanDocumento2 páginasExercícios - Aula 8 - Espectroscopia RamanBárbara ZamaiAinda não há avaliações
- Solucoes Indicadores e Titulacoes Teoria Exercicios ItaDocumento9 páginasSolucoes Indicadores e Titulacoes Teoria Exercicios ItaAline F da CostaAinda não há avaliações
- 2 Lista Hidrocarbonetos 3°ano 2020Documento3 páginas2 Lista Hidrocarbonetos 3°ano 2020Nathan OliveiraAinda não há avaliações
- IV Exercícios Parte 1Documento10 páginasIV Exercícios Parte 1Fernando Alves BarbozaAinda não há avaliações
- Alcoois CDocumento2 páginasAlcoois CvanindesouzaAinda não há avaliações
- Lista de Exercícios Volumetria de ComplexaçãoDocumento2 páginasLista de Exercícios Volumetria de ComplexaçãoFlavia MarquesAinda não há avaliações
- Questões Ansiolíticos Com RespostasDocumento2 páginasQuestões Ansiolíticos Com RespostasMiguel Delanoy PolidoriAinda não há avaliações
- Aula 1 - Estatistica Aplicada A QuimicaDocumento43 páginasAula 1 - Estatistica Aplicada A QuimicaTito Weber CarnavalliAinda não há avaliações
- Cinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesDocumento72 páginasCinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesrafelAinda não há avaliações
- Reações de Adição A C CDocumento57 páginasReações de Adição A C CMercês MendesAinda não há avaliações
- Reações Inorgânicas - Classificação Das Reações - 1 2 QuestõesDocumento4 páginasReações Inorgânicas - Classificação Das Reações - 1 2 QuestõespatriciamartinsAinda não há avaliações
- Prova Química IIDocumento16 páginasProva Química IIAdryana SousaAinda não há avaliações
- Quimica Organica Exercicios Classificacao Nomenclatura GabaritoDocumento26 páginasQuimica Organica Exercicios Classificacao Nomenclatura GabaritoRones DiasAinda não há avaliações
- Aula-Introdução A Química AnalíticaDocumento38 páginasAula-Introdução A Química AnalíticaWanessaAmorimAinda não há avaliações
- Exercícios de VolumetriaDocumento1 páginaExercícios de VolumetriaFabiano VitorAinda não há avaliações
- Lista 01 Ã Cidos e Bases - ResolvidaDocumento5 páginasLista 01 Ã Cidos e Bases - ResolvidaCristielly raamos Raamos100% (1)
- Lista de Exercícios - Cinética QuímicaDocumento2 páginasLista de Exercícios - Cinética QuímicaJoão Valdir Miranda100% (2)
- Lista Exercícios - Equilíbrios QuímicosDocumento4 páginasLista Exercícios - Equilíbrios QuímicosDaiane CambriaiAinda não há avaliações
- CONCENTRA+ç+òES E DILUI+ç+òESDocumento21 páginasCONCENTRA+ç+òES E DILUI+ç+òESEmily RochaAinda não há avaliações
- Preparo de AmostrasDocumento90 páginasPreparo de AmostrastiagomdsdiasAinda não há avaliações
- Aula 1 - Compostos de Coordenação-Introdução NC e GeometriaDocumento50 páginasAula 1 - Compostos de Coordenação-Introdução NC e GeometriaRenan Oliveira100% (2)
- Prática 10Documento12 páginasPrática 10Maria Luiza de Abreu Alves100% (1)
- Prática 09Documento6 páginasPrática 09Maria Luiza de Abreu AlvesAinda não há avaliações
- Química - Tecnologia em Estradas - 2020-09-14 - Conteúdo - Resolução de ExercíciosDocumento16 páginasQuímica - Tecnologia em Estradas - 2020-09-14 - Conteúdo - Resolução de ExercíciosCarlos Wagner WagnerAinda não há avaliações
- Relatorio EstequiometriaDocumento9 páginasRelatorio EstequiometriaHamanda RochaAinda não há avaliações
- Q3 - Reações QuímicasDocumento6 páginasQ3 - Reações QuímicasLuma PimentaAinda não há avaliações
- Exercicios 2012 Aulas1a5Documento6 páginasExercicios 2012 Aulas1a5Filipe GrahlAinda não há avaliações
- Aula 2 - 2 Ano - EstequiometriaDocumento4 páginasAula 2 - 2 Ano - EstequiometriaLúcio BarbozaAinda não há avaliações
- VIERO - Sttuco Flexivel WEB AFDocumento6 páginasVIERO - Sttuco Flexivel WEB AFRui ReboloAinda não há avaliações
- O Que Faz Um Engenheiro de Estimulação - 2021Documento50 páginasO Que Faz Um Engenheiro de Estimulação - 2021Luis Fernando NeumannAinda não há avaliações
- Lista 6 - Condensadores e EvaporadoresDocumento3 páginasLista 6 - Condensadores e EvaporadoresCarlos Augusto Oliveira SettiAinda não há avaliações
- Atividade 2 - Eletricidade Básica - 54-2023Documento3 páginasAtividade 2 - Eletricidade Básica - 54-2023Cavalini Assessoria AcadêmicaAinda não há avaliações
- ENERGIA - Fontes, Formas e TransferênciasDocumento40 páginasENERGIA - Fontes, Formas e TransferênciasJoão RodriguesAinda não há avaliações
- Água Da Chuva, Água Destilada e Água Pura: A Água Na TerraDocumento3 páginasÁgua Da Chuva, Água Destilada e Água Pura: A Água Na TerraVascoRodriguesAinda não há avaliações
- Exercícios - Estudo Dos Gases - 2 SérieDocumento9 páginasExercícios - Estudo Dos Gases - 2 SérieMara MouraAinda não há avaliações
- Aula 08 - Resistencia o Cisalhamento Dos Solos PDFDocumento11 páginasAula 08 - Resistencia o Cisalhamento Dos Solos PDFbruno18Ainda não há avaliações
- 02ano GRAFICADocumento200 páginas02ano GRAFICAquelkondaAinda não há avaliações
- AlginatoDocumento2 páginasAlginatoThalya Nobre100% (1)
- Se CPTM BrasDocumento6 páginasSe CPTM BrasthiagogirouxAinda não há avaliações
- Dimensionamento de Placa de Isopor Com Concreto para Vedação e Estrutura (2) - CópiaDocumento66 páginasDimensionamento de Placa de Isopor Com Concreto para Vedação e Estrutura (2) - CópiaJiuvaniAssisAssingAinda não há avaliações
- Lista Precos INDUSTRIA Ate 08072022Documento38 páginasLista Precos INDUSTRIA Ate 08072022Felipe FelicianoAinda não há avaliações
- BiolucciDocumento54 páginasBiolucciGuaracy SantosAinda não há avaliações
- Donatti Manualtecnico SpecialeDocumento6 páginasDonatti Manualtecnico SpecialeAlice BernardesAinda não há avaliações
- Tipos de LajesDocumento46 páginasTipos de LajesJonathan Muniz100% (1)
- Deslocamento de EquilíbrioDocumento29 páginasDeslocamento de EquilíbrioFernandes YoshimotoAinda não há avaliações
- Recursos MineraisDocumento9 páginasRecursos MineraisBárbara CamõesAinda não há avaliações
- Coletanea Exercicios OU5Documento43 páginasColetanea Exercicios OU5Fabiano Luiz Naves100% (1)
- Mapa Mina 2021 AltaDocumento1 páginaMapa Mina 2021 AltaEuler Felix SalgadoAinda não há avaliações
- Exercícios Sobre Ligas Questões de ConcursosDocumento5 páginasExercícios Sobre Ligas Questões de Concursosauxi tiAinda não há avaliações
- Cálculo Viga MetálicaDocumento6 páginasCálculo Viga MetálicaGustavo FonsecaAinda não há avaliações
- NBR 16790 - Piso CimentícioDocumento30 páginasNBR 16790 - Piso CimentícioKelly RibeiroAinda não há avaliações
- Informações Detalhadas A Respeito Da Atividade de Landfarming PDFDocumento7 páginasInformações Detalhadas A Respeito Da Atividade de Landfarming PDFBalianiAinda não há avaliações
- Teste de Solubilidade em Compostos OrgânicosDocumento12 páginasTeste de Solubilidade em Compostos OrgânicosMichelle SeccoAinda não há avaliações
- Ppap-380 - Qualinyl A01 V6 PR01 HDocumento2 páginasPpap-380 - Qualinyl A01 V6 PR01 HlaboratorioAinda não há avaliações