Escolar Documentos
Profissional Documentos
Cultura Documentos
23 Quimica Aula 27 07
Enviado por
juliocezarfranciscomartinsinfaTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
23 Quimica Aula 27 07
Enviado por
juliocezarfranciscomartinsinfaDireitos autorais:
Formatos disponíveis
Manaus, ____ de ___________ de 2.
021 Aula 05/07/2021
Aluno(a):_______________________________________________________________________________
Disciplina: Química • Professor: Glauco • Conteúdo• Eletroquimica
6 - ELETROQUÍMICA
Introdução
O objeto de estudo da eletroquímica é o aproveitamento prático da
transferência de elétrons entre substâncias de diferentes potenciais
de oxidação ou redução. Esse aproveitamento será feito
transformando energia química em energia elétrica e vice-versa.
Pilha é o nome da conversão espontânea de energia química
em elétrica
Eletrólise é o nome da conversão não espontânea de energia
elétrica em energia química
Oxidação e Redução
A análise da tabela será ensinada por meio de exemplos. Deve-
Já aprendemos isso em química inorgânica então, apenas
se apenas perceber que, as provas de concurso, quando abordam
evisaremos.
esse tópico, fornecem como dados das questões, geralmente, o
potencial padrão de redução dos elementos. Cuidado ao observar
Os ametais possuem grande potencial de reduzir – são fortes
isso! Quando é fornecido um par de elementos, para saber qual
oxidantes
reduz e qual oxida, basta analisar os potenciais de redução (E°) e,
Os metais possuem grande potencial de oxidação – são
aquele que for o de maior valor irá reduzir e o outro oxidar. Vamos
fortes redutores.
aos exemplos:
A substância que contém o elemento que sofre a redução é
o AGENTE OXIDANTE.
o +2 ° –
A substância que contém o elemento que sofre a oxidação e 1) Ca ⇌ Ca + 2e ; ER = – 2,87 v
o AGENTE REDUTOR. o +2 ° –
Fe ⇌ Fe + 2e ; ER = – 0,44 v
Os principais elementos utilizados pela eletroquímica foram
organizados e ordenados pelos potenciais de redução e
oxidação de acordo com a tabela a seguir º º
1° O ER do ferro é maior do que o ER do Ca
2° O Fe reduz e o Ca oxida
3° Semi-reações:
+2 – o
SRR: Fe + 2e → Fe (no sentido da redução)
o +2 –
SRO: Ca → Ca + 2e (sentido da oxidação)
4º Equação de oxi-redução entre Fe e Ca
Fe +2 + 2e − → Fe
Cao → Ca+ 2 + 2e − (cancelamento dos elétrons.)
Fe + 2 +Cao → Fe o + Ca+ 2
5º Energia dessa reação ∆E = E° maior – E° menor
∆E = – 0,44 – (– 2,87) → ∆e = 2,43V
+2
2) Reação entre o Cobre e o zinco.
1° Da tabela:
o +2 –
Zn ⇌ Zn + 2e ; E°R = – 0,76V
o +2 –
Cu ⇌ Cu + 2e ; E°R = + 0,34V
2° E°Cu > E°zn → O cobre reduz e o Zn oxida
3º Semi-reações
“DISCIPLINA, ISSO SEPARA OS BONS DOS MELHORES !!!”
http://www.cursosglaucoleyser.com.br
-1-
o +2 –
SRO Zn → Zn + 2e transferência de elétrons só começará depois que a chave ③ for
+2 – 0
SRR Cu + 2e → Cu fechada. Assim:
___________________________
0 +2 +2 0
Global Zn + Cu → Zn + Cu Chave aberta:
0 0 • Acúmulo de elétrons a serem doados na placa de Zn → Pólo
4º Energia da reação AE = Emaior – Emenor
negativo ou ânodo da pilha.
AE = +0,34 – (–0,76) → AE = 1,10 V • Falta de elétrons na placa de Cu → Pólo positivo ou cátodo da
pilha.
3) Reação entre
o +3 – 0
A ⇌ A + 3e ; ER = –1,66V Chave fechada:
o +2 – 0 Fluxo de elétrons do Zn para o Cu
Zn ⇌ Zn + 2e ; ER = –0,76V •
• Sentido arbitrado da corrente elétrica no fio: do Cu para o Zn
o +2 –
• Reação no ânodo: SRO: Zn → Zn + 2e e com isto haverá o
Tente você:
desgaste da placa de zinco sólido (Znº) transformando-se em zinco
+2
iônico (Zn ).
O elemento que oxida é o: ___________________________ +2 –
• Reação no cátodo: SRR: Cu + 2e → Cuº e isto mostra que
O elemento que reduz é o: ___________________________
ocorrerá um deposito de cobre sólido sobre a placa de cobre, pois
o cobre iônico da solução salina é reduzido a cobre sólido (Cuº).
SRO: ____________________ • Na ponte salina, cuja função é permitir a migração de íons de
SRR: ____________________ uma solução para a outra, de forma a equilibrar a quantidade de
Global: _____________________ cátions e ânions em cada solução, haverá o fluxo de ânions do
A energia envolvida na reação é de: ________________________ cátodo para o ânodo e fluxo de cátions ânodo para cátodo.
De forma esquemática, após algum tempo de chave fechada
teremos:
Pilha
A pilha de Daniel
Foi elaborada por John Frederic DANIELL, químico e metereologista
inglês, em 1836. A grande revolução imposta por Daniell foi a
substituição de soluções ácidas das “antigas” pilhas de Alessandro − Representação da Pilha
VOLTA, por soluções de sais.
1.1.1. Esquematização Metal Cátion Metal
Cátion
que reduzido que
forma do +2
A pilha de Daniell foi elaborada por meio da reação de oxiredução oxida +2 Cu reduz
Zn
entre eletrodos de zinco (Zn) e cobre (Cu). Vejamos: Znº Cuº
− Energia da pilha
∆E = E° maior – E° menor
1.1.2. Interrupção do fluxo de é
Existem alguns motivos para que o funcionamento da
pilha seja interrompido. Vejamos:
a) Desgaste total da placa do ânodo
① Eletrodo sólido de Zinco b) Chave ser aberta
② Eletrodo sólido de cobre c) Término dos ânions em solução no cátodo
③ Chave aberta de circuito d) Perda da neutralidade elétrica das soluções salinas
④ Ponte salina de ambos os eletrodos por mau funcionamento da
⑤ Solução salina de Zn e Cu ponte salina.
Você consegue entender todos? Tente!
Na reação entre Zn e Cu, percebemos por meio de seus potencias de
redução de –0,76V e +0,34V respectivamente que o cobre reduz e o Exercícios de Fixação
zinco oxida ou seja, o zinco doará elétrons para o cobre. Essa
“DISCIPLINA, ISSO SEPARA OS BONS DOS MELHORES !!!”
http://www.cursosglaucoleyser.com.br
-2-
1. Monte a pilha entre Zn e A. Consulte a tabela de potenciais Etapas:
padrão de redução e mostre quem é o ânodo, cátodo; sentido
dos é; da corrente elétrica; que placa é corroída e qual é • Aquecimento do NaCl (s) até 800°C para fundi-lo ou seja,
aumentada; SRO, SRR; global; representação e energia da pilha NaCl(s) → NaCl()
(UFA!!) • Dissociação do NaCl()
º + –
2. Agora para o par Mg e Au ( ER = 1,50V); os mesmos pedidos NaCl() → Na () + C ()
• São colocados os eletrodos e o gerador é ligado e assim:
do exercício anterior. –
– No eletrodo positivo (ânodo) ocorrerá a SRO do ânion Cl (e):
3. Evite comprar conserva cuja lata esteja amassada, porque a
– 0 –
lata de folha-de-flandres (uma liga de ferro e carbono) tem 2 Cl → Cl + 2e
2(g)
uma proteção de estanho que se pode romper quando a lata
sofre um impacto. Nesse caso, formar-se-á uma pilha e haverá
contaminação da conserva. Considerando os valores dos - No eletrodo negativo (cátodo) ocorrerá a SRR do cátion
+ + –
potenciais-padrão de eletrodo: Na (e): Na (e) + 1e → Naº(s)
3+
Fe + 3é ⇌ Fe(s) E° = – 0,036 V Ocorrerão assim as seguintes reações:
2+
Sn + 2é ⇌ Sn(s) E° = – 0,136 V
+ –
Dissociação [NaCl() → Cl () + Cl () ] x 2
– –
a) Escreva a equação de funcionamento desta pilha SRO 2Cl () → Cl2(g) + 2e
+ – 0
b) Diga, apresentando justificativa, se está certo ou errado o SRR [Na () + 1e → Na (s)] x 2
0
conteúdo da seguinte frase: “São os íons Sn2 + que E a global será: 2 NaCl(l) → 2 Na (s) + Cl2(g)
(aq)
contaminam a conserva na situação descrita no texto • No final os produtos da eletrólise ígnea do NaCl são:
acima.”
1) Gás cloro liberado pelo ânodo
ELETRÓLISE 2) Deposição de sódio sólido sobre o eletrodo negativo
cátodo.
É um processo não espontâneo no qual por meio de uma corrente
elétrica gera-se uma reação química. PRONTO, VOCÊ APRENDEU ELETRÓLISE ÍGNEA! NÃO?
A eletrólise pode ser realizada de 2 formas distintas: VEJAMOS MAIS UM EXEMPLO:
– A eletrólise ígnea pela fusão de uma substância iônica (altas 2. Eletrólise ígnea do Iodeto de potássio
temperaturas);
– A eletrólise em meio aquoso na qual a dissociação ou ionização da Agora de forma mais “enxuta”!
substância se dá pela adição de água ao sistema.
∆
A eletrólise é um processo muito importante pois permite obter uma • Fusão do KI: KI(s) → KI()
+ –
série de substâncias que não são encontradas na natureza tais como • Dissociação do KI(): KI() → K () + I ()
cloro, hidróxido de cálcio, iodo e outras tantas. – 0 –
• SRO no ânodo: 2I () → I2 (g)
+ 2e
+ – 0
Eletrólise ígnea • SRR no cátodo: K () +1e → K (s)
Reação global: 2KI() → I0
0
• + 2K (s)
2 (g)
Em uma cuba eletrolítica contendo a substância iônica fundida (na
fase líquida e dissociada) são colocados dois eletrodos inertes • Produtos: gás iodo e deposição de potássio.
ligados, cada um deles, a um pólo de uma bateria ou gerador que
fornecerá uma ddp ao sistema. Essa ddp irá iniciar o processo de AGORA VOCÊ ENTENDEU! NÃO? ENTÃO TREINE VOCÊ
descarga iônica nos eletrodos. FAZENDO A ELETRÓLISE ÍGNEA DOS COMPOSTOS ABAIXO:
– O eletrodo ligado ao pólo positivo da bateria irá atrair o único ânion a) KC
–x 0
em solução. Ocorrerá, ai, a descarga anódica A → A + x . e , que
– b) Na F
será sempre uma oxidação. c) Na2S
– O eletrodo ligado ao pólo negativo da bateria irá atrair o único
+y –
cátion em solução. Ocorrerá, ai, a descarga catódica B + ye →
0
B ,que será sempre uma redução. Eletrólise aquosa
Resumo Na eletrólise aquosa a dissociação ou ionização do composto iônico
será feito pela água. O problema é que a água também se auto ioniza
+ –
liberando H e OH , passando a existir 2 cátions e 2 ânions em
Pólo Positivo Pólo Negativo
solução. Qual será descarregado no cátodo e qual será descarregado
Ânodo Cátodo no ânodo?
Atrai o ânion Atrai o cátion
Ocorre a oxidação Ocorre a redução Para responder a esse questionamento existem tabelas de descarga
seletiva de ânions e cátions que serão fornecidas em prova.(alunos
Glauco leyser saberá, mesmo sem as tabelas!)
Exemplos de eletrólise ígnea resolvidos
1. É o exemplo mais clássico em provas e livros: Eletrólise ígnea do
cloreto de sódio – NaCl.
“DISCIPLINA, ISSO SEPARA OS BONS DOS MELHORES !!!”
http://www.cursosglaucoleyser.com.br
-3-
+ –
São elas: 2 H + 2e → H2(g) ou
+ –
2 H3O + 2e → H2O(e) + H2(g)
Tabela de descarga dos cátions*
–
Descarga anódica do OH
+ +
O cátion H ou H30 só se descarrega antes dos metais alcalinos,
alcalinos terrosos e do alumínio e se descarrega depois dos demais –
4 OH → 2 H2O(e) + 1 O2(g) + 4e
–
cátions.
+ +3
Demais cátions > H > A > 1A e 2A Como tenho a certeza de que você entendeu a eletrólise aquosa,
agora repita tudo aquilo que foi escrito acima fazendo a eletrolise
Tabela de descarga dos ânions*. aquosa das seguintes substâncias:
Os ânions não oxigenadas se descarregam antes do ânion hidróxido, a) Zn (NO3)2 c) KI
–
OH , e este se descarrega antes dos ânions oxigenados e do fluoreto b) Na2 (SO4)2 d) NaF
–1
F .
Aspectos quantitativos da eletrólise
−1 – –1
Anions não oxigenados e HSO 4 > OH > anions oxigenados e F .
Quanto de gás liberado ? Qual massa depositada sobre o eletrodo?
Qual corrente elétrica utilizada no processo? Esses questionamentos
*Fonte: livro de Química Martha Reis – Bibliografia oficial. serão respondidos agora, por meio das leis de FARADAY.
Basicamente, as Leis de Faraday, demonstram que a massa de uma
Após definido o cátion e o ânion que será descarregado em cada substância, formada por eletrólise, é diretamente proporcional à
eletrodo, é só proceder como o outro tipo de eletrólise. carga elétrica utilizada no sistema.
Vejamos a eletrólise aquosa do NaC.
“Alguns livros e apostilas apresentam fórmulas a serem decoradas
Eletrólise aquosa do NaCl para este processo de determinação. Não concordo pois o
procedimento é apenas uma Estequiometria muito básica”. Vejamos
De forma enxuta: por meio de exemplos:
+ –
• Dissociação do NaCl: NaCl (aq) → Na (aq) + Cl (aq) 1) Na eletrólise ígnea do NaC:
+ –
• Ionização da H2O: H2O() → 2H (aq) + OH (aq)
+ + + –
• Deve-se por meio de tabelas saber qual cátion H ou Na será NaC() → Na + C
+ +
descarregado no cátodo → É o H ou H3O . Assim: Reação –
SRO: 2 C → C2 + 2e
–
+ –
catódica: 2H + 2e → H2(g) + –
SRR:2 Na + 2e → 2Naº
–
• Pelas tabelas, a descarga anódica será definida entre o C e o
– –
OH → É o C . Vejamos: Pela SRO constata-se que são formados 1 mol de gás cloro
– –
Assim: Reação anódica: 2 C → C2(g) + 2e e liberada uma carga elétrica correspondente a 2 mols de elétrons (é,
–
são 2 mols de e e não apenas 2 elétrons!)
Então, as reações envolvidas no processo são: Assim a quantidade de gás cloro a ser produzido por meio de outra
carga elétrica deverá ser calculada por uma regra de 3 simples. E só!
+ –
• 2 NaC(aq) → 2 Na (aq) + 2 C (aq)
•
+ –
H2O () → 2H (aq) + OH (aq) Assim: Massa Cl2 Carga
2(+aq) + 2e → H2 (g)
–
•
– –
• 2 C (aq) → C2(g) + 2e
+ –
A global será: 2NaC + 2H2O → H2(g) + C2(g) + 2Na + 2 OH
Os produtos dessa eletrólise são o gás hidrogênio, o gás cloro e o
+ –
hidróxido de sódio, uma vez que o Na (aq) combina-se com o OH
(aq).
Vamos a mais um exemplo comentado; a eletrólise aquosa do
Brometo de cobre II – CuBr2. Onde i = corrente utilizada (Ampéres)
∆t = tempo transcorrido (segundos)
96500 C = constante de Faraday que nada mais é do que a carga em
• Dissociação do sal: CuBr2 → Cu +2 + 2 Br−1
(aq) (aq) coulombs de um mol de elétrons.
+ –
• Ionização da água: H2O → H +OH
+2 –
• Descarga catódica: Cu + 2e → Cu(s) Voltando ao problema anterior: se for pedida a massa de gás cloro
–1 + –
• Descarga anódica: 2 Br → Br2(g) + Cu(s) + H + OH e eliminada liberada devido a uma corrente de 10 A por um tempo de 40s, basta
a H2O de ambos os lados temos: Cu Br2 → Br2(g) + Cu(s) fazer:
Conclusão: A água, nesta eletrólise, serviu apenas para dissociar o 71. 10 . 40
m= → m ≅ 0,147g de Cl2
sal. Os produtos são o gás bromo e a deposição de cobre sólido. 2 x 96500
+
Uma última observação pertinente a respeito da descarga do H e do
–
OH : Agora, se o pedido fosse achar a massa depositada de sódio sobre o
+ + eletrodo, procederíamos da seguinte forma:
Descarga catódica do H ou H3O
“DISCIPLINA, ISSO SEPARA OS BONS DOS MELHORES !!!”
http://www.cursosglaucoleyser.com.br
-4-
–
Pela SRR percebemos que 2 mols de e de carga produzem 2 mols de 2. QUADRO COMPARATIVO ENTRE PILHAS E ELETRÓLISE
sódio sólido assim:
Massa Sódio Carga
2 x 23 _____ 2 x 96500
m = 0,095g
m _____ 10 x 40
Após esses exemplos podemos até elaborar uma fórmula para esses
cálculos:
n.M.i. ∆t
m= onde
n' . 96500
Onde Eº = Potencial padrão de redução.
n = nº de mols da substância formada no eletrodo 3. EXERCÍCIOS DE FIXAÇÃO
M = massa molar da substância
i = corrente elétrica utilizada
1. Uma cuba eletrolítica contém 10,0 L de solução aquosa 0,5 mol/L
∆t = duração da eletrólise de sulfato de cobre II.
n' = nº de mols de elétrons envolvidos na SRO ou SRR em Essa solução é submetida à eletrólise com eletrodos inertes por
questão. 5 minutos e com corrente de 10 A.
96500 = constante de Faraday
m = massa da substância descarregada durante o processo a) Equacione a semi-reação catódica envolvida.
analisado. b) Equacione a semi-reação anódica envolvida.
c) Equacione a reação global envolvida.
d) Calcule a massa de metal depositada no cátodo.
Exercícios de fixação e) Calcule o volume que o gás formado ocupa a 27ºC sob
pressão de 1,0 atm.
f) Calcule a concentração em quantidade de matéria de
1. Qual o volume de gás cloro, medido nas CNTP, e a massa de sulfato de cobre II da solução após a eletrólise.
cálcio metálico obtidos numa eletrólise ígnea do cloreto de
cálcio, sabendo que uma corrente elétrica de intensidade igual 2. Um rádio de pilha ficou ligado durante a partida de um jogo de
a 10 ampères atravessou a cuba eletrolítica durante 965 futebol. Nesse período, sua cápsula de zinco sofre um desgaste
segundos? Dados: C = 35,5 g/mol e Ca = 40 g/mol. de 0,3275 g tendo originado uma corrente de 0,322 A. Qual foi
2
a duração da narração do jogo, em minutos?
2. Uma calota de automóvel de área igual a 500 cm constitui o Dados: Zn = 65,5 g/mol e 1F = 96.500 C.
cátodo de uma cuba eletrolítica que contém solução aquosa de
cloreto de níquel II, NiC2(aq). Para niquelara a calota, faz-se 3. A deposição eletrolítica de 2,975 g de um metal de massa
passar através da cuba uma corrente elétrica de 35,5 A. Calcular atômica 119 u requer 9650 C. Calcule o NOX desse metal.
o tempo necessário para que seja depositada na calota uma
camada de níquel igual a 0,01 mm de espessura. Dados: 4. A deposição eletrolítica de 2,75 g de um metal de massa
3
Densidade do níquel = 8,9 g/cm , Ni = 59 g/mol. atômica 55 requereu 9650 C. Qual o número de oxidação desse
metal?
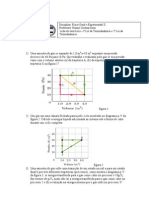
3. Submete-se à eletrólise uma solução aquosa de cloreto de
cobre II, CuC2(aq), com eletrodos inertes durante 4 horas. A 5. Pretende-se oxidar anodicamente 6,35 g de Cu(s) até Cu2 + .
intensidade da corrente elétrica varia com o tempo, conforme o (aq)
seguinte gráfico: Uma certa corrente constante circula pela célula durante 5 hora, 21
minutos e 40 segundos. Pede-se:
a) a quantidade de matéria de elétrons envolvidos na
transformação;
b) o valor da intensidade da corrente. Dados: Cu = 63,5
g/mol e 1 faraday = 96.500 C.
Qual a massa de cobre (Cu = 63,5 g/mol) depositada no cátodo
durante o processo?
“DISCIPLINA, ISSO SEPARA OS BONS DOS MELHORES !!!”
http://www.cursosglaucoleyser.com.br
-5-
Você também pode gostar
- Ciência Dos MateriaisDocumento13 páginasCiência Dos MateriaisLucas BarrosAinda não há avaliações
- Exercicios Corrosão e GabaritoDocumento3 páginasExercicios Corrosão e GabaritoRomildo Junior100% (1)
- 2º Trabalho Elemento, Substância e Mistura - GabaritoDocumento2 páginas2º Trabalho Elemento, Substância e Mistura - GabaritoSabrine Cassia de BoerAinda não há avaliações
- Cromatografia Liquida - Metodos CromatograficosDocumento93 páginasCromatografia Liquida - Metodos CromatograficosbncamelloAinda não há avaliações
- Lista Aula 44-46 Balanceamento de Equações Pelo Método RedoxDocumento7 páginasLista Aula 44-46 Balanceamento de Equações Pelo Método RedoxMatheus Souza100% (1)
- Material Teorico - Eletroquimica - Parte 1Documento15 páginasMaterial Teorico - Eletroquimica - Parte 1nk2 kkrsAinda não há avaliações
- EletroquimicaDocumento51 páginasEletroquimicaAlice ItorbideAinda não há avaliações
- ABRACO CorrosãoDocumento101 páginasABRACO CorrosãoLuis Gustavo Pacheco100% (1)
- EletroquímicaDocumento9 páginasEletroquímicaJoão RicardoAinda não há avaliações
- Material de Eletroquímica PDFDocumento38 páginasMaterial de Eletroquímica PDFQuintaAinda não há avaliações
- 7 Lista EletroquímicaDocumento2 páginas7 Lista EletroquímicaMayra wolfAinda não há avaliações
- Eletroquimica Aula 27 2007Documento11 páginasEletroquimica Aula 27 2007Iara DaherAinda não há avaliações
- Aula 2 Eletroquímica (Modo de Compatibilidade)Documento43 páginasAula 2 Eletroquímica (Modo de Compatibilidade)Ronan MullerAinda não há avaliações
- 4 - UFAL - QUALI 2016 - Equilíbrios de Óxido-ReduçãoDocumento54 páginas4 - UFAL - QUALI 2016 - Equilíbrios de Óxido-ReduçãoMilton Cris.Ainda não há avaliações
- 197747-Aula Oxidação e Redução 2017 PDFDocumento54 páginas197747-Aula Oxidação e Redução 2017 PDFLucas Nunes CorreiaAinda não há avaliações
- Química - Reações de OxirreduçãoDocumento8 páginasQuímica - Reações de Oxirreduçãopedroebiel02Ainda não há avaliações
- 01 Alvaro Vest F1 Aula 08 Reacaode Oxi ReducaoDocumento2 páginas01 Alvaro Vest F1 Aula 08 Reacaode Oxi ReducaoJuliana Araújo MattosAinda não há avaliações
- Aula EletroquimicaDocumento38 páginasAula EletroquimicaJoelma DiasAinda não há avaliações
- Turmadeagosto Química Eletroquímica - Pilha 14 10 2022Documento13 páginasTurmadeagosto Química Eletroquímica - Pilha 14 10 2022lucasgoudardAinda não há avaliações
- Lista EletroquímicaDocumento3 páginasLista Eletroquímicarubens.costaAinda não há avaliações
- EletroquímicaDocumento2 páginasEletroquímicaJess ElizeuAinda não há avaliações
- Exercicios Eletroquimica Coc ResolveDocumento2 páginasExercicios Eletroquimica Coc ResolveRaphael Rodrigues CostaAinda não há avaliações
- Aula Oxirreducao Pilha Eletrolise e RadioatividadeDocumento16 páginasAula Oxirreducao Pilha Eletrolise e RadioatividadeMichele AmaralAinda não há avaliações
- Lista Aula 73-76 Eletrólise - Aspectos GeraisDocumento9 páginasLista Aula 73-76 Eletrólise - Aspectos GeraisGuilherme rochaAinda não há avaliações
- Eletroquímica e Equilibrios Redox PDFDocumento49 páginasEletroquímica e Equilibrios Redox PDFEloy KintanaAinda não há avaliações
- Apostila - Eletroquímica - Química 3.Documento18 páginasApostila - Eletroquímica - Química 3.Geilson Silva100% (1)
- QMC - AP - Eletroquímica - Pilhas e Potencial de ReduçãoDocumento13 páginasQMC - AP - Eletroquímica - Pilhas e Potencial de ReduçãoGabriel Lima PizanoAinda não há avaliações
- Tarefa C6 CursoDE Quimica Prof 20aulasDocumento16 páginasTarefa C6 CursoDE Quimica Prof 20aulasMuttsuriniKunAinda não há avaliações
- 1 - Objetivos: Química e Ciências Dos MateriaisDocumento7 páginas1 - Objetivos: Química e Ciências Dos MateriaisMateus FrancoAinda não há avaliações
- CORROSAO - Eqi 704 - AULA 1 - JUNHO2015 - FINALDocumento34 páginasCORROSAO - Eqi 704 - AULA 1 - JUNHO2015 - FINALIdalba SouzaAinda não há avaliações
- 2 - Características Gerais Dos Elementos Do Bloco SDocumento33 páginas2 - Características Gerais Dos Elementos Do Bloco SRuanAinda não há avaliações
- Apontamentos Reação RedoxDocumento4 páginasApontamentos Reação Redoxsamira100% (1)
- Anotações de Aula - Curso de Corrosão - 1 Aula Rev 2012Documento32 páginasAnotações de Aula - Curso de Corrosão - 1 Aula Rev 2012Ludmila De Almeida CarvalhoAinda não há avaliações
- Relatório VIII CorosãoDocumento8 páginasRelatório VIII CorosãoEtienne Sampaio OliveiraAinda não há avaliações
- ELETROQUÍMICAengDocumento73 páginasELETROQUÍMICAengBruno SchiavoneAinda não há avaliações
- OxirreduçãoDocumento13 páginasOxirreduçãoHistorias MinhasAinda não há avaliações
- RedoxDocumento46 páginasRedoxRita GameiroAinda não há avaliações
- EletroquímicaDocumento1 páginaEletroquímicamaria luiza mauroAinda não há avaliações
- EletroqumicaDocumento6 páginasEletroqumicaVictor CarneiroAinda não há avaliações
- 2 Ano Oxidação e ReduçãoDocumento18 páginas2 Ano Oxidação e ReduçãoRaquel NogueiraAinda não há avaliações
- Aula - 3 PMT3130 2017 NeivaDocumento21 páginasAula - 3 PMT3130 2017 NeivaKalipse FerreiraAinda não há avaliações
- Eletroquimica Pilhas82Documento10 páginasEletroquimica Pilhas82kodzuken007Ainda não há avaliações
- 2º Ano - OxidaçãoDocumento5 páginas2º Ano - OxidaçãoCamila PinheiroAinda não há avaliações
- Apostila de EletroquímicaDocumento5 páginasApostila de EletroquímicaFlávia SouzaAinda não há avaliações
- Titulometria de Oxido Reducao PDFDocumento13 páginasTitulometria de Oxido Reducao PDFFlavia MarquesAinda não há avaliações
- Atividade Avaliativa 8 - RenataDocumento3 páginasAtividade Avaliativa 8 - RenataMaurício OliveiraAinda não há avaliações
- Aula7 8Documento52 páginasAula7 8Matheus Yuri Sasaki FranzoniAinda não há avaliações
- Assunto - Oxidação e Redução PDFDocumento6 páginasAssunto - Oxidação e Redução PDFAlvernes CruzAinda não há avaliações
- Reaccoes Redox 2023-1Documento11 páginasReaccoes Redox 2023-1Alexandre Costa100% (1)
- Q2.2.2. Força Relativa de Oxidantes e RedutoresDocumento20 páginasQ2.2.2. Força Relativa de Oxidantes e RedutoresPedro SilvaAinda não há avaliações
- Aula 5 - EletroquímicaDocumento19 páginasAula 5 - EletroquímicaMartinson FreitasAinda não há avaliações
- turmademaio-química-NOX e Função Inorgânica Óxido - 231126 - 142323Documento18 páginasturmademaio-química-NOX e Função Inorgânica Óxido - 231126 - 142323nathália novoAinda não há avaliações
- Colégio Tiradentes Da Polícia Militar / BarbacenaDocumento3 páginasColégio Tiradentes Da Polícia Militar / BarbacenapixkaraAinda não há avaliações
- Reações de Oxi-ReduçãoDocumento2 páginasReações de Oxi-ReduçãoJuliane Froncheti de MouraAinda não há avaliações
- TeSP ALAB Redox 2022Documento29 páginasTeSP ALAB Redox 2022Afonso VasconcelosAinda não há avaliações
- Apostila 3 e Exercicios de Pilhas e EletroliseDocumento4 páginasApostila 3 e Exercicios de Pilhas e Eletrolisewolferbass100% (1)
- Potenciometria 1Documento63 páginasPotenciometria 1langly_rjAinda não há avaliações
- Química - Pré-Vestibular Impacto - Reações Químicas - Conceito e Classificação IIIDocumento2 páginasQuímica - Pré-Vestibular Impacto - Reações Químicas - Conceito e Classificação IIIQuímica Qui100% (1)
- Reação Oxidação-ReduçãoDocumento25 páginasReação Oxidação-ReduçãoEduardo FernandesAinda não há avaliações
- Trabalho OxidaçãoDocumento5 páginasTrabalho OxidaçãoMúcio Luiz de Rezende JuniorAinda não há avaliações
- 1 Aula de Meteorologia - IntensivoDocumento30 páginas1 Aula de Meteorologia - IntensivoEdoardo MarkezAinda não há avaliações
- AULA 3 - Transporte Através Da Membrana 3 AvançadissimoDocumento22 páginasAULA 3 - Transporte Através Da Membrana 3 AvançadissimoallanfradiqueAinda não há avaliações
- Deq503 2a Avaliacao 2013 2 Parte 2Documento1 páginaDeq503 2a Avaliacao 2013 2 Parte 2Gilson MedeirosAinda não há avaliações
- Conforto TérmicoDocumento3 páginasConforto TérmicoCatharina Helena Dresch GaboardiAinda não há avaliações
- AnaQUESTÃO AULA Nº3 22 Janeiro 2019-2020 10º Ano FINALDocumento2 páginasAnaQUESTÃO AULA Nº3 22 Janeiro 2019-2020 10º Ano FINALJúlia Susana da Silva Conde BarbosaAinda não há avaliações
- Aula 2 - Tabela PeriódicaDocumento1 páginaAula 2 - Tabela PeriódicaVictor FabianoAinda não há avaliações
- Princípio de Medição de UmidadeDocumento5 páginasPrincípio de Medição de UmidadeAlexandre SouzaAinda não há avaliações
- Lista ProfessorDocumento6 páginasLista ProfessorSolismar HarmsAinda não há avaliações
- Grupo 3 - T5Documento25 páginasGrupo 3 - T5Juliana VilhenaAinda não há avaliações
- Relatorio Termo DinamicaDocumento9 páginasRelatorio Termo DinamicaGuilherme DiasAinda não há avaliações
- Slide - CinéticaDocumento62 páginasSlide - CinéticajojojAinda não há avaliações
- Lista - 1 e 2 LeiDocumento3 páginasLista - 1 e 2 LeiAdriano RabeloAinda não há avaliações
- Lista Exercícios Av1 QMDocumento7 páginasLista Exercícios Av1 QMRenata Leal MartinsAinda não há avaliações
- Relatorio Quimica Organica 2Documento11 páginasRelatorio Quimica Organica 2Angelique ViannyAinda não há avaliações
- Pilhas Basico INV PDFDocumento2 páginasPilhas Basico INV PDFGiovanni Cavalcante BarrosAinda não há avaliações
- Fis06 Livro PropostosDocumento64 páginasFis06 Livro PropostosDanielValadãoBastosAinda não há avaliações
- Química 2º AnoDocumento3 páginasQuímica 2º AnoCarlos NeyAinda não há avaliações
- (9º Ano) Avaliação - Substâncias e MisturasDocumento2 páginas(9º Ano) Avaliação - Substâncias e MisturasJéssica LayneAinda não há avaliações
- 2° Trabalho - 2° Etapa - Equipe 4 - Fracionamento Do Gás Natural - FinalDocumento24 páginas2° Trabalho - 2° Etapa - Equipe 4 - Fracionamento Do Gás Natural - FinalCarlos AdrianoAinda não há avaliações
- N-1380 Determinação de Gás Sulfídrico e Enxofre Mercaptídico em Petróleo - Método PotenciométricoDocumento13 páginasN-1380 Determinação de Gás Sulfídrico e Enxofre Mercaptídico em Petróleo - Método PotenciométricoVinícius Santos da CruzAinda não há avaliações
- 9 Ano - CIENCIAS 3° PeriodoDocumento3 páginas9 Ano - CIENCIAS 3° PeriodoEdson MarinhoAinda não há avaliações
- Apostila de PecDocumento120 páginasApostila de PecRoger SaléAinda não há avaliações
- Slides Aula Analise Termica PDFDocumento103 páginasSlides Aula Analise Termica PDFIdalba SouzaAinda não há avaliações
- Química Orgânica Apostila 1Documento8 páginasQuímica Orgânica Apostila 1SamuelAinda não há avaliações
- Por Que Todos Os Nitratos São SolúveisDocumento7 páginasPor Que Todos Os Nitratos São SolúveistinamarquesAinda não há avaliações
- Apostila Módulo 2Documento7 páginasApostila Módulo 2Felipe LimaAinda não há avaliações
- AK59-01-1215-DI (pH-Cond-Temp)Documento8 páginasAK59-01-1215-DI (pH-Cond-Temp)Igor PellegriniAinda não há avaliações