Escolar Documentos
Profissional Documentos
Cultura Documentos
Quociente de Reação
Enviado por
F TAG0 notas0% acharam este documento útil (0 voto)
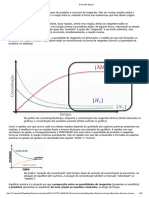
13 visualizações1 páginaO documento descreve o Quociente de Reação (Qc) como uma maneira de determinar se um sistema está em equilíbrio comparando a constante de equilíbrio (Kc) com a razão das concentrações dos produtos sobre as concentrações dos reagentes. Se Qc = Kc o sistema está em equilíbrio. Se Qc < Kc a reação irá ocorrer no sentido da formação de produtos. Se Qc > Kc a reação irá ocorrer no sentido da formação de reagentes.
Descrição original:
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoO documento descreve o Quociente de Reação (Qc) como uma maneira de determinar se um sistema está em equilíbrio comparando a constante de equilíbrio (Kc) com a razão das concentrações dos produtos sobre as concentrações dos reagentes. Se Qc = Kc o sistema está em equilíbrio. Se Qc < Kc a reação irá ocorrer no sentido da formação de produtos. Se Qc > Kc a reação irá ocorrer no sentido da formação de reagentes.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
13 visualizações1 páginaQuociente de Reação
Enviado por
F TAGO documento descreve o Quociente de Reação (Qc) como uma maneira de determinar se um sistema está em equilíbrio comparando a constante de equilíbrio (Kc) com a razão das concentrações dos produtos sobre as concentrações dos reagentes. Se Qc = Kc o sistema está em equilíbrio. Se Qc < Kc a reação irá ocorrer no sentido da formação de produtos. Se Qc > Kc a reação irá ocorrer no sentido da formação de reagentes.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 1
Quociente de Reação
Quociente de Reação, Qc – Tem como
objetivo determinar se um sistema se encontra
ou não num estado de equilíbrio (e, caso não
esteja, em que sentido irá evoluir), comparando
a constante de equilíbrio com este; tem a
mesma fórmula do que Kc;
Qc = Kc, então o sistema está em
equilíbrio;
Qc < Kc, tal significa que a quantidade
de reagentes neste estado é superior à
quantidade de reagentes no estado de
equilíbrio; a reação ocorre
espontaneamente no sentido da
formação de produtos da reação –
sentido da reação direta, até atingir o
equilíbrio;
Se Qc > Kc, tal significa que a
quantidade de produtos da reação neste
estado é superior à quantidade de
produtos da reação no estado de
equilíbrio. A reação ocorre
espontaneamente no sentido da
formação de reagentes – sentido da
reação inversa – até atingir o equilíbrio;
Você também pode gostar
- Apostila de Quimica 24 E28093 Equilibrio QuimicoDocumento3 páginasApostila de Quimica 24 E28093 Equilibrio QuimicoMatilde SaraAinda não há avaliações
- Equilibrio QuimicoDocumento54 páginasEquilibrio Quimicopatriciagalvao100% (1)
- Resumo Equilíbrio-QuímicoDocumento4 páginasResumo Equilíbrio-Químicoantonio josé das chagas100% (1)
- Equilíbrio QuímicoDocumento13 páginasEquilíbrio QuímicojoelalonsoprAinda não há avaliações
- Reagente LimitanteDocumento6 páginasReagente LimitanteSonia Coelho0% (1)
- Aspetos Quantitativos Das Reações-ResumoDocumento4 páginasAspetos Quantitativos Das Reações-ResumoRucasRuiJorgeAinda não há avaliações
- FT 2 - EqulíbrioDocumento16 páginasFT 2 - EqulíbrioMartinha LeãoAinda não há avaliações
- Eq QuímicoDocumento12 páginasEq QuímicoluisaAinda não há avaliações
- Diferentes Estados de Equilíbrio de Um Sistema ReacionalDocumento1 páginaDiferentes Estados de Equilíbrio de Um Sistema ReacionalF TAGAinda não há avaliações
- Quimica 11ºDocumento3 páginasQuimica 11ºSaraAinda não há avaliações
- Tema B. Velocidade Das Reacções Químicas E Equilíbrio QuímicoDocumento3 páginasTema B. Velocidade Das Reacções Químicas E Equilíbrio QuímicobaptistajanicengolofiAinda não há avaliações
- 2021 - 03 - 01 19 - 47 Office LensDocumento1 página2021 - 03 - 01 19 - 47 Office LenscarolinaAinda não há avaliações
- Introdução: Reações Químicas ReversíveisDocumento6 páginasIntrodução: Reações Químicas ReversíveisEduarda SantannaAinda não há avaliações
- 2 Equilibrio Químico-1Documento24 páginas2 Equilibrio Químico-1Yago SilvaAinda não há avaliações
- 2 Equilibrio Químico-1Documento24 páginas2 Equilibrio Químico-1Yago SilvaAinda não há avaliações
- Equilíbrio Químico - 3° AnoDocumento17 páginasEquilíbrio Químico - 3° AnoJeyciane RosaAinda não há avaliações
- Estudo Dirigido Equilibrio Quimico RespostasDocumento2 páginasEstudo Dirigido Equilibrio Quimico RespostasNorcéssio SanháAinda não há avaliações
- Resumos - Quimica - 11º - Novo - Programa - 2016Documento10 páginasResumos - Quimica - 11º - Novo - Programa - 2016Margarida FonsecaAinda não há avaliações
- Apontamento Cinética e Equilíbrio - PauloDocumento1 páginaApontamento Cinética e Equilíbrio - PauloRick EmanuelAinda não há avaliações
- Equilíbrio Químico Exercicios GraficosDocumento2 páginasEquilíbrio Químico Exercicios GraficosGu Trevisan100% (1)
- Apostila 5 - Equilíbrio QuímicoDocumento39 páginasApostila 5 - Equilíbrio QuímicoGustavo MarinhoAinda não há avaliações
- Química 11Documento8 páginasQuímica 11MariassAinda não há avaliações
- Equilíbrio QuímicoDocumento10 páginasEquilíbrio QuímicoAbreu Ngongo Filipa KasanjiAinda não há avaliações
- Equilíbrio Químico Yassin (Salvo Automaticamente)Documento19 páginasEquilíbrio Químico Yassin (Salvo Automaticamente)Fabio MarteAinda não há avaliações
- Equilíbrio QuímicoDocumento3 páginasEquilíbrio QuímicoinesAinda não há avaliações
- 11ano Q 1 2 2 Extensao Das Reacoes QuimicasDocumento10 páginas11ano Q 1 2 2 Extensao Das Reacoes QuimicasHernani MartinsAinda não há avaliações
- Curso Básico de QuímicaDocumento4 páginasCurso Básico de QuímicaRodolfoAinda não há avaliações
- Trabalho Substituitivo de RelatórioDocumento7 páginasTrabalho Substituitivo de RelatórioAgatha Lima FrançoisAinda não há avaliações
- Equilíbrio QuímicoDocumento2 páginasEquilíbrio QuímicoF TAGAinda não há avaliações
- Equilíbrio QuímicoDocumento2 páginasEquilíbrio QuímicoF TAGAinda não há avaliações
- Equilibrio QuimicoDocumento7 páginasEquilibrio QuimicoAnna Clara Alves SáAinda não há avaliações
- Cromato e DicromatoDocumento9 páginasCromato e DicromatoWolney PiresAinda não há avaliações
- 3 - Equilíbrio Químico em Sistemas Ideais e Não IdeaisDocumento61 páginas3 - Equilíbrio Químico em Sistemas Ideais e Não IdeaisRosianeCristinaCandeuAinda não há avaliações
- Equilibrio QuimicoDocumento20 páginasEquilibrio QuimicoGiulliano Carlos ThomazAinda não há avaliações
- Equi Lib RioDocumento17 páginasEqui Lib RioRafael FerreiraAinda não há avaliações
- 01 Equilíbrio QuímicoDocumento4 páginas01 Equilíbrio QuímicoDiogo DiasAinda não há avaliações
- Eletrólitos FortesDocumento3 páginasEletrólitos FortesHenrique SakitaAinda não há avaliações
- Apostila - Equlíbrio QuímicoDocumento2 páginasApostila - Equlíbrio QuímicoCamille SousaAinda não há avaliações
- Equilibrio Quimico Deslocamento-1Documento43 páginasEquilibrio Quimico Deslocamento-1ana laura silva dos santosAinda não há avaliações
- Equilibrio Quimico e Constantes de EquilíbrioDocumento3 páginasEquilibrio Quimico e Constantes de EquilíbrioOlavo RimoliAinda não há avaliações
- Qui MicaDocumento2 páginasQui MicaIsla Leslley Vieira de MoraisAinda não há avaliações
- Conceito de Equilíbrio QuímicoDocumento4 páginasConceito de Equilíbrio QuímicoTainá MartinsAinda não há avaliações
- Cinemática QuímicaDocumento19 páginasCinemática Químicalaiane rabelo bragaAinda não há avaliações
- Equilibrio QuímicoDocumento29 páginasEquilibrio QuímicoIkaro RozaAinda não há avaliações
- Equílibrio QuímicoDocumento2 páginasEquílibrio QuímicoKauan CamposAinda não há avaliações
- Deslocamento Do EquilíbrioDocumento2 páginasDeslocamento Do EquilíbrioThuyline DyandraAinda não há avaliações
- QMC AP Equilíbrio Químico Equilíbrio QuímicoDocumento13 páginasQMC AP Equilíbrio Químico Equilíbrio QuímicoGabriel Lima PizanoAinda não há avaliações
- Relatório 18 Deslocamento de Equilibrio 02Documento9 páginasRelatório 18 Deslocamento de Equilibrio 02Rodrigo SowaAinda não há avaliações
- Resumo 21 Introdução Ao Equilíbrio QuímicoDocumento6 páginasResumo 21 Introdução Ao Equilíbrio QuímicorafaelllllAinda não há avaliações
- Equilibrio QuímicoDocumento13 páginasEquilibrio QuímicoGISELLE FRANCINE BRITO MUNIZAinda não há avaliações
- QuimicaDocumento2 páginasQuimicaKauan CamposAinda não há avaliações
- Trabalho de QuímicaDocumento15 páginasTrabalho de QuímicaJean de Liz RosaAinda não há avaliações
- 06Q - Extensão Das Reações QuímicasDocumento30 páginas06Q - Extensão Das Reações Químicasdiana BaptistaAinda não há avaliações
- Equilíbrio Químico, Oxirredução, EletroquímicaDocumento43 páginasEquilíbrio Químico, Oxirredução, EletroquímicaLucas MarcelinoAinda não há avaliações
- Trabalho de QuimicaDocumento9 páginasTrabalho de QuimicaMarciliaAinda não há avaliações
- QMC AP Equilíbrio Químico Deslocamento de EquilíbrioDocumento11 páginasQMC AP Equilíbrio Químico Deslocamento de EquilíbrioGabriel Lima PizanoAinda não há avaliações
- Trabalho Quimica Miguel N-21 3DDocumento10 páginasTrabalho Quimica Miguel N-21 3DMiguel Baptista RodriguesAinda não há avaliações
- Movimentos, Posições, Trajetória e TempoDocumento1 páginaMovimentos, Posições, Trajetória e TempoF TAGAinda não há avaliações
- MatemáticaDocumento2 páginasMatemáticaF TAGAinda não há avaliações
- FilosofiaDocumento6 páginasFilosofiaF TAGAinda não há avaliações
- Frei Luis de SousaDocumento1 páginaFrei Luis de SousaF TAGAinda não há avaliações
- Replicação Do DnaDocumento1 páginaReplicação Do DnaF TAGAinda não há avaliações
- Constituição Do Testículo: GametogéneseDocumento4 páginasConstituição Do Testículo: GametogéneseF TAGAinda não há avaliações
- Oogénese: Zona Medular - InternaDocumento7 páginasOogénese: Zona Medular - InternaF TAG100% (1)
- Constituição Do DnaDocumento1 páginaConstituição Do DnaF TAGAinda não há avaliações
- Constituição Do Sistema ReprodutorDocumento1 páginaConstituição Do Sistema ReprodutorF TAGAinda não há avaliações
- FecundaçãoDocumento3 páginasFecundaçãoF TAGAinda não há avaliações