Escolar Documentos
Profissional Documentos
Cultura Documentos
Equilíbrio Químico
Enviado por
F TAG0 notas0% acharam este documento útil (0 voto)
3 visualizações2 páginasDireitos autorais
© © All Rights Reserved
Formatos disponíveis
DOCX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
3 visualizações2 páginasEquilíbrio Químico
Enviado por
F TAGDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato DOCX, PDF, TXT ou leia online no Scribd
Você está na página 1de 2
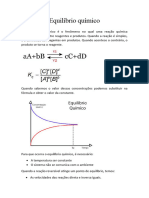
Equilíbrio Químico
colisões entre as moléculas destes e,
Reações completas e portanto, a velocidade da reação direta é
incompletas máxima e a velocidade da reação
inversa é nula, pois ainda não se iniciou
Reação completa – Uma reação química a formação dos produtos da reação;
diz-se completa quando leva ao esgotamento À medida que a reação prossegue,
de, pelo menos, um dos reagentes; diminui o número de moléculas dos
reagentes e aumenta o número de
No estado final, ou existem apenas moléculas de produtos da reação –
produtos da reação, se os regentes Logo, a velocidade da reação direta vai
estiverem nas proporções diminuir e a velocidade da reação
estequiométricas adequadas, ou existe inversa vai aumentando;
uma mistura de produtos da reação com A dada altura, a velocidade da reação
os reagentes que estavam em excesso; direta iguala à velocidade da reação
Reação Incompleta – Uma reação química inversa: atingindo-se o equilíbrio
diz-se incompleta quando, no final, existe uma químico – A partir deste instante as
mistura de todos os reagentes e de todos os concentrações das substâncias presentes
produtos da reação; no equilíbrio mantêm-se constantes;
No equilíbrio químico não se observam
alterações nas propriedades do sistema
(cor, concentração, pressão,
Reações Reversíveis e temperatura, etc.);
Irreversíveis
Reações Irreversíveis – Reações químicas Equilíbrios Homogéneos e
onde os reagentes dão origem aos produtos da
reação, mas os produtos em contacto não Heterogéneos
reagem entre si para regenerar os reagentes,
processando-se num só sentido; Equilíbrio Homogéneo – Um equilíbrio é
homogéneo quando os constituintes do sistema
Reações Reversíveis – Reações que, em se encontram todos na mesma fase;
sistemas fechados, os produtos da reação
reagem entre si regenerando os reagentes; Equilíbrio Heterogéneo – Um equilíbrio
químico é heterogéneo quando os constituintes
Nestas reações coexistem a reação do sistema se encontram em fases diferentes;
direta, em que os reagentes originam os
produtos da reação, e a reação inversa,
em que os produtos da reação
regeneram os reagentes;
Equilíbrio Químico – Verifica-se quando
a reação direta e a reção inversa continuam a
ocorrer, processando-se à mesma velocidade;
Como no início só há moléculas de
reagentes, existe um número maior de
A quantidade química dos componentes
do sistema químico pode ser convertida
na respetiva concentração através da
expressão:
Você também pode gostar
- Equilíbrio QuímicoDocumento2 páginasEquilíbrio QuímicoF TAGAinda não há avaliações
- Quimica 11ºDocumento3 páginasQuimica 11ºSaraAinda não há avaliações
- Química 11Documento8 páginasQuímica 11MariassAinda não há avaliações
- Resumos - Quimica - 11º - Novo - Programa - 2016Documento10 páginasResumos - Quimica - 11º - Novo - Programa - 2016Margarida FonsecaAinda não há avaliações
- Equi Lib RioDocumento17 páginasEqui Lib RioRafael FerreiraAinda não há avaliações
- Estudo Dirigido Equilibrio Quimico RespostasDocumento2 páginasEstudo Dirigido Equilibrio Quimico RespostasNorcéssio SanháAinda não há avaliações
- Aspetos Quantitativos Das Reações-ResumoDocumento4 páginasAspetos Quantitativos Das Reações-ResumoRucasRuiJorgeAinda não há avaliações
- Reagente LimitanteDocumento6 páginasReagente LimitanteSonia Coelho0% (1)
- Cinética QuímicaDocumento3 páginasCinética QuímicaMonte ViajanteAinda não há avaliações
- FT 2 - EqulíbrioDocumento16 páginasFT 2 - EqulíbrioMartinha LeãoAinda não há avaliações
- QMC AP Equilíbrio Químico Deslocamento de EquilíbrioDocumento11 páginasQMC AP Equilíbrio Químico Deslocamento de EquilíbrioGabriel Lima PizanoAinda não há avaliações
- Introdução: Reações Químicas ReversíveisDocumento6 páginasIntrodução: Reações Químicas ReversíveisEduarda SantannaAinda não há avaliações
- Apostila de Quimica 24 E28093 Equilibrio QuimicoDocumento3 páginasApostila de Quimica 24 E28093 Equilibrio QuimicoMatilde SaraAinda não há avaliações
- 2 Equilibrio Químico-1Documento24 páginas2 Equilibrio Químico-1Yago SilvaAinda não há avaliações
- 2 Equilibrio Químico-1Documento24 páginas2 Equilibrio Químico-1Yago SilvaAinda não há avaliações
- Equilíbrio QuímicoDocumento10 páginasEquilíbrio QuímicoAbreu Ngongo Filipa KasanjiAinda não há avaliações
- Trabalho de QuimicaDocumento9 páginasTrabalho de QuimicaMarciliaAinda não há avaliações
- Equilíbrio QuímicoDocumento3 páginasEquilíbrio QuímicoinesAinda não há avaliações
- FQ11 Q1.2 2017-18Documento9 páginasFQ11 Q1.2 2017-18Sala 11Ainda não há avaliações
- Equílibrio QuímicoDocumento2 páginasEquílibrio QuímicoKauan CamposAinda não há avaliações
- Equilíbrio QuímicoDocumento21 páginasEquilíbrio QuímicoMaria RodriguesAinda não há avaliações
- Qui MicaDocumento2 páginasQui MicaIsla Leslley Vieira de MoraisAinda não há avaliações
- Resumo 21 Introdução Ao Equilíbrio QuímicoDocumento6 páginasResumo 21 Introdução Ao Equilíbrio QuímicorafaelllllAinda não há avaliações
- QuimicaDocumento2 páginasQuimicaKauan CamposAinda não há avaliações
- Apostila 5 - Equilíbrio QuímicoDocumento39 páginasApostila 5 - Equilíbrio QuímicoGustavo MarinhoAinda não há avaliações
- Cinemática QuímicaDocumento19 páginasCinemática Químicalaiane rabelo bragaAinda não há avaliações
- 01 Equilíbrio QuímicoDocumento4 páginas01 Equilíbrio QuímicoDiogo DiasAinda não há avaliações
- Equilíbrio Químico - 3° AnoDocumento17 páginasEquilíbrio Químico - 3° AnoJeyciane RosaAinda não há avaliações
- Curso Básico de QuímicaDocumento4 páginasCurso Básico de QuímicaRodolfoAinda não há avaliações
- 5 EquilibrioQuimicoDocumento21 páginas5 EquilibrioQuimicoRute FidalgoAinda não há avaliações
- Reações QuímicasDocumento1 páginaReações QuímicasF TAGAinda não há avaliações
- Equilíbrio Químico Yassin (Salvo Automaticamente)Documento19 páginasEquilíbrio Químico Yassin (Salvo Automaticamente)Fabio MarteAinda não há avaliações
- Resumo Equilíbrio-QuímicoDocumento4 páginasResumo Equilíbrio-Químicoantonio josé das chagas100% (1)
- Cinética QuímicaDocumento26 páginasCinética QuímicaTamiris AssisAinda não há avaliações
- Trabalho Sobre Equilibrio QuimicoDocumento10 páginasTrabalho Sobre Equilibrio QuimicoYasmim Silva100% (1)
- Trabalho Quimica Miguel N-21 3DDocumento10 páginasTrabalho Quimica Miguel N-21 3DMiguel Baptista RodriguesAinda não há avaliações
- Trabalho Substituitivo de RelatórioDocumento7 páginasTrabalho Substituitivo de RelatórioAgatha Lima FrançoisAinda não há avaliações
- Sintese-1 2Documento2 páginasSintese-1 2carlosAinda não há avaliações
- QMC AP Equilíbrio Químico Equilíbrio QuímicoDocumento13 páginasQMC AP Equilíbrio Químico Equilíbrio QuímicoGabriel Lima PizanoAinda não há avaliações
- Relatório 18 Deslocamento de Equilibrio 02Documento9 páginasRelatório 18 Deslocamento de Equilibrio 02Rodrigo SowaAinda não há avaliações
- Equilibrio QuimicoDocumento7 páginasEquilibrio QuimicoAnna Clara Alves SáAinda não há avaliações
- Cromato e DicromatoDocumento9 páginasCromato e DicromatoWolney PiresAinda não há avaliações
- Síntese Do Sulfato de TetraminocobreDocumento15 páginasSíntese Do Sulfato de TetraminocobreHenriques GuilaAinda não há avaliações
- Conceito de Equilíbrio QuímicoDocumento4 páginasConceito de Equilíbrio QuímicoTainá MartinsAinda não há avaliações
- ODocumento2 páginasOLany MesquitaAinda não há avaliações
- Cinética QuímicaDocumento3 páginasCinética QuímicaFabiano MartinsAinda não há avaliações
- WDT A35 BK Uc GZ 76 P 0 L 9 B OVZzs UPsn PT9 Qmixee ALeDocumento26 páginasWDT A35 BK Uc GZ 76 P 0 L 9 B OVZzs UPsn PT9 Qmixee ALearthuraugusto0889Ainda não há avaliações
- Quimica 2 - P1 3triDocumento2 páginasQuimica 2 - P1 3triMarcella MagaldiAinda não há avaliações
- Química: Hellen CâmaraDocumento8 páginasQuímica: Hellen CâmaraXKing X.KAinda não há avaliações
- Equilibrio QuimicoDocumento30 páginasEquilibrio QuimicoAna Raquel DamacenaAinda não há avaliações
- 27 - Cinética QuímicaDocumento37 páginas27 - Cinética QuímicaLuis cordeiroAinda não há avaliações
- Eja - Ciências Da Natureza-2º Semestre - Mod2 - Uni2Documento9 páginasEja - Ciências Da Natureza-2º Semestre - Mod2 - Uni2Leicy Kelly OliveiraAinda não há avaliações
- Quimica 11Documento22 páginasQuimica 11Diana LopesAinda não há avaliações
- Apostila Exercicios CineticaQuimicaDocumento6 páginasApostila Exercicios CineticaQuimicaAngélica BarrosAinda não há avaliações
- Cap Vi - Equilíbrios Químicos HomogêneosDocumento8 páginasCap Vi - Equilíbrios Químicos HomogêneosFilipeufcAinda não há avaliações
- Equilibrio QuimicoDocumento20 páginasEquilibrio QuimicoGiulliano Carlos ThomazAinda não há avaliações
- Equilíbrio QuímicoDocumento2 páginasEquilíbrio Químicogabrielacaluz56Ainda não há avaliações
- Aula 3 Cálculo de ReatoresDocumento29 páginasAula 3 Cálculo de ReatoresDiana De CarvalhoAinda não há avaliações
- Quociente de ReaçãoDocumento1 páginaQuociente de ReaçãoF TAGAinda não há avaliações
- Diferentes Estados de Equilíbrio de Um Sistema ReacionalDocumento1 páginaDiferentes Estados de Equilíbrio de Um Sistema ReacionalF TAGAinda não há avaliações
- Movimentos, Posições, Trajetória e TempoDocumento1 páginaMovimentos, Posições, Trajetória e TempoF TAGAinda não há avaliações
- FilosofiaDocumento6 páginasFilosofiaF TAGAinda não há avaliações
- MatemáticaDocumento2 páginasMatemáticaF TAGAinda não há avaliações
- Replicação Do DnaDocumento1 páginaReplicação Do DnaF TAGAinda não há avaliações
- Frei Luis de SousaDocumento1 páginaFrei Luis de SousaF TAGAinda não há avaliações
- Oogénese: Zona Medular - InternaDocumento7 páginasOogénese: Zona Medular - InternaF TAG100% (1)
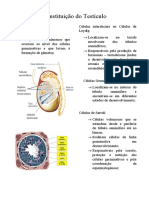
- Constituição Do Testículo: GametogéneseDocumento4 páginasConstituição Do Testículo: GametogéneseF TAGAinda não há avaliações
- Constituição Do DnaDocumento1 páginaConstituição Do DnaF TAGAinda não há avaliações
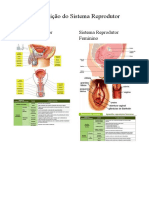
- Constituição Do Sistema ReprodutorDocumento1 páginaConstituição Do Sistema ReprodutorF TAGAinda não há avaliações
- FecundaçãoDocumento3 páginasFecundaçãoF TAGAinda não há avaliações
- NBR 11585 - Pigmentos E Cargas - Determinacao Da Densidade - Metodo Do PicnometroDocumento2 páginasNBR 11585 - Pigmentos E Cargas - Determinacao Da Densidade - Metodo Do PicnometroSamuel Alencar GonçalvesAinda não há avaliações
- Extração Do EugenolDocumento21 páginasExtração Do EugenolLucas KozlinskeiAinda não há avaliações
- Edwin Herbert HallDocumento3 páginasEdwin Herbert HallValdiélio MenezesAinda não há avaliações
- Trabalho MetalurgiaDocumento19 páginasTrabalho MetalurgiaNelo DionisioAinda não há avaliações
- 1 Lista de ExercíciosDocumento4 páginas1 Lista de ExercíciosEduardo SoutoAinda não há avaliações
- RESUMO Introduo Metalurgia Da Soldagem PDFDocumento97 páginasRESUMO Introduo Metalurgia Da Soldagem PDFCris NunesAinda não há avaliações
- Aula 4 ETDocumento18 páginasAula 4 ETStreet VegaAinda não há avaliações
- Processamento Primário Do PetróleoDocumento55 páginasProcessamento Primário Do PetróleoDickson AraujoAinda não há avaliações
- Ficha ! - Atomos Moleculas - Tabela Periodica - 2024Documento9 páginasFicha ! - Atomos Moleculas - Tabela Periodica - 2024mussamarioomarlinhalinhaAinda não há avaliações
- Planta BallestraDocumento17 páginasPlanta BallestraBeatriz MartinsAinda não há avaliações
- 1o Teste q12 2Documento4 páginas1o Teste q12 2Madalena DuqueAinda não há avaliações
- Condução TérmicaDocumento12 páginasCondução TérmicaJuresvalda MarcelaAinda não há avaliações
- Documento 2Documento2 páginasDocumento 2FelipeAinda não há avaliações
- Unid 22 Seriequimicaem 24 Abril 2021Documento34 páginasUnid 22 Seriequimicaem 24 Abril 2021Victoria Oliveira De SouzaAinda não há avaliações
- ColoidesDocumento3 páginasColoidesMaria OliveiraAinda não há avaliações
- AREAL - fq9 - Teste 6 - EnunciadoDocumento5 páginasAREAL - fq9 - Teste 6 - EnunciadoSandra GranjaAinda não há avaliações
- Relatorio de PPQDocumento48 páginasRelatorio de PPQSoares Samuel MuchavaAinda não há avaliações
- NBR 6467 - 1987 - Agregado - Determinação Do Inchamento de Agregado MiúdoDocumento5 páginasNBR 6467 - 1987 - Agregado - Determinação Do Inchamento de Agregado MiúdoHélio JúlioAinda não há avaliações
- 9 - Calor EspecíficoDocumento2 páginas9 - Calor EspecíficoBárbara MourãoAinda não há avaliações
- Troca de CalorDocumento2 páginasTroca de Calormarlon felipeAinda não há avaliações
- Tabela PeriódicaDocumento38 páginasTabela PeriódicaLuizaAinda não há avaliações
- Balanços em Colunas de Destilação Multiestágios - Lista 6Documento2 páginasBalanços em Colunas de Destilação Multiestágios - Lista 6Octavio JacksonAinda não há avaliações
- Lista de Exercícios de Cinética - Físico Química Avançada - 2022Documento3 páginasLista de Exercícios de Cinética - Físico Química Avançada - 2022Fagner MouraAinda não há avaliações
- Primeira Prova de QUI 119 PHTDocumento3 páginasPrimeira Prova de QUI 119 PHTAndré MarquesAinda não há avaliações
- Ácidos e Bases Aula 02Documento60 páginasÁcidos e Bases Aula 02Alécia Maria GonçalvesAinda não há avaliações
- Composição Molecular Das Celulas PDFDocumento60 páginasComposição Molecular Das Celulas PDFgambitAinda não há avaliações
- Tempera Superficial Feixe de Eletrons e Laser (Salvo Automaticamente)Documento8 páginasTempera Superficial Feixe de Eletrons e Laser (Salvo Automaticamente)Ivan PicchiAinda não há avaliações
- Processos de Fabricação-1Documento4 páginasProcessos de Fabricação-1lucasmsn38Ainda não há avaliações
- Aula 1 - Matéria e EnergiaDocumento40 páginasAula 1 - Matéria e EnergiaKaianne LarissaAinda não há avaliações
- Recuperador de Energia LGDocumento8 páginasRecuperador de Energia LGsuspeitaAinda não há avaliações