Escolar Documentos
Profissional Documentos
Cultura Documentos
Modelagem e Simulação Do Biogas
Enviado por
Lucas CostaDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Modelagem e Simulação Do Biogas
Enviado por
Lucas CostaDireitos autorais:
Formatos disponíveis
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
Trabalho apresentado no XXXVII CNMAC, S.J. dos Campos - SP, 2017.
Proceeding Series of the Brazilian Society of Computational and Applied
Mathematics
Modelagem e simulação do processo de formação do biogás
Marline Ilha da Silva1
Programa de Pós-Graduação em Matemática Aplicada - PPGMap, UFRGS, Porto Alegre, RS
Álvaro Luiz de Bortoli2
Departamento de Matemática Pura e Aplicada - DMPA, UFRGS, Porto Alegre, RS
Resumo. O processo de transformação da biomassa em biogás, conhecido como digestão
anaeróbia (Anaerobic Digestion - AD), tem se tornado uma importante fonte de pesquisa
nos últimos anos. O grande interesse neste processo deve-se ao fato desta transformação
apresentar vantagens para a natureza e, consequentemente, para o ser humano. Uma das
vantagens é a transformação de lixo em algo produtivo, que diminui a quantidade de gases
tóxicos lançados na atmosfera e ainda gera energia utilizável. Neste trabalho, será apre-
sentado o processo de digestão anaeróbia, incluindo a modelagem quı́mica e matemáica do
problema. Após a modelagem, o objetivo é simular este processo, resolvendo numericamente
as equações diferenciais do problema. Por fim, são apresentados resultados numéricos que
concordam com os dados encontrados na literatura.
Palavras-chave. Biomassa, Digestão anaeróbia, Biogás, Modelagem, Simulação
1 Introdução
Nos últimos anos, com o aumento do custo do petróleo e com suas reservas mundiais
se esgotando, a necessidade do desenvolvimento de fontes de energia alternativa a partir
de recursos locais vem aumentando rapidamente. Um dos recursos disponı́veis e que tem
grande possibilidade de desenvolvimento e viabilidade é a biomassa [3]. De modo geral,
a biomassa é a matéria-prima mais abundante do mundo, constituı́da por substâncias de
origem orgânica (vegetal, animal e microorganismos) e, ao contrário das fontes fósseis de
energia, como o petróleo e o carvão mineral, a biomassa é renovável em curto intervalo de
tempo [1, 3].
Através do processo de digestão anaeróbia [10], obtém-se um gás de grande relevância
para a geração de energia, conhecido como metano, representado pela fórmula quı́mica
CH4 . O metano é o principal componente do biogás, classificado como biocombustı́vel
que pode auxiliar o ser humano a se emancipar da dependência dos combustı́veis fósseis.
O biogás pode ser usado como combustı́vel em substituição do gás natural ou do Gás
Liquefeito de Petróleo (GLP), ambos extraı́dos de reservas minerais. Além disso, pode
ser utilizado na produção rural como, por exemplo, no aquecimento de instalações para
animais muito sensı́veis ao frio ou no aquecimento de estufas de produção vegetal, e pode
1
marline.ilhadasilva@gmail.com
2
dbortoli@mat.ufrgs.br
DOI: 10.5540/03.2018.006.01.0391 010391-1 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
ser usado também na geração de energia elétrica, através de geradores elétricos acoplados
a motores de explosão adaptados ao consumo de gás.
2 Modelagem
O processo de digestão anaeróbia é complexo e sensı́vel, formado por várias etapas
de interações metabólicas realizado por uma comunidade bem organizada de populações
microbianas. Todo o processo de digestão anaeróbia pode ocorrer em quatro fases:
1) Hidrólise
A degradação anaeróbia começa com a fase de hidrólise, na qual moléculas comple-
xas, tais como carboidratos, proteı́nas e lipı́deos são decompostas em monômeros
e oligômeros solúveis. A hidrólise é catalisada por enzimas excretadas a partir de
bactérias, tais como a celulase, protease e lipase. Os produtos finais desta reação são
os açúcares solúveis, aminoácidos, glicerol e ácidos carboxı́licos de cadeia longa [6].
Este processo pode ser representado pela seguinte reação
(C6 H10 O5 )n + nH2 O =n C6 H12 O6 . (1)
2) Acidogênese
Neste processo, as bactérias acidogênicas transformam os compostos orgânicos de
cadeia simples, geralmente de cadeia curta (volátil) em ácidos, cetonas e álcoois
[4]. As concentrações especı́ficas dos produtos formados nesta fase varia com o
tipo de bactérias bem como com as condições de cultura, tais como temperatura e
pH. A Tabela 1 mostra exemplos de produtos obtidos na fase de acidogênese, suas
respectivas reações quı́micas e a energia livre de Gibss, ∆Go , referente a cada reação.
Tabela 1: Exemplos de produtos obtidos na fase acidogênica.
Produtos Reações ∆Go (KJ/mol)
Ácido butı́rico C6 H12 O6 → C4 H8 O2 + 2CO2 + 2H2 -264,19
Ácido lático C6 H12 O6 → 2C3 H6 O3 -197,62
Ácido acético C6 H12 O6 + 2H2 O → 2CH3 COOH + 2CO2 + 4H2 -221,9
Etanol C6 H12 O6 → 2CH3 CH2 OH + 2CO2 -234,88
3) Acetogênese
Ocorre através da fermentação de hidratos de carbono e resulta em combinação de
acetato, CO2 e H2 . O papel do hidrogênio como intermediário é de importância
fundamental para as reações do processo de digestão anaeróbia. Ácidos graxos de
cadeia longa, formados a partir da hidrólise de lı́pidos, são oxidados para acetato ou
propionato e gás hidrogênio é formado [7]. Na Tabela 2 são mostradas as principais
DOI: 10.5540/03.2018.006.01.0391 010391-2 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
reações que ocorrem na fase de acetogênese e o respectivo valor do ∆Go para cada
uma das reações.
Tabela 2: Exemplos de reações que ocorrem na fase acetogênica.
Reações ∆Go (KJ/mol)
C4 H8 O2 + 2H2 O → 2C2 H4 O2 + 2H2 48
2C4 H8 O2 + 2H2 O + CO2 → 4C2 H4 O2 + CH4 -35
2C4 H8 O2 + 4H2 O → 4C2 H4 O2 + 4H2 96
4) Metanogênese
A metanogênese é o último estágio da decomposição anaeróbia, fase em que o me-
tano é produzido. Este passo é realizado por microorganismos metanogênicos que
são estritamente anaeróbios (não necessitam de oxigênio para o crescimento) [5].
Neste estágio, as arqueas metanogênicas (bactérias que vivem em meios estrita-
mente anaeróbios e que obtêm energia através da produção de metano) convertem
principalmente o ácido acético, o hidrogênio e o dióxido de carbono em metano.
Em função de sua afinidade por substrato e magnitude de produção de metano, as
arqueas metanogênicas são divididas em dois grupos principais [8]:
• Metanogênicas acetoclásticas: formam metano a partir do ácido acético ou
metanol. São os microrganismos predominantes na digestão anaeróbia, res-
ponsáveis por cerca de 60 a 70% de toda a produção de metano. Pertencem
a dois gêneros principais: Methanosarcina (formato de cocos) e Methanosaeta
(formato de filamentos).
• Metanogênicas hidrogenotróficas: praticamente todas as espécies conhecidas de
bactérias metanogênicas são capazes de produzir metano a partir de hidrogênio
e dióxido de carbono. Os gêneros mais frequentemente isolados em reatores
anaeróbios são: Methanobacterium, Methanospirillum e Methanobrevibacter.
Além das reações metanogênicas, a inter-conversão entre hidrogênio e acetato ca-
talisado por bactérias homoacetogênicas também desempenha papel importante na
via de formação de metano. Os homoacetógenos podem oxidar ou sintetizar acetato
dependendo da concentração externa de hidrogênio. Isto torna o hidrogênio capaz
de competir com vários micróbios diferentes, incluindo metanógenos [2]. As reações
relacionadas à fase de metanogênese são apresentadas na Tabela 3, juntamente com
o valor do ∆Go referente a cada reação.
DOI: 10.5540/03.2018.006.01.0391 010391-3 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
Tabela 3: Reações relacionadas à fase de metanogênese.
Nomenclatura Reações ∆Go (KJ/mol)
Metanogênese hidrogenotrófica 4H2 + CO2 → CH4 + 2H2 O -131
Metanogênese acetoclástica C2 H4 O2 → CH4 + CO2 -36
Oxidação do acetato C2 H4 O2 + 2H2 O → 4H2 + 2CO2 104
Homoacetogênese 4H2 + CO2 → C2 H4 O2 + 2H2 O -104
2.1 Formulação matemática e quı́mica do processo
A formulação matemática do processo de digestão anaeróbia está associada ao me-
canismo quı́mico das quatro fases descritas anteriormente: hidrólise, acidogênese, aceto-
genêse e matanogênese. A partir deste mecanismo, o modelo matemático é obtido de
acordo com as reações quı́micas apresentadas no processo de digestão anaeróbia. Esta
modelagem fornece um conjunto de equações diferenciais ordinárias, as quais, na maioria
das vezes são resolvidas numericamente.
A equação estequiometrica geral de qualquer processo quı́mico pode ser definida da
seguinte forma:
Ns
X
νj Yj = 0, (2)
j=1
sendo νj o coeficiente estequiométrico da j-ésima espécie Yj e Ns o número de espécies. Os
coeficientes estequiométricos são negativos para os reagentes e positivos para os produtos.
Além disso, ao multiplicar os coeficientes estequiométricos pelo mesmo escalar, a equação
quı́mica se refere ao mesmo processo quı́mico.
As taxas para reações elementares podem ser calculadas a partir da lei de ação das
massas, proposta por Waage e Guldberg, em 1864 [9], pela fórmula
Ns
ν
Y
ri = ki Yj ij , (3)
j
sendo Yj a concentração molar das espécies j, ri a taxa de reação e ki o coeficiente de taxa
que pode ser calculado por
∆Go
ki = e− RT , (4)
sendo ∆Go a energia livre de Gibss, R = 8, 3144J/Kmol a constante universal dos gases e
T a temperatura absoluta (em Kelvins).
A partir das taxas de produção das espécies e das taxas de reação ri escreve-se o sistema
cinético de equações diferenciais ordinárias (Ordinary Differential Equations - ODEs), da
seguinte maneira:
DOI: 10.5540/03.2018.006.01.0391 010391-4 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
R N
dYj X
= νij ri , j = 1, · · · , Ns . (5)
dt
i
Em geral, o sistema cinético das ODEs é de primeira ordem e não linear, uma vez
que contém derivadas de primeira ordem em relação ao tempo e a derivada temporal é
usualmente uma função não linear das concentrações. Cada espécie participa de várias
reações, sendo as taxas de produção das espécies acopladas. Dessa forma, utiliza-se o
método Runge-Kutta44 para resolução das equações, sendo um dos métodos mais precisos
para obter soluções aproximadas para este tipo de problema.
3 Simulação Numérica
O sistema cinético de ODEs é baseado no mecanismo do processo de digestão anaeróbia,
considerando as reações quı́micas das fases: (I) hidrólise, (II) acidogênese, (III) acetogênese
e metanogênese ((IV) metanogênese hidrogenotrófica e (V) metanogênese acetoclástica).
Utilizando a lei de ação de massa, as taxas r0 a r4 dos passos de reação são calculadas
a partir das concentrações das espécies e dos coeficientes de velocidade. Assim,
(I) C6 H10 O5 + H2 O = C6 H12 O6 r0 = k0 [C6 H10 O5 ][H2 O]
(II) C6 H12 O6 = C4 H8 O2 + 2CO2 + 2H2 r1 = k1 [C6 H12 O6 ]
(III) C4 H8 O2 + 2H2 O = 2C2 H4 O2 + 2H2 r2 = k2 [C4 H8 O2 ][H2 O]2
(IV) CO2 + 4H2 + = CH4 + 2H2 O r3 = k3 [CO2 ][H2 ]4
(V) 2C2 H4 O2 = 2CH4 + 2CO2 r4 = k4 [C2 H4 O2 ]2
O cálculo da produção das concentrações baseia-se na equação (5). Dessa maneira,
tem-se o seguinte conjunto de oito ODEs para resolver:
d
1) [C6 H10 O5 ] = −k0 [C6 H10 O5 ][H2 O]
dt
d
2) [C6 H12 O6 ] = k0 [C6 H10 O5 ][H2 O] − k1 [C6 H12 O6 ]
dt
d
3) [C4 H8 O2 ] = k1 [C6 H12 O6 ] − k2 [C4 H8 O2 ][H2 O]2
dt
d
4) [C2 H4 O2 ] = 2k2 [C4 H8 O2 ][H2 O]2 − 2k4 [C2 H4 O2 ]2
dt
d
5) [CH4 ] = k3 [CO2 ][H2 ]4 + 2k4 [C2 H4 O2 ]2
dt
d
6) [CO2 ] = 2k1 [C6 H12 O6 ] − k3 [CO2 ][H2 ]4 + 2k4 [C2 H4 O2 ]2
dt
d
7) [H2 ] = 2k1 [C6 H12 O6 ] + 2k2 [C4 H8 O2 ][H2 O]2 − 4k3 [CO2 ][H2 ]4
dt
d
8) [H2 O] = −k0 [C6 H10 O5 ][H2 O] − 2k2 [C4 H8 O2 ][H2 O]2 + 2k3 [CO2 ][H2 ]4
dt
Utilizando o valor de ∆Go , para temperatura de 25o C (ver Tabela 1, Tabela 2 e Tabela
3) de cada reação especı́fica, obtém-se os seguintes valores para as constantes procuradas:
k1 = 1, 1125, k2 = 0, 9808, k3 = 1, 054 e k4 = 1, 015.
DOI: 10.5540/03.2018.006.01.0391 010391-5 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
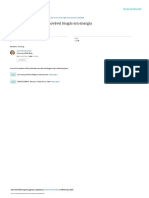
A Figura 1 mostra o comportamento das concentrações, no decorrer do tempo, das oito
espécies quı́micas envolvidas no processo de digestão anaeróbia, descrito anteriormente.
Celulose
6 Celulose
Glucose
Glucose
Acido Butirico
Acido Acetico
Ácido Butírico
Biogas(CO2,CH4)
Ácido Acético
hidrogenio
Biogás
agua
Hidrogênio
5 Água
4
Concentração
0 5 10 15 20 25 30 35 40 45 50
Tempo
Figura 1: Concentrações das espécies intermediárias do processo de digestão anaeróbia e
concentração de biogás resultante.
O resultado da simulação mostra o comportamento da formação de biogás e sua pro-
gressão no tempo. Além disso, observa-se o decaimento do substrato inicial (celulose) e
também das espécies intermediárias.
4 Conclusões
A produção de biogás esta associada as necessidades econômicas das comunidades
humanas, a conservação da natureza e o fim da degradação ecológica. Este processo
de produção de energia alternativa também gera outros materiais valiosos como fertili-
zantes, condicionadores do solo, alimentos para animais, etc. Outros benefı́cios desta
tecnologia podem ser vistos também, por exemplo, na redução de problemas de odor,
controle de patógenos de microorganismos, proteção de recursos hı́dricos, entre outros.
Uma compreensão mais profunda sobre a tecnologia anaeróbia é o ponto-chave para a
produção prática do biogás. Este trabalho apresenta o comportamento da formação deste
DOI: 10.5540/03.2018.006.01.0391 010391-6 © 2018 SBMAC
Proceeding Series of the Brazilian Society of Applied and Computational Mathematics, v. 6, n. 1, 2018.
valioso biocombustı́vel. A partir do processo de hidrólise obteve-se a glucose C6 H12 O6 .
Considerando a glucose como reagente, a reação global para a formação de biogás é
C6 H12 O6 = 3CH4 + 3CO2 . Isto indica que para 1kmol com 100% de glucose obtém-
se 6kmol de biogás, o que esta de acordo com o resultado obtido.
Referências
[1] P. Basu. Biomass gasification and pyrolysis - Practical Design. Academic. Press. Bur-
lington, MA, 2010. ISBN 978-0-12-374988-8.
[2] Boe, K. Online monitoring and control of the biogas process. PhD thesis, Institute
of Environment and Resources. Technical University of Denmark, Lyngby, Denmark,
May 2006. ISBN 87-91855-10-1.
[3] P. A. M. Claassen, A. M. Lopez Contreras, J. B. van Lier, E. W. J. van Niel, L.
Sijtsma, A. J. M. Stams, S. S. de Vries, and R. A. Weusthuis. Utilisation of biomass
for the supply of energy carriers. Appl. Microbiol Biotechnol, 52: 741–755, 1999. DOI:
10.1007/s002530051586.
[4] K. Ostrem. Greening Waste: Anaerobic Disgestion for Treating the Organic Fraction
of Municipal Solid Wastes. PhD thesis, School of Engineering and Applied Science,
Columbia University, may 2004.
[5] Z. Prokopová, and R. Prokop. Modelling and simulation of dry anaerobic fermen-
tation. European Conference on Modelling and Simulation, 200–205, 2010. DOI:
10.7148/2010-0200-0205.
[6] M. Ralph, and G. J. Dong. Environmental Microbiology. John Wiley and Sons, 2a
ed., 2010. ISBN 978-0-470-17790-7.
[7] N. H. S. Ray, M. K. Mohanty, and R. C. Mohanty. Anaerobic digestion of kitchen was-
tes: “biogas production and pretreatment of wastes, a review”. International Journal
of Scientific and Research Publications, 3: 2250–3153, 2013. ISSN 2250-3153.
[8] D. I. M. Schön, Numerical Modelling of Anaerobic Digestion Processes in Agricultural
Biogas Plants. Dissertation, Innsbruck, Februar, 2009.
[9] T. Turányi, and A. S. Tomlin. Analysis of Kinetic Reaction Mechanisms. Springer-
Verlag Berlin Heidelberg, 2014. DOI 10.1007/978-3-662-44562-4.
[10] K. Zieminski and M. Frac. Methane fermentation process as anaerobic digestion of
biomass: Transformations, stages and microorganisms. African Journal of Biotech-
nology, 11: 4127–4139, 2012. DOI: 10.5897/AJBX11.054.
DOI: 10.5540/03.2018.006.01.0391 010391-7 © 2018 SBMAC
Você também pode gostar
- Etanol de biomassa de milho: utilização de aprendizagem de máquina no estudo de casos de caldeirasNo EverandEtanol de biomassa de milho: utilização de aprendizagem de máquina no estudo de casos de caldeirasAinda não há avaliações
- Estequiometria Industrial I - Aula 4 - Balanço de Massa Com Reação QuímicaDocumento31 páginasEstequiometria Industrial I - Aula 4 - Balanço de Massa Com Reação QuímicaErika VieiraAinda não há avaliações
- A Utilização De Material Lignocelulósico Na Produção De BioetanolNo EverandA Utilização De Material Lignocelulósico Na Produção De BioetanolAinda não há avaliações
- Estequiometria Sem MedoDocumento22 páginasEstequiometria Sem Medokely AzevedoAinda não há avaliações
- Crescimento microbiano e formação de produtosDocumento73 páginasCrescimento microbiano e formação de produtosEduardo Anderson0% (1)
- Aula 3.1 Cinética Química - Parte 2 - Com Exercícios Do Lar Resolvidos ParcialDocumento76 páginasAula 3.1 Cinética Química - Parte 2 - Com Exercícios Do Lar Resolvidos ParcialDANIEL DE ALMEIDA KULEVICZAinda não há avaliações
- Estequiometria e reações químicasDocumento28 páginasEstequiometria e reações químicasAraújo NettoAinda não há avaliações
- Cálculo estequiométrico: relações entre reagentes e produtos em reações químicasDocumento17 páginasCálculo estequiométrico: relações entre reagentes e produtos em reações químicasgiselenovoAinda não há avaliações
- Introdução aos Processos QuímicosDocumento83 páginasIntrodução aos Processos QuímicosNáthaly CoelhoAinda não há avaliações
- 1600 Físico Química Aplicada - Exercícios Comentados - Com IsbnDocumento889 páginas1600 Físico Química Aplicada - Exercícios Comentados - Com IsbnGahelyka Aghta Pantano Souza100% (1)
- Relatório de Química-EstequiometriaDocumento8 páginasRelatório de Química-EstequiometriaNatan Camargo100% (1)
- Ficha1 Revisões10Documento5 páginasFicha1 Revisões10Clara Gomes100% (1)
- Mapeamento Tecnológico para Purificação deDocumento9 páginasMapeamento Tecnológico para Purificação deGames ELITEAinda não há avaliações
- 4355 17384 1 PBDocumento20 páginas4355 17384 1 PBSalif JamalAinda não há avaliações
- Travessia para o EnemDocumento93 páginasTravessia para o EnemKetyllyn Souza OliveiraAinda não há avaliações
- BioqúimicaDocumento24 páginasBioqúimicaDianaFurtadoAinda não há avaliações
- Biogás e Bio Digest orDocumento35 páginasBiogás e Bio Digest orapi-3704111100% (7)
- Processos de nitrificação e desnitrificaçãoDocumento5 páginasProcessos de nitrificação e desnitrificaçãoCassiane Ramos BarbosaAinda não há avaliações
- Arquvo10 1Documento17 páginasArquvo10 1lucasnsantos2412Ainda não há avaliações
- Lista Da Unicamp 10 10 2023Documento18 páginasLista Da Unicamp 10 10 2023glendaumeroAinda não há avaliações
- Microorganismos AeróbicosDocumento7 páginasMicroorganismos AeróbicosLaisllaAndradeAinda não há avaliações
- Modalidade 4datahora 15 01 2015 01 59 45 Idinscrito 678Documento6 páginasModalidade 4datahora 15 01 2015 01 59 45 Idinscrito 678Alan LeeAinda não há avaliações
- Artigo 453 Citenel - 2015 - Rev Aneel Maio PDFDocumento12 páginasArtigo 453 Citenel - 2015 - Rev Aneel Maio PDFLudmila LealAinda não há avaliações
- BIOENERGÉTUCADocumento70 páginasBIOENERGÉTUCAjoaoa.queiroz99Ainda não há avaliações
- Questoes Snipe NaturezaDocumento7 páginasQuestoes Snipe NaturezaEmanuel MedeirosAinda não há avaliações
- Apostila Com Todas As Questões Do EnemDocumento121 páginasApostila Com Todas As Questões Do EnemLourenço BotelhoAinda não há avaliações
- Issufo Juma 2Documento17 páginasIssufo Juma 2issufo JumaAinda não há avaliações
- Aula 11 - DIGESTÃO ANAERÓBIADocumento79 páginasAula 11 - DIGESTÃO ANAERÓBIAtstvandecoAinda não há avaliações
- Enem 1Documento20 páginasEnem 1GrimmAinda não há avaliações
- Resp. Celular - EnemDocumento4 páginasResp. Celular - Enemgokuedge2016Ainda não há avaliações
- Biossíntese de carboidratos, ácidos graxos e biopolímerosDocumento46 páginasBiossíntese de carboidratos, ácidos graxos e biopolímerosgaperimAinda não há avaliações
- Calculo de Potencial de BiogásDocumento14 páginasCalculo de Potencial de BiogásAlex LopesAinda não há avaliações
- Artigo AnaNum 2Documento7 páginasArtigo AnaNum 2Artur Pereira Neto artur.netoAinda não há avaliações
- Modelo de Cabeçalho para ProvaDocumento5 páginasModelo de Cabeçalho para Provaclinica malaquitaAinda não há avaliações
- ENRE1 - MES - Biomassa - 1 Exercícios - 2014-Biocombustíveis Líquidos PDFDocumento5 páginasENRE1 - MES - Biomassa - 1 Exercícios - 2014-Biocombustíveis Líquidos PDFtarouca1991Ainda não há avaliações
- Simulado 02Documento8 páginasSimulado 02Anne MoraesAinda não há avaliações
- AULA 5-Atividade de Sistematização-Catalisadores-AlunosDocumento7 páginasAULA 5-Atividade de Sistematização-Catalisadores-AlunosCarlos AlcantaraAinda não há avaliações
- Organica Isomeria PlanaDocumento22 páginasOrganica Isomeria PlanaFabianaSouzaDutraAinda não há avaliações
- AR - Estimativa Geração Biogás - CON10-1527Documento9 páginasAR - Estimativa Geração Biogás - CON10-1527Júlio DaineziAinda não há avaliações
- Resolucao de Prova 2A Sem 1 2010 UABDocumento4 páginasResolucao de Prova 2A Sem 1 2010 UABcassiokawakita75% (4)
- Revisão metabolismo energéticoDocumento157 páginasRevisão metabolismo energéticoHN Harry NetoAinda não há avaliações
- A Conversao Da Fonte Renovavel Biogas em EnergiaDocumento12 páginasA Conversao Da Fonte Renovavel Biogas em EnergiaClaraAinda não há avaliações
- Avaliação da produção e purificação de biogásDocumento22 páginasAvaliação da produção e purificação de biogásDanny BoyAinda não há avaliações
- Biologia - Ciclos biogeoquímicos e disciplinas biológicasDocumento7 páginasBiologia - Ciclos biogeoquímicos e disciplinas biológicasPaulo HenriqueAinda não há avaliações
- Ebook QUMICA Primeiro Bimestre ModificadoDocumento29 páginasEbook QUMICA Primeiro Bimestre Modificadocv8574013Ainda não há avaliações
- 6 - Química 1 - Paulo Alexandre - Psc-Sis 1 - Apostila 3 - 2023Documento48 páginas6 - Química 1 - Paulo Alexandre - Psc-Sis 1 - Apostila 3 - 2023cuca manausAinda não há avaliações
- Produção etanol microrganismosDocumento3 páginasProdução etanol microrganismosWillian De PaulaAinda não há avaliações
- ListinhaDocumento7 páginasListinharayan santanaAinda não há avaliações
- Questões RevisãoDocumento15 páginasQuestões RevisãoChaconAinda não há avaliações
- Metano 0.2Documento14 páginasMetano 0.2Eleuterio de FatimaAinda não há avaliações
- Química 01 - Fatores que influenciam a rapidez das transformações químicasDocumento64 páginasQuímica 01 - Fatores que influenciam a rapidez das transformações químicasfernandalinsAinda não há avaliações
- Simulado - 3 Série - 2 Bimestre - Termo e CineticaDocumento3 páginasSimulado - 3 Série - 2 Bimestre - Termo e CineticaIsaac PEREIRAAinda não há avaliações
- F.Aval Formativa FOTOSSÍNTESEDocumento3 páginasF.Aval Formativa FOTOSSÍNTESEArticAinda não há avaliações
- Relatório - Obtenção de BiodieselDocumento10 páginasRelatório - Obtenção de BiodieselAmanda AlmerindoAinda não há avaliações
- Aula 3Documento83 páginasAula 3Jucelino SantosAinda não há avaliações
- Digestão de nutrientes em anelídeosDocumento20 páginasDigestão de nutrientes em anelídeosAlexandre LimaAinda não há avaliações
- 02-Capitulo 1Documento21 páginas02-Capitulo 1Raíssa MotaAinda não há avaliações
- Tratamento de esgoto e remoção de contaminantes em análise de efluentesDocumento3 páginasTratamento de esgoto e remoção de contaminantes em análise de efluentesGuilherme CoqueiroAinda não há avaliações
- Digestão AnaeróbiaDocumento1 páginaDigestão AnaeróbiaAndreia BrandaoAinda não há avaliações
- Quitosano: propriedades e modificaçõesDocumento6 páginasQuitosano: propriedades e modificaçõesnathaliaAinda não há avaliações
- 14 Fermentação e QuimissínteseDocumento5 páginas14 Fermentação e QuimissínteseSamuelSamuelAinda não há avaliações
- Fotossintese Aula 4Documento19 páginasFotossintese Aula 4Fernanda BrisonAinda não há avaliações
- Syntrophic Biodegradation of Hydrocarbon Contaminants - En.ptDocumento9 páginasSyntrophic Biodegradation of Hydrocarbon Contaminants - En.ptmedasabAinda não há avaliações
- Ecologia - Ciclos Biogeoquimicos - 2008-2012: Página 1 de 22Documento22 páginasEcologia - Ciclos Biogeoquimicos - 2008-2012: Página 1 de 22lucasypldAinda não há avaliações
- Biocombustiveis Cap06Documento89 páginasBiocombustiveis Cap06Zacarias Mascarenhas Simao SimaoAinda não há avaliações
- GRS137-REO2 - 2020 - II - Parte 2Documento48 páginasGRS137-REO2 - 2020 - II - Parte 2rizzoritzoAinda não há avaliações
- Simulado - 2 Série - 2 Bimestre - Termo e CineticaDocumento3 páginasSimulado - 2 Série - 2 Bimestre - Termo e CineticaIsaac PEREIRAAinda não há avaliações
- Estudo da capacidade de geração de biogás para as cidades de Barra Mansa, Resende e Volta Redonda para a implantação de uma usina de biodigestor anaeróbicoNo EverandEstudo da capacidade de geração de biogás para as cidades de Barra Mansa, Resende e Volta Redonda para a implantação de uma usina de biodigestor anaeróbicoAinda não há avaliações
- Aulas de Química da Turma ITADocumento3 páginasAulas de Química da Turma ITAGutierrezAinda não há avaliações
- Processos Químicos Industriais IDocumento19 páginasProcessos Químicos Industriais Ipacesar482Ainda não há avaliações
- 1 UimivwDocumento2 páginas1 Uimivwmmmmhjk67Ainda não há avaliações
- BRUNA MIKAELLA RIBEIRO CARDOSO - (Template) Atividade EstequiometriaDocumento3 páginasBRUNA MIKAELLA RIBEIRO CARDOSO - (Template) Atividade Estequiometriamara thanyaAinda não há avaliações
- Reacoes Quimicas Parte I E1656071153Documento69 páginasReacoes Quimicas Parte I E1656071153marceloAinda não há avaliações
- Caderno de Práticas de Laboratório de Química GeralDocumento232 páginasCaderno de Práticas de Laboratório de Química GeralGabriel SoaresAinda não há avaliações
- Lucas QuímicaDocumento60 páginasLucas QuímicaJeronimo Waterloo MonteiroAinda não há avaliações
- Bibliografia de Química GeralDocumento138 páginasBibliografia de Química GeralRigo RodriguesAinda não há avaliações
- Captura de Tela 2023-10-06 À(s) 08.55.48Documento1 páginaCaptura de Tela 2023-10-06 À(s) 08.55.48arthurgostoso420Ainda não há avaliações
- Aula 7 Introdução A Formulação de Materiais CerâmicosDocumento17 páginasAula 7 Introdução A Formulação de Materiais CerâmicosAdemar Espírito SantoAinda não há avaliações
- Equações Químicas e Concentrações de SoluçõesDocumento20 páginasEquações Químicas e Concentrações de SoluçõesRENATO MOURAAinda não há avaliações
- Estequiometria e Leis PonderaisDocumento9 páginasEstequiometria e Leis PonderaisDanieli PecininiAinda não há avaliações
- Capítulo 02Documento65 páginasCapítulo 02keylarAinda não há avaliações
- Quimica Prof. Rosane Aula 26 05 Calculo Estequiometrico 1oano E.M.Documento19 páginasQuimica Prof. Rosane Aula 26 05 Calculo Estequiometrico 1oano E.M.vanderlanaraujo207Ainda não há avaliações
- Aula 4. Balanço de Massa Com Reação QuímicaDocumento49 páginasAula 4. Balanço de Massa Com Reação QuímicaLéya MateusAinda não há avaliações
- Cinética Química - Velocidade Média de Uma Reação QuímicaDocumento12 páginasCinética Química - Velocidade Média de Uma Reação QuímicaKim LinaAinda não há avaliações
- Neutralização ácido-base: balanceamento e produtosDocumento5 páginasNeutralização ácido-base: balanceamento e produtos•Thyago Borges•Ainda não há avaliações
- Produção de hidrogênio com magnésioDocumento4 páginasProdução de hidrogênio com magnésioThainaradematosAinda não há avaliações
- Eq11 Manual Verifique Aprendeu m1Documento2 páginasEq11 Manual Verifique Aprendeu m1Rui MedeirosAinda não há avaliações
- Relatório 2 - Prática - Química 1Documento15 páginasRelatório 2 - Prática - Química 1TalennyAinda não há avaliações
- Estequiometria Casos ParticularesDocumento4 páginasEstequiometria Casos ParticularesFabiano WelterAinda não há avaliações
- Projetos de Sistemas TérmicosDocumento71 páginasProjetos de Sistemas TérmicosnorthoncristyanAinda não há avaliações