Escolar Documentos
Profissional Documentos
Cultura Documentos
Lista 1 Fensup
Enviado por
maria beatrizTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Lista 1 Fensup
Enviado por
maria beatrizDireitos autorais:
Formatos disponíveis
Fenômenos de Superfície e Eletroquímica
Lista 1
Aluna:
Aluna:
Aluno:
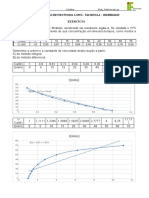
Questão 1)
a) Primeiramente devemos saber que o componente menos volátil é o que
tem maior pressão de vapor quando está puro, que nesse caso é a
Acetona. A pressão de vapor ideal total da solução é a soma das pressões
parciais reais de cada composto
PT =P A + PC
XC PC PA PT
0,00 0 347 347
0,20 35 250 285
0,40 82 175 257
0,60 142 92 234
0,80 200 37 237
1,00 273 0 273
Pressão x Fração Molar
400
350
300
250
200
150
100
50
0
0 0.2 0.4 0.6 0.8 1
Pressão parcial da Acetona Pressão parcial do Clorofórmio
Pressão Total da solução
b) A Lei de Henry é dada para o Clorofórmio por PC= X C . K C e para a
Acetona como P A =X A . K A e a Lei de Raoult é dada para o Clorofórmio
¿ ¿
como PC = X C . PC e para a Acetona como P A =X A . P A, e a pressão ideal da
solução é dada pela soma das leis de Raoult para os dois componentes.
XC LRC LRA L HC L HA P ID
0,00 0 347 0 178 347
0,20 54,6 277,6 34,4 142,4 332,2
0,40 109,2 208,2 68,8 106,8 317,4
0,60 163,8 138,8 103,2 71,2 302,6
0,80 218,4 69,4 137,6 35,6 287,8
1,00 273 0 172 0 273
Você também pode gostar
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- QuimFisica2Cap3 (Diagramas de Fases) (Exercícios)Documento4 páginasQuimFisica2Cap3 (Diagramas de Fases) (Exercícios)Janaina LeitinhoAinda não há avaliações
- Lista de Exercicios Termodinâmica IIDocumento28 páginasLista de Exercicios Termodinâmica IIDavid Santos de França33% (3)
- EER0013 - Lista de Exercícios 2Documento16 páginasEER0013 - Lista de Exercícios 2JulioCezarAlvesJunior0% (2)
- Caldeira Paulo MouraDocumento342 páginasCaldeira Paulo MouraCosta Vagner100% (1)
- Relatório Entropia de VaporizaçãoDocumento9 páginasRelatório Entropia de VaporizaçãoJuliana Giantini100% (1)
- LISTA EXERCÍCIOS 3 - Termodinâmica Das Soluçoes Não-Eletrolíticas ReaisDocumento5 páginasLISTA EXERCÍCIOS 3 - Termodinâmica Das Soluçoes Não-Eletrolíticas ReaisAngenor Geovani AulerAinda não há avaliações
- OP3 ListaDocumento32 páginasOP3 ListaJoão Pedro Aragão0% (1)
- Lista Exercicios 2 Equilibrio Liq Liq PDFDocumento8 páginasLista Exercicios 2 Equilibrio Liq Liq PDFJanaina LeitinhoAinda não há avaliações
- Lista-P2 TermodinamicaDocumento30 páginasLista-P2 TermodinamicaGaby SilveiraAinda não há avaliações
- Exercícios - ELVDocumento4 páginasExercícios - ELVTayla LuizaAinda não há avaliações
- Trabalho ELV Diagrama T-X-Y (Pentano-Heptano)Documento5 páginasTrabalho ELV Diagrama T-X-Y (Pentano-Heptano)Thierry RodriguesAinda não há avaliações
- Lista - DestilaçãoDocumento6 páginasLista - DestilaçãoRui GomesAinda não há avaliações
- Lista 2Documento4 páginasLista 2Barbara LuzAinda não há avaliações
- Destilação: Equilíbrio de FasesDocumento38 páginasDestilação: Equilíbrio de FasesMarceloNunesAinda não há avaliações
- Relatorio Eq. Liq-VapDocumento10 páginasRelatorio Eq. Liq-Vaprsteter2915100% (1)
- Relatório 8 - Diagrama de Fases Líquido-VaporDocumento10 páginasRelatório 8 - Diagrama de Fases Líquido-VaporRenato Alexandre Polins JuniorAinda não há avaliações
- Lista de Exerc Cio - Solu Es Com Componentes Vol TeisDocumento2 páginasLista de Exerc Cio - Solu Es Com Componentes Vol TeisEverton SilvaAinda não há avaliações
- Equilibrio DestilacaoDocumento63 páginasEquilibrio DestilacaoSabrina MaraAinda não há avaliações
- Hidrolise de EsterDocumento4 páginasHidrolise de EsterOscar AlhosAinda não há avaliações
- PVT - Real GasDocumento36 páginasPVT - Real GasEdvalda SebastiãoAinda não há avaliações
- Exercício Cinética QuímicaDocumento6 páginasExercício Cinética QuímicaLucas BentesAinda não há avaliações
- Lista 3Documento3 páginasLista 3Marcello SeveroAinda não há avaliações
- Elemento Químico Tálio e Seus Isótopos e Elemento Químico HipotéticoDocumento14 páginasElemento Químico Tálio e Seus Isótopos e Elemento Químico HipotéticoMARIALUIZAAinda não há avaliações
- REFRATOMETRIADocumento7 páginasREFRATOMETRIAWagner ZwickerAinda não há avaliações
- Atv DestilaçãoDocumento8 páginasAtv DestilaçãoThaísa SantosAinda não há avaliações
- Linhas de AmarraçãoDocumento9 páginasLinhas de AmarraçãoLetícia GarretoAinda não há avaliações
- 2015 FinalDocumento12 páginas2015 FinaliolaAinda não há avaliações
- AAS Por Eletroforese Capilar - CEDocumento7 páginasAAS Por Eletroforese Capilar - CEJessica ReimbergAinda não há avaliações
- Livro D QuímicaDocumento11 páginasLivro D QuímicaKaua Moraes vieiraAinda não há avaliações
- Termômetro À Gás A Volume ConstanteDocumento12 páginasTermômetro À Gás A Volume ConstanteDiego SilvaAinda não há avaliações
- Volumetria de PrecipitaçãoDocumento11 páginasVolumetria de PrecipitaçãoJosefa Virgínia da Silva SouzaAinda não há avaliações
- 1LISTA Modificada Unidade I 2023.1Documento4 páginas1LISTA Modificada Unidade I 2023.1JOAO GOMESAinda não há avaliações
- Lista 5 - Ponchon-SavaritDocumento7 páginasLista 5 - Ponchon-Savaritnandasduarte15Ainda não há avaliações
- Propriedades Dos Gases NaturaisDocumento9 páginasPropriedades Dos Gases NaturaisAlfredö HeidyAinda não há avaliações
- Relatório Volume Molar de Excesso Grupo 10Documento11 páginasRelatório Volume Molar de Excesso Grupo 10rsteter2915Ainda não há avaliações
- Lista 06 Equilibrio Liquido Vapor PDFDocumento3 páginasLista 06 Equilibrio Liquido Vapor PDFShirlei QueirozAinda não há avaliações
- Atividade Cinetica Quimica FQ2 JCSS 2023 1Documento2 páginasAtividade Cinetica Quimica FQ2 JCSS 2023 1Larissa RamosAinda não há avaliações
- Equa - Estado Labz02Documento10 páginasEqua - Estado Labz02Jacinto NhamposseAinda não há avaliações
- FINAL SUBSTITUTIVA FQM 1 RetomadaDocumento3 páginasFINAL SUBSTITUTIVA FQM 1 RetomadaMateus MendesAinda não há avaliações
- Apresentação Lab.1Documento23 páginasApresentação Lab.1Joel PintoAinda não há avaliações
- Experimento III - Destilação FracionadaDocumento11 páginasExperimento III - Destilação FracionadaMurilo MaioliAinda não há avaliações
- Relatório Final - DestilaçãoDocumento12 páginasRelatório Final - DestilaçãoTalles FelipeAinda não há avaliações
- Lista Soluções Termo2Documento28 páginasLista Soluções Termo2Laryssa Mendes100% (1)
- 1a Lista de Equilibrio e FlashDocumento4 páginas1a Lista de Equilibrio e FlashBianca XavierAinda não há avaliações
- 9 Lista FSQ1001Documento4 páginas9 Lista FSQ1001Rodrigo VieiraAinda não há avaliações
- Relatório Fisico Quimica ExperimentalDocumento13 páginasRelatório Fisico Quimica ExperimentalDiego DavidAinda não há avaliações
- Experimento I - Dilatação TérmicaDocumento19 páginasExperimento I - Dilatação TérmicaHaniele Santos RochaAinda não há avaliações
- Volume 01 - Capitulo 1Documento3 páginasVolume 01 - Capitulo 1fabianodeavizAinda não há avaliações
- Gabarito Val Químicafinal BaremaDocumento7 páginasGabarito Val Químicafinal BaremaFabrício BagliAinda não há avaliações
- Equilíbrio Líquido-Vapor de Uma Mistura BináriaDocumento12 páginasEquilíbrio Líquido-Vapor de Uma Mistura BináriaAna Luiza GorgulhoAinda não há avaliações
- Capítulo-Umidade Relativa Do ArDocumento16 páginasCapítulo-Umidade Relativa Do Arvanw wAinda não há avaliações
- Engenharia Química Operações Unitárias C Primeira Avaliação Teórica (10,0)Documento2 páginasEngenharia Química Operações Unitárias C Primeira Avaliação Teórica (10,0)Vinícius HigutiAinda não há avaliações
- Aquecimento de Tanque Soda Caustica 50% - 2 in Rev. A (ALF)Documento11 páginasAquecimento de Tanque Soda Caustica 50% - 2 in Rev. A (ALF)Eng Alf100% (1)
- Lista - de - Exerci - Cios - Espectrofotometria GabrielDocumento3 páginasLista - de - Exerci - Cios - Espectrofotometria GabrielTiago MB2112Ainda não há avaliações
- Resolução Da Prova de Quimica - ITA 2010 PDFDocumento20 páginasResolução Da Prova de Quimica - ITA 2010 PDFcaacerqueiraAinda não há avaliações
- Exercicios Resolvidos de Refrigeracao MultipressaoDocumento23 páginasExercicios Resolvidos de Refrigeracao MultipressaoJoão VictorAinda não há avaliações
- Prática - Tensão SuperficialDocumento6 páginasPrática - Tensão SuperficialgabrielAinda não há avaliações
- Cinetica Hidrolise EsterDocumento4 páginasCinetica Hidrolise EsterdutramarciaAinda não há avaliações
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Relatório Fluidização - LADEQ - Grupo 5Documento12 páginasRelatório Fluidização - LADEQ - Grupo 5maria beatrizAinda não há avaliações
- Gestão Ambiental Trabalho 4Documento3 páginasGestão Ambiental Trabalho 4maria beatrizAinda não há avaliações
- Questões PIDocumento10 páginasQuestões PImaria beatrizAinda não há avaliações
- Espectrofotometria Uv-Vis (All) Aula 3Documento38 páginasEspectrofotometria Uv-Vis (All) Aula 3maria beatrizAinda não há avaliações
- Iqa364 - Lista de Exerícios CromatografiaDocumento8 páginasIqa364 - Lista de Exerícios Cromatografiamaria beatrizAinda não há avaliações
- Fen.S.E RESUMO P2Documento32 páginasFen.S.E RESUMO P2maria beatrizAinda não há avaliações
- Lista de Exercícios - Espectrofotometria No UV-Vis IQA 364 - Análise Instrumental Prof : Ana Lúcia de LimaDocumento7 páginasLista de Exercícios - Espectrofotometria No UV-Vis IQA 364 - Análise Instrumental Prof : Ana Lúcia de Limamaria beatrizAinda não há avaliações
- EQE 364 - 2023 - 1 - 1 Lista de ExercíciosDocumento1 páginaEQE 364 - 2023 - 1 - 1 Lista de Exercíciosmaria beatrizAinda não há avaliações
- EQE 364 - 2023 - 1 - 1 Lista de ExercíciosDocumento1 páginaEQE 364 - 2023 - 1 - 1 Lista de Exercíciosmaria beatrizAinda não há avaliações
- Resumo Cinetica e Reatores Aplicacao Na Engenharia Quimica Martin SchmalDocumento2 páginasResumo Cinetica e Reatores Aplicacao Na Engenharia Quimica Martin Schmalmaria beatrizAinda não há avaliações
- Polímeros para Tintas 1Documento11 páginasPolímeros para Tintas 1maria beatriz100% (1)