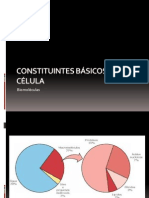
0% acharam este documento útil (0 voto)
17 visualizações67 páginasBiomoléculas
Enviado por
Joana alexandraDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato PDF, TXT ou leia on-line no Scribd
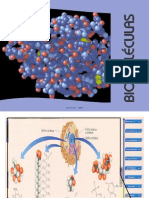
0% acharam este documento útil (0 voto)
17 visualizações67 páginasBiomoléculas
Enviado por
Joana alexandraDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato PDF, TXT ou leia on-line no Scribd