Escolar Documentos
Profissional Documentos
Cultura Documentos
2011 Física e Química A 2. Fase Resolução
Enviado por
mia filipaTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
2011 Física e Química A 2. Fase Resolução
Enviado por
mia filipaDireitos autorais:
Formatos disponíveis
Exame disponvel em http://www.gave.min-edu.pt.
Grupo I
1. cotao: 5
Grupo II
1.
; facilidade: 0,64
c.d.o. crescente
2. cotao: 10
frequncia decrescente
Ordenando a radiao por ordem crescente de comprimento de onda (e ordem decrescente de frequncia), temos:
radiao gama
radiao X
radiao ultravioleta
radiao visvel
radiao infravermelha
ondas de rdio FM e AM
1.2. cotao: 5
O ndice de refraco para um meio ptico dado
por
c
n=
v
onde c a velocidade da luz no vcuo e v a velocidade da luz nesse meio.
Portanto, quanto menor for o ndice de refraco n
maior a velocidade da luz v, uma vez que so duas
grandezas inversamente proporcionais. Ou seja, a
radiao vermelha (ndice de refraco 1,51, menor
que 1,53, ndice da radiao violeta) propaga-se com
maior velocidade no vidro do que a radiao violeta.
3. cotao: 5
; facilidade: 0,56
3,00 10 m/s
1
4,86 102 9 m
10
3,00 108 m/s
1
4,86 7 m
10
3,00 108
4,86 107
1
s
E
5,02 107 J
=
35%
100%
Donde:
E=
5,02 107 J
100%
35%
= 1,43 108J
Cada colector, por m2 e por dia, recebe 1,0 107 J.
Portanto, a rea de colectores que se pretende dada
por:
1,0 107 J
Donde:
1 m2
A=
1,43 108J
=
A
1,43 108J 1 m 2
1,0 107 J
= 14 m 2
5. cotao: 5
; facilidade: 0,38
(B)
A temperatura de um corpo negro depende apenas
da radiao emitida por esse corpo negro. De acordo
com a lei de Wien, o comprimento de onda da radiao de mxima intensidade emitida por um corpo
negro inversamente proporcional sua temperatura.
; facilidade: 0,69
quantidade de O2
quantidade de todas as espcies
0,047 mol
=
0,174 mol + 0,047 mol + 0,002 mol
0,047
=
0,174 + 0,047 + 0,002
2 mol
3,00 108
4,86 10
; facilidade: 0,59
Proporo estequiomtrica:
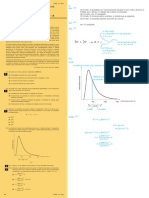
Espectro de emisso do hlio: inclui riscas de 587nm
e de 667 nm.
Espectro de absoro da estrela Rigel:
= 5,02 107 J
Como o rendimento de apenas 35%, necessrio
utilizar maior quantidade de energia da radiao, de
acordo com a proporo:
6,02 1023
Massa de butano: 23,26 g
Quantidade de matria de butano:
n
1 mol
=
58,14 g 23,26 g
1 mol
n=
23,26 g
58,14 g
= 0,4001 mol
4. cotao: 15
Energia mdia diria necessria para o aquecimento
da gua, sob a forma de calor:
Q = m c
J
= 300 kg 4,18 103
40 C
kg C
4. cotao: 5
5. cotao: 10
; facilidade: 0,50
xO
3,00 108 m/s
1
486 9 m
10
1.3. cotao: 10
1,18 103 103 J
fraco molar de O 2 =
(A)
A velocidade da luz no vidro menor do que a velocidade da luz no ar. Logo, o feixe aproxima-se da
normal superfcie de separao ar-vidro no ponto
de incidncia.
1,18 103 kJ
mol
(B)
; facilidade: 0,60
c= f
c
f =
1,18 103 kJ mol1 =
; facilidade: 0,58
(D)
Espectro de emisso: conjunto de radiaes emitidas
(em geral, riscas de cor num fundo negro).
Espectro de absoro: conjunto de radiaes absorvidas (em geral, riscas negras num fundo de cor).
; facilidade: 0,27
; facilidade: 0,59
(D)
1.1. cotao: 5
(B)
3. cotao: 5
Hz
7
13 mol
8 mol
10 mol
2 C4 H10 (g) + 13 O2 (g) 8 CO2 (g) + 10 H 2 O (g)
; facilidade: 0,29
667 nm
58,14 g
mol
23,36 g
0,4001 mol
Clculo da quantidade de matria de oxignio O2
necessrio para a combusto completa de 23,26 g
(0,4001mol) de butano:
2 mol de C4 H10 0,4001 mol
=
13 mol de O2
n de O2
0,4001 mol 13 mol
2 mol
= 2,601 mol
587 nm
No espectro de absoro, as riscas de um certo
elemento tm os mesmos comprimentos de onda do
espectro de emisso desse elemento.
Portanto, como no espectro de Rigel surgem riscas
negras que correspondem absoro de radiao dos
comprimentos de onda referidos para o espectro de
hlio, podemos concluir que provvel a presena de
hlio na atmosfera da estrela Rigel.
2. cotao: 5
; facilidade: 0,47
(C)
Para o tomo de H, a emisso de radiao na zona
do visvel ocorre nas transies de nveis n > 2 para
o nvel n = 2. Portanto, apenas as opes (B) e (C)
podem estar corretas.
Na emisso de radiao, o tomo perde energia: a
variao de energia associada transio negativa,
como indicado na opo (C).
n=
Clculo do volume correspondente a 2,601 mol de
O2 em condies PTN:
V
22,4 L
=
2,601 mol
mol
22,4 L
V=
2,601 mol
mol
= 58,3 L
6. cotao: 5
Grupo III
1. cotao: 5
; facilidade: 0,64
Ltio.
O raio atmico tende a diminuir ao longo de cada
perodo: o elemento com maior raio atmico dever
ser o primeiro de cada perodo. O oxignio est no
2. perodo e o ltio o primeiro elemento do 2.
perodo.
2. cotao: 5
; facilidade: 0,41
Esquema da molcula de O2:
O O
; facilidade: 0,48
(B)
Som harmnico: uma nica frequncia.
Se o som se propagar na gua a sua velocidade
maior do que no ar. O perodo e a frequncia do som
mantm-se (so caratersticos do som) mas como a
velocidade maior, o comprimento de onda menor.
Grupo IV
1.
1.1. cotao: 10
; facilidade: 0,45
Por leitura do grfico, obtm-se o valor de Kw:
Facilidade de cada item: cotao mdia, numa escala de 0 a 1.
Resoluo do Exame de Fsica e Qumica A (11. ano), 2011, 2. Fase
As concentraes dos ies hidrnio e hidrxido na
gua pura so iguais: [H O+] = [OH]
Clculo da concentrao do io hidrnio:
K w = H 3O+ OH
14
+
3,0 10 = H 3O OH
3,0 1014 = c c
3,0 1014 = c 2
c = 3,0 1014
mol
L
O pH correspondente a esta concentrao :
= 1,73 107
pH = log 1,73 107
= 6,76
= 6,8
1.2. cotao: 5
; facilidade: 0,34
(B)
O carcter neutro da gua independente da temperatura.
Do grfico, conclui-se que Kw aumenta com a temperatura: logo, a concentrao de H3O+ (e, claro, a de
OH) tambm aumenta com a temperatura. Quanto
maior for a concentrao de H3O+, menor o pH.
1.3. cotao: 10
; facilidade: 0,19
Do grfico, conclui-se que Kw aumenta com a temperatura.
Aumentando Kw, aumentam as concentraes de
H3O+ e OH. Isto , favorece-se a reao direta:
2 H 2 O (l) ! H 3O+ (aq) + OH (aq)
De acordo com a lei de Le Chtelier, o aumento de
temperatura favorece a reao que tende a diminuir a
temperatura, ou seja, a reao endotrmica.
Portanto, conclui-se que a reao de autoionizao da
gua endotrmica.
2. cotao: 5
; facilidade: 0,87
(C)
As molculas de gua tanto podem ceder como
receber ies H+.
3. cotao: 5
; facilidade: 0,62
(D)
Grupo VI
Grupo V
1. cotao: 10
; facilidade: 0,44
Valor mdio da velocidade (valor mais provvel):
0,846 + 0,853+ 0,842
v=
m/s
3
= 0,847 m/s
Desvio mximo, em mdulo, entre o valor mdio e
cada um dos valores medidos:
0,847 0,853 m/s = 0,006 m/s
Este desvio mximo pode ser considerado como a
incerteza absoluta da velocidade:
v = (0,847 0,006) m/s
2. cotao: 15
; facilidade: 0,40
O cronmetro mede intervalos de tempo. Com o
cronmetro podiam medir o tempo t que demora a
percorrer a distncia d, que podia ser medida com a
fita mtrica.
Assumindo acelerao constante de magnitude a ao
longo do plano, tem-se (o carrinho deixado cair,
sem velocidade inicial):
1
d = a t2
2
Conhecendo d e t podiam calcular a:
2d
a= 2
t
Uma vez obtido o valor de a, que constante, como a
distncia d percorrida no tempo t, podiam calcular
a velocidade v ao fim desse tempo t:
v=at
Ou, tendo em conta a expresso que permite calcular
a acelerao:
v=at
2d
= 2 t
t
2d
=
t
Concluindo: para calcular a velocidade no final da
rampa, multiplicavam a distncia d percorrida pelo
carrinho por 2 e dividiam por t, o tempo que demorou a descida da rampa.
3. cotao: 5
; facilidade: 0,55
(A)
Do grfico, obtm-se, por extrapolao:
1. cotao: 5
; facilidade: 0,58
(C)
A menor diviso no eixo do tempo vale 0,2 s. Podese estimar valores de meia diviso: 0,1 s.
Ao fim de 3,3 s, a velocidade atinge um valor mximo, apontando para o lado positivo do eixo.
Ao fim desse tempo, a velocidade diminui at se anular, quando j tinham passado 3,9 s, passando a partir
da a apontar para o lado negativo do eixo, durante
aproximadamente mais 0,2 s, de 3,9 s a 4,1 s.
De 4,1 s a 5,0 s, a velocidade aponta para o lado
negativo, mas cada vez mais prxima de zero.
Ao fim de 5,0 s, a velocidade anula-se e passa a
apontar para o lado positivo, aumentando e diminuindo at se anular novamente ao fim de 6,3 s.
H inverso do sentido do movimento quando a velocidade se anula e passa a apontar para o lado oposto
ao lado para que apontava, antes de se anular.
Dos intervalos referidos nas opes, tal sucede apenas no intervalo (C).
2. cotao: 10
; facilidade: 0,21
Entre 0,0 s e 1,4 s a acelerao praticamente constante e vale:
m/s
0,40 m/s
= 0,286
s
1,4 s
Sendo a acelerao constante e a velocidade inicial
nula, a distncia d percorrida ao fim do tempo t
dada por:
1
d = a t2
2
1
= 0,286 1,42
2
= 0,28 m
3. cotao: 5
; facilidade: 0,49
(B)
Ao fim de 3,4 s, a velocidade est a diminuir, apontando para o lado positivo do eixo Ox.
Como a velocidade est a diminuir, a acelerao
aponta para o lado oposto ao lado para onde aponta
a velocidade. Aponta, pois, para o lado negativo do
eixo.
Apenas a opo (B) est de acordo com a situao
descrita.
4. cotao: 10
Ec = 0,170 J
; facilidade: 0,20
Molcula de gua: um tomo central de O e duas
ligaes covalentes simples OH.
No tomo de O h dois pares de eletres no ligantes.
A teoria da ligao qumica relaciona a geometria
das molculas com as foras de atrao e de repulso
(eletres-ncleos; eletres-eletres; ncleos-ncleos). As foras que se estabelecem entre os pares
de eletres no ligantes e os dois pares de eletres ligantes (ligaes OH) e os trs ncleos fazem com
que o ngulo de ligao HOH seja inferior a 180,
assumindo a molcula uma geometria angular.
1
m v 2 = 0,170
2
Resolvendo em ordem a v, temos:
1
0,4570 v 2 = 0,170
2
4. cotao: 5
v=
2 0,170
m/s
0,4570
; facilidade: 0,40
(A)
A energia cintica diretamente proporcional
massa e ao quadrado da velocidade. Portanto,
medida que a massa tende para 0, a energia cintica
tende tambm para 0: o grfico da energia cintica
tem de passar pela origem. As opes (C) e (D) esto
erradas.
Colocando uma sobrecarga no carrinho, aumenta-se a
massa, logo aumenta-se a energia cintica. o que se
representa na opo (A).
Você também pode gostar
- (CEF) Resolucao Da Lista - FOTONICADocumento32 páginas(CEF) Resolucao Da Lista - FOTONICAFelipe Almeida WuAinda não há avaliações
- Cpen fq11 Prova Modelo 2020 ResolucaoDocumento9 páginasCpen fq11 Prova Modelo 2020 Resolucaosonia silvaAinda não há avaliações
- 4.1. F.Q. 11 Prova Modelo 2020 ResolucaoDocumento9 páginas4.1. F.Q. 11 Prova Modelo 2020 ResolucaoMaria João100% (1)
- Resulução Exame Nacional Fisica QuimicaDocumento8 páginasResulução Exame Nacional Fisica QuimicacidcidAinda não há avaliações
- Ti11 30 04 2010 SRDocumento4 páginasTi11 30 04 2010 SRLurdes LamasAinda não há avaliações
- 2013 Exame FQ A 11 Ano 2a Fase, ResolucaoDocumento2 páginas2013 Exame FQ A 11 Ano 2a Fase, ResolucaoAntónio CostaAinda não há avaliações
- KIT Phywe Velocidade Da LuzDocumento5 páginasKIT Phywe Velocidade Da LuzFabio MtbAinda não há avaliações
- Agrupamento de Escolas de Alcácer Do SalDocumento8 páginasAgrupamento de Escolas de Alcácer Do SalRuben FernandesAinda não há avaliações
- Res Ex Fqa715 F1 2022Documento7 páginasRes Ex Fqa715 F1 2022Mariana B.M.Ainda não há avaliações
- Espalhamento de ComptonDocumento13 páginasEspalhamento de ComptonLuciana CerdeiraAinda não há avaliações
- 2014 Exame FQA 11 Ano 2a Fase, Resolucao PDFDocumento2 páginas2014 Exame FQA 11 Ano 2a Fase, Resolucao PDFJoana R. SilvaAinda não há avaliações
- Exame Fqa11 2011 Ee SR PDFDocumento6 páginasExame Fqa11 2011 Ee SR PDFLuis BerenguerAinda não há avaliações
- Relatório Da Disciplina Transferência de Massa: DETERMINAÇÃO EXPERIMENTAL DO COEFICIENTE DE DIFUSÃO DO ÁLCOOL PROPÍLICO NO AR POR MEIO DO AJUSTE DA EQUAÇÃO DE STEFANDocumento11 páginasRelatório Da Disciplina Transferência de Massa: DETERMINAÇÃO EXPERIMENTAL DO COEFICIENTE DE DIFUSÃO DO ÁLCOOL PROPÍLICO NO AR POR MEIO DO AJUSTE DA EQUAÇÃO DE STEFANLaís Barbosa0% (1)
- Avaliação Proposta Ao 2 CicloDocumento6 páginasAvaliação Proposta Ao 2 CicloErnesto King LegeendsAinda não há avaliações
- Halliday Física 2 - Cap 16 SoluçõesDocumento31 páginasHalliday Física 2 - Cap 16 SoluçõesRoney PinhoratiAinda não há avaliações
- Ad1 Fis RespDocumento5 páginasAd1 Fis RespLohans MirandaAinda não há avaliações
- Exame Fqa 2008 1faseDocumento4 páginasExame Fqa 2008 1faseRita MariaAinda não há avaliações
- 2015 2 FaseDocumento13 páginas2015 2 FaseLara MouraAinda não há avaliações
- Atividade 2 - Ingrid Eduarda Alves PaivaDocumento5 páginasAtividade 2 - Ingrid Eduarda Alves PaivaINGRID EDUARDA ALVES PAIVAAinda não há avaliações
- Prova de Fisica UFPEDocumento5 páginasProva de Fisica UFPEmarcosfilho10100% (1)
- Exame F.Q. 2007 1 Fase - ResoluçãoDocumento6 páginasExame F.Q. 2007 1 Fase - ResoluçãoHugo FerreiraAinda não há avaliações
- Biprisma de FresnelDocumento7 páginasBiprisma de FresnelAlex SilvaAinda não há avaliações
- Covest 2011 2 FaseDocumento7 páginasCovest 2011 2 Faseadelmar2008Ainda não há avaliações
- 2012 Exame FQ A 11 Ano 2a Fase, ResolucaoDocumento2 páginas2012 Exame FQ A 11 Ano 2a Fase, ResolucaoAntónio CostaAinda não há avaliações
- Relatorio DispersaoDocumento5 páginasRelatorio DispersaoJosvy EllonAinda não há avaliações
- Ita PDFDocumento12 páginasIta PDFRoberto NeivaAinda não há avaliações
- Condutividade Do CobreDocumento9 páginasCondutividade Do CobreGuilherme Arantes RibeiroAinda não há avaliações
- Gabarito - simulado.4.2020.ENEM 2Documento5 páginasGabarito - simulado.4.2020.ENEM 2Ana BeatrizAinda não há avaliações
- Obf 1e2 Series 3fase 2011Documento25 páginasObf 1e2 Series 3fase 2011Sahhwe AsdaksjdlAinda não há avaliações
- Circuitos Com CapacitoresDocumento17 páginasCircuitos Com CapacitoresNath BarbosaAinda não há avaliações
- SOLUcões - Ficha GlobalDocumento3 páginasSOLUcões - Ficha GlobalCarolina Faria(8D)Ainda não há avaliações
- 4 - Calculo - Papel - Perfil - Atenuação - Exercícios No FinalDocumento4 páginas4 - Calculo - Papel - Perfil - Atenuação - Exercícios No FinalbarbosamanddaAinda não há avaliações
- 2014-07-07 - Simulado de FÃ Sica - Poliedro - Rumo Ao ITA PDFDocumento9 páginas2014-07-07 - Simulado de FÃ Sica - Poliedro - Rumo Ao ITA PDFAllison DavisAinda não há avaliações
- UFC 2000 0 1a FisicaDocumento6 páginasUFC 2000 0 1a FisicaAdeValdo GonçalvesAinda não há avaliações
- UECE 2005 2ºsemestre Prova Física QuímicaDocumento11 páginasUECE 2005 2ºsemestre Prova Física QuímicaFelipe FerreiraAinda não há avaliações
- Cap3 - Função ExponencialDocumento21 páginasCap3 - Função ExponencialcspmafiAinda não há avaliações
- CanaisDocumento10 páginasCanaisJosé GasparimAinda não há avaliações
- CTG - 2dia - Provas - Mat - FisDocumento9 páginasCTG - 2dia - Provas - Mat - FisMarcelo da SilvaAinda não há avaliações
- Relatório Experimental Física REFRAÇÃODocumento17 páginasRelatório Experimental Física REFRAÇÃOthiago_lml100% (3)
- cpq126 Banco de Questoes Eq1Documento10 páginascpq126 Banco de Questoes Eq1Pedro FloresAinda não há avaliações
- Prova Avaliativa 1º Bimestre 3º AnoDocumento3 páginasProva Avaliativa 1º Bimestre 3º AnoSirleia Aparecida Rezende SilvaAinda não há avaliações
- Grupo06 CiDocumento9 páginasGrupo06 CiJessica ReimbergAinda não há avaliações
- Questões Pré e Pós Relatório FQDocumento3 páginasQuestões Pré e Pós Relatório FQbeatriz silvaAinda não há avaliações
- Relatorio 4Documento7 páginasRelatorio 4Joyce GuimarãesAinda não há avaliações
- Relatório MCUDocumento13 páginasRelatório MCUCaio Kawamura GoncalvesAinda não há avaliações
- Op1 OutremDocumento8 páginasOp1 OutremVinicius VenturaAinda não há avaliações
- Acs2 FisicaDocumento4 páginasAcs2 FisicaGenito JohnAinda não há avaliações
- Resolucao IME Fisica 1989Documento4 páginasResolucao IME Fisica 1989luquithaAinda não há avaliações
- Exame Fqa 2021 EeDocumento10 páginasExame Fqa 2021 EeRita MariaAinda não há avaliações
- Física - Questoes Discursivas - Modulo de Revisao - GabaritoDocumento11 páginasFísica - Questoes Discursivas - Modulo de Revisao - Gabaritofernandapmferreira94Ainda não há avaliações
- Aula 3 - Introdução À Física QuânticaDocumento11 páginasAula 3 - Introdução À Física QuânticaCarlos LimaAinda não há avaliações
- 11F NL (Teste3) Fev.2021Documento4 páginas11F NL (Teste3) Fev.2021Sofia CarvalhoAinda não há avaliações
- Exame Fqa 2009 2faseDocumento6 páginasExame Fqa 2009 2faseRita MariaAinda não há avaliações
- Física Experimental Circuito RLCDocumento13 páginasFísica Experimental Circuito RLCRafael FerreiraAinda não há avaliações
- Aula 09Documento5 páginasAula 09pedromaccorsiAinda não há avaliações
- Pendulo SimplesDocumento9 páginasPendulo Simplesckastro2004Ainda não há avaliações
- Camões Lírico - Caract. Corrente Tradicional e Renascentista (Blog10 13-14)Documento2 páginasCamões Lírico - Caract. Corrente Tradicional e Renascentista (Blog10 13-14)TâniaRolo100% (1)
- FF Teste1A 1617Documento2 páginasFF Teste1A 1617mia filipaAinda não há avaliações
- Slide 1Documento19 páginasSlide 1marybettyAinda não há avaliações
- Os MaiasDocumento16 páginasOs Maiasmia filipa67% (3)
- Arranjos Ou CombinacoesDocumento1 páginaArranjos Ou Combinacoesmia filipaAinda não há avaliações
- FF Teste2 1617Documento2 páginasFF Teste2 1617mia filipaAinda não há avaliações
- 2010 Fisica Quimica v1Documento16 páginas2010 Fisica Quimica v1OdenilzasantosAinda não há avaliações
- 2011 Física e Química A 1. FaseDocumento16 páginas2011 Física e Química A 1. Fasemia filipaAinda não há avaliações
- Versão 1: Prova Escrita de Física e Química ADocumento15 páginasVersão 1: Prova Escrita de Física e Química AsofiaarosoAinda não há avaliações
- 715 2010 2 v2Documento16 páginas715 2010 2 v2Claudia ResendeAinda não há avaliações
- 2010 Física e Química A 2. Fase ResoluçãoDocumento7 páginas2010 Física e Química A 2. Fase Resoluçãomia filipaAinda não há avaliações
- 2007 Física e Química A 2. Fase ResoluçãoDocumento7 páginas2007 Física e Química A 2. Fase Resoluçãomia filipaAinda não há avaliações
- 2011 Física e Química A 1.a Fase ResoluçãoDocumento2 páginas2011 Física e Química A 1.a Fase Resoluçãomia filipaAinda não há avaliações
- 2010 Física e Química A 1. Fase ResoluçãoDocumento6 páginas2010 Física e Química A 1. Fase Resoluçãomia filipaAinda não há avaliações
- 2015 Física e Química A 1.a Fase ResoluçãoDocumento2 páginas2015 Física e Química A 1.a Fase Resoluçãomia filipaAinda não há avaliações
- HTTP WWW - Gave.min-Edu - PT Np3content NewsId 254&FileName Fis Quim715 P2 v2 09Documento16 páginasHTTP WWW - Gave.min-Edu - PT Np3content NewsId 254&FileName Fis Quim715 P2 v2 09Iana MocanuAinda não há avaliações
- 2009 Física e Química A 2. Fase ResoluçãoDocumento8 páginas2009 Física e Química A 2. Fase Resoluçãomia filipaAinda não há avaliações
- 2015 Física e Química A 2.a Fase ResoluçãoDocumento2 páginas2015 Física e Química A 2.a Fase Resoluçãomia filipaAinda não há avaliações
- 2015 Física e Química A Época EspecialDocumento15 páginas2015 Física e Química A Época Especialmia filipa0% (1)
- 1 Fase 2009Documento16 páginas1 Fase 2009silvia_lfrAinda não há avaliações
- 2015 Física e Química A 1. FaseDocumento16 páginas2015 Física e Química A 1. Fasemia filipaAinda não há avaliações
- 2014 Física e Química A Teste Intermédio 11 Ano 12.02.2014 ResoluçãoDocumento1 página2014 Física e Química A Teste Intermédio 11 Ano 12.02.2014 Resoluçãomia filipaAinda não há avaliações
- 2015 Física e Química A 2. Fase PDFDocumento16 páginas2015 Física e Química A 2. Fase PDFalmeida.agostinho8406Ainda não há avaliações
- 2009 Física e Química A 1. Fase ResoluçãoDocumento8 páginas2009 Física e Química A 1. Fase Resoluçãomia filipaAinda não há avaliações
- Exame FQA11 2007 2faseDocumento16 páginasExame FQA11 2007 2fasetitaaahhhAinda não há avaliações
- 2007 Física e Química A 1. Fase ResoluçãoDocumento10 páginas2007 Física e Química A 1. Fase Resoluçãomia filipaAinda não há avaliações
- 2006 Física e Química A 2. Fase ResoluçãoDocumento9 páginas2006 Física e Química A 2. Fase Resoluçãomia filipaAinda não há avaliações
- 2006 Física e Química A 1. Fase ResoluçãoDocumento10 páginas2006 Física e Química A 1. Fase Resoluçãomia filipaAinda não há avaliações
- Exame FQA11 2006 2faseDocumento16 páginasExame FQA11 2006 2faselurdes_lamasAinda não há avaliações
- Tuina Apostila Final 15-10-12Documento129 páginasTuina Apostila Final 15-10-12haczelAinda não há avaliações
- Análise de Viabilidade EconômicaDocumento17 páginasAnálise de Viabilidade Econômicael_ruso__83Ainda não há avaliações
- Alavanca CambioDocumento52 páginasAlavanca CambioPauloFeitoza100% (1)
- Teste Ciências Da NaturezaDocumento2 páginasTeste Ciências Da NaturezaMarisaAinda não há avaliações
- Pontos Positivos e Negativos Dos TemperamentosDocumento4 páginasPontos Positivos e Negativos Dos TemperamentosRosiane Portela de Paula Santos100% (1)
- Tabela de Preços A - Area - Externa Athermic 2023 PDFDocumento5 páginasTabela de Preços A - Area - Externa Athermic 2023 PDFDieniffer PortoAinda não há avaliações
- 1 Astrologia e PsicologiaDocumento33 páginas1 Astrologia e PsicologiaCristina GameiroAinda não há avaliações
- Caso Clínico SAEDocumento7 páginasCaso Clínico SAEValdir GomesAinda não há avaliações
- Simples Carregador de Bateria (CIR3302)Documento2 páginasSimples Carregador de Bateria (CIR3302)Darilho Batista IgnacioAinda não há avaliações
- Service Training 110 - 160-7E PTDocumento160 páginasService Training 110 - 160-7E PTCarlos Paranhos100% (2)
- 1 SEGURANÇA NO MANUSEIO DE PRODUTOS QUÍMICOS PDF PDFDocumento41 páginas1 SEGURANÇA NO MANUSEIO DE PRODUTOS QUÍMICOS PDF PDFsorayabergonziAinda não há avaliações
- Musculação Do Iniciante Ao Avançado PDFDocumento20 páginasMusculação Do Iniciante Ao Avançado PDFTiago FerreiraAinda não há avaliações
- Filosofos ContratualistasDocumento2 páginasFilosofos Contratualistasricardoprimo456Ainda não há avaliações
- CAMILO - PolemicasDocumento8 páginasCAMILO - Polemicasw0lf3nst3inAinda não há avaliações
- Faltas - Quadro ResumoDocumento4 páginasFaltas - Quadro ResumoAnonymous a39FXdueJoAinda não há avaliações
- Aspectos Do Fantastico e Tradução de Um Conto de Marcel AyméDocumento42 páginasAspectos Do Fantastico e Tradução de Um Conto de Marcel AyméThiago TimAinda não há avaliações
- Folheto Polo Hatch 2013 PDFDocumento2 páginasFolheto Polo Hatch 2013 PDFIvan MedinaAinda não há avaliações
- PPC Farmacia 2012 Final PDFDocumento300 páginasPPC Farmacia 2012 Final PDFcgtnetoAinda não há avaliações
- Rauski. Michelato. Música e Inclusão Social - o Trabalho Da Banda Marcial MaristaDocumento49 páginasRauski. Michelato. Música e Inclusão Social - o Trabalho Da Banda Marcial MaristaEgon Eduardo SAinda não há avaliações
- 10 - Deus e Universo - Pietro Ubaldi (Volume Revisado e Formatado em PDF para Ipad - Tablet - E-Reader)Documento254 páginas10 - Deus e Universo - Pietro Ubaldi (Volume Revisado e Formatado em PDF para Ipad - Tablet - E-Reader)Glen Peach100% (4)
- Fichas de Matematica 2º AnoDocumento15 páginasFichas de Matematica 2º AnoAlzira Mesquita0% (2)
- Manual Fechadura HDL C-90Documento1 páginaManual Fechadura HDL C-90Adriano Gomes100% (1)
- N.T. Revista Literaria em Traducao N 4 PDFDocumento266 páginasN.T. Revista Literaria em Traducao N 4 PDForg22559Ainda não há avaliações
- 2° Prova 7° Ano 4° BimestreDocumento2 páginas2° Prova 7° Ano 4° BimestreElielson Dos Santos FernandesAinda não há avaliações
- O Insólito Nos Contos de O Fio Das Missangas, de Mia CoutoDocumento87 páginasO Insólito Nos Contos de O Fio Das Missangas, de Mia CoutoTiago Souza Motocrossplays100% (1)
- Dimensionamento de Vigas de Concreto Armado À TorçãoDocumento16 páginasDimensionamento de Vigas de Concreto Armado À TorçãoCezar DantasAinda não há avaliações
- Caderno de Exercicios Excel 2007Documento12 páginasCaderno de Exercicios Excel 2007Paulo Jose de Lima100% (2)
- Dissertação Isadora de AlbuquerqueDocumento43 páginasDissertação Isadora de AlbuquerqueIvyAinda não há avaliações
- Modelo de AprDocumento6 páginasModelo de AprGilmar JuniorAinda não há avaliações
- Aula 4 - Método de Crout e CholeskyDocumento6 páginasAula 4 - Método de Crout e CholeskynarlochosvaldoAinda não há avaliações