Escolar Documentos
Profissional Documentos
Cultura Documentos
Lista de Exercios
Enviado por
Kamily SoaresDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Lista de Exercios
Enviado por
Kamily SoaresDireitos autorais:
Formatos disponíveis
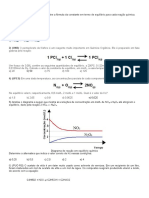
UFRRJ – IQ – DQA - IC 610 – Química Analítica II - LISTA DE EXERCÍCIO No.
EQUILÍBRIO EM MISTURAS ÁCIDO-BASE
(1) Utilizando a planilha EXCELL disponibilizada no quiosque, fazer o diagrama LogCxpH para
os sistemas ácido-base abaixo. Após, retirar de cada diagrama, na interseção de interesse, a
concentração de todas as espécies em equilíbrio e o pH das seguintes soluções. Checar se o
pH lido nos diagramas satisfazem a equação geral e exata de ácidos dentro de um erro relativo
de 10%.
(a) HAc 0,0053 mol/L, Ka= 1,75x10-5.
R: [HAc]=0,0053mol/L; [H3O+]=[Ac-]=2,96x10-4 mol/L; [-OH]=3,38x10-11mol/L; pH=3,53.
(b) HAc 0,40 mol/L.
R: [HAc]=0,40 mol/L; [H3O+]=[Ac-]=2,64x10-3 mol/L; [-OH]=3,79x10-12mol/L; pH=2,58.
(c ) HCN 0,1 mol/L, Ka= 4,8x10-10.
R: [HCN]=0,1 mol/L; [H3O+]=[CN-]=6,9x10-6mol/L; [-OH]=1,45x10-9mol/L; pH=5,16.
(d) HF 1,0x10-6 mol/L, Ka= 6,75x10-4.
R: [HF]=1,48x10-9 mol/L; [H3O+]=[F-]=1,0x10-6 mol/L; [-OH]=1,0x10-8mol/L; pH=6,0.
(e) HAc 1,0x10-6 mol/L.
R: [HAc]=5,2x10-8mol/L; [H3O+]=9,6x10-7mol/L; [Ac-]=9,5x10-7mol/L; [-OH]=1,04x10-8 mol/L; pH=6,02.
(f) NH30,01 mol/L, dado Kb=1,78x10-5
0,0
-1,0
-2,0
-3,0
-4,0
C -5,0
g
o
L -6,0
-7,0
-8,0
-9,0
-10,0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
(f) Resolução: pKb=4,75pKa=9,25
Linhas: Verde: H3O+; roxa: -OH; Vermelha: NH4+; Azul: NH3
- Resolução gráfica:
A equação do balanço de cargas (3) é que tem que ser satisfeita. (3) [H3O+]+[NH4+]=[-OH].
(Prof. Cristina Maria Barra) – Lista 04
UFRRJ – IQ – DQA - IC 610 – Química Analítica II - LISTA DE EXERCÍCIO No. 4
Pela análise de predominância, seguindo a linha de [-OH], pode-se ver que ela encontra a linha
de [NH4+] antes da linha de [H3O+]. Então, a interseção vermelho=roxa entre [NH4+] e [-OH ] é a
resposta gráfica. Nesse ponto traçar uma perpendicular. Onde essa perpendicular corta cada
linha, fazer a leitura.
pH=10,6
Log[-OH]=Log[NH4+]=-3,4 [NH4+]=[-OH]=4,0x10-4mol/L
Log[NH3]=-2,0 [NH3]=1,0x10-2 mol/L
Log[H3O+]<-10 [H3O+]<10-10mol/L
- Checando na equação geral:
C=(4,0x10-4)2/1,78x10-5+4,0x10-4+1,0x10-14/4,0x10-4+1,0x10-14/1,78x10-5
C=0,0090+4,0x10-4=0,0094mol/L (ER=6%)
- Resolução numérica:
(1) [NH4+][-OH]=1,78x10-5[NH3]
(2) [H3O+]+[-OH]=1,00x10-14
(3) [H3O+]+[NH4+]=[HO-]
(4) [NH4+]+[NH3]=1,0x10-2
- Primeira aproximação: Solução é básica, desprezar [H3O+] em (3):
(3a) [NH4+]=[-OH]
- Segunda aproximação, base pouco dissociada, desprezar [NH4+] em (4):
(4a) [NH3]=1,0x10-2 mol/L
Que substituindo em (1):
[NH4+]x[-OH]=1,78x10-5[NH3]
[-OH]x[-OH]=1,78x10-5x1,0x10-2=[-OH]2
[-OH]=4,2x10-4 mol/L
De (2): [H3O+]=2,4x10-11mol/L
De (3): [NH4+]=4,2x10-4mol/L
- Checando na equação geral:
C=(4,2x10-4)2/1,78x10-5+4,2x10-4+1,0x10-14/4,0x10-4+1,0x10-14/1,78x10-5
C=0,0099mol/L (ER=1%)
(2) Utilizando como base as características dos diagramas Log C x pH (Figura 13 – aula 06) em
concentração 0,01 mol L-1, faça uma análise do efeito da diluição nos cálculos de pH (resolução
numérica). Tomar como exemplo para a discussão, 0,001mol L-1, 0,0001mol L-1 e
0,0000001mol L-1.
Observação: Quando as soluções são diluídas, as relações entre as concentrações variam e
estas interpretações podem ser diferentes. Checar na equação geral, e quando o erro for maior
que 10%, equacionar o método matemático para resolver o problema.
(3) O diagrama abaixo foi construído para um diácido (H2A) cujos valores de pka1=1,25 e
pKa2=4,28.
(Prof. Cristina Maria Barra) – Lista 04
UFRRJ – IQ – DQA - IC 610 – Química Analítica II - LISTA DE EXERCÍCIO No. 4
0,0
-1,0
-2,0
-3,0
-4,0
-5,0
C
g
o -6,0
L
l
-7,0
-8,0
-9,0
-10,0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
(a) Assinalar no diagrama acima as espécies representadas em cada linha. Retirar a linha base
que representa a concentração analítica desse sistema ácido-base.
(b) Calcule todas o pH e as concentrações das espécies em equilíbrio numa solução aquosa do
sal Na2A na concentração expressa pelo diagrama.
(c) Calcular o pH de uma solução aquosa de H2A na concentração expressa pelo diagrama.
Checar na equação geral se o valor é aceitável dentro de erro relativo de 10%. Em função
do diagrama, que aproximações devem ser feitas no método matemático para resolver
numericamente este problema.
(d) Calcular o pH do hidrogenossal representado nesse diagrama. Checar o resultado utilizando
a equação geral para hidrogenossais.
(4) O diagrama abaixo foi construído para ácido fosfórico.
(a) Assinalar no diagrama as espécies ácido-base representadas em cada linha. Retirar do
diagrama a linha base que representa a concentração analítica do diagrama ácido-base.
(b) Retirar do diagrama todas as concentrações das espécies em uma solução aquosa do sal
Na3PO4 na concentração expressa pelo diagrama. Qual é o pH dessa solução? A [-OH]
satisfaz a equação geral para bases dentro de um erro relativo de 10%?
(c) Retirar do diagrama o pH de uma solução aquosa de H3PO4 na concentração expressa pelo
diagrama. A [H3O+] satisfaz a equação geral para ácidos dentro de um erro relativo de 10%?
(d) Retirar do diagrama o pH de uma solução aquosa de NaH2PO4 na concentração expressa
pelo diagrama. A [H3O+] satisfaz a equação geral para hidrogenossais dentro de um erro
relativo de 10%?
(e) Retirar do diagrama o pH de uma solução aquosa de Na2HPO4 na concentração expressa
pelo diagrama. A [H3O+] satisfaz a equação geral para hidrogenossais dentro de um erro
relativo de 10%?
Observação: Como base de estudo comparar os resultados obtidos com os da aula 05 (método
matemático).
(Prof. Cristina Maria Barra) – Lista 04
UFRRJ – IQ – DQA - IC 610 – Química Analítica II - LISTA DE EXERCÍCIO No. 4
0
-1
-2
-3
-4
-5
-6
-7
C
g -8
o -9
L
-10
-11
-12
-13
-14
-15
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
(5) O diagrama abaixo foi construído para o gás carbônico. Retirar do diagrama a concentração
analítica (linha de base) e os pKs. Indicar a linha de cada espécie desse diácido. Destacar
cada interseção de importância, indicando o que cada interseção representa.
(a) Retirar do diagrama o pH de uma solução aquosa de Na2CO3 na concentração expressa
pelo diagrama. A [-OH] satisfaz a equação geral para bases dentro de um erro relativo de
10%?
(b) Retirar do diagrama o pH de uma solução aquosa de NaHCO3 na concentração expressa
pelo diagrama. A [H3O+] satisfaz a equação geral para hidrogenossais dentro de um erro
relativo de 10%?
(Prof. Cristina Maria Barra) – Lista 04
UFRRJ – IQ – DQA - IC 610 – Química Analítica II - LISTA DE EXERCÍCIO No. 4
0,0
-1,0
-2,0
-3,0
-4,0
C -5,0
g
o
L -6,0
-7,0
-8,0
-9,0
-10,0
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
pH
(Prof. Cristina Maria Barra) – Lista 04
Você também pode gostar
- Modelo de Prova - P2Documento11 páginasModelo de Prova - P2Kamily SoaresAinda não há avaliações
- 02 - Lista de Exercicios - Acidos-Bases Fortes e Fracos - SaisDocumento6 páginas02 - Lista de Exercicios - Acidos-Bases Fortes e Fracos - SaisGustavo Silva De Paiva PereiraAinda não há avaliações
- Projetos Com Esp8266 Programado Em Lua - Parte XxiNo EverandProjetos Com Esp8266 Programado Em Lua - Parte XxiAinda não há avaliações
- 2 Lista de Exercícios - Laboratório de Química - 2023.1Documento4 páginas2 Lista de Exercícios - Laboratório de Química - 2023.1elainelopes78Ainda não há avaliações
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Lista1 Exercicios ADocumento4 páginasLista1 Exercicios ALucas TestaAinda não há avaliações
- Projetos Em Clp Ladder Baseado No Twidosuite Parte XiiNo EverandProjetos Em Clp Ladder Baseado No Twidosuite Parte XiiAinda não há avaliações
- Respostas 13 Ao 17 SkoogDocumento4 páginasRespostas 13 Ao 17 SkoogHauster M. CamposAinda não há avaliações
- Enviando A Medição De Ph Para Monitoramento No Vb Com A Stm8 Programada Em ArduinoNo EverandEnviando A Medição De Ph Para Monitoramento No Vb Com A Stm8 Programada Em ArduinoAinda não há avaliações
- Lista de Exercícios Equilíbrio de NeutralizaçãoDocumento5 páginasLista de Exercícios Equilíbrio de NeutralizaçãoLUÍS FELIPE SANTANA AGUIARAinda não há avaliações
- Enviando A Medição De Ph Para Monitoramento No Vc# Com A Stm8 Programada Em ArduinoNo EverandEnviando A Medição De Ph Para Monitoramento No Vc# Com A Stm8 Programada Em ArduinoAinda não há avaliações
- QUÍMICA ANALÍTICA QUALITATIVA LISTA DE EXERCÍCIOSDocumento2 páginasQUÍMICA ANALÍTICA QUALITATIVA LISTA DE EXERCÍCIOSMatheus TavaresAinda não há avaliações
- Monitorando A Concentração De Glp Com O Pic E Visual C#No EverandMonitorando A Concentração De Glp Com O Pic E Visual C#Ainda não há avaliações
- Lista de exercícios de química ácido-baseDocumento3 páginasLista de exercícios de química ácido-baseLuiza PolitanoAinda não há avaliações
- Monitorando A Concentração De Glp Com O Pic E Visual BasicNo EverandMonitorando A Concentração De Glp Com O Pic E Visual BasicAinda não há avaliações
- Solução Tampão de Química AnalíticaDocumento3 páginasSolução Tampão de Química AnalíticaNeiliane Souza100% (1)
- Projetos Com Esp32 Programado Em Arduino - Parte XxiNo EverandProjetos Com Esp32 Programado Em Arduino - Parte XxiAinda não há avaliações
- Lista 1 - água (3)Documento3 páginasLista 1 - água (3)tainaramachoca23Ainda não há avaliações
- pH e equilíbrio ácido-baseDocumento2 páginaspH e equilíbrio ácido-baseliAinda não há avaliações
- Lista Com GabaritoDocumento3 páginasLista Com GabaritoKety CostaAinda não há avaliações
- Química Analítica Qualitativa - ExercíciosDocumento3 páginasQuímica Analítica Qualitativa - ExercíciosAna Caroline FernandesAinda não há avaliações
- Respostas Dos Exercà Cios de Equilà Brio à Cido-Base 13 03 2023Documento3 páginasRespostas Dos Exercà Cios de Equilà Brio à Cido-Base 13 03 2023larinha40037Ainda não há avaliações
- Lista de exercícios ácido-baseDocumento3 páginasLista de exercícios ácido-baseMilena AlmeidaAinda não há avaliações
- Fundamentos da Teoria Moderna da Dissociação EletrolíticaDocumento11 páginasFundamentos da Teoria Moderna da Dissociação EletrolíticaLara ReisAinda não há avaliações
- Aula 5 - Acidos e BasesDocumento70 páginasAula 5 - Acidos e BasesarianesouzaAinda não há avaliações
- Lista de Exercícios de Química Analítica QualitativaDocumento3 páginasLista de Exercícios de Química Analítica QualitativaGabriela BuenoAinda não há avaliações
- Análise hidroquímica de amostras de água da Europa e Bacia de ResendeDocumento3 páginasAnálise hidroquímica de amostras de água da Europa e Bacia de ResendeFelipe TorresAinda não há avaliações
- Lista1 - Fisicoquimica FarmaciaDocumento23 páginasLista1 - Fisicoquimica FarmaciapatriciamartinsAinda não há avaliações
- Lista TVC3Documento4 páginasLista TVC3Abner Franco HermsdorfAinda não há avaliações
- Alcenos, Alcinos, Álcoois e ÉteresDocumento3 páginasAlcenos, Alcinos, Álcoois e ÉteresOrlando FirmezaAinda não há avaliações
- Determinação da concentração de ácido fosfórico em Coca-ColaDocumento12 páginasDeterminação da concentração de ácido fosfórico em Coca-ColaHellen MacêdoAinda não há avaliações
- Exercícios de tampões e equilíbrios ácido-baseDocumento9 páginasExercícios de tampões e equilíbrios ácido-baseAluana Santana CarlosAinda não há avaliações
- Exercícios Equilíbrio Ácido-BaseDocumento2 páginasExercícios Equilíbrio Ácido-BaseFabio WuAinda não há avaliações
- Bibliografia e soluções tampãoDocumento6 páginasBibliografia e soluções tampãoBruno Paccola Meirelles80% (5)
- Exercícios - Ácido-Base - QG - 2018Documento7 páginasExercícios - Ácido-Base - QG - 2018Melissa CoutoAinda não há avaliações
- Lista 3 IC608 Equilbrio Qumico e Clculo de PHDocumento4 páginasLista 3 IC608 Equilbrio Qumico e Clculo de PHCris PowerAinda não há avaliações
- Prova CorrigidaDocumento16 páginasProva CorrigidaPatrick BrandãoAinda não há avaliações
- Lista 2 de Exercicios Equilibrio Acido BaseDocumento3 páginasLista 2 de Exercicios Equilibrio Acido Baseisma_jr50% (2)
- 21 titulacoesABDocumento2 páginas21 titulacoesABCarolina RodriguesAinda não há avaliações
- Estudo_dirigido_de_QuimicaDocumento14 páginasEstudo_dirigido_de_Quimicahenrylopes2007Ainda não há avaliações
- IC 607 1a. Lista de Exercicios Prof Otavioic607Documento5 páginasIC 607 1a. Lista de Exercicios Prof Otavioic607Toni EltonAinda não há avaliações
- pH, pOH e equilíbrio aquosoDocumento12 páginaspH, pOH e equilíbrio aquosoJanaína RibeiroAinda não há avaliações
- Aula de Quarta1Documento27 páginasAula de Quarta1Sabrina sampaioAinda não há avaliações
- Funções Químicas, pH e soluçõesDocumento8 páginasFunções Químicas, pH e soluçõesmatheus mgaAinda não há avaliações
- Cenro Universitário de Sete LagoasDocumento13 páginasCenro Universitário de Sete LagoasElizangela GomesAinda não há avaliações
- Relações estequiométricas - Tarefa da aula 7 de Qui-2Documento3 páginasRelações estequiométricas - Tarefa da aula 7 de Qui-2Rayssa AguiarAinda não há avaliações
- Equilíbrio químicoDocumento4 páginasEquilíbrio químicoAriélly RolimAinda não há avaliações
- TquimicaDocumento13 páginasTquimicaklcsribeiro14Ainda não há avaliações
- Ficha Problemas 1Documento18 páginasFicha Problemas 1giglepurpleAinda não há avaliações
- Padronização de HClDocumento9 páginasPadronização de HClBrenoAinda não há avaliações
- Exercícios pH e Soluções TampãoDocumento3 páginasExercícios pH e Soluções TampãoKarine EstrelaAinda não há avaliações
- Qui2.qui3 2017-18Documento2 páginasQui2.qui3 2017-1877nandex2005Ainda não há avaliações
- Lista de Exercícios de Química Geral sobre Ácidos e BasesDocumento3 páginasLista de Exercícios de Química Geral sobre Ácidos e BasesvitorAinda não há avaliações
- Equilíbrio Ácido-Base: Exercícios Resolvidos de Química GeralDocumento3 páginasEquilíbrio Ácido-Base: Exercícios Resolvidos de Química GeralGabriella GamaAinda não há avaliações
- PL2 - Equilíbrios Ácido-Base e de Solubilidade 2Documento13 páginasPL2 - Equilíbrios Ácido-Base e de Solubilidade 2Ines Silva NevesAinda não há avaliações
- Al2 2Documento4 páginasAl2 2Lourenço MarquesAinda não há avaliações
- Seminario Diagrama Ternario 2Documento74 páginasSeminario Diagrama Ternario 2Roberta Lopes de PaulaAinda não há avaliações
- Lista de Fisica 2Documento4 páginasLista de Fisica 2Kamily SoaresAinda não há avaliações
- Extração de óleos essenciais por hidrodestilaçãoDocumento2 páginasExtração de óleos essenciais por hidrodestilaçãoKamily SoaresAinda não há avaliações
- Termodinamica e Gases Fisica BasicaDocumento2 páginasTermodinamica e Gases Fisica BasicaKamily SoaresAinda não há avaliações
- Destilação de água e etanolDocumento7 páginasDestilação de água e etanolKamily SoaresAinda não há avaliações
- Princípios da destilação: pontos de ebulição e tiposDocumento4 páginasPrincípios da destilação: pontos de ebulição e tiposKamily SoaresAinda não há avaliações
- Destilação de água e etanolDocumento7 páginasDestilação de água e etanolKamily SoaresAinda não há avaliações
- EstudoDocumento23 páginasEstudoMichelAinda não há avaliações
- Josephine PatersonDocumento11 páginasJosephine Patersonirislane-rodriguesAinda não há avaliações
- A Questao Espaco-Temporal em Bakhtin Cro PDFDocumento19 páginasA Questao Espaco-Temporal em Bakhtin Cro PDFRosivaldo GomesAinda não há avaliações
- ELPIS (Ensaio Sobre A Morte)Documento15 páginasELPIS (Ensaio Sobre A Morte)Marcelo LafontanaAinda não há avaliações
- Estratégias de Mobilização Na Minimização de Lesões Por Pressão em Pacientes No Âmbito HospitalarDocumento16 páginasEstratégias de Mobilização Na Minimização de Lesões Por Pressão em Pacientes No Âmbito HospitalarlidiaAinda não há avaliações
- Calculo de Vo2 em Repouso - Pesquisa GoogleDocumento1 páginaCalculo de Vo2 em Repouso - Pesquisa GoogleMichelle DantasAinda não há avaliações
- Desinfetante Pet FinoDocumento4 páginasDesinfetante Pet FinomislanyngAinda não há avaliações
- Manual Gerenciamento Residuos PGRSSDocumento189 páginasManual Gerenciamento Residuos PGRSSwww.cadilhac.com.br100% (2)
- Avaliação da cumbuca de ouroDocumento12 páginasAvaliação da cumbuca de ouroPriscilaAlmeida0% (1)
- Recursos Naturais ClassificaçãoDocumento4 páginasRecursos Naturais ClassificaçãoJuniorAinda não há avaliações
- Aula 04 - SonoDocumento36 páginasAula 04 - SonoAlissa CarolineAinda não há avaliações
- GUIA DE APRENDIZAGEM SOBRE TEATRO DE ANIMAÇÃODocumento3 páginasGUIA DE APRENDIZAGEM SOBRE TEATRO DE ANIMAÇÃOMARCELO OLIVEIRAAinda não há avaliações
- Enem Presencial 2022Documento47 páginasEnem Presencial 2022Junior SouzaAinda não há avaliações
- Filósofos gregos e modernos para Enem e vestibularesDocumento14 páginasFilósofos gregos e modernos para Enem e vestibularesBeatriz Ferreira AlvesAinda não há avaliações
- Questões PortuguesDocumento16 páginasQuestões PortuguescreativemediabelAinda não há avaliações
- Protocolo ICA avalia comportamentos autistasDocumento2 páginasProtocolo ICA avalia comportamentos autistasSusana AmaralAinda não há avaliações
- Classificação Protistas PadrõesDocumento28 páginasClassificação Protistas PadrõesRaphael AlvesAinda não há avaliações
- Representando e interpretando resultados experimentaisDocumento14 páginasRepresentando e interpretando resultados experimentaisGenesioAinda não há avaliações
- 20 Atividade de Matemática 8º Ano - Semana (22-08-22 À 26-08-22)Documento2 páginas20 Atividade de Matemática 8º Ano - Semana (22-08-22 À 26-08-22)José Benedito Dos SantosAinda não há avaliações
- MOFs para armazenamento de gasesDocumento2 páginasMOFs para armazenamento de gasesMarilia Gabriela FerreiraAinda não há avaliações
- A escrita da história escolar: memória e historiografiaDocumento20 páginasA escrita da história escolar: memória e historiografiaJohny AAinda não há avaliações
- Personalidade "Arquiteto" (INTJ) - 16personalitiesDocumento8 páginasPersonalidade "Arquiteto" (INTJ) - 16personalitiesLeonamAinda não há avaliações
- Portaria MJSP #367 - FuncionalDocumento15 páginasPortaria MJSP #367 - FuncionalLerimael AJURIDICAAinda não há avaliações
- MPS Planejamento e Controle da ProduçãoDocumento17 páginasMPS Planejamento e Controle da ProduçãoJeanAinda não há avaliações
- SAA ManualDocumento14 páginasSAA ManualThyago HenryqueAinda não há avaliações
- Lubrificação automática x manualDocumento18 páginasLubrificação automática x manualLincoln MartinsAinda não há avaliações
- Um Homem de Sorte - Michael J Fox+Documento144 páginasUm Homem de Sorte - Michael J Fox+Sandra Regina Jeronymo GaniniAinda não há avaliações
- 3.2 Método de Custeio Por Ordem de Produção IDocumento21 páginas3.2 Método de Custeio Por Ordem de Produção IsergioAinda não há avaliações
- Prata Breve HistóriaDocumento3 páginasPrata Breve HistóriaeveltoncAinda não há avaliações
- Hermenêutica - Caderno Segunda Unidade PDFDocumento23 páginasHermenêutica - Caderno Segunda Unidade PDFGeovane PedreiraAinda não há avaliações
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- Inteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNo EverandInteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNota: 5 de 5 estrelas5/5 (3)
- Biomecânica Básica dos Exercícios: Membros InferioresNo EverandBiomecânica Básica dos Exercícios: Membros InferioresNota: 3.5 de 5 estrelas3.5/5 (8)
- Instalações elétricas e o projeto de arquiteturaNo EverandInstalações elétricas e o projeto de arquiteturaAinda não há avaliações
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- Eletricista Residencial E PredialNo EverandEletricista Residencial E PredialNota: 3 de 5 estrelas3/5 (1)
- Exclusão e abraço: Uma reflexão teológica sobre identidade, alteridade e reconciliaçãoNo EverandExclusão e abraço: Uma reflexão teológica sobre identidade, alteridade e reconciliaçãoAinda não há avaliações
- Motores automotivos: evolução, manutenção e tendênciasNo EverandMotores automotivos: evolução, manutenção e tendênciasNota: 5 de 5 estrelas5/5 (1)
- O Que Todo Atirador Precisa Saber Sobre BalísticaNo EverandO Que Todo Atirador Precisa Saber Sobre BalísticaNota: 5 de 5 estrelas5/5 (1)
- Estratégias E Macetes Matemáticos Para ConcurseirosNo EverandEstratégias E Macetes Matemáticos Para ConcurseirosAinda não há avaliações
- Dimensionamento e Planejamento de Máquinas e Implementos AgrícolasNo EverandDimensionamento e Planejamento de Máquinas e Implementos AgrícolasNota: 1 de 5 estrelas1/5 (2)
- Educação ambiental: A formação do sujeito ecológicoNo EverandEducação ambiental: A formação do sujeito ecológicoAinda não há avaliações
- Uma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNo EverandUma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNota: 4 de 5 estrelas4/5 (13)