Escolar Documentos
Profissional Documentos
Cultura Documentos
Artigo 4 - Reginaldo Sales
Enviado por
Reginaldo SalesDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Artigo 4 - Reginaldo Sales
Enviado por
Reginaldo SalesDireitos autorais:
Formatos disponíveis
WWW.SCIELO.
BR/EQ
VOLUME 36, NÚMERO 1, 2011
DISTRIBUIÇÃO DE ELEMENTOS TÓXICOS NO ESTUÁRIO DO RIO AMAZONAS
Simone de Fátima Pinheiro PEREIRAa
Otílio Othon PIRESa
Augusto Fonseca SARAIVAb
Geiso Rafael OLIVEIRAa
Pedro Moreira de SOUSA JUNIORa
Rafaella Galvão MIRANDAa
Cleber Silva e SILVAa
Reginaldo da Silva SALES a
a
- Laboratório de Química Analítica e Ambiental (LAQUANAM) - Instituto de Ciências Exatas
e Naturais - Universidade Federal do Pará - Rua Augusto Correa, S/N - Guamá - Belém - PA -
Brasil, CEP 66075-900; Tel: 55-91-32018136; Fax: 55-91-32018136; Corresponding author:
simonefp@ufpa.br
b
- Laboratório Central - ELETRONORTE - Av. Tancredo Neves S/N - Terra Firme - Belém -
PA-Brasil
Resumo:
______________________________________________________________________________
A presença de elementos não essenciais nas águas superficiais do rio Amazonas é uma
preocupação global, o objetivo da pesquisa foi estudar a distribuição dos elementos As, Al, Mn,
e Pb na água do estuário do rio Amazonas. As amostras foram coletadas em três regiões
distintas: Canal Norte (AP), Canal Sul (PA) e rio Pará (PA) em três profundidades, com um total
de 84 amostras. A espectrometria de emissão atômica com plasma indutivamente acoplado
(ICPAES) foi utilizada para avaliar os teores de Al, Mn e Pb e a espectrofotometria de absorção
atômica com geração de hidretos (HGAAS) foi usada para a análise do As. O As variou de <0,35
Ecl. Quím., São Paulo, 36 ,2011 46
a 50,60 µg/L, o Al de <1,88 a 3347,70 µg/L, o Mn de 0,13 a 403,39 µg/L e Pb de <0,18 a 57,78
µg/L. Em média As (canal Sul), Al (todas as regiões), Mn (canal Norte e Sul) e Pb (canal Norte e
Sul) se encontraram em valores acima do permitido pela legislação brasileira. Os elementos
podem ter origem antrópica originária de atividade de mineração e industrial e origem natural
proveniente de decomposição de rochas ígneas da bacia de drenagem do rio Amazonas que
disponibilizam o elemento na forma ligada ao material particulado em suspensão.
Palavras-chave:Elementos tóxicos, foz do rio Amazonas, análise multivariada
Introdução
O rio Amazonas nasce a 5.300 metros de altitude na montanha Nevado Mismi, nos Andes
peruanos. Já é reconhecido como o maior rio do mundo, tanto em extensão com 6.885 km como
em volume d’água. A área de drenagem do rio Amazonas é de 6x106 km2 e sua descarga anual de
5,5x109 m3 ano-1, o equivalente a 1/5 de todos os rios do planeta que representa cerca de 20% do
fluxo mundial de água doce para o oceano [1].
A água é o principal veículo de transporte e distribuição de elementos químicos no
ambiente. Geralmente os metais são transportados associados à partícula de sedimento e solo, ou
de forma dissolvida nas águas dos rios, mares, estuários e na chuva [2]. Os elementos de baixo
potencial iônico tendem a permanecerem em solução, os de potencial iônico intermediário
geralmente apresentam pouca mobilidade geoquímica pela sua baixa solubilidade e forte
tendência a adsorver nas superfícies de partículas finas de sedimentos [3].
A introdução dos elementos químicos para o meio onde ocorre sua dispersão depende do
intemperismo químico, ou seja, da decomposição dos minerais das rochas, originadas por uma
série de reações de oxidação, redução, hidrólise e hidratação. Esses processos se devem
principalmente á ação das águas, ácido carbônico, ácidos fúlvicos, fúlmicos e chuva ácida [4].
Vários autores têm avaliado a presença dos elementos químicos na bacia do rio Amazonas
[5], [6]. Seyler & Boaventura [7] avaliaram a concentração e a variabilidade temporal de V, Cr,
Mn, Co, Cu, Zn, As, Rb, Sr, Mo, Cd, Sb, Cs, Ba, U no rio Amazonas e seus afluentes principais
(Negro, Madeira e Solimões) até a estação de Óbidos. Concluíram que As e Mn são elementos
transportados por fluxos de inundação sugerindo uma lixiviação destes elementos na época da
cheia de solos ricos em laterita que é uma formação que representa 80% do solo da bacia
amazônica rica em Fe e Al. Miranda et al. [8] avaliaram a presença de Ca, Mg, Al, Fe, Ba, Mn,
Ecl. Quím., São Paulo, 36 ,2011 47
Sr, Ti, Ag, Be, Cd, Co, Cr, Cu, Mo, Ni, Pb e Zn na água do rio Tapajós no encontro com o rio
Amazonas em frente a cidade de Santarém e encontraram os elementos Al e Fe em altas
concentrações.
O objetivo deste estudo foi efetuar a caracterização dos elementos As, Al, Mn e Pb no
estuário do rio Amazonas sua distribuição pelos canais Norte e Sul e rio Pará e estudar a
significância dos resultados usando a estatística multivariada.
Experimental
As amostras foram coletadas na foz do rio Amazonas (figura 1) em triplicata da camada
superficial (1 m), intermediária (5 m) e fundo (10 m) totalizando 84 amostras. As coletas foram
realizadas com o auxilio de um navio da Marinha do Brasil (NP Bocaina) e lanchas de apoio ao
longo do canal Norte (12 estações - N1 a N12), canal Sul (10 estações - S1 a S10) e rio Pará (6
estações - RP1 a RP6). Os locais de amostragem foram georeferenciados através de um GPS
(global positioning system), modelo Garmin, Etrex. Para o planejamento da amostragem foi
utilizada a tábua de maré fornecida pelo DHN e a carta náutica da área de estudo. A foz do
Amazonas se constitui no grande depositário dos elementos químicos de toda a bacia do
Amazonas daí sua importância como indicador do enriquecimento de metais na região.
Ecl. Quím., São Paulo, 36 ,2011 48
Ecl. Quím., São Paulo, 36 ,2011 49
Figura 1. Foz do rio Amazonas com pontos amostrais
Fonte: Adaptado [9]
As amostras coletadas foram preservadas sob refrigeração a 4o C e encaminhadas ao
laboratório para análise. Para a análise dos elementos solúveis as amostras foram filtradas em
filtro milipore 0,22 m que retêm pequenas partículas permitindo a análise somente dos
elementos solúveis, acidificadas com ácido nítrico até pH 2 e encaminhadas para as análises.
Um espectrofotômetro de absorção atômica (AAS), modelo SPECTRAA-55, com
acessório para geração de hidreto, modelo VGA-77, Varian Ind. & Com. Ltda foi usado na
análise do As e um espectrômetro de emissão atômica com plasma indutivamente acoplado
(ICPAES), modelo Vista-Pro, Varian Ind. & Com. Ltda foi usado na análise do Al, Mn e Pb.
A calibração dos instrumentos utilizados foi realizada através da confecção de curvas
analíticas visando à determinação do coeficiente angular (a) e linear (b), e coeficiente de
correlação (r) além do cálculo dos limites de detecção (LD) através da análise de 15 brancos (3S)
e cálculo do limite de quantificação (LQ). Todas as curvas se mostraram lineares com
coeficientes de correlação acima de 0,9945. Os resultados para o limite de detecção e limite de
quantificação mostraram que a técnica do ICPAES pode ser usada na determinação de elementos
traço em amostras de água, onde os mesmos se encontram em baixas concentrações. O estudo da
exatidão foi realizado com a análise do material padrão de referência de água de rio (SRM 1640
NIST), no geral os resultados estão dentro da faixa aceitável para a recuperação dos padrões. Al
apresentou excelente recuperação (96-101%), Mn apresentou perdas (86-89%) e As e Pb com
incrementos na concentração (109-110%).
Os resultados obtidos foram tratados utilizando-se estatística descritiva e multivariada
como ferramenta auxiliar e os programas Microsoft® Office Excel 2007 e Statistica® 7 no
cálculo dos resultados. Os gráficos foram executados nos mesmos programas.
Resultados e discussão
Os resultados médios para a distribuição de As, Al, Mn e Pb na foz do rio Amazonas são
apresentados na tabela 1, neste estudo o rio Amazonas foi classificado como rio de classe 2 de
acordo com a resolução 357/05 do CONAMA.
Ecl. Quím., São Paulo, 36 ,2011 50
Tabela 1. Distribuição de As, Al, Mn e Pb no Canal Norte, Canal Sul e Rio Pará (µg/L)
Estações As Al Mn Pb Estações As Al Mn Pb Estações As Al Mn Pb
RC357/05 10 100 100 10 RC357/05 10 100 100 10 RC357/05 10 100 100 10
N1 3,10 472,26 57,75 28,67 S1 50,60 525,91 250,46 <0,18 RP1 <0,35 106,74 41,81 13,44
N2 6,35 979,52 100,20 19,32 S2 8,33 175,82 253,37 <0,18 RP2 1,51 290,89 53,63 <0,18
N3 3,38 3225,4 403,39 51,96 S3 12,70 196,14 275,06 10,85 RP3 6,84 <1,88 <1,92 12,23
N4 5,71 663,89 81,18 <0,18 S4 4,68 250,42 276,71 11,62 RP4 7,03 <1,88 17,19 <0,18
N5 6,64 694,88 91,61 <0,18 S5 10,13 118,05 271,95 <0,18 RP5 4,77 <1,88 8,18 <0,18
<0,18 108,0
N6 S6 RP6 5,00 263,42 12,07
7,28 2295,50 184,05 41,72 4,70 60,54 238,04 5
N7 7,81 2317,60 151,33 12,41 S7 11,37 214,17 272,46 <0,18
N8 16,05 2302,90 167,83 14,59 S8 7,72 257,13 266,51 <0,18
N9 7,58 3347,70 258,19 42,19 S9 5,92 58,84 239,42 <0,18
N10 9,19 1686,80 129,98 9,80 S10 3,76 228,56 269,79 <0,18
N11 8,84 886,40 71,51 <0,18
N12 14,22 978,08 85,67 <0,18
Média 8,01 1654,24 148,56 18,39 Média 11,99 208,56 261,38 2,25 Média 4,19 110,18 38,14 6,29
SD 3,83 1018,45 98,72 18,64 SD 13,90 132,92 14,77 4,74 SD 2,86 136,07 39,83 6,91
Mínimo 3,10 472,26 57,75 <0,18 Mínimo 3,76 58,84 238,04 <0,18 Mínimo <0,35 <1,88 <1,92 <0,18
108,0
Máximo Máximo Máximo
16,05 3347,70 403,39 51,96 50,60 525,91 276,71 11,62 7,03 290,89 5 13,44
Resultados em negrito acima da RC: Resolução CONAMA, N: Canal Norte; S: Canal Sul; RP: Rio Pará; SD: Desvio padrão
O As apresentou na foz do rio Amazonas uma média de 8,61±8,98 µg/L variando de <0,35
a 50,60 µg/L. Constatou-se um enriquecimento do As de cerca de 4 vezes em relação ao
encontrado por Seyler & Boaventura [7], com alguns pontos (N8, N12, S1, S3, S5 e S7)
apresentando teores acima do que estabelece a resolução 357/05 do CONAMA (10 µg/L), no
Ecl. Quím., São Paulo, 36 ,2011 51
canal Sul este enriquecimento é em torno de 7 vezes. O enriquecimento se repete no canal Norte
e rio Pará em menor intensidade.
Os efeitos do As em excesso nos seres vivos envolvem danos em vários órgãos e sistemas
como o sistema cardiovascular (distúrbios vasculares seguido de gangrena e doença do pé
negro), sistema sangüíneo, sistema reprodutor (incremento de freqüência nos abortos
espontâneos), pele (tumores, hiperpigmentação, hiperqueratose), fígado (disfunção hepática),
sistema nervoso e sistema respiratório [10].
Förstner & Wittmann [11] encontraram teores de As variando de 2,0-3,0 µg/L em água de
rio. O As de origem natural na foz do rio Amazonas pode ser explicado pelo transporte de
materiais (dissolvidos, particulado), oriundos dos Andes, que atingem valores da ordem de 1,53
µg/L de As dissolvido registrado no rio Solimões a 2.500 km da foz do rio Amazonas, estes
valores vão diminuindo em direção a estação de Óbidos devido a diluição proveniente dos rios
que drenam do escudo cristalino, que apresentam teores da ordem de 0,1 µg/L ou menores [7] e
aumentam repentinamente na foz de acordo com os resultados obtidos neste estudo. A presença
de As de origem antrópica na foz do rio Amazonas são explicados nos estudos de Seyler &
Boaventura [7] que realizaram estimativas sobre emissões atmosféricas de As oriundas de
atividades antrópicas (notadamente desmatamentos e queimadas), que chegam à cerca de 250
toneladas de As anualmente. Outra possibilidade da origem antrópica do elemento na foz do
Amazonas diz respeito a lixiviação de rejeitos ricos em As provenientes de uma usina de
pelotização da mineradora ICOMI que atuava na cidade de Santana localizada as margens do rio
Amazonas próxima a cidade de Macapá capital do estado do Amapá.
Segundo o box-plot da distribuição do As (figura 2) a maior variabilidade dos resultados
foi observada no canal Sul que também apresentou os maiores resultados para o elemento. As
condições de corrente e outros aspectos hidrológicos podem estar contribuindo para o
enriquecimento do As neste local. Foram identificados dois resultado anômalos no canal Norte e
um resultado extremo no canal Sul, entretanto, através do testes de hipóteses (teste de Dixon) foi
observado que somente o resultado de As para a amostra S1 (Canal Sul) foi considerada fora da
normalidade de resultados.
Ecl. Quím., São Paulo, 36 ,2011 52
Figura 2. Box-plot da distribuição do As na foz do rio Amazonas
Nos estudos da correlação (Pearson) o As não apresentou correlações significativas com os
outros elementos no canal Norte, apenas uma regular correlação negativa (r= -0,428; ρ= 0,1652;
y= 35,0659 - 2,0814x) sem significância foi encontrada entre o As e Pb e no rio Pará a correlação
negativa foi entre o As e Al (r= -0,522; ρ= 0,2882; y = 214,3588 - 24,855x) também com pouca
significância. A ausência de fortes correlações do As em relação aos outros elementos,
principalmente Al e Mn no canal Norte e rio Pará mostra que nestes locais o elemento pode ter
origem antrópica, já que o Al e Mn fazem parte da geoquímica local. No canal Sul foi encontrada
uma excelente correlação positiva (r= 0,833; ρ=0,0028; y= 113,0736 + 7,963x) com um grau de
confiança de 95% ou 0,05 entre o As e o Al indicando uma provável origem natural do As
associada a intensa exploração da bauxita na região. Como as principais fontes de As natural são
a arsenopirita e a pirita enriquecida em As, a exploração de depósitos contendo quantidades
Ecl. Quím., São Paulo, 36 ,2011 53
significativas destes minerais constitui também uma importante fonte natural de liberação de
compostos de As para o ambiente [10].
Elevadas concentrações de Al com média de 807,06±995,73 µg/L, foram observadas para
toda a região estuarina do rio Amazonas (variação de <1,88 a 3347,70 µg/L), acima do que
preconiza a resolução 357-05 do CONAMA (100 g/L) [12], estes altos valores podem estar
associados a presença de argilominerais, principalmente a caulinita, tido como o principal
contribuinte de Al na região amazônica. O Al ocorre no ambiente sob a forma de silicatos,
óxidos e hidróxidos, combinado com outros elementos tais como sódio e flúor e complexado
com a matéria orgânica. O Al é um constituinte maior e não reativo dos argilominerais, que por
sua vez constituem a maior parte do material em suspensão e sedimentos [13]. O Al, embora seja
o terceiro elemento mais abundante da crosta terrestre, possui reduzida função biológica. Esse
elemento pode interferir no metabolismo de diversas formas de vida. No fitoplâncton, é capaz de
inibir a absorção e os processos fisiológicos do fósforo; enquanto que, nos peixes, o excesso de
Al torna-se uma potencial causa de problemas respiratórios. Existe forte possibilidade de que
uma dieta contendo Al causa neurotoxicidade, principalmente a doença de Alzheimer [14].
De acordo com Baird [15] águas naturais apresentam concentração de Al na ordem de
26,98 µg/L valor em torno de 60 vezes menor que a média encontrada no canal Norte. Altas
concentrações de Al também foram encontrados por Miranda et al. [8] que avaliaram o rio
Tapajós na sua foz onde ocorre o encontro deste rio com o rio Amazonas, com teores médios de
280,01±294,69 µg/L (variação de 47,55 a 788,14 µg/L). O Al ocorre no ambiente sob a forma de
silicatos, óxidos e hidróxidos, combinado com outros elementos tais como sódio e flúor e
complexado com a matéria orgânica. O Al é um constituinte maior e não reativo dos
argilominerais, que por sua vez constituem a maior parte do material em suspensão e sedimentos.
No ambiente estuarino o Al em solução é estabilizado em complexos orgânicos, podendo
precipitar na forma de óxidos hidratados, e com o aumento do pH pode reagir com o silício e
formar aluminossilicatos hidratados [13].
Pelo estudo do box plot (figura 3) percebe-se um incremento maior e uma maior
variabilidade da concentração de Al no canal Norte, tendo sido verificado um resultado anômalo
para o elemento no canal Sul, entretanto este valor não pode ser descartado de acordo com o teste
Q. O Al se correlacionou positivamente com o Mn (r=0,891; ρ=0,0001; y= 5,6682 + 0,0864x) e
Pb (r=0,723; ρ=0,0079; y= -3,4943 + 0,0132x) no canal Norte, mesmo comportamento foi
Ecl. Quím., São Paulo, 36 ,2011 54
observado para a correlação do Al com o Mn no rio Pará (r= 0,860; ρ= 0,0279; y= 10,3987 +
0,2518x).
Figura 3. Box-plot da distribuição do Al na foz do rio Amazonas
O Mn está presente em águas naturais tanto na forma dissolvida ou em suspensão, que
podem conter entre 1 e 500 µg/L de Mn total, podendo ser maior em áreas onde o Mn ocorre
naturalmente [16]. O Mn variou de <1,92 a 403,39 g/L, com média de 165,19±107,11 g/L, na
foz do rio Amazonas, teores acima da resolução 357/05 (100 g/L). O Mn foi encontrado em
baixas concentrações por Miranda et al. [8] na foz do rio Tapajós, afluente do rio Amazonas,
com teores médios de 12,02±6,93 µg/L (variação de 2,20 a 22,95 µg/L). O Mn natural dissolvido
é proveniente do intemperismo de seus compostos em rochas ígneas, sob forma de Mn2+, sendo
precipitado com o aumento do pH [16]. O enriquecimento do Mn na foz do rio Amazonas pode
ser devido à intensa exploração mineral de Mn ocorrida na área de Serra do Navio no Amapá por
50 anos e pela deposição de rejeitos ricos em Mn e em outros elementos oriundos de indústria de
pelotização de minério na cidade de Santana.
Ecl. Quím., São Paulo, 36 ,2011 55
Segundo Salomons & Forstner [17], este elemento pode ser liberado dos sedimentos
recentemente depositados através de processos de difusão, bioturbação e erosão para ser
novamente mobilizado. O Mn é amplamente distribuído na natureza, mas não ocorre como metal
livre. Os compostos mais abundantes são os óxidos, sulfetos, carbonatos e os silicatos. A
precipitação pode ocorrer sempre que o pH aumentar, desde que carbonatos ou silicatos
presentes estejam em altas concentrações.
De acordo com o box-plot (figura 4) os teores de Mn no canal Norte apresentam maior
variabilidade, os maiores valores foram observados no canal Sul com um valor anômalo no canal
Norte que não foram descartados pelo teste Q. O Mn se correlacionou positivamente com o Pb
no canal Norte (r= 0,788; ρ= 0,0023; y= -3,7053 + 0,1487x) e canal Sul (r= 0,518; ρ= 0,1249; y
= -41,2202 + 0,1663x) com baixa significância.
Figura 4. Box-plot da distribuição do Mn na foz do rio Amazonas
O Pb se apresentou em altas concentrações com média de 10,03±14,64 µg/L e variação de
<0,18 a 51,96 µg/L, estes valores estão em não conformidade com a resolução 357/05 do
Ecl. Quím., São Paulo, 36 ,2011 56
CONAMA, indicando um enriquecimento, que pode ser de origem natural ou antrópica. Pereira
et al. [18] avaliaram os níveis de Pb e outros elementos no rio Murucupi, e encontraram uma
média de 2,8±5,4 µg/L (variação de <9,7 a 15,0 µg/L) para o Pb, nível médio em torno de 4
vezes abaixo do encontrado neste estudo. O rio Murucupi é afluente do rio Pará e está localizado
em área impactada pela indústria de Al.
A intoxicação por Pb no homem causa danos ao sistema sangüíneo (destruição de glóbulos
vermelhos), nervoso (cérebro, espinha dorsal, nervos sensores e motores), renal, cardiovascular
[19]. O Pb que entra no organismo é inicialmente encontrado no sangue, eventualmente o Pb se
deposita nos ossos, onde ele substitui o cálcio devido os íons Pb2+ e Ca2+ serem de tamanhos
similares. O Pb permanece no corpo humano por vários anos acumulando-se no organismo [15].
Livingstone [20] estimou que a média global do teor de Pb em lagos e rios é de 1-10 g/L.
Embora essa estimativa inclua a contribuição antrópica, ela provavelmente ainda representa uma
aproximação justa de condições naturais, pois a água que flui através dos ecossistemas tem uma
considerável capacidade de auto-recuperação. Grandes descargas também podem ocorrer
diretamente em águas naturais, mas, nesses casos, o Pb tende a se localizar perto de pontos de
descarga, devido à baixa solubilidade dos compostos que são formados em contato com o solo e
a água [21]. Fontes de descargas de Pb na foz do rio Amazonas podem ter origem na exploração
mineral e atividade industrial na área considerada. O maior teor de Pb foi encontrado na estação
S1 (Canal Sul próximo a cidade de Santana (AP) e Afuá (PA)) local que apresentou também o
maior teor de As. A presença de Pb e As em elevadas concentrações neste local necessita ser
melhor avaliada em relação as prováveis fontes antrópicas de contribuição.
De acordo com o box-plot (figura 5) os maiores valores de Pb foram encontrados no Canal
Norte, local com maior variabilidade de resultados, foi encontrado um resultado extremos para o
Pb no canal Sul.
Ecl. Quím., São Paulo, 36 ,2011 57
Figura 5. Box-plot da distribuição do Pb na foz do rio Amazonas
A maior contribuição dos elementos As, Al, Mn e Pb na foz do rio Amazonas dá-se apenas
pelas três primeiras componentes principais, com seus respectivos valores de variância:
componente 1 (Al =45,62 %), componente 2 (Mn= 38,23 %) e a componente 3 (Pb= 12,32 %),
totalizando uma variância acumulada de 96,17 %. Com base nessas informações é possível
afirmar que dentre as variáveis As, Al, Mn e Pb as que detêm a maior parte da informação (96,17
%) sobre o conjunto de dados são: Al, Mn e Pb. O As se manteve isolado na análise de
componentes principais (PCA) que comprova a provável origem antrópica do elemento.
Foi observado por meio do valor da significância (ANOVA) que as médias dos resultados
das variáveis Al (ρ=3,08E-05), Mn (ρ=5,23E-06) e Pb (ρ=0,022) diferem significativamente e
são as que apresentam informações para explicar as características da área estudada, com um
grau de confiança de 95% ou 0,05. As médias para o As não diferiram significativamente com F
calculado < F crítico e significância de 0,239.
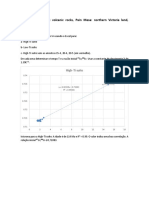
No gráfico dos scores (figura 6) foi observada a formação de agrupamentos influenciados
pelas variáveis selecionadas. O primeiro agrupamento é formado pelas amostras correspondentes
ao canal sul (S) que são influenciadas pela concentração de Mn. O segundo agrupamento
Ecl. Quím., São Paulo, 36 ,2011 58
influenciado pelo Al e o Pb e constituído pelas amostras do canal norte (N) e do rio Pará (RP)
devido à característica de alguns metais que se encontram associados à fração dissolvida da água
de apresentarem uma tendência pela forma iônica. Este fato foi evidenciado em trabalhos
realizados por Cavalcante [22] na região sob influência da descarga do rio Amazonas.
Figura 6. Gráfico dos scores destacando os agrupamentos de amostras.
O método de análise por agrupamento hierárquico (HCA) foi usado com o objetivo de
verificar as semelhanças entre as amostras com base nos teores de elementos determinados para
as diversas amostras na foz do rio Amazonas, através do cálculo de similaridade (calculada
utilizando a distância euclidiana entre as amostras). O resultado de acordo com o dendrograma
(figura 7) mostra a formação de três grupos, tomando-se como base uma distância euclidiana
inferior a 500 unidades.
Ecl. Quím., São Paulo, 36 ,2011 59
Figura 7. Dendrograma da distribuição de As, Al, Mn e Pb nos canais Norte e Sul e rio Pará
As principais similaridades observadas confirmam os resultados obtidos na análise de
componentes principais, no que diz respeito à composição dos agrupamentos onde é observado
um cluster que identifica uma grande similaridade entre os grupos das amostras correspondentes
ao rio Pará (RP) e as amostras que formam o Canal Norte (N) e os grupos das amostras do Canal
Sul (S) separado dos demais indicando que esta área possui características únicas que contribuem
para o enriquecimento anômalo dos elementos principalmente As e Pb.
Conclusões
No presente estudo procurou-se mostrar a distribuição dos elementos As, Al, Mn e Pb no
estuário do rio Amazonas e constatou-se a presença de elementos tóxicos, principalmente As e
Pb, com provável origem antrópica, os resultados deste estudo servem de alerta aos órgãos de
controle ambiental, para um controle maior dos lançamentos de efluentes nos recursos hídricos
locais. Os elementos se distribuíram pelas três áreas estudadas sendo mais evidente o
enriquecimento dos elementos nos Canais Norte (Al, Mn) e Sul (As, Pb), o rio Pará sofre um
enriquecimento próximo à área industrial de Barcarena-PA, local de industrialização de Al e
outros produtos. Os teores médios para Al, Mn e Pb estiveram em não conformidade com a
Ecl. Quím., São Paulo, 36 ,2011 60
resolução 357/05 do CONAMA, assumindo um caráter anômalo. O As apresentou elevadas
concentrações principalmente no Canal Sul, próximo a cidade de Afuá na ilha do Marajó-PA.
Similaridades foram encontradas entre os grupos de amostras oriundas do Canal Norte e Rio Pará
comprovando a influência do Rio Amazonas na formação do Rio Pará. O Canal Sul ficou isolado
dos demais indicando a influência do Oceano Atlântico e de outros fatores hidrodinâmicos e
geoquímicos característicos da área da Ilha do Marajó no enriquecimento dos elementos tóxicos.
Agradecimentos
Agradecemos o apoio da Eletronorte, CNPq, CAPES, FINEP e ao Programa de Pós-Graduação
em Química da UFPA.
PEREIRA, S.F.P.; PIRES, O.O.; SARAIVA, A.F.; OLIVEIRA, G.R.; SOUSA JUNIOR, P.M.;
MIRANDA, R.G.; SILVA, C.S.; REGINALDO, S.S.
TOXIC ELEMENTS DISTRIBUTION IN THE AMAZON RIVER ESTUARY
Abstract: The non-essential elements found in the superficial waters of the Amazon River is a
global worry since the local hydric resources represent the world’s largest fresh water reservoir.
This research aimed at studying the occurrence of As, Al, Mn and Pb in the waters of the
Amazon River estuary. The 84 samples in three depths were collected in three different regions:
North Channel of the Amazon River, in the state of Amapá; South Channel of the Amazon River,
in the state of Pará; and Pará River, also in the state of Pará. Inductively coupled plasma atomic
emission spectrometry (ICPAES) method was employed to determine the concentrations of Al,
Mn and Pb in the samples while hydride generation atomic absorption spectrometry (HGAAS)
method was employed in determining their As concentrations. As concentrations varied from
<0.35 to 50.60 µg/L; Al concentrations varied from <1.88 to 3347.70 µg/L; Mn concentrations
varied from <1.92 to 403.39 µg/L; and Pb concentrations varied from <0.18 to 51.96 µg/L. On
average, the concentrations of As (samples from the South Channel), of Al (samples from the
three regions), of Mn (samples from the North Channel and from the South Channel), and of Pb
(samples from the North Channel) were higher than allowed by the Brazilian legislation. The
origin of the elements can be anthropogenic due to mining and industrial activities as well as
natural due to decomposition of igneous rocks from the drainage basin of the Amazon River
which releases the element linked to the suspended particulate matter. High concentrations of
toxic elements, especially of As and Pb, put the health of the populations who consume water of
the Amazon River and the Pará River at risk.
Ecl. Quím., São Paulo, 36 ,2011 61
Keywords: Toxic elements, Amazon River mouth, multivariate study
Referências
[1] M. Molinier, J.L. Guyot, J. Callède, V. Guimarães, E. Oliveira, N. Filizola, Hydrologie du
bassin amazonien, Environnement et développement en Amazonie brésilienne, Théry H. (ed.),
Publ. Belin, Paris, 1997, 24.
[2] R. Cidu, R. Biddau, Applied Geochemistry. 22(12) (2007) 2777.
[3] J.C. Fernandez-Caliani, C. Barba-Brioso, J.D. de la Rosa, Geoderma. 149(3-4) (2009) 393.
[4] M.L.W. Tuttle, G.N. Breit, M.B. Goldhaber, Applied Geochemistry. 24(8) (2009) 1565.
[5] J. Viers, G. Barroux, M. Pinelli, P. Seyler, P. Oliva, B. Dupre, G.R. Boaventura, Science of
the Total Environment. 339(1-3) (2005) 219.
[6] A.-M. Aucour, F.-X. Tao, P. Moreira-Turcq, P. Seyler, S. Sheppard, M. F. Benedetti,
Chemical Geology. 197(1-4) (2003) 271.
[7] P.T. Seyler, G.R. Boaventura, Trace elements in the mainstream Amazon River. In: M.E.
McClain, F.R.L.Victoria, J.E. Richey, (Eds.) The Biogeochemistry of the Amazon Basin. Oxford
Press, (2001) 307.
[8] R.G. Miranda, S.F.P. Pereira, G.R. Oliveira, D.T.V. Alves, Revista Ambiente & Água. 4
(2009) 75.
[9] Photo of Amazon River's Mouth, Brazil, September. Acesso em 10/12/09, Disponível em:
http://www.zonu.com/brazil_maps (2000).
[10] WHO - World Health Organization, Arsenic and Arsenic Compounds. Environmental
Health Criteria. Geneva, (2001) 224.
[11] U. Förstner, G.T.W. Wittmamn, Metal Pollution in the Aquatic. Environment. Berlin,
Springer-Verlag. (1983) 486.
[12] CONAMA. Conselho Nacional do Meio Ambiente, Resolução nº 357/05. Acesso em
07/08/09, Disponível em: http://www.mma.gov.br/port/conama/res/res05/ res35705.pdf, (2005).
[13] E.R. Sholkovitiz, N.B. Price, The major element of suspended matter in Amazon estuary.
Geochimica Cosmochimica Acta. 44(2) (1980) 163.
[14] World Health Organization, Aluminium. Environmental Health Criteria, Geneva, (1997)
194.
[15] C. Baird, Environmental Chemistry. 2ª. ed., W. H. Freeman and Company, New York,
(1999) 557.
Ecl. Quím., São Paulo, 36 ,2011 62
[16] World Health Organization, Manganese. Environmental Health Criteria, Geneva, (1981) 17.
[17] W. Salomons, U. Förstner, Metals in Hidrocycle. Berlin, Springer-Verlag, (1984) 349.
[18] S.F.P. Pereira, M.A. Lima, K.H. Freitas, C.S. Mescouto, A.F. Saraiva, Revista Ambiente &
Água. 2(3) (2007) 62.
[19] L. W. Newland, K. A. Daum, Lead. In: Hutzinger, O. The Handbook of Environmental
Geochemistry. 3, part B. Anthropogenic Compounds. Berlin, Springer-Verlag: (1982) 1.
[20] D.A. Livingstone, Data of geochemistry. Sixth Edition. Chapter of chemical composition of
rivers and lakes. US Geol. Survey Prof. Paper (1963) 440.
[21] World Health Organization, Lead. Environmental Health Criteria, Geneva, (1977) 3.
[22] P.R.S. Cavalcante, Partição de metais de transição na foz do rio Amazonas. Universidade
Federal Fluminense. Rio de Janeiro. Dissertação de Mestrado em Geoquímica, (1991) 127.
Ecl. Quím., São Paulo, 36 ,2011 63
Você também pode gostar
- Unidades evaporíticas carboníferas do Depósito Potassífero de Autazes, região ocidental da Bacia do Amazonas: análises estratigráficas de sequências, geoquímicas, mineralógicas e paleoambientaisNo EverandUnidades evaporíticas carboníferas do Depósito Potassífero de Autazes, região ocidental da Bacia do Amazonas: análises estratigráficas de sequências, geoquímicas, mineralógicas e paleoambientaisAinda não há avaliações
- Índice de Larson e de SaturaçãoDocumento4 páginasÍndice de Larson e de SaturaçãoThomas_BrasilAinda não há avaliações
- Eletroanálises: aspectos teóricos e práticosNo EverandEletroanálises: aspectos teóricos e práticosAinda não há avaliações
- Artigo para Journal of DevelopmentDocumento7 páginasArtigo para Journal of DevelopmentÉlitonSanclérAinda não há avaliações
- LorraneDocumento10 páginasLorranezannakarinalimatrindadeAinda não há avaliações
- Produção de Corpos Cerâmicos A Partir de Argila Vermelha E Pó de DespoeiramentoDocumento9 páginasProdução de Corpos Cerâmicos A Partir de Argila Vermelha E Pó de DespoeiramentoCarlosAlbertoFrançaJr.Ainda não há avaliações
- Interpretação Análise de SolosDocumento10 páginasInterpretação Análise de SolosAllison Macambira100% (1)
- Trabalho NaylaDocumento10 páginasTrabalho NaylawemillynobreAinda não há avaliações
- Análise Da Dureza Total, Dureza de Cálcio e Dureza de Magnésio em Amostra de Água Do Córrego Riacho FundoDocumento9 páginasAnálise Da Dureza Total, Dureza de Cálcio e Dureza de Magnésio em Amostra de Água Do Córrego Riacho FundoNelson LuizAinda não há avaliações
- Seperação de Minerais Pesados de Sedimentos Do Rio Amazonas e Rio SolimõesDocumento10 páginasSeperação de Minerais Pesados de Sedimentos Do Rio Amazonas e Rio SolimõesHelton PantojaAinda não há avaliações
- Modelo para Trabalhos Tecnicos 31 CongressoDocumento8 páginasModelo para Trabalhos Tecnicos 31 CongressoSaara BoteonAinda não há avaliações
- Determinação Da Concentração de NaCl em Soro Fisiológico Comercial Pelo Método de MohrDocumento9 páginasDeterminação Da Concentração de NaCl em Soro Fisiológico Comercial Pelo Método de MohrJLPGEMEINDERAinda não há avaliações
- Dissertacao CaracterizacaoAssinaturaIsotopicaDocumento104 páginasDissertacao CaracterizacaoAssinaturaIsotopicaRobinson AndradeAinda não há avaliações
- Determinação Do Teor de Cloreto em Águas de Abastecimento Da Região Agreste PotiguarDocumento6 páginasDeterminação Do Teor de Cloreto em Águas de Abastecimento Da Região Agreste PotiguarIlena RebecaAinda não há avaliações
- Lais Azevedo CostaDocumento66 páginasLais Azevedo CostaIaneAinda não há avaliações
- CromatoDocumento29 páginasCromatoFelipe SebbenAinda não há avaliações
- Dimensionamento Lagoas AeradasDocumento21 páginasDimensionamento Lagoas AeradasrafaelAinda não há avaliações
- 13 AdafqdaecchsnmdccpDocumento5 páginas13 AdafqdaecchsnmdccpJean CarneiroAinda não há avaliações
- Programa ICV 2011-2012 Relatório Final Análise Da Qualidade Das Águas Do Rio Parnaíba No Meio Urbano Da Cidade de Teresina - PIDocumento15 páginasPrograma ICV 2011-2012 Relatório Final Análise Da Qualidade Das Águas Do Rio Parnaíba No Meio Urbano Da Cidade de Teresina - PIBruno DuarteAinda não há avaliações
- ExemploDocumento9 páginasExemploUgeda JuniorAinda não há avaliações
- Solubilidade e Formação de PrecipitadosDocumento2 páginasSolubilidade e Formação de PrecipitadosJoão CarlosAinda não há avaliações
- Lista de Exercício 3 - Necessidade de CalagemDocumento1 páginaLista de Exercício 3 - Necessidade de CalagemAristóteles de Jesus Teixeira FilhoAinda não há avaliações
- Remoção de Nitrogênio Amoniacal em Efluentes de Sistemas AnaeróbiosDocumento5 páginasRemoção de Nitrogênio Amoniacal em Efluentes de Sistemas AnaeróbiosAndré TelesAinda não há avaliações
- Relatório Da Aula Prática 01 - Análises de Parâmetros de ÁguaDocumento6 páginasRelatório Da Aula Prática 01 - Análises de Parâmetros de ÁguaSantini VagnoniAinda não há avaliações
- Interpretação Análises de SoloDocumento11 páginasInterpretação Análises de SoloLeonardo Ribas AmaralAinda não há avaliações
- Determinação de CloretosDocumento14 páginasDeterminação de CloretosIldemarFernandesAinda não há avaliações
- Quantificação de Nitrato em Água de AbastecimentoDocumento9 páginasQuantificação de Nitrato em Água de AbastecimentoJoherbson DeividAinda não há avaliações
- DISSERTAÇÃO Augusto Maia 2°VERSÃODocumento86 páginasDISSERTAÇÃO Augusto Maia 2°VERSÃOaugustoAinda não há avaliações
- Icp OesDocumento9 páginasIcp OesLilian Benchimol100% (1)
- Investigação Sobre o Efeito Da Taxa de Varredura Do Ensaio de Polarização Potenciodinâmica e Da Concentração de Íons Cloreto Sobre o Comportamento de Corrosão Do Aço Inoxidável Aisi 304Documento9 páginasInvestigação Sobre o Efeito Da Taxa de Varredura Do Ensaio de Polarização Potenciodinâmica e Da Concentração de Íons Cloreto Sobre o Comportamento de Corrosão Do Aço Inoxidável Aisi 304Brendha EstácioAinda não há avaliações
- EstudoDocumento6 páginasEstudoGerencia produçãoAinda não há avaliações
- Quilombo RibeiraoDocumento12 páginasQuilombo RibeiraoalexpiaiAinda não há avaliações
- QualidaidiadaDocumento23 páginasQualidaidiadahillarypaschoal121Ainda não há avaliações
- Relatorio Quimica Analitica 2Documento18 páginasRelatorio Quimica Analitica 2ADMINISTRATIVO CAMPOSVIDALAinda não há avaliações
- Relatório de Química Analitica IIDocumento8 páginasRelatório de Química Analitica IIjhorgelourrizAinda não há avaliações
- Relatório Jar TestDocumento6 páginasRelatório Jar TestMariana MyriamAinda não há avaliações
- Relatório Análise - Prática 5Documento21 páginasRelatório Análise - Prática 5Amanda MyrnaAinda não há avaliações
- Análise 3 - R5 - 31 - 05 - 2023 Soro FisiológicoDocumento5 páginasAnálise 3 - R5 - 31 - 05 - 2023 Soro FisiológicoGabrielli AlvesAinda não há avaliações
- XXVIII-ENTMME-TEMPLATE-1 - Hidroxiapatita OficialDocumento7 páginasXXVIII-ENTMME-TEMPLATE-1 - Hidroxiapatita OficialLidia DelyAinda não há avaliações
- Gestao de Qualidade Mas DetalhadoDocumento12 páginasGestao de Qualidade Mas DetalhadoAna Beatriz de CastroAinda não há avaliações
- Roteiro #06 - Volumetria Por Precipitação Pelo Método de MohrDocumento3 páginasRoteiro #06 - Volumetria Por Precipitação Pelo Método de MohrericksoulssouzaAinda não há avaliações
- Avaliacao Acidez Picles PepinoDocumento9 páginasAvaliacao Acidez Picles PepinoAdilson Mendes de Lima0% (1)
- Determinação de Cloreto de Sódio em Soro FisiológicoDocumento18 páginasDeterminação de Cloreto de Sódio em Soro FisiológicoEvelynSchweitzerAinda não há avaliações
- Indice de Qualidade Da Água de Igarapés Da Bacia Do Tarumã-AçuDocumento8 páginasIndice de Qualidade Da Água de Igarapés Da Bacia Do Tarumã-AçuRamisson Pessoa MotaAinda não há avaliações
- Relatório Parcial Parnaíba Programa ICV Análise Da Qualidade Das Águas Do Rio Parnaíba No Meio Urbano Da Cidade de Teresina - PIDocumento5 páginasRelatório Parcial Parnaíba Programa ICV Análise Da Qualidade Das Águas Do Rio Parnaíba No Meio Urbano Da Cidade de Teresina - PIBruno DuarteAinda não há avaliações
- Apostila de Água Corr.Documento26 páginasApostila de Água Corr.Tayenne Lira LucenaAinda não há avaliações
- Aula 01 Controle Poluição Das Águas Caracterização Qualidade 09nov18 T3 PDFDocumento73 páginasAula 01 Controle Poluição Das Águas Caracterização Qualidade 09nov18 T3 PDFlucasmgimenesAinda não há avaliações
- Webinar Eletrodos - Metrohm 1590598793Documento34 páginasWebinar Eletrodos - Metrohm 1590598793Ligia TeodoroAinda não há avaliações
- Flotação Seletiva para o Reprocessamento deDocumento8 páginasFlotação Seletiva para o Reprocessamento deJP Junior ReisAinda não há avaliações
- Artigo WebArtigosDocumento9 páginasArtigo WebArtigosMarcosChaprãoAinda não há avaliações
- Manual Phmetro - Webinar - Eletrodos - PDFDocumento38 páginasManual Phmetro - Webinar - Eletrodos - PDFAurenice MotaAinda não há avaliações
- 29583-Texto Do Artigo-109318-1-10-20190818Documento10 páginas29583-Texto Do Artigo-109318-1-10-20190818mariselimamcaAinda não há avaliações
- Relatorio de Química Ambiental UlbraDocumento8 páginasRelatorio de Química Ambiental UlbraEduardo BruzzaAinda não há avaliações
- Fotometria de ChamaDocumento11 páginasFotometria de ChamaMilena de Oliveira100% (1)
- Estimativa Oferta Demanda Hidrica PratagyDocumento16 páginasEstimativa Oferta Demanda Hidrica PratagyANDRESSA ELLEN APOLINÁRIO SILVAAinda não há avaliações
- Síntese Do Alúmen Como CoagulanteDocumento58 páginasSíntese Do Alúmen Como CoagulanteThuanne Braúlio HennigAinda não há avaliações
- Exercícios AnalíticaDocumento3 páginasExercícios AnalíticaJean Francisco100% (5)
- Detreminação de IodetoDocumento11 páginasDetreminação de IodetoSannyele AlcantaraAinda não há avaliações
- Gilvan I Aker CIA de OliveiraDocumento116 páginasGilvan I Aker CIA de Oliveiracsmaues1Ainda não há avaliações
- Avaliacao Da RazaoDocumento5 páginasAvaliacao Da RazaoGerencia produçãoAinda não há avaliações
- Química Aula 15 - IsomeriaDocumento1 páginaQuímica Aula 15 - IsomeriaReginaldo SalesAinda não há avaliações
- Slide 5 - Radioatividade, Leis Da RadioatividadeDocumento12 páginasSlide 5 - Radioatividade, Leis Da RadioatividadeReginaldo SalesAinda não há avaliações
- Química Aula 14 - Revisão IsomeriasDocumento1 páginaQuímica Aula 14 - Revisão IsomeriasReginaldo SalesAinda não há avaliações
- Slide 4 - Radioatividade, Leis Da RadioatividadeDocumento13 páginasSlide 4 - Radioatividade, Leis Da RadioatividadeReginaldo SalesAinda não há avaliações
- Slide 2 - Radioatividade, HistóriaDocumento11 páginasSlide 2 - Radioatividade, HistóriaReginaldo SalesAinda não há avaliações
- Slide 1 - Radioatividade, IntroduçãoDocumento19 páginasSlide 1 - Radioatividade, IntroduçãoReginaldo SalesAinda não há avaliações
- Capítulo 31 - Ousados Como Comenius (Quinteto)Documento22 páginasCapítulo 31 - Ousados Como Comenius (Quinteto)Reginaldo SalesAinda não há avaliações
- Capítulo 4 - Tabuquímico (Jarlisson e Niza)Documento25 páginasCapítulo 4 - Tabuquímico (Jarlisson e Niza)Reginaldo SalesAinda não há avaliações
- Capítulo 29 - Maquetes Tateis (Edivanda)Documento23 páginasCapítulo 29 - Maquetes Tateis (Edivanda)Reginaldo SalesAinda não há avaliações
- Capítulo 7 - BNCC e Os Professores de Química (Thatiana)Documento32 páginasCapítulo 7 - BNCC e Os Professores de Química (Thatiana)Reginaldo SalesAinda não há avaliações
- Cap 1 - Politicas Públicas em MADocumento21 páginasCap 1 - Politicas Públicas em MAReginaldo SalesAinda não há avaliações
- Soren SorensenDocumento1 páginaSoren SorensenReginaldo SalesAinda não há avaliações
- Cap 1 - Politicas Públicas em MADocumento21 páginasCap 1 - Politicas Públicas em MAReginaldo SalesAinda não há avaliações
- Cap 1 - Politicas Públicas em MADocumento21 páginasCap 1 - Politicas Públicas em MAReginaldo SalesAinda não há avaliações
- Revisão (Prova Final de Física) - EM1Documento2 páginasRevisão (Prova Final de Física) - EM1Adriano GomesAinda não há avaliações
- Sedimentos e Rochas SedimentaresDocumento35 páginasSedimentos e Rochas SedimentaresFABIO JOSE DA SILVAAinda não há avaliações
- A Improbabilidade de Deus PDFDocumento5 páginasA Improbabilidade de Deus PDFIsrael DantasAinda não há avaliações
- Quimica 9ano Prof Roberto PDFDocumento53 páginasQuimica 9ano Prof Roberto PDFAlexandre Freitas NogueiraAinda não há avaliações
- Resumo Física A, 10º e 11º Ano.Documento61 páginasResumo Física A, 10º e 11º Ano.Tito CunhaAinda não há avaliações
- Bacias de Drenagem Da Baia de GuanabaraDocumento8 páginasBacias de Drenagem Da Baia de GuanabaraMiguel Jorge SouzaAinda não há avaliações
- Meditação Sobre o Mundo Interior - Alceu Amoroso LimaDocumento89 páginasMeditação Sobre o Mundo Interior - Alceu Amoroso LimaRicardo Maddalena100% (1)
- 15 - Ensaio Nao Destrutivo - UltrassomDocumento10 páginas15 - Ensaio Nao Destrutivo - UltrassomBhertrand GomesAinda não há avaliações
- Máquinas de Fluxos - 1º AulaDocumento43 páginasMáquinas de Fluxos - 1º AulaChristian Moreira0% (1)
- Exercícios RB-SRDocumento8 páginasExercícios RB-SRNati FerroAinda não há avaliações
- Simulado Princípio de Le Chatlier PDFDocumento2 páginasSimulado Princípio de Le Chatlier PDFNinja SplitAinda não há avaliações
- 2011-2 Aula 1 Introdução Ao Estudo Dos EcossistemasDocumento48 páginas2011-2 Aula 1 Introdução Ao Estudo Dos EcossistemasAlessandro de PaulaAinda não há avaliações
- Sebenta (Módulo 4 (E3F1) ) 1ºK, NDocumento13 páginasSebenta (Módulo 4 (E3F1) ) 1ºK, NCarla CostaAinda não há avaliações
- 1 - Geografia Bíblica - 1 AulaDocumento35 páginas1 - Geografia Bíblica - 1 AulafbtudelaAinda não há avaliações
- Memorial Calculo - Trocador de Calor Casco e TuboDocumento4 páginasMemorial Calculo - Trocador de Calor Casco e TuboVictor OliveiraAinda não há avaliações
- O SELF E SEU AMBIENTE COMPORTAMENTAL - Irving HallowellDocumento31 páginasO SELF E SEU AMBIENTE COMPORTAMENTAL - Irving HallowellAnticristopher Feliphe Ramos Xirú100% (1)
- Calorimetria 2018Documento3 páginasCalorimetria 2018Emilson MoreiraAinda não há avaliações
- Teste Avaliacao 3Documento5 páginasTeste Avaliacao 3paula.silva.cidadaniaambientalAinda não há avaliações
- Laudo Aterramento PDFDocumento77 páginasLaudo Aterramento PDFJuliano André Petry100% (3)
- TRANE Catalogo-Comercial-Piso-Teto-InverterDocumento2 páginasTRANE Catalogo-Comercial-Piso-Teto-InverterPaulo Damaceno100% (1)
- Balanços de Massa Com ELV de Liquidos ImisciveisDocumento4 páginasBalanços de Massa Com ELV de Liquidos ImisciveisGuilherme DiasAinda não há avaliações
- Manual de Geologia GeralDocumento184 páginasManual de Geologia GeralHelio Armazia50% (2)
- Questoes Substancias e MisturasDocumento11 páginasQuestoes Substancias e MisturasKarina Fernandes ValeAinda não há avaliações
- 2 Aula Ecossistema Luciano LeiteDocumento52 páginas2 Aula Ecossistema Luciano LeitealanaAinda não há avaliações
- Ciencia Do Ambiente - Aula 4 - Ecossistemas Terrestres A PDFDocumento5 páginasCiencia Do Ambiente - Aula 4 - Ecossistemas Terrestres A PDFALEXANDRE SALES BRAZ JUNIORAinda não há avaliações
- Polímero Reticulado - Bórax+PVADocumento20 páginasPolímero Reticulado - Bórax+PVADenis LimaAinda não há avaliações
- Texto Meio AmbienteDocumento1 páginaTexto Meio AmbienteJoelMarcosOliveiraAinda não há avaliações
- Livro-O Fogo e o Cerrado-VfmenorDocumento17 páginasLivro-O Fogo e o Cerrado-VfmenorrsumiyaAinda não há avaliações
- Quadros 2.1 e 2.2Documento3 páginasQuadros 2.1 e 2.2Daniel FonsecaAinda não há avaliações
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- Biomecânica Básica dos Exercícios: Membros InferioresNo EverandBiomecânica Básica dos Exercícios: Membros InferioresNota: 3.5 de 5 estrelas3.5/5 (8)
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- História dos Testes Psicológicos: Origens e TransformaçõesNo EverandHistória dos Testes Psicológicos: Origens e TransformaçõesAinda não há avaliações
- 365 Ideias De Posts Para Ter Um Instagram De Sucesso!No Everand365 Ideias De Posts Para Ter Um Instagram De Sucesso!Ainda não há avaliações
- Inteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNo EverandInteligência artificial: Como aprendizado de máquina, robótica e automação moldaram nossa sociedadeNota: 5 de 5 estrelas5/5 (3)
- Cérebro Singular: Como estimular crianças no espectro autista ou com atrasos no desenvolvimentoNo EverandCérebro Singular: Como estimular crianças no espectro autista ou com atrasos no desenvolvimentoNota: 5 de 5 estrelas5/5 (1)