Escolar Documentos
Profissional Documentos
Cultura Documentos
Resumao
Resumao
Enviado por
Fabianno FabeniTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Resumao
Resumao
Enviado por
Fabianno FabeniDireitos autorais:
Formatos disponíveis
FRUM 3 EXTRAO LQUIDO-LQUIDO Pergunta 1 "Destilar bonito (...).
. Antes de tudo, porque um ofcio lento, filosfico e silenciosos, que matm ocupado mas deixa tempo para pensar noutras coisas, um pouco como andar de bicicleta. Mais ainda porque comporta uma metamorfose: de lquido a vapor (invisvel), e deste novamente a lquido; mas neste caminho duplo, para cima e para baixo, atige-se a pureza, condio ambgua e fascinante, que parte da qumica e vai muito longe (...)" LEVI, P. A tabela peridica. Rio de Janeiro: Relume-Dumar, 1994. O que diferencia a destilao simples da destilao fracionada? Destilao simples: utilizada quando h interesse nas duas fases ou apenas na lquida. A mistura aquecida em um balo e gua entra em ebulio. O vapor passa pelo interior do condensador, que refrigerado por gua corrente. Ento o vapor condensa-se e o lquido isento do slido recolhido por um erlenmeyer, ao final restar apenas o slido no balo de vidro. A destilao fracionada um aprimoramento da destilao simples, e empregado para separar gases lquidos com PEs prximos. Uma coluna de vidro cheia de obstculos ( bolinhas ou cacos de vidro) colocado entre o condensador e o balo no qual a mistura aquecida. Os obstculos permitem que o componente de menor PE, chegue rapidamente ao condensador e destile primeiro. Assim que ele destilar totalmente, destilar o prximo componente lquido da mistura , em ordem de PE que recolhido em outro frasco.
Pergunta 2 a) O que so agentes secantes? Agente secante um sal inorgnico anidro e que tem a capacidade de se ligar s molculas de gua, formando hidratos. nH2O + agente secante agente secante X nH2O b) Quais os fatores que devem ser observados na escolha de um agente secante? 1- Capacidade: refere-se ao nmero de moles de molculas de gua a que se liga de modo a formar um sal hidratado. Expressa-se pela quantidade de gua/g de agente secante; 2- Eficincia: expressa-se pela quantidade de gua deixada pelo agente secante para trs na fase orgnica; 3- Velocidade a que trabalha: quanto tempo o agente necessita de estar
em contacto com a soluo orgnica; 4- Inatividade qumica: no pode ser reativo nem com o solvente orgnico nem com o composto orgnico nele dissolvido.
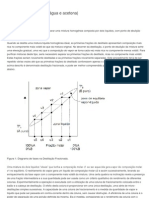
Pergunta 3 A Extrao lquido - lquido consiste na separao de componentes de uma mistura heterognea, por meio de uma distribuio das substncias entre o meios lquidos que formam as fases distintas. O que diz a lei da distribuio ou lei da partio? A uma dada temperatura, se a um sistema formado por duas camadas lquidas for adicionado um terceiro componente slido, solvel individualmente em ambas as camadas, ento esse slido ir se distribuir entre os solventes na proporo que faz a razo entre as suas concentraes C A e CB, em cada um dos solventes, permanecer uma concentrao K=CA/CB. Essa razo K, denominada coeficiente de distribuio ou coeficiente de participao. FRUM 4 DESTILAO FRACIONADA 1) O que eficincia da coluna de destilao fracionada? A eficincia da coluna de destilao fracionada medida pelo poder de separao dos componentes de uma mistura por parte definida de seu tamanho. Essa eficincia expressa pela altura equivalente por prato terico(AEPT). Quanto maior a variao dos calores de vaporizao dos lquidos envolvidos melhor ser a capacidade de separao que ser realizada pela coluna de destilao fracionada.
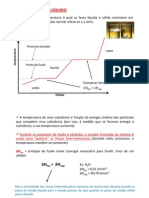
2) "O poder de separao de lquidos, por destilao fracionada, aumenta proporcionalmente com a diferena entre os calores de vaporizao dos lquidos envolvidos." O que significa calor latente de vaporizao? A quantidade de calor necessria para vaporizar a gua presso e temperatura constantes de 1 atmosfera e 100 o C, respectivamente. A energia absorvida pelas molculas de gua durante a evaporao usada somente para dar-lhes o movimento necessrio para escapar da superfcie do lquido e tornar-se um gs. Esta energia, que posteriormente liberada como calor quando o vapor volta a ser lquido, denominada calor latente de vaporizao. OBS.: Alguns alunos responderam apenas o que calo latente e o que calor latente de vaporizao. 3) Qual diferena entre:
Liquefao e condensao
Liquefao a passagem do estado gasoso para o estado lquido, quando a substncia se encontra "geralmente" no estado gasoso. Condensao a passagem do estado gasoso para o estado lquido, quando a substncia se apresenta geralmente no estado lquido e passa para o estado gasoso. Com os termos podemos determinar o estado fsico da substncia, se lquida ou um gs. Por exemplo: a gua passa do estado lquido para o estado gasoso (vapor) e ao passar do estado gasoso para o lquido ela sofre condensao. O oxignio por sua vez, j um gs, portanto quando ele passa para o estado lquido, ele sofre liquefao.
Evaporao e ebulio
A evaporao a mudana lenta de uma substncia lquida em vapor. Pode ocorrer espontaneamente, dependendo das condies ambientes. Podemos constatar a evaporao na secagem de roupas no varal, de poas de gua, da gua das chuvas, dos rios, etc. A ebulio ocorre quando fornecemos calor a um lquido ou reduzimos a presso que atua sobre ele. Colocando-se uma panela com gua comeara a ferver, isto , entrar em ebulio, e bolhas de vapor se formaro em toda a parte lquida. Vapor e gs
Por definio, o gs um dos estados fsicos da matria, enquanto que o vapor a matria no estado gasoso. Porm, temos algumas outras caractersticas que devem ser levadas em considerao: - O gs no tem forma e volume definidos, pois consiste em uma " coleo" de partculas (molculas, tomos, ons, eltrons, etc) cujos movimentos so aleatrios. Existe sim um campo de fora em todo o espao sua volta, com interaes que do origem s foras moleculares, que influenciam a movimentao dessas partculas. - O gs tem a densidade relativamente baixa e sua viscosidade pode ser comparada aos estados lquido e slido. O volume muito sensvel s alteraes de temperatura e presso. Preenche completamente qualquer recipiente, j que possui a difuso rpida. (distribui-se homogeneamente). - O vapor, em temperatura igual ou abaixo de sua temperatura crtica, capaz de estar em equilbrio com o lquido ou o slido do qual se formou, pelo aumento de presso. - O vapor originado da vaporizao, que se divide em vaporizao e ebulio.
FRUM 5 DESTILAO POR ARRASTE COM VAPOR QUESTO 1 - Como o funcionamento de uma destilao por arraste de vapor? - Cite exemplos de compostos orgnicos (aromticos ou no) que podem ser
extrados de fontes naturais. O princpio de funcionamento da destilao por arraste de vapor feita quando o vapor de gua passa pela membrana das clulas arrastando substncias solveis e insolveis em gua e posteriormente realiza-se uma extrao utilizando solventes orgnicos. Esse processo muito utilizado para separar e purificar compostos orgnicos. Exemplos: Noz moscada, anil, limonemo, citral, eugenol entre outros. Ou Empregada para destilar substncias que se decompem nas proximidades de seus pontos de ebulio e que so insolveis em gua ou nos seus vapores de arraste. Esta operao baseia-se no fato de que, numa mistura de lquidos imiscveis, o ponto de ebulio ser a temperatura na qual a soma das presses parciais dos vapores igual da atmosfera, o que constitui uma decorrncia da lei das presses parciais de Dalton. Se, em geral, o arraste se faz com vapor dgua, a destilao, presso atmosfrica, resultar na separao do componente de ponto de ebulio mais alto, a uma temperatura inferior a 100C. Por outro lado, quando uma mistura de dois lquidos imiscveis destilada, o ponto de ebulio da mistura permanece constante at que um dos componentes tenha sido separado, j que a presso total do vapor independe das quantidades relativas dos componentes. O ponto de ebulio, a partir da, eleva-se rapidamente, at atingir o do lquido remanescente. O vapor que se separa de tal mistura contm os componentes na mesma proporo, em volume, que suas presses de vapor relativas. Por meio de clculos simples e aplicando as leis dos gases, podemos estabelecer a proporo dos vapores em funo de seus pesos moleculares e das suas presses parciais
QUESTO 2 Quando a tcnica de destilao por arraste de vapor deve ser utilizada? A destilao por arraste de vapor uma destilao de misturas imiscveis de compostos orgnicos e gua. Misturas imiscveis no se comportam como solues. Os componentes de uma mistura imiscvel "fervem" a temperaturas menores do que os pontos de ebulio dos componentes individuais. Enquanto ambos componentes da mistura estiverem destilando junto, o ponto de ebulio ficar constante. Portanto, uma mistura de compostos de alto ponto de ebulio e gua pode ser destilada temperatura constante e menor que 100C, que o ponto de ebulio da gua. Podendo ser utilizada nos seguintes casos: Para separar substncias pouco miscveis em gua, cuja presso de vapor seja prxima a da gua a 100C, o que muito importante para as substncias que se decompem nestas temperaturas; Quando se deseja separar, ou purificar uma substncia, cujo ponto de ebulio alto e/ou apresente risco de decomposio; Para separar ou purificar substncias contaminadas com impurezas resinosas; Para retirar solventes com elevado ponto de ebulio, quando em soluo existe uma
substncia no voltil.
QUESTO 3 Por que a destilao por arraste de vapor preferida destilao simples quando se trata de leos essenciais? Porque muitos leos essenciais se decompem devido alta temperatura de ebulio. E por isso, realizada a destilao por arraste de vapor, pelo qual ocorrer a destilao sem que os leos essenciais se decompem visto que no h necessidade de temperaturas to elevadas. Ou Porque muitos componentes dos leos essenciais tm ponto de ebulio muito alto. Os leos essenciais mais gua (vapor) formam uma mistura imiscvel, sendo que estas misturas podem ser destiladas, usando a destilao por arraste de vapor, a uma temperatura menor que 100C.
QUESTO 4 Por que o ponto de ebulio da mistura em uma destilao a vapor menor do que o ponto de ebulio de cada componente puro A destilao por arraste de vapor uma destilao de misturas imiscveis de compostos orgnicos e gua (vapor). Misturas imiscveis no se comportam como solues. A destilao a vapor baseia-se no fato de que a presso total de vapor de uma mistura de lquidos imiscveis igual soma da presso de vapor dos componentes puros individuais (Ptotal = Pgua + Pleo = Patmosfrica), a Lei de Dalton. A presso total de vapor da mistura torna-se igual presso atmosfrica ( Ptotal = Patmosfrica) numa temperatura menor que o ponto de ebulio de qualquer um dos componentes. Assim, quanto maior a presso de vapor dos componentes menor ser a temperatura de ebulio. Ou Uma substncia lquida entra em ebulio quando a presso do sistema ao qual faz parte atinge a presso de vapor dessa substncia, esse ponto recebe o nome de ponto de ebulio ou temperatura de ebulio. A presso de vapor uma medida da tendncia de evaporao de um lquido. Quanto maior for a sua presso de vapor, mais voltil ser o lquido, e menor ser sua temperatura de ebulio. Na destilao a vapor onde temos uma mistura de substncias imiscveis de compostos orgnicos e gua (vapor), a presso total de vapor igual soma das presses de vapor individuais de cada componente. Assim, como a presso total de vapor da mistura ser maior que a presso de vapor dos
componentes puros, logo, a temperatura de ebulio da mistura ser menor.
Você também pode gostar
- Atividades Números InteirosDocumento3 páginasAtividades Números InteirosAline Tavares Soares100% (17)
- Manual de Instruções - Estufa de Secagem e Esterilização DigitalDocumento7 páginasManual de Instruções - Estufa de Secagem e Esterilização DigitalEduardo MatheusAinda não há avaliações
- 08 Separação de MisturasDocumento5 páginas08 Separação de MisturasLucas KaiqueAinda não há avaliações
- Lista de Alarmes No Conversor BaumuellerDocumento33 páginasLista de Alarmes No Conversor Baumuellerjonas hiperroll100% (3)
- Relatorio de Quimica Solubilidade 02Documento13 páginasRelatorio de Quimica Solubilidade 02Marcus Vinícius Nascimento FreireAinda não há avaliações
- E-Book (Tubulação)Documento16 páginasE-Book (Tubulação)Odagil Banzato80% (5)
- 10344804042012quimica Organica Experimental Aula 5Documento23 páginas10344804042012quimica Organica Experimental Aula 5Artur Pereira NetoAinda não há avaliações
- Destilação Simples É Um Processo Que Permite A Separação de Um Líquido de Uma Substância Não VolátilDocumento13 páginasDestilação Simples É Um Processo Que Permite A Separação de Um Líquido de Uma Substância Não VolátilValsergio BarrosAinda não há avaliações
- Química Revisão 2022 - Elementos, Substâncias e Reações QuímicasDocumento16 páginasQuímica Revisão 2022 - Elementos, Substâncias e Reações QuímicasTiagoViFAinda não há avaliações
- Relatório Separação de MisturasDocumento8 páginasRelatório Separação de MisturasVINICIUS VANDER LIMA TOMAINAinda não há avaliações
- Biofísica IDocumento88 páginasBiofísica Ireginalddvictor.sAinda não há avaliações
- Introduçao À Quimica 1 PDFDocumento28 páginasIntroduçao À Quimica 1 PDFAilton VarelaAinda não há avaliações
- Propriedades ColigativasDocumento11 páginasPropriedades Coligativaszenta.angoAinda não há avaliações
- DestilaçãoDocumento5 páginasDestilaçãoBruno SouzaAinda não há avaliações
- Destilação Fracionada PDFDocumento6 páginasDestilação Fracionada PDFJohann Costa CastelliAinda não há avaliações
- Apresentação - OperaçõesUnitáriaspartell - Aula 13-10-23Documento111 páginasApresentação - OperaçõesUnitáriaspartell - Aula 13-10-23ing.fatimaferreiragomezAinda não há avaliações
- Aula de Química Básica-SoluçõesDocumento11 páginasAula de Química Básica-SoluçõesHellen PatriciaAinda não há avaliações
- Química - Separação de MisturasDocumento11 páginasQuímica - Separação de MisturasJunior GuimarãesAinda não há avaliações
- Destilação FracionadaDocumento5 páginasDestilação FracionadaEdu AntunesAinda não há avaliações
- Exp 4 RelatórioDocumento7 páginasExp 4 RelatórioAlice CordeiroAinda não há avaliações
- Relatório de Líquidos - Julia MainiDocumento7 páginasRelatório de Líquidos - Julia Mainijulia.maini99Ainda não há avaliações
- Apostila Físico-Química1Documento29 páginasApostila Físico-Química1Diego E MarinaAinda não há avaliações
- Tratamento AguaDocumento14 páginasTratamento AguaThiago JhonnyAinda não há avaliações
- Congelamento Dos LíquidosDocumento5 páginasCongelamento Dos LíquidosJamesCRBAinda não há avaliações
- Trabalho de QuímicaDocumento8 páginasTrabalho de QuímicamariaAinda não há avaliações
- Experimento de Destilação DiferencialDocumento13 páginasExperimento de Destilação DiferencialL#renaAinda não há avaliações
- Química Orgânica ExperimentalDocumento2 páginasQuímica Orgânica ExperimentalLuanna PinheiroAinda não há avaliações
- Soluções 1Documento5 páginasSoluções 1Sabrina SantosAinda não há avaliações
- Destilação Simples - QuestionárioDocumento1 páginaDestilação Simples - QuestionárioAbel Tavares100% (2)
- A Natureza Nos Disponibiliza Diversas SubstânciasDocumento22 páginasA Natureza Nos Disponibiliza Diversas SubstânciasSavequinho SavecaAinda não há avaliações
- SOLUÇÕESDocumento98 páginasSOLUÇÕESSidney JesusAinda não há avaliações
- Apostila Aula 2 Estados Físicos Da MatériaDocumento16 páginasApostila Aula 2 Estados Físicos Da Matériaanne dayseAinda não há avaliações
- Destilação Fracionada e Destilação Por Arraste de VaporDocumento13 páginasDestilação Fracionada e Destilação Por Arraste de VaporNatáliaCabralAinda não há avaliações
- Aula 11 - Notas de AulaDocumento17 páginasAula 11 - Notas de AulaDanielAinda não há avaliações
- Quimica 18Documento29 páginasQuimica 18ascatanho100% (1)
- DESTILAÇÃO1Documento10 páginasDESTILAÇÃO1Roberta BelazAinda não há avaliações
- DestilacaoDocumento6 páginasDestilacaoMartinõ MarcellAinda não há avaliações
- Solution OdpDocumento57 páginasSolution OdpAntonio Da Costa FreireAinda não há avaliações
- Propriedades ColigativasDocumento23 páginasPropriedades ColigativasAnne IngridAinda não há avaliações
- Revisão Química GeralDocumento53 páginasRevisão Química GeralLuciano MachadoAinda não há avaliações
- Modelo - Slides - ISPB - 2023 - (1) (1) 1aula # 6 Liquidos e Solucoes 2Documento16 páginasModelo - Slides - ISPB - 2023 - (1) (1) 1aula # 6 Liquidos e Solucoes 2Jackson CacondaAinda não há avaliações
- Universidade Estadual de MaringáDocumento14 páginasUniversidade Estadual de MaringáRobert AlephyAinda não há avaliações
- Relatorio 03 ExperiementalDocumento17 páginasRelatorio 03 ExperiementalelenitabastosAinda não há avaliações
- Relatório Inorganica I (Vinho)Documento8 páginasRelatório Inorganica I (Vinho)mauricelioaraujoAinda não há avaliações
- Química Inorgânica e OrgânicaDocumento110 páginasQuímica Inorgânica e OrgânicaRaquel Sena100% (1)
- 5-Solucoes e SeparacaoDocumento6 páginas5-Solucoes e SeparacaoAdriano FuriniAinda não há avaliações
- SolubilidadeDocumento4 páginasSolubilidadeDmingos JúniorAinda não há avaliações
- Pet 02 - 2º emDocumento21 páginasPet 02 - 2º emAna Elisa Teixeira AlcobaAinda não há avaliações
- Turmafevereiro-química-Estados Físicos Da Matéria, Gráficos de Mudança de Fase e Métodos de Separação de Misturas Heterogêneas-09!02!2021Documento19 páginasTurmafevereiro-química-Estados Físicos Da Matéria, Gráficos de Mudança de Fase e Métodos de Separação de Misturas Heterogêneas-09!02!2021luunobr99Ainda não há avaliações
- Propriedades Coligativas Das Soluções 1Documento37 páginasPropriedades Coligativas Das Soluções 1BruAinda não há avaliações
- Questionarios de Organica ExperimentalDocumento11 páginasQuestionarios de Organica ExperimentalLuiz LimaAinda não há avaliações
- Separação de Misturas Homogêneas-EvaporaçãoDocumento3 páginasSeparação de Misturas Homogêneas-EvaporaçãoLourdes NascimentoAinda não há avaliações
- Biofísica para ciências biomédicas – 4ª ediçãoNo EverandBiofísica para ciências biomédicas – 4ª ediçãoAinda não há avaliações
- Utilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosNo EverandUtilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosAinda não há avaliações
- Tratamento de Lodos de Estações de Tratamento de ÁguaNo EverandTratamento de Lodos de Estações de Tratamento de ÁguaAinda não há avaliações
- Enem 2018 - Ciências Da Natureza E Suas TecnologiasNo EverandEnem 2018 - Ciências Da Natureza E Suas TecnologiasAinda não há avaliações
- Compressor ECB ECMDocumento10 páginasCompressor ECB ECMfabiofgfAinda não há avaliações
- Central de Material - EsterilizaçãoDocumento68 páginasCentral de Material - EsterilizaçãoJoão Pedro AraújoAinda não há avaliações
- Apostila Paisagismo PDFDocumento71 páginasApostila Paisagismo PDFoctavianijrAinda não há avaliações
- 01 - PARÂMETROS FÍSICO e QUIMICOSDocumento15 páginas01 - PARÂMETROS FÍSICO e QUIMICOSNilmara MachadoAinda não há avaliações
- Automação, Instrumentação e ControleDocumento112 páginasAutomação, Instrumentação e ControleMarcus ToméAinda não há avaliações
- HidrocinemáticaDocumento6 páginasHidrocinemáticaCarlos SaAinda não há avaliações
- TD CalorimetriaDocumento2 páginasTD Calorimetriaray Sousa SilvaAinda não há avaliações
- Ficha Técnica: Sistemas de Drenagem ValsirDocumento6 páginasFicha Técnica: Sistemas de Drenagem ValsirNilton SousaAinda não há avaliações
- Manual de Instrução T500Documento88 páginasManual de Instrução T500Erisson100% (1)
- Vestibular 2023 - Prova 26-11-22Documento24 páginasVestibular 2023 - Prova 26-11-22Rafael OtavioAinda não há avaliações
- Trabalho e Energia Mecanica Energia Cinetica Energia Potencial GravitacionalDocumento17 páginasTrabalho e Energia Mecanica Energia Cinetica Energia Potencial GravitacionalortenciavasconcelosAinda não há avaliações
- Análise Estrutural Com o SAP 2000 PDFDocumento49 páginasAnálise Estrutural Com o SAP 2000 PDFDave CaramelloAinda não há avaliações
- A Linguagem AudiovisualDocumento70 páginasA Linguagem AudiovisualAline RodriguesAinda não há avaliações
- Exerc - Cios - REGRA - DE - TR - S - COMPOSTA - DIRETA - INVERSA - E - DIRETA - E - INVERSA 2Documento19 páginasExerc - Cios - REGRA - DE - TR - S - COMPOSTA - DIRETA - INVERSA - E - DIRETA - E - INVERSA 2Victoria DesanAinda não há avaliações
- Relatorio Tratamento TERMICODocumento9 páginasRelatorio Tratamento TERMICOThyago LopesAinda não há avaliações
- NBR 11853 - 91 (EB-2153) - CANC - Cabos para Autoveículos Com Isolação Extrudada de Cloreto de Polivinila, para Tensões Até 300V - 10pagDocumento10 páginasNBR 11853 - 91 (EB-2153) - CANC - Cabos para Autoveículos Com Isolação Extrudada de Cloreto de Polivinila, para Tensões Até 300V - 10pagClaudio LorenzoniAinda não há avaliações
- Matemática 5a 6a Série Apostila Treino Livre CompletaDocumento149 páginasMatemática 5a 6a Série Apostila Treino Livre CompletaOtacilio LangAinda não há avaliações
- Manual Utilizador Bee2fire v2Documento38 páginasManual Utilizador Bee2fire v2Alex MachadoAinda não há avaliações
- Ficha - Exercicios - Física Moderna - 2020Documento2 páginasFicha - Exercicios - Física Moderna - 2020HonestoAlarcoFranciscoMambrançaAinda não há avaliações
- Manual de InstruçõesDocumento100 páginasManual de InstruçõesDiego FreitasAinda não há avaliações
- Caldeira de Recuperação IIDocumento54 páginasCaldeira de Recuperação IIAgeu DE Souza Rosa100% (7)
- Ime - 2019 - 2020Documento14 páginasIme - 2019 - 2020Prof Rodrigo Fraga Resolvendo a FísicaAinda não há avaliações
- 1 LEI - CONCEITOS BAìSICOS DE TERMODINAMICADocumento50 páginas1 LEI - CONCEITOS BAìSICOS DE TERMODINAMICARigobertoAinda não há avaliações
- Aps de Trocadores de Calor - para A v1-2019-2Documento5 páginasAps de Trocadores de Calor - para A v1-2019-2PH Oli0% (1)
- Estudo Dirigido Atividade IDocumento19 páginasEstudo Dirigido Atividade IMarcio TexAinda não há avaliações
- Determinação Do Coeficiente de Dilatação Linear de Um MetalDocumento7 páginasDeterminação Do Coeficiente de Dilatação Linear de Um MetalNathan CunhaAinda não há avaliações