Destilao Fracionada (gua e acetona)
INTRODUO: A destilao fracionada serve para separar uma mistura homognea composta por dois lquidos, com ponto de ebulio prximos. Quando se destila uma mistura lquida homognea ideal, as primeiras fraes do destilado apresentam composio mais rica no componente mais voltil do que da mistura original. No decorrer da destilao, o ponto de ebulio da mistura sofre uma elevao gradual, uma vez que a composio do vapor se torna cada vez mais rica no componente menos voltil. Para purificar misturas deste tipo, seria necessrio separar as primeiras fraes do destilado, ricas no componente mais voltil. Estas fraes seriam novamente destiladas e as primeiras fraes novamente separadas. Este procedimento teria de ser repetido vrias vezes at que as primeiras fraes do destilado contivessem apenas o componente mais voltil. O processo acima descrito denominado destilao fracionada, e pode ser melhor compreendido pelo exame do diagrama de fases abaixo.
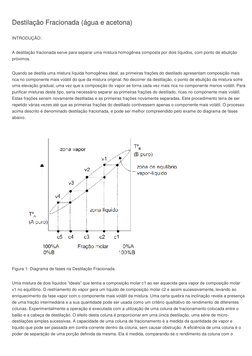
Figura 1: Diagrama de fases na Destilao Fracionada. Uma mistura de dois lquidos ideais que tenha a composio molar c1 ao ser aquecida gera vapor de composio molar v1 no equilbrio. O resfriamento do vapor gera um lquido de composio molar c2 e assim sucessivamente, levando ao enriquecimento da fase vapor com o componente mais voltil da mistura. Uma certa quebra na inclinao revela a presena de uma frao intermediria e a sua quantidade pode ser usada como um critrio qualitativo do rendimento de diferentes colunas. Experimentalmente a operao executada com a utilizao de uma coluna de fracionamento colocada entre o balo e a cabea de destilao. O efeito desta coluna proporcionar em uma nica destilao, uma srie de microdestilaes simples sucessivas. A capacidade de uma coluna de fracionamento a medida da quantidade de vapor e lquido que pode ser passada em contra-corrente dentro da coluna, sem causar obstruo. A eficincia de uma coluna o poder de separao de uma poro definida da mesma. Ela medida, comparando-se o rendimento da coluna com o
�calculado para uma coluna de pratos teoricamente perfeitos em condies similares. Um prato terico definido como sendo a seo de uma coluna de destilao de um tamanho tal que o vapor esteja em equilbrio com o lquido; isto , o vapor que deixa o prato tem a mesma composio que o vapor que entra e o vapor em ascendncia no prato est em equilbrio com o lquido descendente. O nmero de pratos tericos no pode ser determinado a partir das dimenses da coluna; computado a partir da separao efetuada pela destilao de uma mistura lquida, cujas composies de vapor e de lquido so conhecidas com preciso. Por exemplo, uma coluna com 12 pratos tericos satisfatria para a separao prtica de uma mistura de cicloexano e tolueno. H uma grande variedade de colunas de fracionamento, porm as mais encontradas nos laboratrios so as do tipo Vigreux e Hempel. A primeira um tubo de vidro com vrias reentrncias em forma de dentes, distribudas de modo que as pontas de um par de dentes quase se toquem. A coluna do tipo Hempel formada por um tubo de vidro empacotado com pequenas bolas ou anis de vidro, entre outros. A eficincia de uma coluna de fracionamento expressa pelo nmero de vezes que uma soluo vaporizada e recondensada durante a destilao ou nmero de pratos tericos, medido em termos de altura. Quanto menor for a altura equivalente a um prato terico (AEPT) tanto maior ser o nmero de pratos tericos da coluna e, portanto, mais eficiente ela ser. A escolha de uma coluna depende da diferena dos pontos de ebulio dos componentes da mistura. Quanto menor a diferena de ponto de ebulio, maior ser o nmero de pratos tericos necessrios para uma separao eficiente.
Figura 2: Representao esquemtica da aparelhagem de Destilao Fracionada. A acetona (tambm conhecida como dimetilcetona, 2-propanona, propan-2-ona ou simplesmente propanona) com frmula qumica CH3(CO)CH3, um composto orgnico sinttico que tambm ocorre naturalmente no meio ambiente. um lquido incolor de odor e sabor fceis de distinguir. Evapora facilmente, inflamvel e solvel em gua.J a gua uma substncia qumica composta de hidrognio e oxignio OBJETIVO: Separar dois lquidos miscveis atravs do procedimento de destilao fracionada. PROCEDIMENTO EXPERIMENTAL:
�-Montou-se o sistema de destilao; -Colocou-se no balo prolas de vidro e a mistura binria de lquidos volteis; -Iniciou-se o aquecimento -Quando o primeiro lquido comeou a ser separado anotou-se a temperatura; -Quando a temperatura comeou a variar trocou-se o frasco; - Mediu-se com a proveta o volume obtido no primeiro lquido, anotando este volume; -Quando a temperatura ficou novamente constante anotou-se a temperatura; -O lquido do frasco coletor desta vez foi descartado; -Reservou-se o lquido do balo, ps resfriar mediu-se o volume deste lquido; -Com os dados obtidos identificou- se os lquidos. RESULTADOS E DISCUSSES: Dados tabelados: SOLVENTES PEC
gua
100,0
Etanol
78,4
Acetona
56,5
ter etlico
34,6
Clorofrmio 61,3
Dados obtidos: Temperatura ambiente: 19C. Primeiro Lquido(substncia1) estabilizou a temperatura em 52 C obteve-se como volume final 31mL da substncia. O segundo lquido(substncia2) coletado teve sua temperatura estabilizada em 96 C, com um volume final de 56mL de substncia obtida.
�Comparando-se os dados obtidos com os tabelados, podemos dizer que a substncia 1 acetona, SegundoCRC-Handbook of Physics and Chemistry (ed) a temperatura de ebulio da acetona de 56,5C. Percebeu-se que o incio do gotejamento de soluo iniciou-se o termmetro indicava uma temperatura de aproximadamente 52 C e esta permaneceu constante por um longo perodo de tempo. Em um dado tempo o gotejamento cessou e a temperatura foi aumentando paulatinamente. Quando a temperatura atingiu aproximadamente 96 C o gotejamento reiniciou-se. Portanto, pode-se inferir que a primeira soluo cuja evaporao se deu a uma temperatura constante a 52 C refere-se acetona(fato que comprovado pelo odor desta soluo ser o caracterstico da acetona) e da substncia2 que ebuliu temperatura constante de 96 C, aproximadamente, sua composio refere-se da gua. Com relao aos volumes obtidos das substncias, obteve-se 31mL de acetona sendo que o volume correto seria 30mL, mas o valor obtido aceitvel, porm o volume obtido de gua no experimento teve erro pois dos 70mL que deveriam ter sido obtidos ,obtivemos apenas 56mL, sendo assim no est dentro de uma margem de erro pequena e sim uma grande, pois isso acarretou em um volume de 14mL que foram perdidos na destilao, o erro pode ter ocorrido devido a falta de constncia de temperatura e at mesmo uma impreciso na observao do termmetro. SUBSTNCIA 1: 30mL................100% 31mL................. X X= 103% SUBSTNCIA 2 : 70mL ...............100% 56mL................. X X= 80% CONCLUSO : A partir do experimento podemos concluir que as substncias se tratam de acetona sendo esta a mais voltil e gua(menos voltil),as temperaturas obtidas de ponto de ebulio nos permitiram concluir que se tratavam destas duas substncias, na realidade todos os lquidos so volteis. No entanto, para lquidos que apresentam presso de vapor muito baixa, a vaporizao chega a ser praticamente nula em expanses volumtricas rotineiras, nestes casos a fase gasosa no difere muito do vcuo ideal, o que est de acordo com o fato de a presso ser prxima a zero, o conceito de lquido voltil, como utilizado na prtica, um conceito comparativo, ou seja, um lquido voltil, em relao a outro, quando o grau de vaporizao do segundo for desprezvel em relao ao do primeiro, para condies experimentais semelhantes. Sendo que no caso da acetona o cheiro era bem caracterstico, o que tambm contribuiu para identificao. Apesar de terem ocorridos erros no experimento os resultados foram satisfatrios. REFERNCIAS:
�ZUBRICK, J.W. Manual de Sobrevivncia no laboratrio de qumica orgnica.6a Edio, L.T.C. Rio de Janeiro, 2005. LIDE,David R., et al. CRC- Handbook of Physics and Chemistry. 73rd Edition- Special Student Edition. 1992-1993. CRCPress, Bocahaton-Miami. USA. DIAS, Ayres Guimares. COSTA, M. A. da. GUIMARES, P. I. C. Guia Pratico de Qumica Orgnica. Volume I. Tcnicas e Procedimentos: Aprendendo a fazer. Editora Intercincia. Rio deJaneiro, 2004.