UNIVERSIDADE FEDERAL FLUMINENSE
GQA - Departamento de Química Analítica
Análise Instrumental I Experimental
CROMATOGRAFIA LÍQUIDA DE ALTA
EFICIÊNCIA (HPLC)
Aluna: Ursula Rodrigues Cabral
Professor: Marco Antonio Oliveira
Rio de Janeiro
30 de Junho de 2023
1
�1 INTRODUÇÃO
A cromatografia é uma técnica analítica utilizada para separar o analito dos constituintes
de uma mistura em uma amostra antes de sua detecção auxiliando assim na eliminação de
possíveis interferentes durante a medida do sinal analítico. Na cromatografia líquida de alta
eficiência, CLAE ou HPLC (High Performance Liquid Chromatography), são utilizadas duas
fases denominadas de fase móvel e fase estacionária. [1]
A fase estacionária é um líquido que é forçado a passar através da coluna com o uso de
pressão fornecida por uma bomba. A amostra é introduzida em um injetor com uso de
microsseringa e o injetor, que por sua vez, introduz a amostra na coluna onde os constituintes
da mesma são separados em bandas. No final da coluna, as bandas são detectadas por um
detector apropriado e os sinais gerados são registrados por um registrador. Além da coluna, o
aparelho também possui uma pré-coluna, que tem como objetivo evitar danos maiores a coluna
principal. Quanto maior o tamanho da coluna, maior número de pratos teóricos e com isso,
ocorre uma melhor separação e uma resolução do cromatograma mais eficiente. Os detectores
para CLAE podem ser são baseados na absorção da radiação ultravioleta ou visível,
espectrometria de massas, de fluorescência, entre outros. [1] [2]
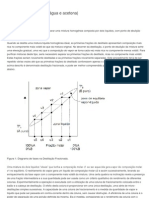
O diagrama de blocos abaixo (Figura 1) é um esquema simplificado de um cromatógrafo
a líquido. [1]
Figura 1. Diagrama esquemático simplificado de um cromatógrafo a líquido. [1]
A cromatográfica líquida de alta eficiência é uma técnica analítica utilizada para
determinação de diversos analitos em diferentes tipos de amostra com alta seletividade e
sensibilidade. É considerada um método eficiente, mas com grande custo operacional e com
análises que podem ser consideradas longas, já que dependem do tempo de eluição da amostra.
[2]
Após a análise, os picos obtidos são correlacionados com a identidade dos analitos com
base em seus tempos de retenção por simples comparação com os tempos obtidos na análise
2
�dos padrões presentes na curva de calibração. O sinal analítico é valido pela integração da área
do pico cromatográfico, quanto maior a área maior a concentração dos analitos na amostra. [1]
Figura 2. Cromatogramas de soluções padrão de cafeína sobrepostos. [3]
Uma cromatografia pode ser de fase normal ou fase reversa, diferenciadas pela
polaridade das fases. Na CLAE de fase reversa, a fase estacionária é apolar e a fase móvel é
polar ou contém um componente polar. A fase estacionária mais comum é uma sílica
quimicamente modificada com grupos C18 que confere caráter hidrofóbico à coluna. Os
compostos menos polares tendem a ser retidos com mais força pela fase estacionária, enquanto
os compostos mais polares são eluídos mais rapidamente. Cromatografias em fase reversa são
o mais comum no mundo atualmente. Uma eluição com um único solvente ou com uma mistura
de solventes de composição constante é isocrática. Na eluição por gradiente, dois (e às vezes
mais) sistemas solventes que diferem significativamente em polaridade são empregados. [2]
A cafeína é um alcaloide presente em diversos tipos de bebida e possui a seguinte
formula estrutural: [3]
Figura 3. Molécula da cafeína (1,3,7-trimetilxantina). [3]
3
�2 OBJETIVO
Os objetivos da prática foram plotar uma curva analítica com padrões de cafeína e
avaliação de seus parâmetros e a determinação da concentração de cafeína em uma amostra de
bebida energética utilizando calibração externa.
3 METODOLOGIA
Todas as amostras para análise foram preparadas previamente (banho ultrassônico,
filtração a vácuo).
No cromatógrafo, foram adicionadas soluções de distintas concentrações, 5, 10, 25 e 50
ppm, separadamente utilizando uma microsseringa e um volume de 60-80 μL. Após inserir a
amostra para análise, a válvula era girada, a corrida cromatográfica iniciava e após um
determinado tempo, aparecia um sinal no computador ligado ao cromatógrafo. Esse processo
foi realizado para todas as concentrações e para a amostra de TNT.
O perfil do cromatograma apresentou áreas crescentes à medida que se aumentava a
concentração de cafeína. As condições do método de cromatografia líquida de alta eficiência
foram realizadas da seguinte maneira: Cromatógrafo a líquido Shimadzu Prominence modo
isocrático operando em coluna de C18 e detecção no UV-Vis (𝜆 = 273 𝑛𝑚 𝑒 250 𝑛𝑚); Coluna
de C18 Shim-pack VP-ODS (P/N 228-34937-92): 250 x 4,6 mm i.d., tamanho da partícula 4,60
um; fase móvel composta de Metanol:Água (50:50, v/v), com vazão de 0,6 mL/min.
4 RESULTADOS E DISCUSSÃO
4.1 TABELA
Após as corridas cromatográficas, foi possível observar que o ponto de maior
sensibilidade para a cafeína foi em 273 nm. O tempo de retenção da cafeína foi de
aproximadamente 7,7 minutos. Na corrida cromatográfica da análise de TNT, foi possível
observar outros sinais além do pico da cafeína no mesmo comprimento de onda, referente aos
outros componentes da bebida.
A partir dos resultados obtidos nas corridas cromatográficas foi possível saber a área do
pico de cada amostra analisada e, assim, construir a tabela abaixo.
4
� Tabela 1. Valores da área obtidos a partir do cromatograma das soluções padrão de cafeína e da
amostra.
Concentração (ppm) Área (u. A.)
5 548247
10 1051125
25 2681301
50 5318503
Amostra 1979960
4.2 GRÁFICOS
A partir dos valores obtidos na tabela, foi possível construir um gráfico da curva
analítica e a partir da equação da reta de regressão linear, determinar a concentração da amostra
de energético.
Gráfico 1. Curva de calibração em função da área do pico versus a concentração.
A equação da reta obtida a partir do gráfico (𝑦 = 106309𝑥 + 7838,3) permite calcular
a concentração de cafeína na amostra, considerando que 𝑦 = á𝑟𝑒𝑎 𝑑𝑜 𝑝𝑖𝑐𝑜 𝑑𝑎 𝑎𝑚𝑜𝑠𝑡𝑟𝑎.
𝑦 = 106309𝑥 + 7838,3
1979960 = 106309𝑥 + 7838,3
𝑚𝑔
𝑥 = 18,55
𝐿
A amostra do energético estava diluída (5% v/v), então a concentração de cafeína na
amostra original é:
5
� 18,55 − − − − − − − 5%
𝑥 − − − − − − 100%
𝑚𝑔
𝑥 = 371,02 𝑑𝑒 𝑐𝑎𝑓𝑒í𝑛𝑎 𝑛𝑎 𝑎𝑚𝑜𝑠𝑡𝑟𝑎.
𝐿
O rótulo do energético da marca TNT indica que a quantidade de cafeína presente é de
70 mg/200 mL, logo:
70 𝑚𝑔 − − − −200 𝑚𝐿
𝑦 − − − − 1000 𝑚𝐿
𝑚𝑔
𝑦 = 350 𝑑𝑒 𝑐𝑎𝑓𝑒í𝑛𝑎 𝑛𝑜 𝑇𝑁𝑇.
𝐿
Calculada todas as concentrações é possível calcular o erro relativo da técnica:
371,02 − 350
𝐸𝑟𝑟𝑜𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = × 100
350
𝐸𝑟𝑟𝑜𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = 6,00%
5 CONCLUSÃO
Em conclusão, a prática utilizando demonstrou ser eficaz na determinação da
concentração de cafeína em uma amostra de bebida energética. A curva analítica plotada
permitiu a avaliação dos parâmetros necessários para uma análise precisa, fornecendo uma base
confiável para a quantificação da cafeína presente na amostra. Com base na concentração de
cafeína obtida experimentalmente, pôde-se realizar a comparação com o valor descrito no rótulo
do energético. Os resultados obtidos revelaram que a concentração de cafeína na amostra
analisada foi de 371,02 ppm, enquanto o rótulo do produto indicava uma concentração
declarada de 350 ppm.
Assim, o valor experimental encontra-se acima do valor mencionado no rótulo do
produto. Tal distância entre os valores pode ser explicada por alguns fatores como: preparação
inadequada da amostra, precisão das soluções padrão, calibração inadequada, contaminação do
sistema, variações na condição de análise e erros de medição ou detecção. É importante destacar
que a identificação das possíveis causas de erros requer uma análise criteriosa de todo o
procedimento analítico, desde a preparação da amostra até a análise propriamente dita. A
6
�utilização de controles de qualidade, como análises de brancos, padrões adicionais e replicatas,
também é recomendada para avaliar a precisão e a exatidão dos resultados obtidos. [2] [4]
6 REFERÊNCIAS
[1] “Apostila de Análise Instrumental I Experimental,” GQA, Niterói, 2020.
[2] D. A. Skoog, D. M. West, F. J. Holler e S. R. Crouch, Fundamentos de
Química Analítica, São Paulo: Thomson, 2009.
[3] A. Fuentes López, E. García Martínez e C. Fuentes López, “Determinación
de cafeína en café mediante cromatografía líquida de alta resolución (HPLC)”.
[4] D. C. Harris, Análise Química Quantitativa, LTC, 2017.
[5] N. Tro's, Chemistry: A Molecular Approach, 5ª ed., Pearson, 2019.