Escolar Documentos
Profissional Documentos
Cultura Documentos
Equilíbrios Químicos
Enviado por
Aline Katiane Freire0 notas0% acharam este documento útil (0 voto)
63 visualizações9 páginasslides de equilibrio químico
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PPTX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoslides de equilibrio químico
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
63 visualizações9 páginasEquilíbrios Químicos
Enviado por
Aline Katiane Freireslides de equilibrio químico
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
Você está na página 1de 9
EQUILÍBRIOS QUÍMICOS
REAÇÕES IRREVERSÍVEIS E REVERSÍVEIS
Reação irreversível é aquela em que não se pode ter
regeneração dos produtos em reagentes, ou seja, ela não pode ser
revertida.
EXEMPLO: papel + O2 → CO2 + H2O
Reação reversível é a reação na qual os reagentes se
transformam nos produtos, e estes, à medida que se formam,
regeneram os reagentes iniciais.
EXEMPLO:
CO (g) + NO2 (g) → CO2 (g) + NO (g)
CO2 (g) + NO (g) → CO (g) + NO2 (g)
No exemplo anterior nada impede que as duas reações ocorram
simultaneamente, logo podemos afirmar que:
Reação reversível é aquela que se processa simultaneamente
nos dois sentidos.
CONCEITO DE EQUILÍBRIO QUÍMICO
Equilíbrio químico é o estado no qual as velocidades das
reações direta e inversa se igualam.
CO (g) + NO2 (g) V1 V2 CO2 (g) + NO (g)
EQUILÍBRIOS HOMOGÊNEOS E HETEROGÊNEOS
EQUILÍBRIOS HOMOGÊNEOS : ocorre quando todos os reagentes e
produtos se apresentam na mesma fase de agregação.
Exemplo: N2(g) + 3 H2(g) ↔ 2 NH3(g)
EQUILÍBRIOS HETEROGÊNEOS : ocorre quando os reagentes e produtos
apresentas fases de agregação diferentes.
Exemplo: HCl(aq) + AgNO3(aq) ↔ AgCl(s) + HNO3(aq)
Observação:
- A pressão do sistema em equilíbrio só será alterada por substâncias
gasosas, as substâncias sólidas e liquidas quando adicionadas ao
sistema não altera a pressão.
EXERCÍCIOS
Página 120
Questão 1
Questão 2
Questão 3
Questão 4
Questão 5
Questão 6
CONSTANTE DE EQUILÍBRIO
Dada a reação genérica:
aA + bB cC + dD
Temos:
V 1 = k 1 [ A ] a [ B ]b e V2 = k2 [ C ]c [ D ]d
Quando V1 for igual a V2(V1 = V2), temos:
k1 [ A ]a [ B ]b = k2 [ C ]c [ D ]d , Isolando as constantes:
k1 = [ C ]c [ D ]d Kc = [ C ]c [ D ]d (produtos)
k2 [ A ]a [ B ]b [ A ]a [ B ]b (reagentes)
Aplicando a fórmula da constante para o equilíbrio
CO (g) + NO2 (g) CO2 (g) + NO (g)
Temos:
Kc = __[CO2] [NO]_
[CO] [NO2]
A constante de equilíbrio em função das concentrações em mol/L é o
produto das concentrações dos produtos da reação dividido pelo produto
das concentrações dos reagentes, todas elevadas a expoentes iguais aos seus
coeficientes na equação química considerada.
Observação:
Na expressão de Kc, não são representadas as concentrações de
sólidos nem as de líquidos
EXERCÍCIOS EM SALA DE AULA
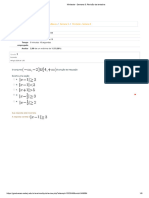
Escreva as expressões matemáticas da constante Kc, dando
as respectivas unidades, dos seguintes equilíbrios em
fase gasosa:
a) N2O4 ↔ 2 NO2
b) 2 CO + O2 ↔ 2 CO2
c) C(s) + O2(g) ↔ CO2(g)
d) H2 + I2 ↔ 2 HI
e) 2 N2H4 + 2 NO2 ↔ 3 N2 + 4 H2O
f) HCl(aq) + AgNO3(aq) ↔ AgCl(s) + HNO3(aq)
Você também pode gostar
- IFPB - Campus João Pessoa Química: Equilíbrio QuímicoDocumento29 páginasIFPB - Campus João Pessoa Química: Equilíbrio QuímicoMaysa AlessandraAinda não há avaliações
- Apostila Equilíbrio QuímicoDocumento5 páginasApostila Equilíbrio QuímicoAmanda SoteroAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Fisico Quimica Slides 2Documento60 páginasFisico Quimica Slides 2BRITTO12Ainda não há avaliações
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- Equilíbrio Químico-Lq2Documento49 páginasEquilíbrio Químico-Lq2Pedro H. FassarellaAinda não há avaliações
- Equilibrio PpsDocumento85 páginasEquilibrio PpsLarissa SantosAinda não há avaliações
- Eq. QuímicoDocumento82 páginasEq. QuímicoFábio Luiz SeribeliAinda não há avaliações
- Equilibrio Químico, Iônico, PHDocumento103 páginasEquilibrio Químico, Iônico, PHRomeuComastriAbdalaAinda não há avaliações
- Equilíbrio QuímicoDocumento40 páginasEquilíbrio QuímicovictorhugonenseAinda não há avaliações
- Equilíbrio QuímicoDocumento43 páginasEquilíbrio QuímicoSarah MartinsAinda não há avaliações
- Química Analítica Qualitativa I (3a Aula Equilibrio) PDFDocumento37 páginasQuímica Analítica Qualitativa I (3a Aula Equilibrio) PDFJonatha SantosAinda não há avaliações
- EquilibrioDocumento85 páginasEquilibrioRobson SilvaAinda não há avaliações
- Equilibrio Resumo PDFDocumento8 páginasEquilibrio Resumo PDFMatiasWakaMalembeAinda não há avaliações
- Aula11 Equilibrio QuimicoDocumento38 páginasAula11 Equilibrio QuimicoscreamoutAinda não há avaliações
- Unidade 5-Cinetica e Equilibrio Quimico-Parte B-2021Documento20 páginasUnidade 5-Cinetica e Equilibrio Quimico-Parte B-2021Pedro RosárioAinda não há avaliações
- 5 - Equilíbrio QuímicoDocumento40 páginas5 - Equilíbrio QuímicoAdemir PereiraAinda não há avaliações
- Aula 3 - Equilíbrio QuímicoDocumento28 páginasAula 3 - Equilíbrio QuímicoThadilla SouzaAinda não há avaliações
- EquilibrioDocumento46 páginasEquilibrioBianca conceiçãoAinda não há avaliações
- Helio Trabalho de QuimicaDocumento9 páginasHelio Trabalho de QuimicaHélio BorgesAinda não há avaliações
- Equilíbrio Químico 2Documento52 páginasEquilíbrio Químico 2Sergio Gabriel Souza ZanonAinda não há avaliações
- Equilibrio Quimico 1Documento7 páginasEquilibrio Quimico 1Leonel PaulinoAinda não há avaliações
- Equilíbrio QuímicoDocumento13 páginasEquilíbrio QuímicoRadcliffe LimaAinda não há avaliações
- Apostila Equilíbrio Químico (1) ..Documento5 páginasApostila Equilíbrio Químico (1) ..goldminer2Ainda não há avaliações
- Aula08 - Equilíbrios QuímicosDocumento43 páginasAula08 - Equilíbrios QuímicosLAURA PALADINOAinda não há avaliações
- 151417-AULA - IFRN-equil - Quim - 1 - 1Documento41 páginas151417-AULA - IFRN-equil - Quim - 1 - 1Débora WeberAinda não há avaliações
- Topico 11 - EquilibrioDocumento47 páginasTopico 11 - EquilibrioJuliano15rockAinda não há avaliações
- 6 ConstanteEquilibrioDocumento20 páginas6 ConstanteEquilibrioRute FidalgoAinda não há avaliações
- Equilibrio Quimico KC e KPDocumento2 páginasEquilibrio Quimico KC e KPjparatyAinda não há avaliações
- Equilíbrio QuímicoDocumento59 páginasEquilíbrio QuímicoGustavo Nazareno MonteiroAinda não há avaliações
- Equilíbrio QuímicoDocumento25 páginasEquilíbrio QuímicoMilkelison LavorAinda não há avaliações
- Equilibrio QuimicoDocumento11 páginasEquilibrio QuimicoMonica Elias100% (1)
- 2018 - Equilíbrio QuímicoDocumento83 páginas2018 - Equilíbrio QuímicoAugusto TanamatiAinda não há avaliações
- Aula Eq Quimico 2 INFDocumento145 páginasAula Eq Quimico 2 INFIcy GreekAinda não há avaliações
- Equilibrio QuimicoDocumento33 páginasEquilibrio QuimicoThamilis AguiarAinda não há avaliações
- Equilibrio QuímicoDocumento24 páginasEquilibrio QuímicoMatson EdwardsAinda não há avaliações
- Thomas Vest F2 Aula 22 Equilibrio Quimico Kce KPDocumento2 páginasThomas Vest F2 Aula 22 Equilibrio Quimico Kce KPPaula AyabeAinda não há avaliações
- Caderno de QuimicaDocumento9 páginasCaderno de QuimicaUelder Jeferson SantosAinda não há avaliações
- Aula Equilíbrio QuímicoDocumento32 páginasAula Equilíbrio QuímicoRodrigo LuizAinda não há avaliações
- Química - Equilíbrio QuímicoDocumento29 páginasQuímica - Equilíbrio QuímicoANHAN ANA SilVAAinda não há avaliações
- 5 EquilibrioDocumento77 páginas5 EquilibrioGleison Paulino GonçalvesAinda não há avaliações
- Equilibrio Quimico CompletoDocumento56 páginasEquilibrio Quimico CompletoEvisson de S. TavaresAinda não há avaliações
- 2T.EQUILIBRIO MOLECULAR - Apostilaconteúdo.exercícios.2023Documento10 páginas2T.EQUILIBRIO MOLECULAR - Apostilaconteúdo.exercícios.2023Iara DaherAinda não há avaliações
- Equilibrio QuimicoDocumento44 páginasEquilibrio QuimicoJohnatas MathewsAinda não há avaliações
- AULA 3 - Equilíbrio QuímicoDocumento40 páginasAULA 3 - Equilíbrio Químicofel198337Ainda não há avaliações
- Aula - Equilibrio QuimicoDocumento18 páginasAula - Equilibrio QuimicoWellen BarbosaAinda não há avaliações
- Resumo Quimica Geral IIDocumento7 páginasResumo Quimica Geral IIElaine NiedzielskiAinda não há avaliações
- Pcasd - Uploads - Rogerio - Arquivos - Lista 12 - Equilbrio Qumico - Constante de Equlibrio KCDocumento9 páginasPcasd - Uploads - Rogerio - Arquivos - Lista 12 - Equilbrio Qumico - Constante de Equlibrio KCRaisson HolandaAinda não há avaliações
- Equilibrio Químico 1pptDocumento73 páginasEquilibrio Químico 1pptamanda mirandaAinda não há avaliações
- Ficha de Equilíbrio Químico IDocumento14 páginasFicha de Equilíbrio Químico IdornelioheldermAinda não há avaliações
- Basica Equilibrio TeoriaDocumento26 páginasBasica Equilibrio TeoriaErica ItoAinda não há avaliações
- Acerto EquacoesDocumento8 páginasAcerto EquacoesanitadiogoAinda não há avaliações
- Lista de Exercícios - Equilíbrios QuímicosDocumento15 páginasLista de Exercícios - Equilíbrios QuímicosLucas GarceteAinda não há avaliações
- Aula 6 - Equilibrio QuímicoDocumento99 páginasAula 6 - Equilibrio QuímicoAbner AlmeidaAinda não há avaliações
- AULA 16 - Equilibrio Quimico Quimica GeralMET1832Documento18 páginasAULA 16 - Equilibrio Quimico Quimica GeralMET1832Victor MarcosAinda não há avaliações
- CAPITULO VII - Equilibrio QuimicDocumento9 páginasCAPITULO VII - Equilibrio QuimicHélder ViegasAinda não há avaliações
- Spm@Testes: Matriz de Referência 12.º AnoDocumento4 páginasSpm@Testes: Matriz de Referência 12.º AnoNocasAinda não há avaliações
- Lista 1 - Dimensionamento de CanaisDocumento2 páginasLista 1 - Dimensionamento de CanaisRenato AsprinoAinda não há avaliações
- CoerênciaDocumento5 páginasCoerênciaRafael GuañabensAinda não há avaliações
- Desafios Matemática Fundamental IDocumento17 páginasDesafios Matemática Fundamental Iosnildo carvalhoAinda não há avaliações
- Aula 2 SegurancaDocumento27 páginasAula 2 SegurancaHeeulerAinda não há avaliações
- 03 - Vetores No EspaçoDocumento19 páginas03 - Vetores No EspaçoMarcelo MottaAinda não há avaliações
- Lista Geo 2Documento6 páginasLista Geo 2clodonilda ferreiraAinda não há avaliações
- Miniteste - Semana 5 - Revisão Da TentativaDocumento6 páginasMiniteste - Semana 5 - Revisão Da TentativaManoel SantanaAinda não há avaliações
- Ler e Escrever - Jornada Da MatemáticaDocumento162 páginasLer e Escrever - Jornada Da MatemáticaAna DieguezAinda não há avaliações
- Apostila Legislação e Segurança Do Trabalho PDFDocumento79 páginasApostila Legislação e Segurança Do Trabalho PDFLeandro CostaAinda não há avaliações
- Determinação Da Constante de Velocidade e Tempo de Meia Vida Da Reação de Decomposição Do Peróxido de HidrogênioDocumento18 páginasDeterminação Da Constante de Velocidade e Tempo de Meia Vida Da Reação de Decomposição Do Peróxido de HidrogênioLeonardo FreitasAinda não há avaliações
- StataDocumento9 páginasStataNadielle BiduAinda não há avaliações
- NBR 10662 - Isolantes Termicos Dos de Silicato de CalcioDocumento9 páginasNBR 10662 - Isolantes Termicos Dos de Silicato de CalcioBarbara Gama FariasAinda não há avaliações
- Problema de Alocação de Salas de Aulas - Uma Abordagem Via Algoritmos GenéticosDocumento7 páginasProblema de Alocação de Salas de Aulas - Uma Abordagem Via Algoritmos GenéticosLeandro PereiraAinda não há avaliações
- Revisado 2.0Documento9 páginasRevisado 2.0RonyeAinda não há avaliações
- ObjetivoDocumento93 páginasObjetivolucasAinda não há avaliações
- 99.matemática 4ºDocumento6 páginas99.matemática 4ºWillyaneAlcantaraAinda não há avaliações
- Leis Complementares Zoneamento Ouro PretoDocumento22 páginasLeis Complementares Zoneamento Ouro PretoPaola SimonatoAinda não há avaliações
- MatematicaDocumento13 páginasMatematicaAquenio IreneuAinda não há avaliações
- FTP VentiladoresDocumento8 páginasFTP VentiladoresPaulo FerreiraAinda não há avaliações
- NBR 6403 (Jun 1992) - Séries de Números NormalizadosDocumento4 páginasNBR 6403 (Jun 1992) - Séries de Números NormalizadosYuri Bahia de Vasconcelos100% (2)
- Racional Ou HiperacionalDocumento36 páginasRacional Ou HiperacionalAlexandrino Rosa de SouzaAinda não há avaliações
- Argumentar, Inferir e DeduzirDocumento21 páginasArgumentar, Inferir e DeduzirJosé Alexandre Durry GuerzoniAinda não há avaliações
- Matemática - 1º Ano Eja - Semana 1Documento5 páginasMatemática - 1º Ano Eja - Semana 1barbara.c.gomesAinda não há avaliações
- Aula24 PDFDocumento13 páginasAula24 PDFJohn PiterAinda não há avaliações
- Atividadei - 1 - RecuperaçãoDocumento5 páginasAtividadei - 1 - RecuperaçãoPaulo Cec Figueredo20% (5)
- Manual Access 2007Documento37 páginasManual Access 2007Antonio Manuel SaramagoAinda não há avaliações
- Aula 3 Teoria Do Consumidor Introducao A EconomiaDocumento10 páginasAula 3 Teoria Do Consumidor Introducao A EconomiaEmilio MaocheAinda não há avaliações
- Introdução A AcústicaDocumento78 páginasIntrodução A AcústicaAngoAcoustics Som & AcústicaAinda não há avaliações
- 1 - Herança e PolimorfismoDocumento16 páginas1 - Herança e PolimorfismoMilton AguiarAinda não há avaliações
- Os Códigos do Mindset da Prosperidade: destrave os bloqueios em sua mente e cresça em todos os aspectos de sua vidaNo EverandOs Códigos do Mindset da Prosperidade: destrave os bloqueios em sua mente e cresça em todos os aspectos de sua vidaAinda não há avaliações
- Psicologia sombria: Poderosas técnicas de controle mental e persuasãoNo EverandPsicologia sombria: Poderosas técnicas de controle mental e persuasãoNota: 4 de 5 estrelas4/5 (92)
- Focar: Supere a procrastinação e aumente a força de vontade e a atençãoNo EverandFocar: Supere a procrastinação e aumente a força de vontade e a atençãoNota: 4.5 de 5 estrelas4.5/5 (53)
- Elaboração de programas de ensino: material autoinstrutivoNo EverandElaboração de programas de ensino: material autoinstrutivoAinda não há avaliações
- Técnicas Proibidas de Manipulação Mental e PersuasãoNo EverandTécnicas Proibidas de Manipulação Mental e PersuasãoNota: 5 de 5 estrelas5/5 (3)
- Treinamento cerebral: Como funcionam a inteligência e o pensamento cognitivo (2 em 1)No EverandTreinamento cerebral: Como funcionam a inteligência e o pensamento cognitivo (2 em 1)Nota: 4.5 de 5 estrelas4.5/5 (29)
- O psicólogo clínico em hospitais: Contribuição para o aperfeiçoamento da arte no BrasilNo EverandO psicólogo clínico em hospitais: Contribuição para o aperfeiçoamento da arte no BrasilAinda não há avaliações
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNo EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisNota: 4.5 de 5 estrelas4.5/5 (169)
- E-TRAP: entrevista diagnóstica para transtornos de personalidadeNo EverandE-TRAP: entrevista diagnóstica para transtornos de personalidadeNota: 5 de 5 estrelas5/5 (3)
- Diálogo entre Terapia do Esquema e Terapia Focada na Compaixão: Contribuição à integração em Psicoterapias Cognitivo-ComportamentaisNo EverandDiálogo entre Terapia do Esquema e Terapia Focada na Compaixão: Contribuição à integração em Psicoterapias Cognitivo-ComportamentaisNota: 5 de 5 estrelas5/5 (1)
- Inteligência artificial: O guia completo para iniciantes sobre o futuro da IANo EverandInteligência artificial: O guia completo para iniciantes sobre o futuro da IANota: 5 de 5 estrelas5/5 (6)
- Como aprender mais rápido: Métodos e dicas para se tornar mais inteligenteNo EverandComo aprender mais rápido: Métodos e dicas para se tornar mais inteligenteNota: 3.5 de 5 estrelas3.5/5 (8)
- Focar: Elimine distrações, perfeccionismo e faça maisNo EverandFocar: Elimine distrações, perfeccionismo e faça maisNota: 5 de 5 estrelas5/5 (21)
- Psicanálise de boteco: O inconsciente na vida cotidianaNo EverandPsicanálise de boteco: O inconsciente na vida cotidianaNota: 5 de 5 estrelas5/5 (1)
- Vou Te Ajudar A Fazer As Pessoas Clicar No Seu LinkNo EverandVou Te Ajudar A Fazer As Pessoas Clicar No Seu LinkNota: 5 de 5 estrelas5/5 (1)