Escolar Documentos
Profissional Documentos
Cultura Documentos
Al3 3-Areal
Enviado por
iolaTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Al3 3-Areal
Enviado por
iolaDireitos autorais:
Formatos disponíveis
lOMoARcPSD|17843307
DOSSIÊ DO PROFESSOR FÍSICA A 10
GUIÕES DE EXPLORAÇÃO DAS ATIVIDADES LABORATORIAIS
ATIVIDADE LABORATORIAL 3.3.
Balanço energético num sistema termodinâmico
OBJETIVO GERAL
Estabelecer balanços energéticos e determinar a entalpia de fusão do gelo.
METAS ESPECÍFICAS
1. Prever a temperatura final da mistura de duas massas de água a temperaturas diferentes e comparar com
o valor obtido experimentalmente.
2. Medir massas e temperaturas.
3. Estabelecer balanços energéticos em sistemas termodinâmicos aplicando a Lei da Conservação da
Energia, interpretando o sinal positivo ou negativo da variação da energia interna do sistema.
4. Medir a entalpia de fusão do gelo e avaliar a exatidão do resultado a partir do erro percentual.
EXPLORAÇÃO DA ATIVIDADE LABORATORIAL
QUESTÕES PRÉ-LABORATORIAIS
1. Qual é o principal mecanismo de transferência de energia que ocorre quando se misturam duas massas de
água a temperaturas iniciais diferentes?
Transferência de energia sob a forma de calor, por condução e convecção, da água a maior
temperatura para a água a menor temperatura.
2. Obtenha a expressão da temperatura final da mistura de duas massas de água m1 e m2, com temperaturas
iniciais diferentes, respetivamente, T1 e T2, sabendo que m1 é quatro vezes maior do que de m2 e T2 é 20 ºC
superior a T1. Considere desprezáveis as transferências de energia com o meio envolvente.
A temperatura final deverá ser igual para as duas massas de água e terá um valor intermédio das
duas temperaturas iniciais. No entanto, não será uma temperatura média pois trata-se de massas
diferentes logo a temperatura final deverá ser mais próxima da temperatura inicial da água com
maior massa, a qual necessita de mais energia para variar a temperatura.
Δ = 0 ⇔ Δá = − Δá ⇔
⇔ Δ = − Δ ⇒
⇒ Δ = − Δ ⇔
⇔ 4 − = − − ( + 20) ⇔
⇔ 4 − 4 = − + + 20 ⇔
! "# $ %
⇔ 5 = 5 + 20 ⇔ = !
℃
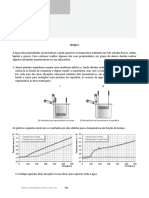
3. Considere um recipiente com água à temperatura ambiente, à qual se adicionou água no estado sólido (um
cubo de gelo), a uma temperatura de 0 °C. Apresente um esboço do perfil do gráfico da temperatura da água,
inicialmente no estado sólido, em função do tempo, T = f(t), até que esta atinja o equilíbrio térmico.
1
© Areal Editores
Downloaded by Luis Jesus (luisduartejesus@gmail.com)
lOMoARcPSD|17843307
DOSSIÊ DO PROFESSOR FÍSICA A 10
GUIÕES DE EXPLORAÇÃO DAS ATIVIDADES LABORATORIAIS
4. Relativamente à questão anterior, a energia que é fornecida ao cubo de gelo, sob a forma de calor,
apresenta duas parcelas. Identifique-as.
A primeira parcela corresponde à energia necessária à fusão do gelo e a segunda à energia
necessária à elevação da temperatura já no estado líquido, desde os 0 °C até ser atingido o
equilíbrio térmico.
5. Quando um cubo de gelo, à temperatura de fusão, é adicionado a uma bebida, à temperatura ambiente, de
onde provém a energia utilizada para fundir o cubo de gelo?
É transferida energia da bebida para o cubo de gelo.
6. Na realização desta atividade sugere-se a utilização de um calorímetro, recipiente de paredes finas
envolvido por outro recipiente de paredes mais grossas e isolantes. Qual a finalidade do uso deste
equipamento na atividade?
O calorímetro evita transferências de energia, sob a forma de calor, entre o mesmo e o meio
ambiente, aproximando o sistema em estudo de um sistema isolado.
REGISTO E TRATAMENTO DE RESULTADOS
Exemplos de valores obtidos na realização da atividade.
Tabela I – Incertezas de leitura
Instrumento de medida Grandeza medida Incerteza de leitura
Termómetro Temperatura ' 0,5 °C
3
Balança digital Massa ' 0,01 × 10− kg
Tabela II – Registo dos resultados da mistura de duas massas de água
mágua / kg Ti / °C Tf / °C
Água fria −3
120,72 × 10 24,5
−3
27,8
Água quente 30,50 × 10 44,8
Tabela III – Registo de resultados da mistura de água com gelo
mágua / kg Ti / °C Tf / °C
Água quente −3
120,17 × 10 45,4
−3
23,2
Gelo 20,66 × 10 0,0
2
© Areal Editores
Downloaded by Luis Jesus (luisduartejesus@gmail.com)
lOMoARcPSD|17843307
DOSSIÊ DO PROFESSOR FÍSICA A 10
GUIÕES DE EXPLORAÇÃO DAS ATIVIDADES LABORATORIAIS
1. Efetue o balanço energético para cada uma das duas massas de água, identificando os sistemas que
recebem e que fornecem energia.
Δá = Δ ⇒
⇒ Δá = 30,50 × 10,- × 4186 × (27,8 − 44,8) ⇔
⟺ Δá = − 2,17 × 10- J
< 4 porque a água quente cede energia, sob a forma de calor, à água fria, por se encontrar a
maior temperatura, consequentemente, a variação de energia interna da água quente será
negativa
Δá = Δ ⇒
⇒ Δá = 120,72 × 10,- × 4186 × (27,8 − 24,5) ⟺
⇔ Δá = 1,67 × 10- J
> 4, atendendo a que a água fria recebe energia sob a forma de calor até se atingir o equilíbrio
térmico. Consequentemente, a variação de energia interna da água fria será positiva.
2. Determine a energia transferida para o gelo a 0 °C, considerando o sistema isolado.
∆ = 0 ⇔ ∆78 + ∆á = 0 ⟺ ∆78 = −∆á ⟺
⟺ ∆78 = − m c ∆Tá<=> ⟹
⟹ ∆78 = − 120,17 × 10,- × 4186 × (23,2 − 45,4) = 1,12 × 10@ J
QUESTÕES PÓS-LABORATORIAIS
1. Determine o valor teoricamente previsto da temperatura final da mistura das duas massas de água (água fria
e água quente), se o sistema fosse perfeitamente isolado, e compare-o com o valor obtido experimentalmente.
Δ = 0 ⇔ Δá = − Δá ⇔
⇔ Δ = − Δ ⇒
⇒ Δ = − Δ ⇔
⇔ 120,72 × 10,- × − 24,5 = − 30,50 × 10,- × − 44,8 ⇔
⇔ 120,72 × 10,- − 2,96 = −30,50 × 10,- + 1,37 ⇔
4,33
⇔ = = 28,7 ℃
0,151
A temperatura final da água obtida experimentalmente é inferior ao valor previsto teoricamente, uma
vez que ao efetuar o cálculo não é tido em consideração a dissipação de energia, ou seja, as perdas
de energia para o meio envolvente.
2. Determine a variação da energia interna do sistema constituído pelas duas massas de água e interprete o
sinal do resultado obtido.
Δ = Δá + Δá ⇔
⇔ Δ = − 2,17 × 10- + 1,67 × 10- = − 5,00 × 10 J
A variação de energia interna do sistema deverá ser negativa porque como o equilíbrio térmico se
atinge a uma temperatura superior à temperatura ambiente é transferida energia do sistema para a
vizinhança.
Note-se que se adotaram estratégias para evitar esta transferência de energia, não sendo contudo
possível ter um sistema perfeitamente isolado.
3. Atendendo à energia transferida para o gelo a 0 ºC e considerando o sistema isolado, determine a variação
de entalpia de fusão do gelo.
3
© Areal Editores
Downloaded by Luis Jesus (luisduartejesus@gmail.com)
lOMoARcPSD|17843307
DOSSIÊ DO PROFESSOR FÍSICA A 10
GUIÕES DE EXPLORAÇÃO DAS ATIVIDADES LABORATORIAIS
Desprezando a dissipação de energia:
Δ = 0 ⇔ Δ78 + Δá = 0 ⇔
⇔ Δ78 = − Δá ⇔ Δ78 = 1,12 × 10@ J
Como:
Δ78 = ΔBã8 + Δá ⇒
⇒ Δ78 = ΔBã8 + Δá ⇔
⇔ 1,12 × 10@ = 78 ΔD + 78 Δ78 ⇔
⇔ 1,12 × 10@ = 20,66 × 10,- ΔD + 20,66 × 10,- × 4186 × (23,2 − 0) ⇔
⇔ ΔD = 4,45 × 10! J kg ,
4. Compare o valor obtido experimentalmente com o valor tabelado para a entalpia de fusão do gelo,
determinando o erro percentual. A que se pode dever esta diferença?
|valor experimental − valor teórico|
G = ⇒
valor teórico
|4,45 × 10! − 3,33 × 10! |
⇒ G = = 0,336 ⇔ G = 33,6%
3,33 × 10!
A diferença entre o valor obtido experimentalmente com o valor tabelado para a entalpia de fusão do
gelo deve-se uma vez mais, a que não é tido em consideração a dissipação de energia, embora, na
realidade, esta parcela não possa ser desprezada.
4
© Areal Editores
Downloaded by Luis Jesus (luisduartejesus@gmail.com)
Você também pode gostar
- AL 3.3 - Balanço Energético1 - ResoluçãoDocumento4 páginasAL 3.3 - Balanço Energético1 - ResoluçãoSofia FigueiredoAinda não há avaliações
- Guiao Expl Al 3 3 QDocumento5 páginasGuiao Expl Al 3 3 QDiogoAinda não há avaliações
- A.L. 3.3 - Balanço Energético Num Sistema TermodinâmicoDocumento20 páginasA.L. 3.3 - Balanço Energético Num Sistema Termodinâmicomaria ferreiraAinda não há avaliações
- Apoio Às Atividades Laboratoriais - AL 3.3 Balanço Energético Num Sistema TermodinâmicoDocumento5 páginasApoio Às Atividades Laboratoriais - AL 3.3 Balanço Energético Num Sistema TermodinâmicoSonia CoelhoAinda não há avaliações
- Salesianos Do Estoril - Escola: A.L.3.3. Balanço Energético de Um Sistema TermodinâmicoDocumento7 páginasSalesianos Do Estoril - Escola: A.L.3.3. Balanço Energético de Um Sistema TermodinâmicoiolaAinda não há avaliações
- AL 3.3 Balanço Energetico Alunos TextoDocumento2 páginasAL 3.3 Balanço Energetico Alunos Textolara felgueirasAinda não há avaliações
- Ae rf10 Teste Resol 3 Preciso de AcessoDocumento5 páginasAe rf10 Teste Resol 3 Preciso de AcessoafaaaafsAinda não há avaliações
- Relatório 2 - Condutividade Térmica Do CobreDocumento11 páginasRelatório 2 - Condutividade Térmica Do CobreIgor SantosAinda não há avaliações
- Fisica AL 3 3 ProfessorDocumento2 páginasFisica AL 3 3 Professorsimoes_sandraAinda não há avaliações
- FQ rf10 Teste 3Documento10 páginasFQ rf10 Teste 3Francisco MonterrosoAinda não há avaliações
- Experimento 9 - Documentos GoogleDocumento4 páginasExperimento 9 - Documentos GoogleClara BatistaAinda não há avaliações
- Relatório 05 - CalorimetriaDocumento7 páginasRelatório 05 - CalorimetriaCarlos AlbertoAinda não há avaliações
- Relatório 5Documento9 páginasRelatório 5Maria Isabele Almeida CoelhoAinda não há avaliações
- Detalhamento Do Processo TérmicoDocumento23 páginasDetalhamento Do Processo TérmicoAna Clara Miranda BatistaAinda não há avaliações
- Equivalente em Água de Um CalorímetroDocumento16 páginasEquivalente em Água de Um CalorímetroNatalia GomezAinda não há avaliações
- Calor Sensível, Capacidade Térmica e Calor EspecíficoDocumento20 páginasCalor Sensível, Capacidade Térmica e Calor EspecíficofertonettoAinda não há avaliações
- Fisica - AL 3 3 - AlunoDocumento2 páginasFisica - AL 3 3 - Alunosimoes_sandraAinda não há avaliações
- Ae rf10 Quest Lab 6Documento2 páginasAe rf10 Quest Lab 6marina lopesAinda não há avaliações
- Ficha 10º Física - Subdomínio 3 - Exercícios ExameDocumento11 páginasFicha 10º Física - Subdomínio 3 - Exercícios ExameTeam StradaAinda não há avaliações
- Experimento - Lei Do ResfriamentoDocumento8 páginasExperimento - Lei Do ResfriamentoKamila VitóriaAinda não há avaliações
- Ficha Trabalho 2Documento1 páginaFicha Trabalho 2PedroAinda não há avaliações
- Relatório Trocas de CalorDocumento12 páginasRelatório Trocas de CalorMarcos Santos AlvesAinda não há avaliações
- P3 Gabarito PER 1Documento2 páginasP3 Gabarito PER 1LucasAinda não há avaliações
- 1.3.9-Determinação Do Balanço Energético de Um Sistema - Variação de Entalpia Mássica de Transição de FaseDocumento8 páginas1.3.9-Determinação Do Balanço Energético de Um Sistema - Variação de Entalpia Mássica de Transição de Faseantonioluis081207Ainda não há avaliações
- Relatório Perda de CargaDocumento12 páginasRelatório Perda de CargaRicardo LapolliAinda não há avaliações
- Calor Latente de Fus o Do GeloDocumento7 páginasCalor Latente de Fus o Do GeloMiguel LopesAinda não há avaliações
- Calor EspecíficoDocumento11 páginasCalor EspecíficoWadla TorresAinda não há avaliações
- Relatório 2 - TermodinâmicaDocumento8 páginasRelatório 2 - TermodinâmicaGabrielle OliveiraAinda não há avaliações
- FIcha AL 3.3Documento1 páginaFIcha AL 3.3Rita AguiarAinda não há avaliações
- 1º Relatorio de Fisica LilDocumento10 páginas1º Relatorio de Fisica LilDenner EdsonAinda não há avaliações
- Entalpia de NeutralizaçãoDocumento11 páginasEntalpia de NeutralizaçãoLivia NeriAinda não há avaliações
- 05 - Lei Do Resfriamento de NewtonDocumento5 páginas05 - Lei Do Resfriamento de NewtonRaizenAinda não há avaliações
- Manual 09 - CalorimetriaDocumento4 páginasManual 09 - CalorimetriaDaisy de SousaAinda não há avaliações
- Teste 3Documento8 páginasTeste 3anitadiogoAinda não há avaliações
- Fa10 Exploracao Detalhada Al 3 3Documento3 páginasFa10 Exploracao Detalhada Al 3 3DekiisterBRAinda não há avaliações
- Prova Fisica Mudança de Estado AngloDocumento6 páginasProva Fisica Mudança de Estado AnglolucasAinda não há avaliações
- Prova Fisica Mudança de Estado Anglo PDFDocumento6 páginasProva Fisica Mudança de Estado Anglo PDFlucasAinda não há avaliações
- Relatorio 07 - Calor de Fusão Do GeloDocumento4 páginasRelatorio 07 - Calor de Fusão Do GeloMaria SidorAinda não há avaliações
- Atividade Adaptada IXDocumento5 páginasAtividade Adaptada IXAbraão LinconAinda não há avaliações
- Relatório Troca de CalorDocumento9 páginasRelatório Troca de CalorClovis AlmeidaAinda não há avaliações
- Relatório N.º3 - Determinação Da Entalpia de Vaporização Da ÁguaDocumento12 páginasRelatório N.º3 - Determinação Da Entalpia de Vaporização Da ÁguaGuilherme SantosAinda não há avaliações
- Física Experimental para Engenharia - Relatório 9 - UFCDocumento10 páginasFísica Experimental para Engenharia - Relatório 9 - UFCtrabalhosufcAinda não há avaliações
- Lab de APFQ IIDocumento4 páginasLab de APFQ IIJuliana AlvesAinda não há avaliações
- Exp 5Documento9 páginasExp 5bentodesaAinda não há avaliações
- Projeto RefrigeraçãoDocumento4 páginasProjeto RefrigeraçãoLaryssa BatistelaAinda não há avaliações
- Termodinamica e Gases Fisica BasicaDocumento2 páginasTermodinamica e Gases Fisica BasicaKamily SoaresAinda não há avaliações
- TesteDocumento5 páginasTesteDavi BenAinda não há avaliações
- Exercicios Resolvidos de Fisica BasicaDocumento7 páginasExercicios Resolvidos de Fisica BasicaEder CecluskiAinda não há avaliações
- Ebook Exatas - Semana 5 PDFDocumento229 páginasEbook Exatas - Semana 5 PDFadasdaAinda não há avaliações
- Relatório Laborátorio de Fundamentos IIDocumento12 páginasRelatório Laborátorio de Fundamentos IICatiucia BerkembrockAinda não há avaliações
- Relatório Calor Específico Da ÁguaDocumento11 páginasRelatório Calor Específico Da ÁguaLuiz Henrique100% (2)
- Calor Específico: Engenharia de MateriaisDocumento7 páginasCalor Específico: Engenharia de MateriaisMATHEUS DA SILVA RODRIGUESAinda não há avaliações
- Exercicios Cap3 PDFDocumento13 páginasExercicios Cap3 PDFCleverson SouzaAinda não há avaliações
- Pratica - 03 - Convecção NaturalDocumento2 páginasPratica - 03 - Convecção NaturalJoão PauloAinda não há avaliações
- Resolução Comentada - UNIFESP - 2004 - Curso ObjetivoDocumento2 páginasResolução Comentada - UNIFESP - 2004 - Curso ObjetivoRoberto Neiva NeivaAinda não há avaliações
- Análise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018No EverandAnálise das tensões em estruturas de concreto devido a variações de temperatura entre os anos de 2009 e 2018Ainda não há avaliações
- Tratamento de Lodos de Estações de Tratamento de ÁguaNo EverandTratamento de Lodos de Estações de Tratamento de ÁguaAinda não há avaliações
- Teste4 - 1.1Documento8 páginasTeste4 - 1.1iolaAinda não há avaliações
- 10º Ano - Física - Ficha de Trabalho Nº7: Objetivo GeralDocumento4 páginas10º Ano - Física - Ficha de Trabalho Nº7: Objetivo GeraliolaAinda não há avaliações
- Teste2 - 1.1Documento6 páginasTeste2 - 1.1iolaAinda não há avaliações
- Teste5 - 1.1Documento13 páginasTeste5 - 1.1iolaAinda não há avaliações
- O Menino Da Sua Mãe: Educação LiteráriaDocumento3 páginasO Menino Da Sua Mãe: Educação Literáriaiola100% (1)
- FT4 - SubU-1.1Documento4 páginasFT4 - SubU-1.1iolaAinda não há avaliações
- FF2 Al1.1Documento6 páginasFF2 Al1.1iolaAinda não há avaliações
- AL 1.2 Movimento Vertical de Queda e de Ressalto de Uma BolaDocumento8 páginasAL 1.2 Movimento Vertical de Queda e de Ressalto de Uma BolaSara Raquel Costa Pinto100% (3)
- Al1 1-SantillanaDocumento2 páginasAl1 1-SantillanaiolaAinda não há avaliações
- Al1 2-ArealDocumento5 páginasAl1 2-ArealiolaAinda não há avaliações
- Al2 1-Relatório1Documento7 páginasAl2 1-Relatório1iolaAinda não há avaliações
- Resumo Al1.1Documento1 páginaResumo Al1.1iolaAinda não há avaliações
- Al2.1 Fisica Manual10fDocumento10 páginasAl2.1 Fisica Manual10fiolaAinda não há avaliações
- Resumo1-Al3 3Documento1 páginaResumo1-Al3 3iolaAinda não há avaliações
- Al3 3-SantillnaDocumento5 páginasAl3 3-SantillnaiolaAinda não há avaliações
- Relatório-Al1 2,10FDocumento3 páginasRelatório-Al1 2,10FiolaAinda não há avaliações
- Al1 1-SantillanaDocumento7 páginasAl1 1-SantillanaiolaAinda não há avaliações
- Al1 1-Manual10fDocumento16 páginasAl1 1-Manual10fiolaAinda não há avaliações
- Resumo-4-Gases e Dispersões PDFDocumento2 páginasResumo-4-Gases e Dispersões PDFiolaAinda não há avaliações
- Resumo-2-Gases e Dispersões PDFDocumento6 páginasResumo-2-Gases e Dispersões PDFiolaAinda não há avaliações
- Resumo-3-Gases e DispersõesDocumento81 páginasResumo-3-Gases e DispersõesiolaAinda não há avaliações
- Correção - FF3.5 - 2.2.3Documento3 páginasCorreção - FF3.5 - 2.2.3iolaAinda não há avaliações
- Correção - FF3.6 - 2.2.3Documento10 páginasCorreção - FF3.6 - 2.2.3iolaAinda não há avaliações
- FF3.9 - 2.2.3Documento5 páginasFF3.9 - 2.2.3iolaAinda não há avaliações
- FF3.8 - 2.2.3 - CCDocumento2 páginasFF3.8 - 2.2.3 - CCiolaAinda não há avaliações
- FF2.1 - 2.2.2Documento4 páginasFF2.1 - 2.2.2iolaAinda não há avaliações
- Forças de Atrito Estático e Cinético PDFDocumento5 páginasForças de Atrito Estático e Cinético PDFMax Leite100% (1)
- Relatório 1 RADIAÇÃO DE STEFAN BOLTZMANN RailsonDocumento8 páginasRelatório 1 RADIAÇÃO DE STEFAN BOLTZMANN RailsonRailson MarquesAinda não há avaliações
- Atividade Teleaula IiiDocumento3 páginasAtividade Teleaula IiiLourenço RossetoAinda não há avaliações
- Afa2003 FisDocumento4 páginasAfa2003 FisEddy LimaAinda não há avaliações
- Física em Nível Olímpico Vol. 1Documento328 páginasFísica em Nível Olímpico Vol. 1TheAsleepHylian l Clara100% (2)
- Criatividade para Memorizar Formulas PDFDocumento13 páginasCriatividade para Memorizar Formulas PDFJoão FranciscoAinda não há avaliações
- Listade Exerciciosde Equilibriodo Corpo ExtensoDocumento12 páginasListade Exerciciosde Equilibriodo Corpo ExtensoPatricia Pestana CoelhoAinda não há avaliações
- Texto de Apoio 5Documento11 páginasTexto de Apoio 5EdurdoAinda não há avaliações
- Serpentina para Tanque Memorial de CalculoDocumento20 páginasSerpentina para Tanque Memorial de CalculoInspetor Soldagem67% (3)
- Cinematica Eng MecDocumento2 páginasCinematica Eng MecManjolo Janfar WilsonAinda não há avaliações
- Indução Eletromagnetica - UERJDocumento5 páginasIndução Eletromagnetica - UERJPaulo HenriqueAinda não há avaliações
- Ficha de Trabalho 7Documento2 páginasFicha de Trabalho 7Rafaek PereiraAinda não há avaliações
- Revis o para ProvaDocumento10 páginasRevis o para ProvaYasmin MendesAinda não há avaliações
- Guiatopico 5 Mecanica 12010Documento8 páginasGuiatopico 5 Mecanica 12010luccasAinda não há avaliações
- Plano Anual de Física - 1º AnoDocumento6 páginasPlano Anual de Física - 1º AnomarianemuraseAinda não há avaliações
- Campo de ProcaDocumento23 páginasCampo de ProcaManuel RodriguesAinda não há avaliações
- Caixa de Transferencia MagnumDocumento5 páginasCaixa de Transferencia MagnumDEUSMARAinda não há avaliações
- Apostila de Movimento Circular - IDocumento17 páginasApostila de Movimento Circular - IrareisAinda não há avaliações
- Estruturas Metálicas - Fator de SegurançaDocumento9 páginasEstruturas Metálicas - Fator de SegurançaVinicius RenardAinda não há avaliações
- 01 Everton 2 ANOF2 Aula E10Documento2 páginas01 Everton 2 ANOF2 Aula E10Lucas JuniorAinda não há avaliações
- Termodinâmica - 3Documento46 páginasTermodinâmica - 3moises20caAinda não há avaliações
- Propiedades Refrigerante 134a (Inglesas)Documento4 páginasPropiedades Refrigerante 134a (Inglesas)DiegoFernandoMontenegroAinda não há avaliações
- Unidade01 Pendulo Carro MIMODocumento4 páginasUnidade01 Pendulo Carro MIMOAlcides SabainiAinda não há avaliações
- Relatório P StevinDocumento10 páginasRelatório P StevinGrayce KellyAinda não há avaliações
- A Lei de Rayleigh-JeansDocumento3 páginasA Lei de Rayleigh-JeansCHRISTOPHERJIMYAinda não há avaliações
- Coeficiente Global de Transferencia de CalorDocumento31 páginasCoeficiente Global de Transferencia de Calorjoao nunesAinda não há avaliações
- Resumo - Trabalho e Potência - RevisãoDocumento1 páginaResumo - Trabalho e Potência - RevisãoEuvaldo Soares da SilvaAinda não há avaliações
- Relatório 5 - BernoulliDocumento20 páginasRelatório 5 - BernoulliVinícius Silva100% (1)
- Relatório de Física - Experiencia Rotação e Momento de InérciaDocumento7 páginasRelatório de Física - Experiencia Rotação e Momento de InérciaJaquelyni GonçalvesAinda não há avaliações