Escolar Documentos
Profissional Documentos
Cultura Documentos
Fisiologia Módulo 8 (Endócrino)
Enviado por
vargas.pedro2003Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Fisiologia Módulo 8 (Endócrino)
Enviado por
vargas.pedro2003Direitos autorais:
Formatos disponíveis
Fisiologia Módulo 8
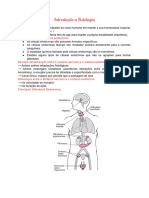
Funções do sistema endócrino
Manter a homeostasia;
Regulação das funções corporais: metabolismo, crescimento, desenvolvimento, balanço hidroeletrolítico,
reprodução e comportamento;
Hormônios
Substâncias químicas secretadas para o sangue por células especializadas que regulam funções metabólicas de
outras células do organismo;
Hormônio endócrinos: produção a partir de células endócrinas;
Neurormônios: produzidos por neurônios e lançados na corrente sanguínea e atuam em uma célula distante;
Sinalização parácrina: libera uma substância em células muito próximas a célula sinalizadora;
Sinalização autócrina: a célula libera sinalizador na sua própria superfície;
Estrutura química dos hormônios
Esteróides: derivados do colesterol, secretados pelo córtex supra-renal; por exemplo a aldosterona, cortisol,
estrogênio, progesterona, testosterona; extremamente lipossolúveis; circulam ligados a proteínas; receptores
nucleares;
Peptídicos ou protéicos: sintetizados a partir de AA; por exemplo hormônios liberados pela hipófise anterior
e posterior, insulina, glucagon, paratormônio; circulam de forma livre; receptores de membrana;
Amínicos: derivados da tirosina; exemplo T3, T4 (comporta mais como esteroidal- circulam ligados a proteínas
e receptores nucleares), epinefrina e NE (receptores de membrana);
Síntese de hormônios
Acontece primeiro nos ribossomos aderidos ao RER;
É fabricado na forma de pré-pró-hormônio, que é uma molécula muito grande que tem hormônios e AA
extras;
Dentro do RER tem-se a primeira clivagem formando o pró-hormônio que vai para o CG;
No complexo de golgi sofre mais clivagem e forma hormônios em sua forma final que ficam nas vesículas até
um estímulo que pode ser despolarização da membrana por entrada de cálcio dentro da célula ou pelo
amento do AMPcíclico;
Sua meia vida no sangue é curta e ele não tem dificuldade de ficar no sangue, sem necessidade de se ligar a
proteínas;
Isabel Oliveira Gusman
Solubilidade dos hormônios
Hidrossolúveis: peptídicos e amínicos excluindo-se os tireoidianos;
Lipossolúveis: derivados do colesterol (esteróides)e os dipeptídeos tireoidianos (T3 e T4);
Depuração dos hormônios
Destruição metabólica pelos tecidos: enzimas que degradam;
Ligação com os tecidos: liga com o receptor, internaliza os dois juntos e no citoplasma degrada o hormônio e
o receptor volta para a membrana;
Excreção da bile pelo fígado;
Excreção da urina pelos rins;
Mecanismo de ação hormonal
Regulação por retroalimentação negativa (principalmente) ou positiva;
Negativo: temperaturas mais frias liberam TRH; sai do hipotálamo e vai para a hipófise; libera o TSH
(tireotropina); vai pela circulação até a tireóide; estimula produção de T3 e T4; o hormônio faz seu efeito;
envia o feedback negativo para hipotálamo e hipófise que diminuem a secreção de TRH e TSH;
Negativo: alimentação rica em glicose; pâncreas produz insulina; tira glicose da circulação, vai para célula;
Positivo: no parto; dilata o cérvix; estimula liberação da ocitocina; aumenta a contração do útero; dilata
mais o cérvix;
Positivo: na amamentação; quanto mais o bebe suga mais libera ocitocina; que atua na glândula mamária; produz
leite e libera mais leite;
Os únicos com feedback positivo são ocitocina e prolactina;
OBS: testosterona tem seu pico pela manhã assim como o cortisol.
Regulação para baixo do número de receptores
Nos casos de excesso da ação de algum hormônio. Inativação de algumas moléculas de receptor;
Inativação de partes das moléculas de sinalização das proteínas intracelulares;
Seqüestro temporário do receptor para o interior das células;
Isabel Oliveira Gusman
A regulação da ação hormonal pode ser por meio da regulação do número de receptores que no caso de
excesso de hormônios pode diminuir em quantidade e no caso de falta de hormônio podem aumentar em
quantidade.
Destruição de receptores depois de serem interiorizados;
Diminuição da produção de receptores;
Mecanismo de ação dos hormônios
Os receptores dos hormônios são ligados a proteína G;
A ligação do receptor metabotrópico com o hormônio ativa a proteína G e ativa também a cascata intracelular
que vai se seguir;
O efeito final pode ser abertura ou fechamento de um canal iônico ou mudança na atividade de alguma
enzima;
Insulina tem seu receptor ligado à tirosina-quinase e é de membrana; a ativação desse receptor já ativa uma
ação enzimática.
Hormônios esteróides, da tireóide, retinoides e vitamina D receptores intracelular;
Podem ser acoplados a proteína Gq, Gi e Gs;
Receptores intracelulares alteram a transcrição e tradução;
Hipotálamo
Localização: abaixo do tálamo, na região do diencéfalo;
Liga-se ao SN e ao sistema endócrino, controlando a maioria das funções vegetativas, endócrinas,
comportamentais e emocionais do corpo;
Representa cerca de 1% da massa total do encéfalo;
Função: regulação da temperatura corpórea, apetite, atividade GI, regulação hídrica, atividade sexual e
emoções; Centro coletor de informações relativas ao bem estar interno do organismo;
Internamente relacionado com a hipófise no comando das atividades;
Controla a secreção hipofisária, produz ocitocina e ADH que são armazenados pela hipófise;
Regulação cardiovascular: responsável pela modificação da PA e da FC. Esses estímulos são conduzidos para
a formação reticular da ponte e bulbo;
Regulação da temperatura: o sangue que passa no hipotálamo determina a temperatura corporal e faz com
que o hipotálamo tente regular a temperatura;
Regulação hídrica: controla de duas formas estimulando a sede ou retendo a água na urina;
Contração do útero e ejeção do leite: relaciona-se com a produção da ocitocina;
Regulação GI: possui uma área que é o centro da fome e está relacionado com a ingestão de alimentos e
saciedade;
Controle sobre a hipófise: secreta hormônio que atuam como liberadores ou inibidores dos hormônios da
hipófise anterior;
A liberação de hormônios na hipófise posterior é controlada por sinais neurais do hipotálamo e da hipófise
anterior por hormônios do hipotálamo (hormônios liberadores ou hormônios hipotalâmicos inibidores);
Hormônios hipotalâmicos circulação porta hipotalâmica hipofisária hipófise anterior;
Todos os hormônios hipotalâmicos são neurormônios;
ADH e ocitocina são produzidos nos corpos celulares localizados nos núcleos supraóptico (ADH) e
paraventricular (ocitocina) e então transportados em associação às neurofisinas para as terminações nervosas
na hipófise posterior;
2 hormônios inibitórios: dopamina e somatostatina;
Via túbero-infundibular libera dopamina constante e impede a secreção de prolactina;
Tireotrofo local da adeno-hipófise que é estimulado pelo TRH e vai produzir o TSH;
Somatotrofo célula da adeno-hipófise que é estimulado pelo GHRH e produz o GH;
Corticotrofo célula da adeno-hipófise que é estimulado pelo CRH e estimula a secreção de ACTH
Gonadotrofo célula da adeno-hipófise que é estimulado pelo GnRH e estimula a secreção de LH e FSH;
Lactotrofo célula da adeno-hipófise que vai ser estimulada pelo PIH inibindo a secreção de prolactina; mas é
a célula que também produz a prolactina;
Isabel Oliveira Gusman
Produzido no hipotálamo
Hipófise
Localização: na sela turca do osso esfenóide;
Ligada ao hipotálamo pelo pendúculo hipofisário;
Anterior= adeno-hipófise: formada por tecido epitelial; dividia em pars distalis, pars tuberalis e pars intermédia;
Posterior= neuro-hipófise: formada por tecido neural; dividida em pars nervosa; presença de corpos de Hering;
é uma projeção do hipotálamo;
Entre a adeno e a neuro hipófise existe uma zona avascular chamada de parte intermédia;
Hormônio adrenocorticotrófico: hipotálamo libera CRH que atua na hipófise anterior e estimula a
liberação do ACTH, que vai para a adrenal onde estimula a produção de cortisol que produzido manda
feedback negativo para a hipófise e hipotálamo; geralmente é aumentado sua liberação as 6h da manhã; e 8h do
cortisol; estresse é estimulador da liberação do CRH, por isso o cortisol é chamado de hormônio do estresse;
Hormônio estimulador da tireóide: hipotálamo libera TRH que atua na adeno-hipófise que vai liberar TSH
que vai atuar na tireóide produzindo T3 e T4 mandando feedback negativo para a hipófise e hipotálamo para
parar a liberação; a tireóide também produz calcitonina, que é estimulada pela quantidade de Ca na circulação;
o estresse é inibitório da liberação de TRH;
Isabel Oliveira Gusman
Hormônios folículo estimulante e luteinizante: nos homens o FSH induz a produção de sptz e o LH
induz a produção de testosterona; nas mulheres o FSH estimula a formação do folículo e o LH a ovulação;
do hipotálamo é liberado o GnRH que vai atuar na adeno-hipófise formando FSH e LH que vão liberar
hormônios sexuais; nos homens quem faz o feedback negativo é a testosterona e o estrogênio e nas
mulheres é a progesterona (fraca), testosterona e o estrogênio (forte) a depender da dose (só se for
baixa, se for alta é feedback positivo); inibina é seletiva para fazer feedback negativo do FSH;
Prolactina: lactotrofo na hipófise anterior é continuamente inibida pela dopamina; a diminuição da dopamina
produz prolactina devido a estímulos como estresse, sono (principal estimulante) e sucção; a inibição pode ser
também pela somastostatina, TSH e GH; não se definiu se tem hormônio que estimula a liberação da
prolactina;
Hipófise posterior
Hormônio antidiurético (ADH): atua no ducto coletor para a reabsorção de água, que depende desse
hormônio nessa porção; controla a volemia; estimula a inserção de canais para água na membrana de células
principais do ducto coletor; aumenta aquaporinas na membrana por meio da fosforilação delas; queda de PA
também aumenta a secreção de ADH por uma não estimulação dos barorreceptores, e assim ele atua no
receptor V1 que faz vasoconstricção (por isso também tem o nome de vasopressina) e reabsorve água pelo
receptor V2;
OBS: osmorreceptores ficam no hipotálamo e percebem a osmolaridade de sangue para saber se vai ter ou não a
liberação do ADH;
Ocitocina: contração do miométrio ou ejeção do leite estimula a liberação da ocitocina; segue o feedback
positivo; produz a contração do útero, que a cada contração estimula a contrair mais; orgasmo pode causar um
aumento da liberação de ocitocina;
Lactação
Níveis altíssimos de ocitocina e prolactina, quanto mais sucção mais libera ocitocina; na lactação tem baixa
dopamina e libera lactotrofo; aumento da prolactina diminui GnRH e diminui a liberação de FSH e LHe não
desenvolve o folículo e não ovula, mas não se pode contar com isso pois a liberação é pulsátil e vão ter
momentos com ala ou baixa prolactina.
Isabel Oliveira Gusman
Tireóide
Os efeitos dos hormônios tireoidianos são feitos pelo T3, mas ele é secretado em menor quantidade, logo, o
organismo converte o T4 em T3 e assim consegue os efeitos esperados;
Células foliculares: sintetizam o HT, T3, T4 e tireoglobulina;
Colóide: fica no interior dos folículos; constituído pela tireoglobulina, cuja molécula contém os hormônios
tireoidianos;
Entre os folículos tem as células parafoliculares que vão produzir a calcitonina;
Fabricação dos hormônios tireoidianos
O iodo é captado por um transportador NIS que fica localizado na membrana basal da célula folicular;
Transportador NIS: é simporte iodo sódio; transportador ativo secundário, que depende da bomba de
sódio e potássio;
A ação da NIS é estimulada por TSH;
Com o iodo na célula folicular, ele tem que passar para o colóide;
Ele passa pela membrana apical por um transportador pendrina que é iodeto-cloreto;
O iodo agora no colóide encontra a enzima peroxidase que vai oxidar o iodeto;
A proteína tireoglobulina foi fabricada, e é uma proteína com vários AA tirosina;
Com essa proteína e iodo é feita a iodização/organificação, que a tireoperoxidase insere o iodo na
tireoglobulina, formando uma monoiodotirosina (MIT), se inserir uma molécula, um diiodotirosina (DIT)
se inserir duas moléculas e triiodotirosina se inserir 3 moléculas e tetraiodotirosina;
A união de duas DIT forma um T4 e a união de uma MIT e uma DIT forma o T3;
Os hormônios quando produzidos vão ficar estocados dentro do colóide que dura de 2 a 3 meses;
Liberação de tiroxina e triiodotironina
O TSH também estimula a exocitose dos hormônios tireoidianos;
Inicia com a liberação de pseudópodes para captura de um colóide que vem a proteína tireoglobulina com
várias MIT, DIT, T3 e T4;
Dentro da célula lisossomos começam a degradar essa molécula de tireoglobulina liberando o T3 e o T4 que
vão sofrer exocitose;
As MIT e DIT ficam dentro da célula e sofrem ação da desiodinase, para retirada do iodo dessas moléculas;
O iodo retirado volta para o colóide para formação de mais hormônios- reciclagem e hormônios;
Transporte plasmático do HT
1% circula de forma livre e 99% ligado a proteína;
Isabel Oliveira Gusman
Essas proteínas podem ser a globulina ligadora de tiroxina (TBG-pouca quantidade), a pré-albumina
ligadora de tiroxina e a albumina; SHBG- compete o sítio de ligação entre T4 e estrogênio;
Em situações especiais pode haver o aumento da proteína TBG: gravidez (aumento de estrogênios),
terapia com estrogênios e anticoncepcionais- reduz a forma livre- diminui HT- hipotireoidismo;
Diminuição da TBG: androgênios, glicocorticóides- aumenta a forma livre- aumenta HT-
hipertireoidismo;
A latência e ação prolongada se devem às ligações com as proteínas e o modo como agem nas células;
A ação dos HT é mais demorada por seus receptores são nucleares e dependem da síntese de proteínas, o
que faz com que seja um processo demorado;
Desiodação da tiroxina
Ação da enzima deiodinase: é necessária nos tecidos para que o T4 possa ser convertido em T3;
Nas células foliculares ela é necessária para reciclagem do iodo;
D1: fígado, rins, ME e leucócitos; estresse físico e emocional reduzem sua atividade reduzindo o T3
circulante levando a síndrome do T3 baixo; é uma desiodinase de anel externo e pode tirar também do
interno em situações como hipertireoidismo; T3 reverso e funcional; diminui a atividade com glicocorticóides;
D2: hipófise, SNC, tecido adiposo e placenta; atividade e expressão reduzidas na presença dos hormônios
tireoidianos e aumentada no hipotireoidismo; é uma desiodinase de anel externo; T3 funcional;
D3: expressa no tecido embrionário e após o nascimento; inativação biológica dos hormônios tireoidianos;
atividade e depressão aumentada no hipertireoidismo; é uma desiodinase de anel interno; T3 reverso;
A retirada de um iodo de anel interno forma um iodo não funcional, chamado de T3 reverso;
A retirada do iodo de anel externo que forma um T3 funcional;
Funções dos HT
Funções do T3: metabolismo, crescimento, atividades mentais e atividade das glândulas endócrinas;
Os HT influenciam no metabolismo das proteínas, carboidratos e gorduras;
Insere bombas de sódio e potássio nas células;
O receptor fica ligado na fita dupla do DNA, sendo ele nuclear;
A alteração na transcrição e tradução faz a ação desses hormônios tireoidianos;
Acaba não sendo nem hipoglicemico nem hiperglicêmico, pois por mais que aumente a absorção de glicose,
aumenta também a liberação dela por outras vias.
O aumento da gliconeogênese pode causar o aumento da necessidade de insulina;
No embrião os problemas são mais especificamente neurológicos, além de problemas gerais no caso de falta
de equilíbrio de HT;
Crescimento- síntese de proteínas;
Isabel Oliveira Gusman
Regulação da secreção dos hormônios tireoidianos
Tem seu pico durante a noite e níveis mais baixos na hora do jantar (inicio da noite);
Liberado o TRH, ele vai atuar no receptor nos tireotrofos liberando TSH;
O TSH atua nas células foliculares para a liberação do T3 e T4;
Como o TSH libera o T3 e T4: aumenta a proteólise de tireoglobulina, aumenta a atividade da bomba de
iodeto, aumento da iodização da tirosina, aumenta o tamanho e atividade secretória das células tireoidianas,
aumenta o número de células tireoidianas;
Estresse e função tireoidiana
Inibição central: o estresse inibe a liberação do cortisol (glicocorticóides) que vai diminuir a expressão de
receptores de TRH no tireotrófos, o que diminui a resposta do TSH ao TRH;
Inibição periférica: o estresse libera muito cortisol que inibe a atividade da D1 e diminui a quantidade de
T3 formado;
Antitireoidianos
Inibidores da captação de iodeto: perclorato e tiocianato inibem a NIS e capta menos iodo;
Tioaminas: propiotiluracila e tiamazol que impedem a ação da peroxidase e bloqueiam o acoplamento das
iodotirosinas;
Iodetos: efeito de Wolff-chaikoff causa uma inibição reversível e transitória que funciona no início da
administração; o aumento excessivo inibe a DUOX que é necessário para formar peróxido de hidrogênio e sem
ele não tem a formação do HT;
Importância do iodo
Alimentos derivados do ambiente marinho como frutas e vegetais cultivados próximos ao mar são ricos
em iodo;
Queda de iodo em crianças: cretinismo;
Falta da ingestão de iodo
Queda do iodo em adultos: bócio endêmico;
Isabel Oliveira Gusman
Anticorpo que copia
excessivamente o TSH
Anticorpo que degrada a tireoide
Hipotireoidismo primário: por causas de doenças da tireóide com altos níveis de TSH; baixos níveis de T4 livre;
Hipotireoidismo secundário: doenças hipofisárias e hipotalâmicas com baixos níveis de TSH; T4 livre baixo; se
fosse dosado o TRH estaria elevado;
Hipotireoidismo terciário: hipotálamo produz TRH insuficiente ou a hipófise produz TSH baixo; T4 baixo;
Fisiologia do GH
Funções
Indução do crescimento: divisão celular, síntese protéica, aumento da utilização de ácidos graxos como fonte
de energia, redução da utilização de glicose no organismo; a utilização de AG cria um efeito lipolítico;
OBS: o crescimento é uma soma de fatores endócrinos, genéticos e ambientais;
Síntese e liberação
Começa no núcleo ventromedial do hipotálamo, que é a mesma região que é sensível a concentração da glicose
no sangue e que leva a saciedade na hiperglicemia e fome na hipoglicemia;
Esse núcleo libera o GHRH que é o hormônio liberador de GH que cai na circulação porta-hipotalâmica-
hipofisária;
Na adeno-hipófise encontra o somatotrofo que vai produzir o GH;
O GH vai atuar em várias células induzindo a síntese de proteínas, preferindo AG para fonte de energia, etc;
O GH também vai para o fígado, onde será transformado em um metabólito, que são fatores de crescimento
semelhantes à insulina (somatomedinas), sendo o mais importante o IGF-1;
O IGF-1 atua em tecidos estimulando a síntese de proteínas e favorecendo o processo de crescimento;
Existe uma região do hipotálamo que secretam somatostatina, que é o hormônio inibidor de GH;
O próprio GH é capaz de diminuir sua liberação estimulando o hipotálamo a produzir somatostatina;
O IGF-1 faz feedback negativo na hipófise anterior e feedback para o hipotálamo para liberação de
somatostatina;
Grelina e arginina estimulam o somatotrofo para produzir GH;
Durante a puberdade que aumenta os hormônios sexuais é que acontece o estirão de crescimento, já que esses
são fatores estimulatórios;
As primeiras horas do sono profundo é o momento que tem maior liberação de GH do dia;
Isabel Oliveira Gusman
Senescência: à medida que envelhece, diminui a capacidade de produzir GH;
Gh exógeno,suprime o GH fisiológico;
Uma alimentação rica em carboidratos diminui os níveis de GH e aumenta os níveis de insulina, que cria um
estoque de calorias;
Em jejum há o aumento do GH e a diminuição da insulina, mobilizando o tecido adiposo formado como fonte de
energia;
O GH faz parte dos hormônios hiperglicemiantes;
Regulação da síntese de GH pelo GHRH e Somatostatina
GHRH atua no receptor dele no somatotrofo, e seu receptor é acoplado a proteína Galfa-S;
Essa proteína ativa a adenilase ciclase, formando AMP cíclico que vai ativar a PKA (quinase A);
Essa PKA vai fosforilar fatores de transcrição, que vai induzir a transcrição e tradução para formação da proteína
GH;
A PKA também vai estimular canais de cálcio, e o seu influxo faz a exocitose do GH;
A somatostatina atua no seu receptor do somatotrofo que é acoplado a proteína Gi, que inibe a secreção do
GH além de ativar canais de K causando seu efluxo e hiperpolarizando a célula;
Transporte de GH na corrente sanguínea
Uma porção dele fica ligado de maneira fraca a proteínas;
Essas proteínas são formadas através da proteólise dos receptores de membrana;
A ligação com proteínas evita degradação precoce do GH;
Tem uma meia vida de 20 minutos;
IGF-1 já é ligado a uma proteína de ligação específica que o próprio GH estimula a formação quando ele passa
dentro do fígado;
Isso faz com que a meia-vida do IGF seja muito mais longa do que a do GH, durando 20 horas;
Perfil de secreção de GH ao longo da vida
A partir do nascimento tem-se um crescente aumento do GH até seu pico na puberdade;
Na vida adulta ele cai lentamente;
Na senescência fica com menos do que na infância
Secreção de GH no sono
Principalmente durante as duas primeiras horas de sono profundo, tem-se um grande pico de liberação de
GH;
Crescimento ósseo
O crescimento de ossos longos acontece por um processo de ossificação endocondral;
Isabel Oliveira Gusman
O crescimento acontece com a multiplicação de condrócitos e proliferação dos vasos sanguíneos e
osteoblastos;
Placa proliferativa epifisária é o local de ação do IGF para formação de cartilagem e os osteoblastos chegam para
produção do tecido ósseo;
O fechamento das epífises acontece com o aumento dos hormônios sexuais, principalmente o estrogênio;
Outros hormônios envolvidos no crescimento
T3 regula a resposta normal dos somatotrofos ao GHRH, o que indiretamente aumenta a secreção de GH;
T3 e T4: potencializam efeito do GH nos ossos, músculos e fígado;
Insulina age em receptores de IGF: aumenta a formação de receptores de GH e IGF, aumenta liberação de
IGF, diminui a glicemia que aumenta o GH;
Glicocorticóides: podem ser estimulantes da liberação de GH, se for agudo, ou inibidor da liberação
de GH, se for crônico;
Síndromes características do mal funcionamento do GH
Gigantismo: superprodução de GH na infância e período pré-pubere, isto é, quando as epífises ainda estão
abertas e permitem o crescimento linear do indivíduo; geralmente a causa é um tumor na hipófise;
Acromegalia: superprodução de GH após o fechamento das epífises, que leva ao crescimento das
extremidades e ossos chatos; pode causar diabetes e ICC;
Nanismo: deficiência do GH; só 1/3 dos casos de nanismo é por deficiência única de GH; na maior parte, a
deficiência é de todos os hormônios da adeno-hipófise; a causa pode ser congênita ou tumor;
Deficiência do GH: tratamento com uso terapêutico do GH exógeno; pode ser de base genética ou lesão da
hipófise e hipotálamo; na infância, esses casos se apresentam com baixa estatura e adiposidade, hipoglicemia,
hipodesenvolvimento dos ossos da face, dentição atrasada, aumento da gordura subcutânea e diminuição da
massa muscular;
Síndrome de prader-willi: síndrome genética que causa baixa estatura e pode ser tratado com GH exógeno;
quadro de hipotonia, hiperfagia, obesidade, baixa estatura, hipogonadismo, atraso do desenvolvimento;
Síndrome de Turner: síndrome que causa baixa estatura e pode ser tratado com GH; baixa estatura,
infertilidade, malformações cardíacas, dificuldade de aprendizagem;
Adultos: deficiência de GH que pode ser normal ou no caso de pacientes com AIDS que é feita a reposição de
GH para o aumento de massa muscular e melhoria da qualidade de vida; pode acontecer também em pacientes
que tem lesão de hipotálamo ou hipófise, infecção, cirurgia ou radioterapia, que pode ser feita também a
reposição;
Isabel Oliveira Gusman
Uso do GH exógeno
Usado de forma errônea para aqueles que desejam aumento de eficiência corporal;
Combate a deficiência de crescimento;
Aumento da massa muscular;
Redução da gordura corporal;
Aumento de energia;
Manutenção dos tecidos;
Efeitos colaterais: sobrecarga hepática, diabetes, síndrome do túnel do carpo e do tarso, hipertensão
intracraniana (efeito mais comum na infância), acromegalia;
Pâncreas
Porção superior do abdômen;
Anfícrino: órgão com função exógena e endógena;
Ducto pancreático: libera as secreções no intestino;
Função exócrina: através da qual se produzem enzimas e sucos digestivos que são secretados no intestino;
Função endócrina; produz e secreta hormônios peptídicos que regulam o metabolismo energético do
organismo;
Possui dois principais tipos de tecidos: ácinos e ilhotas de langehans;
Ácinos: secretam sucos digestivos no duodeno;
Ilhotas de langehans: secretam hormônios peptídicos diretamente no sangue; 1 a 2 milhões; possui várias
células em sua composição:
Células α: produzem glucagon;
Células β: produzem insulina; ficam mais no centro da ilhota;
Células 𝜹 ou D: secretam somatostatina; inibe a secreção de insulina e glucagon;
Células PP ou F: secretam polipeptídeo pancreático que tem ação antagônica da colecistocinina;
Locais diferentes secretam somatostaina;
Insulina
Formado pelas células beta;
É um hormônio peptídico;
Composição do pró-hormônio: cadeia A com 21 AA, cadeia B com 30 AA, e ligação por duas pontes
dissulfeto e um peptídeo que liga a cadeia A com a B que é chamado de peptídeo C, que é importante para o
diagnóstico de ausência de insulina nos pacientes, caracterizando o diabetes tipo I; na última clivagem dentro
das vesículas do complexo de golgi, esse peptídeo fica separado das cadeias; na liberação da vesícula, peptídeo C
e insulina são liberados em mesma quantidade;
Meia vida da insulina: 5 a 8 minutos (curta) devido à insulinase que degrada a insulina nos rins, fígado,
músculo...
A insulinase não degrada peptídeo C, por isso ele é dosado para os diagnósticos;
Síntese da insulina
Inicialmente sintetizado dentro dos ribossomos do RER na forma de pré-pró-hormônio, que não é
funcional;
No CG, é retirado o peptídeo sinalizador, e é lançado nas vesículas do CG;
Nas vesículas, retira-se o peptídeo C e fica só a cadeia A e B;
Ele espera a sinalização de aumento da entrada de cálcio na célula para a exocitose da vesícula;
A exocitose libera na circulação insulina e peptídeo C;
Mecanismo de secreção da insulina
O aumento da glicemia é um estimulo para liberação da insulina;
Isabel Oliveira Gusman
O aumento da glicose no sangue faz com que ela entre nas células por meio de um transportador chamado de
GLUT-2;
Dentro da célula, ela vai ser fosforilada virando glicose-6-fosfato pela glucoquinase;
A glicose-6-fosfato vai ser oxidada transformando-se em ATP;
Os canais de K na membrana da célula são sensíveis ao nível de ATP, e se fecham quando a quantidade de
ATP aumenta, e esse fechamento deixa o potássio cada vez mais retido dentro da célula que tem carga positiva-
despolarização da membrana da célula beta pancreática;
Na membrana da célula também tem canal de cálcio, que é sensível a voltagem;
Essa despolarização da membrana coloca cálcio para dentro da célula e causa a exocitose das vesículas com
hormônios e peptídeo C;
Mecanismo de ação da insulina
O receptor da insulina é um tetrâmero, que possui 2 subunidades α e duas subunidades β;
Todas as subunidades são ligadas entre si por pontes dissulfeto;
As α ficam bem extracelular e as β ficam na membrana mesmo;
Todas as nossas células têm receptores de insulina para captação da glicose e geração de insulina;
As moléculas de insulina se ligam cada uma nas subunidades α que ativa as subunidades β, que é ligada na
tirosina quinase que vai fosforilar vários fatores de transcrição;
Entre os fatores de transcrição, transcreve aqueles que adicionam transportadores de glicose, GLUT, na
membrana da célula;
GLUTs: fazem difusão facilitada da glicose para dentro da célula; podem ser de 1 a 7;
GLUT 2: hepatócitos e célula beta pancreática;
GLUT 4: MEE e tecido adiposo;
GLUT 1: barreira hematocefálica; captam glicose mesmo sem insulina;
GLUT3: neurônios; captam a glicose mesmo sem insulina;
SGLT: transportadores de glicose associados ao sódio nas células do intestino e túbulo proximal do néfron;
permite a reabsorção da glicose;
Metabolismo dos carboidratos
Após uma refeição rica em carboidratos, a glicose que é absorvida para o sangue causa secreção de insulina;
A insulina atua em todos os tecidos para aumentar a captação de glicose para geração de energia, mas acontece
especialmente nos músculos, tecido adiposo e fígado;
Músculo: gasta muita energia, precisa captar muito como fonte de energia; a glicose é a primeira escolha e na
falta usa AG; a glicose fica armazenada na forma de glicogênio útil para os períodos curtos de uso energético
extremo; fornece pico de energia anaeróbica em poucos minutos; o glicogênio vira ácido lático e gera
energia;
Fígado: capta para dentro das células e forma glicogênio para armazenamento para manter constante a
glicemia; insulina inativa a fosforilase hepática (quebra o glicogênio em glicose) e aumenta a ação das
enzimas glicocinase (fosforila a glicose no fígado e não consegue sair por difusão) e glicogênio sintase (faz a
síntese do glicogênio); se estocou tudo e ainda tem excesso, a glicose vira TG; a insulina no fígado inibe a
gliconeogênese;
Cérebro: permeáveis a glicose, podendo usá-la sem a intermediação da insulina; os neurônios utilizam
normalmente apenas a glicose como fonte de energia; o choque hipoglicêmico causa irritabilidade nervosa
progressiva que leva a perda da consciência, convulsões e coma;
Metabolismo das gorduras
Síntese e armazenamento da gordura no tecido adiposo;
Insulina inibe ação da lipase hormônio-sensível e faz o transporte de glicose para as células adiposas inibe a
lipólise e armazena gordura no tecido adiposo;
Insulina: poupador de gordura- impede a utilização da gordura como fonte de energia e usa a glicose para isso;
Isabel Oliveira Gusman
A ausência de insulina a longo prazo provoca aterosclerose extrema pois deixa de inibir a lipase hormônio-
sensível ataques cardíacos, AVC e outros acidentes vasculares;
O AG em excesso no sangue pela ausência de insulina, chega no fígado, vai ser processado nas mitocôndrias e
vai liberar acetil-CoA formando ácido acético criando um quadro de acidose pela produção de corpos cetônicos;
Metabolismo das proteínas
Síntese de proteínas e armazenamento de AA;
Incentiva o transporte de AA: fenilalanina, valina, leucina, isoleucina e tirosina;
Aumenta a tradução de RNAm;
Aumenta o processo de transcrição de sequências genéticas selecionadas de DNA no núcleo celular;
Inibe o catabolismo de proteínas- gera menos AA livres;
Deprime a gliconeogênese no fígado devido a falta de AA livres;
Fatores estimuladores da liberação da insulina
Aumento da glicose sanguínea;
Aumento de AG livres no sangue: insulina encaminha AG para estoque no tecido adiposo;
Aumento de AA no sangue: transporta AA para síntese de proteínas;
Hormônios GI: liberação antecipada da insulina;
Glucagon, GH e cortisol: hormônios hiperglicêmicos;
Estimulação parassimpática pela acetilcolina;
Estimulação β-adrenérgica;
Resistência insulínica; obesidade;
Medicamentos do grupo sulfonilureia;
Fatores que diminuem a secreção da insulina
Diminuição da glicose sanguínea;
Jejum;
Somatostatina;
Atividade α-adrenérgica;
Leptina;
OBS: glicemia maior que 100 aumenta muito a liberação de insulina;
Glucagon
Hormônio protéico hiperglicemiante;
Cadeia peptídica de 29 aa;
Células α das ilhotas pancreáticas;
Meia vida: 6 minutos;
Estimulado pelo baixo nível de glicemia, aumento de AA no sangue (arginina e alanina- fonte de
gliconeogênese), exercício severo, epinefrina e norepinefrina (ação mediada pelos receptores β-
adrenérgicos);
Aumenta a degradação hepática de glicogênio, ativando as enzimas fosforilase e glicose fosfatase, liberando
glicose e fosfato- 4h acaba com o glicogênio hepático;
Aumenta a captação de AA pelo fígado incentivando a gliconeogênese;
Ativa a lípase do tecido adiposo, disponibilizando ácidos graxos para os sistemas de energia do organismo.
Também inibe o armazenamento de TG no fígado;
Aumenta a força do coração, o fluxo sanguíneo para alguns tecidos, secreção de bile e diminuir secreção de AG;
Glucagon, GH, adrenalina e cortisol são de ação contrária da insulina= hiperglicemiantes;
Mecanismo de ação
Isabel Oliveira Gusman
Atua em um receptor metabotrópico acoplado a proteína Gαs que ativa adenilato ciclase, aumenta AMP
cíclico e ativa uma proteína quinase que ativa uma fosforilase quinase b, que vai ser convertida em fosforilase
quinase a que faz glicogenólise;
Aumenta glicogenólise e gliconogênese aumenta glicose no sangue;
Formação de muitos corpos cetônicos que levam a alteração de pH;
Ativa a lípase hormônio-sensível;
Somatostatina
Liberada pela célula delta do pâncreas;
É um polipeptídeo de 14 aa;
Meia-vida: 3 minutos no sangue circulante (a meia-vida é curta por ser hormônio protéico);
Inibe a liberação da insulina e glucagon;
Ação parácrina: células vizinhas da ilhota pancreática;
Sua secreção é estimulada quando aumenta a glicose, AA, AG e hormônios GI;
Inibe a motilidade do estômago, duodeno e vesícula biliar;
Inibe a absorção de nutrientes: prolonga o esvaziamento gástrico, diminui a secreção de gastrina e de HCl,
diminui a secreção de suco pancreático, diminui o fluxo sanguíneo esplênico, diminui a absorção de glicose,
diminui a secreção de gastrina, secretina, colecistoquinina, peptídeo vasoativo intestinal, GTP e motilina;
Prolongar o tempo que os alimentos ficam no TGI sem ser degradados;
Polipeptídeo pancreático
Sintetizado pelas células PP da ilhota e pela mucosa intestinal;
É um hormônio protéico;
Colecistocinina: contração da vesícula biliar e liberação das enzimas do pâncreas;
Formado por 36 aa;
Antagonista da colecistocinina: inibe a secreção de enzimas pancreáticas e estimula a secreção gástrica;
A secreção é estimulada por refeições protéicas, jejum, exercício e hipoglicemia aguda;
Somatostatina e níveis elevados de glicose inibem a secreção;
Diabetes
Insulina sem ação ou não secretada= diabetes;
Hiperglicemia como resultado de defeitos na ação ou secreção da insulina;
Isabel Oliveira Gusman
Glicemia de jejum normal é <100; valores acima de 126 é diabético;
Glicemia pós prandial normal é <140; acima de 200 é diabético;
Glicemia casual normal é menor que 200;
Tipo I: autoimune; degradação das células beta do pâncreas; ausência de insulina; acontece com indivíduos
mais jovens; causa complicação aguda como cetoacidose; complicação crônica como neuropatia, retinopatia,
nefropatia...; pouca ou nenhuma insulina endógena; pode ser desencadeada por infecção viral na infância; o
quadro habitual de início é polidipsia, polifagia, poliúria e perda de peso; excreção de glicose na urina;
Tipo II: resistência à insulina, com função inadequada nas células beta para compensação; níveis mais altos
que o normal; complicação aguda hiperglicemia e crônicas iguais a do tipo I; forte componente hereditário e
relacionado com a obesidade; quadro habitual de início lento e tipicamente insidioso com sintomas de fadiga,
ganho de peso, cicatrização retardada de feridas e infecções recidivas;
Hormônios adrenocorticais
Glândulas adrenais: formadas pelo córtex e pela medula;
Córtex adrenal: cortisol, cortisona, aldosteona e hormônios sexuais;
Zona glomerulosa: secreta mineralocorticóide, principalmente a aldosterona;
Zona fasciculada: secreta glicocorticóide como o cortisol;
Zona reticular: secreta hormônios sexuais do tipo androgênios; androsterediona e
desidroepiandrosterona (é mais comumente dosado);
Medula adrenal: adrenalina e noradrenalina;
Todos são hormônios esteroidais derivados do colesterol;
Síntese dos hormônios adrenocorticais
Todos são derivados do colesterol LDL;
Nas mitocôndrias são clivadas pela colesterol desmolase formando pregnenolona;
ACTH e angiotensina II que estimulam a conversão do colesterol em pregnenolona;
O LDL é captado da circulação por meio da formação de receptores de LDL;
O LDL é endocitado e sofre ação do lisossomo liberando o colesterol;
O ACTH estimula a formação em vários pontos como aumentando receptores de LDL;
Zona glomérulosa: a pregnenolona vai para o RE e mitocôndria virando aldosterona;
Zona fasciculada: a pregnenonola forma o cortisol;
Zona reticular: a pregnenolona vira os androgênios;
Transporte
Cortisol se liga principalmente em proteínas plasmáticas, em especial a globulina ligadora de cortisol (CBG)
e o restante na albumina;
Meia vida: 60 a 90 minutos;
CBG pode sofrer saturação, e ai pode ligar na albumina ou ficar livre, causando um aumento de efeito;
Aumento da CBG: gravidez, administração de estrogênio, hipertireoidismo (aumento da formação de
proteínas)- diminui cortisol livre;
Diminui CBG: hipotireoidismo (diminuição da formação de proteínas), defeito genético em sua síntese,
deficiência de proteínas- aumenta cortisol livre;
Aldosterona se liga menos as proteínas plasmática, só 60% deixando sua meia vida mais curta de 20 minutos;
Estrogênio aumentado aumenta CBG- diminui a quantidade livre;
Metabolismo
Altamente lipossolúveis;
Precisa metabolizar no fígado para que seja eliminada na urina- principal via de eliminação (renal);
Sofre principalmente conjugação com ácido glicurônico;
Excretados na bile e em seguida nas fezes (25%) e o restante pelos rins;
Isabel Oliveira Gusman
Funções dos mineralocorticóides
Secreção de potássio e reabsorção de sódio, principalmente nas células epiteliais dos túbulos renais;
O aumento da liberação do sódio diminui o volume sanguíneo e o debito cardíaco;
A aldosterona atravessa a membrana das células e encontra os receptores no citoplasma;
Depois de ligados eles vão para o núcleo da célula e alteram transcrição e tradução;
Eles aumentam a quantidade de bombas de sódio e potássio e transportadores de sódio(Enac);
Capta mais Na para célula e ele volta para o sangue pela bomba de sódio e potássio que deixa o sangue
positivo e estimula a secreção de potássio e íons H+;
Aumenta o volume de líquido extracelular e a PA, mas apresenta pouco efeito na concentração
plasmática de sódio;
O aumento da reabsorção de sódio promove aumento da absorção osmótica de água e sede;
Secreção de íons hidrogênio que pode levar alcalose: troca de íons hidrogênio em troca de sódio nas
células intercaladas podendo levar à alcalose metabólica;
Estimulação a absorção intestinal de sódio: especialmente no cólon, o que impede a perda de sódio nas
fezes;
Regulação da secreção da aldosterona
Aumento do K extracelular: estimula zona glomerulosa a produzir aldosterona- principal via de secreção da
aldosterona;
Aumento da angiotensina II: pelo sistema renina angiotensina aldosterona; remédios inibidores de ECA
diminuem a produção de Ang II e consequentemente de aldosterona; a produção da aldosterona é dependente
da Ang II, mas não do cortisol;;
Aumento do fator natriurético atrial: inibe a liberação de aldosterona (mais importante inibidor);
Aumento do ACTH: permite a síntese da aldosterona; é um cofator necessário;
Funções dos glicocorticóides
Efeitos do cortisol sobre o metabolismo dos carboidratos: estimula a gliconeogênese, aumenta o
glicogênio hepático reduz a utilização celular de glicose e eleva a concentração sanguínea de glicose; é
hiperglicêmico; aumenta a glicemia- hiperglicemiantes, junto com o glucagon, GH e adrenalina; diminui a captação
de glicose para dentro das células;
Efeitos do cortisol sobre o metabolismo das proteínas: redução das proteínas celulares e aumenta as
concentrações plasmáticas e hepáticas de proteínas; transporta aminoácidos só para o fígado; estimula o
catabolismo de proteínas;
Efeito do cortisol sobre o metabolismo dos lipídeos: mobilização de AG e oxidação e obesidade
visceral e deposição de gordura no rosto e acima das clavículas; usa os AG como fonte de energia com um efeito
lipolítico já que reduz a glicose intracelular; a obesidade é pelo efeito central de estímulo a fome; redistribuição
de gordura- é lipolítico e lipogênico;
Efeitos anti-inflamatórios dos altos níveis de cortisol: estabiliza a membrana dos lisossomos, redução da
permeabilidade dos capilares (evita edema), redução da migração de leucócitos, redução da reprodução de
linfócitos, diminuição da febre e provoca a resolução da inflamação. Impede a ativação da fosfolipase A2 e não
forma PGE; forma liporcortina que inibe a fosfolipase A2 no início da cascata de inflamação;
Efeito permissivo sobre a liberação de catecolaminas: responde mais a substâncias vasoconstrictoras;
Estimula a síntese de eritropoetina: aumenta o número de hemácias;
Diminuição da função reprodutora;
Antagoniza a vitamina D, aumenta a reabsorção óssea e inibe os osteoblastos: pode levar a
osteoporose; ativa osteoclasto; inibe osteoblasto;
Inibe a proliferação fibroblástica e formação de colágeno: facilita formação de estrias;
Antagoniza ADH e aumenta a taxa de filtração glomerular: devido ao aumento do DC;
Fraqueza muscular: catabolismo da proteína muscular;
Aumento do ácido gástrico e pepsina: diminuição da produção de prostaglandina;
Isabel Oliveira Gusman
Efeitos psicológicos: pode ser pela falta ou excesso, depressão ou euforia;
Aumento da produção de surfactante pulmonar;
Inibe a secreção de GH: diminui a quantidade de receptores de GH, diminui atividade do IGF e diminui a
síntese de colágeno;
Mecanismo de ação
Altera transcrição reprimindo ou aumentando certas proteínas;
Liberação de CRH pelo hipotálamo, depois ACTH pela adeno-hipófise que atua na adrenal;
Pico de liberação de glicocorticóide é no início da manhã;
O cortisol que faz feedback negativo;
CRH hipófise ACTH córtex adrenal glicocorticóide, androgênios;
Androgênios adrenais
O mais importante é desidroepiandrosterona;
Secretado especialmente durante a vida fetal;
Precursores da progesterona e estrogênio em quantidades minúsculas;
Possivelmente promove desenvolvimento precoce dos órgãos sexuais masculinos na infância- aumento deles
indica início da puberdade na criança;
Efeitos leves nas mulheres ao longo da vida- crescimento de pelo púbico e axilar;
Em tecidos extra-adrenais alguns androgênios adrenais são convertidos em testosterona;
Anormalidades da secreção adrenococrtical
Doença de addison: deficiência mineralocorticóide; deficiência de glicocorticóide (dificuldade de manter
glicemia entre refeições); pigmentação por melanina (o aumento do ACTH faz sua clivagem liberando
hormônio melanócito estimulante que aumenta a pigmentação);
Síndrome de cushing: aumento da glicemia, mobilização de gordura, acne e hirsutismo, perda de proteínas,
estrias arroxeadas, osteoporose; pode acontecer com alta concentração de glicocorticóide exógeno;
Sindrome de conn: hipocalemia, alcalose metabólica leve, ligeira diminuição do volume de LEC, aumento
pequeno de sódio, hipertensão, diminuição da renina- tumor da célula da zona glomerulosa que leva ao excesso
de aldosterona;
Síndrome adrenogenital: na mulher causa crescimento de barba, masculinização da voz, aumento dos pelos
corporais, aumento do clitóris, aumento das proteínas musculares; nos homens pré-puberes tem rápido
desenvolvimento dos órgãos masculinos e aumento; em homens pós-puberes quase não tem efeito;
Isabel Oliveira Gusman
Você também pode gostar
- Equilíbrio hormonal _ Recupere equilíbrio hormonal, libido, sono e emagreça já!No EverandEquilíbrio hormonal _ Recupere equilíbrio hormonal, libido, sono e emagreça já!Nota: 5 de 5 estrelas5/5 (2)
- Eixo Hipotálamo-HipófiseDocumento3 páginasEixo Hipotálamo-HipófiseVictor D'Andrade100% (1)
- A Infertilidade Não É Apenas Um Problema Do CasalNo EverandA Infertilidade Não É Apenas Um Problema Do CasalNota: 2 de 5 estrelas2/5 (1)
- Trabalho - Hormonas Hipotálamo HipófiseDocumento44 páginasTrabalho - Hormonas Hipotálamo Hipófiseturma4md100% (2)
- Prolactina e Diabetes Melito do tipo 2: o efeito protetor de um hormônio sobre o metabolismo glicídicoNo EverandProlactina e Diabetes Melito do tipo 2: o efeito protetor de um hormônio sobre o metabolismo glicídicoAinda não há avaliações
- Fisiologia - Eixo Hipotálamo-HipofisárioDocumento3 páginasFisiologia - Eixo Hipotálamo-HipofisárioEduvaldo JúniorAinda não há avaliações
- Sistema endócrino e seus principais hormôniosDocumento33 páginasSistema endócrino e seus principais hormôniosGabriela MirandaAinda não há avaliações
- A3 - Sistema Digestório e EndócrinoDocumento4 páginasA3 - Sistema Digestório e EndócrinoLuciana100% (1)
- Aula EndócrinoDocumento78 páginasAula EndócrinoAlana GranemannAinda não há avaliações
- ROTEIRO DE ESTUDOS - Sistemas EndócrinosDocumento9 páginasROTEIRO DE ESTUDOS - Sistemas Endócrinosra119897Ainda não há avaliações
- Aula 10. Endocrinologia IDocumento43 páginasAula 10. Endocrinologia IanacleidecelestiniAinda não há avaliações
- Introdução à Endocrinologia e seus Principais HormôniosDocumento18 páginasIntrodução à Endocrinologia e seus Principais HormôniosWaldman Santos100% (1)
- Fisiologia Endócrina2023 Introdução (Modo de Compatibilidade)Documento18 páginasFisiologia Endócrina2023 Introdução (Modo de Compatibilidade)csbentaquiAinda não há avaliações
- Sistemas Fisiológicos Do Ser HumanoDocumento86 páginasSistemas Fisiológicos Do Ser Humanofejare2171Ainda não há avaliações
- 995 - Aula Do Eixo Hipotalamico Hipofisario Gonadal UterinoDocumento57 páginas995 - Aula Do Eixo Hipotalamico Hipofisario Gonadal UterinoJoão Paulo Da MataAinda não há avaliações
- Resumo Fisio EndocrinoDocumento19 páginasResumo Fisio EndocrinoDeise FariasAinda não há avaliações
- Fisiologia Do Sistema EndócrinoDocumento7 páginasFisiologia Do Sistema Endócrinoargosalves3091Ainda não há avaliações
- Sistema EndócrinoDocumento7 páginasSistema Endócrinolaisacarvalho27Ainda não há avaliações
- Eixo Hipotálamo-PituitáriaDocumento2 páginasEixo Hipotálamo-PituitáriaCoconut TcmAinda não há avaliações
- Sistema Talâmico HipofisárioDocumento7 páginasSistema Talâmico HipofisárioGiovanna MazzettiAinda não há avaliações
- Sistema EndócrinoDocumento28 páginasSistema EndócrinoBruno Felipe100% (1)
- Cap 74 - Introdução A EndocrinologiaDocumento7 páginasCap 74 - Introdução A Endocrinologiaisabella dacroceAinda não há avaliações
- Glândulas Endócrinas - Capitulo 18Documento10 páginasGlândulas Endócrinas - Capitulo 18rodrigo justoAinda não há avaliações
- Sistema EndócrinoDocumento52 páginasSistema EndócrinocamilaamenezessalustianoAinda não há avaliações
- 9 Fisiologia EndócrinaDocumento13 páginas9 Fisiologia EndócrinaThiago Henrique Oliveira100% (1)
- Reprodução - Fisiologia e Endocrinologia Do Ciclo EstralDocumento13 páginasReprodução - Fisiologia e Endocrinologia Do Ciclo EstralRebeca MoreiraAinda não há avaliações
- Fisiologia EndócrinaDocumento5 páginasFisiologia EndócrinaperronebiancaAinda não há avaliações
- Controle hipotalâmico do eixo hipotálamo-hipófise-ovárioDocumento27 páginasControle hipotalâmico do eixo hipotálamo-hipófise-ovárioAline Moura Savassini LucenaAinda não há avaliações
- Introdução A FisiologiaDocumento4 páginasIntrodução A Fisiologializ de andradeAinda não há avaliações
- Controle hormonal e doenças endócrinasDocumento29 páginasControle hormonal e doenças endócrinasmustafinha0% (1)
- Problema 5Documento12 páginasProblema 5Moises Popp de OliveiraAinda não há avaliações
- Sistema Endócrino 40Documento44 páginasSistema Endócrino 40Tiago PedroAinda não há avaliações
- Ciclo MenstrualDocumento11 páginasCiclo MenstrualNaro SantAinda não há avaliações
- Fisiologia Humana 5Documento5 páginasFisiologia Humana 5Alessandro PedrettiAinda não há avaliações
- Embriologia CICLOS REPRODUTIVOSDocumento3 páginasEmbriologia CICLOS REPRODUTIVOSKemily MarquesAinda não há avaliações
- Questionário FisioDocumento7 páginasQuestionário FisioLuísa Lima FernandesAinda não há avaliações
- Fisiologia do Sistema Endócrino: Funções, Hormônios e ControleDocumento7 páginasFisiologia do Sistema Endócrino: Funções, Hormônios e ControlePhelipe PessanhaAinda não há avaliações
- Sistema endócrino: glândulas e hormôniosDocumento44 páginasSistema endócrino: glândulas e hormôniosJanderson SousaAinda não há avaliações
- AIEsDocumento13 páginasAIEsLucasAinda não há avaliações
- O Eixo Hipotálamo-Hipófise e Seus HormôniosDocumento10 páginasO Eixo Hipotálamo-Hipófise e Seus HormôniosRebeca SleepyOakAinda não há avaliações
- Endocrinologia BásicaDocumento3 páginasEndocrinologia Básicajocely matheus de moraes netoAinda não há avaliações
- Fisiologia EndócrinaDocumento31 páginasFisiologia EndócrinaJuliana CampbellAinda não há avaliações
- 2018 Aula EndocrinoDocumento42 páginas2018 Aula EndocrinoVitoria GarcezAinda não há avaliações
- Sistema Endócrino em 40Documento56 páginasSistema Endócrino em 40Inês Lapa100% (1)
- Captura de Tela 2022-11-10 À(s) 01.13.49Documento19 páginasCaptura de Tela 2022-11-10 À(s) 01.13.49Rayane LopesAinda não há avaliações
- A Interpretaçoes de ResultadosDocumento1 páginaA Interpretaçoes de ResultadosDenise BengeAinda não há avaliações
- Fisiologia Do Sistema Endócrino (Veterinária) - Rosiane GomesDocumento50 páginasFisiologia Do Sistema Endócrino (Veterinária) - Rosiane GomesMaria GabriellyAinda não há avaliações
- Sistemas endócrinos dependentes e independentes do eixo hipotalâmico-hipofisárioDocumento11 páginasSistemas endócrinos dependentes e independentes do eixo hipotalâmico-hipofisárioDeize SantosAinda não há avaliações
- Controle Neuroendócrino Da ReproduçãoDocumento27 páginasControle Neuroendócrino Da ReproduçãoLuiz Henrique Ferreira100% (2)
- GH PRLDocumento31 páginasGH PRLTatiana PetroffAinda não há avaliações
- Fisio Endócrino LidianeDocumento26 páginasFisio Endócrino LidianeLaura SanchesAinda não há avaliações
- Sistema HormonalDocumento23 páginasSistema HormonalEster MelloAinda não há avaliações
- Sistema EndócrinoDocumento3 páginasSistema EndócrinoMatheus FranklinAinda não há avaliações
- Sistema endócrino: glândulas e hormôniosDocumento14 páginasSistema endócrino: glândulas e hormôniosVinicius Eduardo Brito KochAinda não há avaliações
- Anatomofisio ResumoDocumento6 páginasAnatomofisio ResumoAmanda BlaskaAinda não há avaliações
- Resumo Fisiologia EndocrinoDocumento6 páginasResumo Fisiologia EndocrinoStella CaceresAinda não há avaliações
- Sistema Hipotálamo-Hipofisário e suas HormonasDocumento21 páginasSistema Hipotálamo-Hipofisário e suas HormonasCarlos Francisco MacuveleAinda não há avaliações
- Secreçao HormonalDocumento21 páginasSecreçao HormonalFernando Baptista Felipe Leão LeãoAinda não há avaliações
- Fisiologia Veterinaria IIDocumento9 páginasFisiologia Veterinaria IIMelyssa NacaratiAinda não há avaliações
- Psico Aula01Documento61 páginasPsico Aula01adriellydutra2608Ainda não há avaliações
- Lista de Exerccios - Adio Eletroflica A Ligaes MltiplasDocumento7 páginasLista de Exerccios - Adio Eletroflica A Ligaes Mltiplasvi.andrade.6612Ainda não há avaliações
- CROMATOGRAFIADocumento6 páginasCROMATOGRAFIAfesfeAinda não há avaliações
- Duratar 3715 - Rev05Documento2 páginasDuratar 3715 - Rev05Eduardo SosnitzkiAinda não há avaliações
- Prática+10 AçúcaresDocumento12 páginasPrática+10 AçúcaresEdwin73952Ainda não há avaliações
- Exercicios 1Documento180 páginasExercicios 1Silva JoãoAinda não há avaliações
- Ilovepdf MergedDocumento725 páginasIlovepdf MergedWallace RodriguesAinda não há avaliações
- 9 Questões Nox, Oxidação e Redução - Parte 2Documento4 páginas9 Questões Nox, Oxidação e Redução - Parte 2SirlianeAinda não há avaliações
- Estudo Dirigido - Solubilidade Das Substâncias OrgânicasDocumento14 páginasEstudo Dirigido - Solubilidade Das Substâncias OrgânicasNathalia IsekiAinda não há avaliações
- Fundamentos de Cinética AplicadaDocumento62 páginasFundamentos de Cinética AplicadaEdson Eurico Salvador NipuedaAinda não há avaliações
- Exercícios de Análise de ÁguaDocumento8 páginasExercícios de Análise de ÁguaWiliam AkiraAinda não há avaliações
- Avaliação 2o bimestre EEE001-P011Documento6 páginasAvaliação 2o bimestre EEE001-P011Ricardo Pasquati PontarolliAinda não há avaliações
- 16 - Química II - Rodrigo Bandeira - RevisadaDocumento52 páginas16 - Química II - Rodrigo Bandeira - RevisadaRonald AbreuAinda não há avaliações
- Reoflux Hs BDocumento9 páginasReoflux Hs BDéboraAinda não há avaliações
- Regras de segurança para equipamentos em ambientes explosivosDocumento12 páginasRegras de segurança para equipamentos em ambientes explosivosNunoAinda não há avaliações
- Manual - Caldeiroes A Gas Série 900Documento21 páginasManual - Caldeiroes A Gas Série 900Alex de Jesus CostaAinda não há avaliações
- RoteiroDocumento3 páginasRoteiroThalita KattulyAinda não há avaliações
- Biologia - 10ºDocumento7 páginasBiologia - 10ºDuarte Ayres PereiraAinda não há avaliações
- Tabela de Preços 2011Documento27 páginasTabela de Preços 2011Tiago SantosAinda não há avaliações
- Detergente Desengraxante DcasaDocumento12 páginasDetergente Desengraxante Dcasapoliana.motaAinda não há avaliações
- Extração DNA kiwiDocumento4 páginasExtração DNA kiwibeatriz mouraAinda não há avaliações
- Sumaterm 400Documento2 páginasSumaterm 400antonio carlosAinda não há avaliações
- Síntese de Zeólita Faujasita usando Rejeito de CaulimDocumento144 páginasSíntese de Zeólita Faujasita usando Rejeito de CaulimNoberto Fontenele FrotaAinda não há avaliações
- M2 - Lista Revisional - Prova 01 - Bloco 03Documento11 páginasM2 - Lista Revisional - Prova 01 - Bloco 03Conteúdos de PRAinda não há avaliações
- Os fios da extensão de cílios: PBT, qualidade e reaçõesDocumento1 páginaOs fios da extensão de cílios: PBT, qualidade e reaçõesCarol CaramelloAinda não há avaliações
- Aulas TRat Gua Convencional Rennio PDFDocumento149 páginasAulas TRat Gua Convencional Rennio PDFMonaliza AraújoAinda não há avaliações
- Ácidos nucleicosDocumento2 páginasÁcidos nucleicosDaniele Castro AguiarAinda não há avaliações
- Prodesign M: técnica de instrumentação com limas manuais de níquel-titânioDocumento5 páginasProdesign M: técnica de instrumentação com limas manuais de níquel-titânioruan fernandesAinda não há avaliações
- Avaliação da qualidade do ar em área de influência de usina termelétricaDocumento18 páginasAvaliação da qualidade do ar em área de influência de usina termelétricaSuelem MontesAinda não há avaliações
- Processamento de RNA mensageiro em eucariotasDocumento3 páginasProcessamento de RNA mensageiro em eucariotasairton barrosAinda não há avaliações
- NBR NM11 2Documento30 páginasNBR NM11 2Engenheiro Eliton LeonardoAinda não há avaliações
- Equilíbrio hormonal _ Recupere equilíbrio hormonal, libido, sono e emagreça já!No EverandEquilíbrio hormonal _ Recupere equilíbrio hormonal, libido, sono e emagreça já!Nota: 5 de 5 estrelas5/5 (2)
- Atlas de anatomia: Imagens humanas e veterináriasNo EverandAtlas de anatomia: Imagens humanas e veterináriasNota: 4.5 de 5 estrelas4.5/5 (2)
- Equilíbrio iônico: aplicações em química analíticaNo EverandEquilíbrio iônico: aplicações em química analíticaAinda não há avaliações
- Química da Cerveja: Uma Abordagem Química e Bioquímica das Matérias-Primas, Processo de Produção e da Composição dos Compostos de Sabores da CervejaNo EverandQuímica da Cerveja: Uma Abordagem Química e Bioquímica das Matérias-Primas, Processo de Produção e da Composição dos Compostos de Sabores da CervejaAinda não há avaliações
- Problemas de Cinética e Reatores Químicos: 100 Problemas Resolvidos, 500 Problemas Propostos (Com Respostas)No EverandProblemas de Cinética e Reatores Químicos: 100 Problemas Resolvidos, 500 Problemas Propostos (Com Respostas)Ainda não há avaliações
- Simetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaNo EverandSimetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- Para Gostar de Química: Introdução à Química GeralNo EverandPara Gostar de Química: Introdução à Química GeralAinda não há avaliações
- Detetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseNo EverandDetetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseAinda não há avaliações
- Uso do Policloreto de Alumínio (PAC): vantagens sobre o Sulfato de Alumínio em sistema de tratamento de águaNo EverandUso do Policloreto de Alumínio (PAC): vantagens sobre o Sulfato de Alumínio em sistema de tratamento de águaAinda não há avaliações
- Princípios de química analítica: Abordagem teórica qualitativa e quantitativaNo EverandPrincípios de química analítica: Abordagem teórica qualitativa e quantitativaNota: 5 de 5 estrelas5/5 (1)
- Química na Educação Básica: Ferramentas teóricas e práticasNo EverandQuímica na Educação Básica: Ferramentas teóricas e práticasNota: 4 de 5 estrelas4/5 (1)
- Uma breve história da química: Da alquimia às ciências moleculares modernasNo EverandUma breve história da química: Da alquimia às ciências moleculares modernasAinda não há avaliações
- Reologia do Concreto: Fatores influentes para previsão da retração e fluênciaNo EverandReologia do Concreto: Fatores influentes para previsão da retração e fluênciaAinda não há avaliações
- Reatores Químicos em Leito Fluidizado: modelagem e simulaçãoNo EverandReatores Químicos em Leito Fluidizado: modelagem e simulaçãoAinda não há avaliações