Escolar Documentos
Profissional Documentos
Cultura Documentos
Apostila FQII PDF
Apostila FQII PDF
Enviado por
Renato ZanTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Apostila FQII PDF
Apostila FQII PDF
Enviado por
Renato ZanDireitos autorais:
Formatos disponíveis
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
MINISTRIO DA EDUCAO
UNIVERSIDADE FEDERAL DO CEAR
CENTRO DE CINCIAS
DEPARTAMENTO DE QUMICA
ANALTICA E FSICO-QUMICA
MANUAL DE PRTICAS
DISCIPLINA: FSICO-QUMICA II
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
EXPERIMENTOS
1. DETERMINAO DO COEFICIENTE DE VISCOSIDADE PELO
VISCOSMETRO DE OSTWALD.......................................................................3
2. INFLUNCIA DA TEMPERATURA NO COEFICIENTE DE
VISCOSIDADE DE LQUIDOS ...........................................................................7
3. POLARIMETRIA: VERIFICAO DA LEI DE BIOT EM SOLUO.......9
4. CONSTRUO DO DIAGRAMA TERNRIO DE COMPOSIO
CIDO ACTICO CLOROFRMIO GUA............................................13
5. CONSTRUO DO DIAGRAMA TERNRIO DE COMPOSIO
GUA ETANOL BENZENO ........................................................................15
6. DETERMINAO DO VOLUME MOLAR PARCIAL NaCl/H2O ...........16
7. DETERMINAO DA CONCENTRAO MICELAR CRTICA DE
UM SURFACTANTE...........................................................................................19
8. MEDIDA DA TENSO SUPERFICIAL: MTODO DA GOTA ...................22
9. ABAIXAMENTO DO PONTO DE FUSO ......................................................26
10. ANEXOS................................................................................................................27
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
DETERMINAO DO COEFICIENTE DE VISCOSIDADE PELO VISCOSMETRO
DE OSTWALD
1. Objetivos: Determinar o coeficiente de viscosidade relativa, dinmica e cinemtica de
solues, utilizando o viscosmetro de Ostwald ou de Cannon-Fenske.
2. Teoria:
Reologia a cincia que trata das deformaes e fluxo de materiais causados pela
aplicao de uma fora. O estudo da reologia importante pois o conhecimento das propriedades
reolgicas do material (como viscosidade) permite conhecer o comportamento dos materiais nas
mais variadas situaes durante a produo, transporte, armazenagem, etc.
As faixas de viscosidade apresentadas por materiais comuns, encontram-se abaixo.
Viscosidades de alguns materiais muito comuns:
MATERIAL
VISCOSIDADE (Pa-s)
Vidro
1040
Vidro Fundido
1012
Polmeros Fundidos
103
Mel
10
Glicerol
1
leo de oliva
0,1
gua
0,001
Ar
10-6
Quando um lquido escoa atravs de um tubo estreito, sem turbulncia, isto , de modo
contnuo e regular, a velocidade de escoamento depende, em primeiro lugar, da fora que o
produz. Alm disso, uma vez que as diferentes partes do lquido no se movem no interior do
tubo com a mesma velocidade, isto , as camadas mais prximas s paredes do tubo se movem
mais lentamente que as camadas centrais, e a velocidade alcana um mximo no centro do tubo,
podemos considerar a corrente lquida como composta de um grande nmero de cilindros
concntricos, cada um movendo-se com velocidade constante, qual superior do vizinho
imediato e de maior dimetro. Produz-se, assim, um deslizamento ou movimento das diferentes
camadas, umas em relao s outras, na direo do escoamento. A este deslocamento das
diferentes camadas, ope-se o atrito interno (atrito entre os cilindros sucessivos) e o coeficiente
de viscosidade de um lquido uma medida deste atrito.
Se considerarmos uma camada retangular e delgada (de espessura dx) do lquido, cuja
superfcie superior (de rea A) se move relativamente superfcie inferior (tambm de rea A)
com uma velocidade dV, a fora F que se necessita aplicar, tangencialmente, s superfcies
superior e inferior, para manter o gradiente de velocidade (dV/dx), depender da viscosidade do
lquido, isto :
(F/A) (dV/dx) ou (F/A) = (dV/dx)
(1)
A grandeza (eta), definida por esta equao, o coeficiente de viscosidade dinmica.
Este coeficiente de viscosidade numericamente igual fora tangencial, por unidade de
rea, necessria para manter uma unidade de velocidade de deslocamento de dois pontos
paralelos, afastados de uma unidade de distncia, o espao entre eles estando cheio com um
lquido viscoso. A viscosidade de um fluido pode ser determinada por vrios mtodos
experimentais, como, por exemplo, a medida do tempo de vazo de um lquido atravs de um
capilar (neste caso o coeficiente de viscosidade dado pela Lei de Poiseuille); a medida do
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
tempo de queda de uma esfera atravs de um lquido (utilizando-se a lei de Stoke obtm-se o
coeficiente de viscosidade) etc.
No sistema CGS a unidade de viscosidade dinmica o Poise (g/cm.s). A viscosidade
cinemtica, definida como = /, onde a viscosidade dinmica e a massa especfica do
lquido, tem por unidade o Stoke (cm2/s).
No caso da vazo de um lquido atravs de um capilar o coeficiente de viscosidade,
segundo Poiseuille, :
.r 4 .t. p
(2)
8.V .l
onde: P a presso hidrosttica sobre o lquido, em N.m-2,
V o volume em m3 (volume do lquido que flui em t segundos atravs do capilar de raio
r e de comprimento l, ambos em metros).
O viscosmetro de Ostwald (Fig.1) ou de Cannon-Fenske permite uma determinao
simples do coeficiente de viscosidade desde que seja conhecida sua constante.
No entanto, quando se desconhece a constante, as medidas de viscosidade so feitas
por comparao entre o tempo de vazo do lquido cuja viscosidade se deseja determinar e
de um lquido de viscosidade conhecida, geralmente gua. Na mesma temperatura e no
mesmo aparelho.
Lquido
Figura 1 : Viscosmetro de Ostwald .
A partir da equao (2) aplicada ao lquido de viscosidade desconhecida e ao lquido
padro, obtm-se a equao (3), a qual nos permite determinar a viscosidade relativa do lquido:
rel
1
2
t
t
1
(3)
onde : 1 e 2 so os coeficientes de viscosidade dinmica, do lquido em estudo e da gua,
respectivamente.
1 e 2 so os valores de massa especfica dos fluidos desconhecido e conhecido,
respectivamente, e t1 e t2 so os tempos gastos para que se escoem volumes iguais.
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
As viscosidades dinmica e cinemtica podem ser calculadas, respectivamente, atravs
das equaes: 1 = rel . 2 (4) e = 1 / 1 (5).
A viscosidade uma propriedade importante, tanto em trabalhos prticos como tericos.
Em biologia e fisiologia o viscosmetro utilizado no estudo das propriedades do sangue. Em
tecnologia, tem sido aplicado na soluo de uma grande variedade de problemas relacionados
com: tintas, fibras, colas, borracha e outros produtos industriais. Em projetos de Engenharia
Qumica, a viscosidade um fator importante, pois o custo de bombas muitas vezes
considervel e isto depende muito da viscosidade dos lquidos ou gases a serem transportados.
A preciso na operao, com este viscosmetro, depende do controle e da medida das
seguintes variveis: temperatura, tempo, alinhamento vertical do capilar e volume da substncia
estudada.
3. Material Necessrio:
1 viscosmetro de Ostwald, 1 cronmetro, 1 picnmetro, tubo de borracha, 1 pipeta (seu volume
depende do volume do viscosmetro), 1 termmetro 0-100 0C , 1 banho termosttico.
4. Tcnica Experimental:
1. O viscosmetro deve estar limpo e seco.
2. Prepare 100 mL de uma soluo de NaCl 0,500 mol/L e, por diluio, 50 mL das solues
de 0,300 e 0,100 mol/L.
3. Prepare 100 mL de uma soluo de C12H22O11 (sacarose) 0,010 mol/L e, por diluio, 50
mL das solues de 0,006 e 0,002 mol/L.
4. Coloque um certo volume (6mL) de gua no viscosmetro pela extremidade 1. Por suco
com um tubo de borracha na extremidade 2, eleve o lquido no interior do tubo e
verifique se este volume suficiente para ultrapassar a marca A sem que falte lquido
entre as marcas A e C (ver Figura 1 b).
5. Verifique se o nvel do lquido em repouso est a +/- 1 cm abaixo da marca B.
6. Determine (com uma pipeta), o volume de gua do viscosmetro que satisfaa estas
condies e ANOTE este valor.
7. Coloque o viscosmetro, contendo o volume de gua acima determinado, num banho
termosttico a 25 0C (a parte do viscosmetro que contm o lquido deve ficar submersa).
Espere que o sistema atinja o equilbrio trmico.
8. Por suco, atravs do tubo de borracha, eleve o lquido no interior do tubo at a marca
A. Deixe o lquido escoar para verificar se o escoamento est se processando
convenientemente e sem que gotas fiquem aderidas s paredes do tubo. Se isto acontecer,
o viscosmetro deve ser esvaziado e novamente limpo com cuidado. Torne a aspirar o
lquido at uns 2 centmetros acima da marca superior (reproduzir sempre esta mesma
posio em todas as medidas, no devendo elevar-se acima do nvel da gua do banho
termosttico) e tire o tubo de suco.
Quando o menisco do lquido passar pelo trao superior, d partida ao cronmetro.
Quando o menisco alcanar a marca inferior, trave o cronmetro.
Repita a determinao trs vezes com o mesmo lquido.
Se o viscosmetro estiver convenientemente limpo, os tempos de escoamento no
diferiro de mais de 0,2%. No caso de tempos de escoamento diferirem de mais de 0,2%,
precisa-se examinar cuidadosamente a tcnica e o material para encontrar a origem dos erros.
9. Retire o viscosmetro do banho termosttico e seque-o. Lave ento com o lquidoproblema para se ter certeza de que no ficou nenhum resduo do lquido anterior.
10. Torne a colocar o viscosmetro no banho termosttico. Por meio da pipeta coloque no
viscosmetro, o volume da substncia (ou soluo) cuja viscosidade deve ser
determinada. Espere 5 minutos para que se estabelea o equilbrio trmico, e repita o
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
procedimento, tendo o cuidado de conduzir as operaes nas mesmas condies
anteriores.
11. Observe que necessrio determinar a massa especfica de cada lquido ou soluo.
PICNMETRO: Utilize um picnmetro de 25 ou 50 ml para determinar a massa especfica de
cada lquido nas respectivas temperaturas em que foram feitas as determinaes das
viscosidades.
COMO PROCEDER: Pese o picnmetro vazio. Depois de pesado, encha o picnmetro com o
lquido-problema (faa primeiro para a gua) e coloque-o para termostatizar (mesma temperatura
do viscosmetro) durante +/- 5 minutos. Tire o picnmetro do banho rapidamente, seque-o bem e
pese-o. Repita este procedimento para as outras temperaturas utilizadas (30 e 40 0C) (menos para
a gua). Atravs da frmula ( = m / v) voc obtm o valor da massa especfica do lquido
naquela temperatura. (No esquea de descontar a massa do picnmetro vazio).
OBS: Este procedimento feito para a gua a 25 0C para aferir o volume do picnmetro. O
valor da massa especfica da gua se encontra na TABELA I, para a temperatura utilizada.
presso de uma atmosfera, a viscosidade da gua, segundo o National Bureau of
Standards, dada na TABELA I.
TABELA I - Coeficiente de viscosidade e massa especfica da gua a vrias temperaturas. Obs:
1 Poise = din.s.cm-2
Temperatura
Coeficiente de viscosidade
Massa especfica (g.cm-3)
0
( C)
(milipoise)
10
13,070
0,99973
15
11,390
0,99913
20
10,020
0,99822
25
8,904
0,99707
30
7,975
0,99568
35
7,194
0,99406
40
6,529
0,99225
50
5,468
0,98807
60
4,665
0,98323
5. Tratamento dos Dados Experimentais:
Para cada lquido-problema, complete a seguinte tabela em seu caderno:
H2O =
H2O (g/mL) =
tH2O (segundos) =
Lquido
t (segundos)
1
Concentrao (mM)
(g/mL)
Rel
t1
t2
t3
gua
Tire a mdia dos 3 tempos de cada soluo, faa um clculo de erro.
Faa um grfico do coeficiente de viscosidade dinmica pela concentrao da soluo.
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
INFLUNCIA DA TEMPERATURA NO COEFICIENTE DE VISCOSIDADE DE
LQUIDOS
1. Objetivos: Determinar o coeficiente de viscosidade de alguns lquidos a vrias
temperaturas, utilizando o viscosmetro de Ostwald ou de Cannon-Fenske.
2. Teoria:
O efeito da temperatura sobre o coeficiente de viscosidade de um fluido difere
notadamente segundo o fluido lquido ou gs. Nos gases, o coeficiente aumenta com a
temperatura, mas nos lquidos diminui marcadamente com a elevao da temperatura.
A relao dos coeficientes de viscosidade dos lquidos com a temperatura dada pela
equao de Carrancio:
B
= A . exp B/RT
ou
(1)
ln = ln A +
R.T
onde : A e B so constantes prprias dos lquidos dados, sendo B uma medida de energia
necessria para fazer o lquido fluir.
A partir da determinao do coeficiente de viscosidade de um lquido em diferentes
temperaturas possvel, graficamente, determinar-se os valores das constantes A e B.
Neste experimento tambm ser determinado o coeficiente de viscosidade relativa para
posterior clculo do coeficiente de viscosidade da substncia ou soluo.
3. Tcnica Experimental:
Repita o processo descrito anteriormente (para uma nica temperatura), para diferentes
temperaturas 30 e 40 0C, desde que a temperatura de ebulio do lquido-problema no esteja
muito prximo da temperatura do banho termosttico. Para cada temperatura, faa os
experimentos com gua e com os lquidos-problemas.
1. O viscosmetro deve estar limpo e seco.
2. Coloque um certo volume de gua no viscosmetro pela extremidade 1. Por suco com
um tubo de borracha na extremidade 2, eleve o lquido no interior do tubo e verifique se
este volume suficiente para ultrapassar a marca A sem que falte lquido entre as marcas
A e C (ver Figura 1 b, do roteiro anterior).
3. Verifique se o nvel do lquido em repouso est a +/- 1 cm abaixo da marca B.
4. Determine (com uma pipeta), o volume de gua do viscosmetro que satisfaa estas
condies e ANOTE este valor.
5. Coloque o viscosmetro, contendo o volume de gua acima determinado, num banho
termosttico a 25 0C (a parte do viscosmetro que contm o lquido deve ficar submerso).
Espere que o sistema atinja o equilbrio trmico.
6. Por suco, atravs do tubo de borracha, eleve o lquido no interior do tubo at a marca
A. Deixe o lquido escoar para verificar se o escoamento est se processando
convenientemente e sem que gotas fiquem aderidas s paredes do tubo. Se isto acontecer,
o viscosmetro deve ser esvaziado e novamente limpo com cuidado. Torne a aspirar o
lquido at uns 2 centmetros acima da marca superior (reproduzir sempre esta mesma
posio em todas as medidas, no devendo elevar-se acima do nvel da gua do banho
termosttico) e tire o tubo de suco.
Quando o menisco do lquido passar pelo trao superior, d partida ao cronmetro.
Quando o menisco alcanar a marca inferior, trave o cronmetro.
Repita a determinao trs vezes com o mesmo lquido.
Se o viscosmetro estiver convenientemente limpo, os tempos de escoamento no
diferiro de mais de 0,2%. No caso de tempos de escoamento diferirem de mais de 0,2%,
precisa-se examinar cuidadosamente a tcnica e o material para encontrar a origem dos erros.
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
7. Retire o viscosmetro do banho termosttico e seque-o. Lave ento com o lquidoproblema para se ter certeza de que no ficou nenhum resduo do lquido anterior.
8. Torne a colocar o viscosmetro no banho termosttico. Por meio da pipeta coloque no
viscosmetro o volume da substncia (ou soluo) cuja viscosidade deve ser determinada
(mesmo volume utilizado anteriormente). Espere 5 minutos para que se estabelea o
equilbrio trmico, e repita o procedimento, tendo o cuidado de conduzir as operaes nas
mesmas condies anteriores.
9. Observe que necessrio determinar a massa especfica de cada lquido ou soluo
em cada temperatura.
4. Tratamento dos Dados Experimentais:
Para cada lquido e para cada temperatura, complete a seguinte tabela em seu caderno:
Lquido =
Temperatura H2O
H2O (g/mL)
tH2O (seg.)
Liq (g/mL) t Liq (seg.)
Liq
Lquido =
Temperatura H2O
H2O (g/mL)
tH2O (seg.)
Liq (g/mL) t Liq (seg.)
Liq
Lquido =
Temperatura H2O
H2O (g/mL)
tH2O (seg.)
Liq (g/mL) t Liq (seg.)
Liq
Em seguida complete a tabela abaixo:
Lquido
T(K)
T-1
ln
Faa um grfico do logaritmo do coeficiente de viscosidade dinmica em funo do
inverso da temperatura absoluta, para cada lquido (inclusive a gua). Usando a equao (1),
determine graficamente as duas constantes A e B para cada lquido.
Se for necessrio, calcule estas constantes pelo mtodo dos mnimos quadrados.
Apresente os resultados de viscosidades utilizando as unidades em Pa.s (kG.m-1s-1) e os
termos relacionados com energia em Joules/mol.
Compare os valores de A e B dos diferentes lquidos.
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
POLARIMETRIA: VERIFICAO DA LEI DE BIOT EM SOLUO
1. Objetivos:
Determinar o poder rotatrio tico especfico da sacarose, e o teor de sacarose em uma
amostra impura (com contaminante no ativo oticamente).
2. Introduo:
Sabe-se que a luz natural constituda de ondas eletromagnticas que se propagam em
todas as direes, em infinitos planos de vibrao. Como exemplo cita-se a luz solar, uma
lmpada incandescente etc. Por outro lado, quando a luz natural passada atravs de um prisma
polarizador de Nicol a radiao emergente vibra em apenas um plano de vibrao e
denominada luz polarizada. Poder ser policromtica ou monocromtica, dependendo da fonte
luminosa.
Quando um feixe de luz plano-polarizada monocromtica atravessa um tubo de
comprimento igual a L, cheio com uma soluo contendo uma substncia oticamente ativa
(possui em sua molcula um tomo de carbono assimtrico ou chiral), de concentrao C, o
desvio angular do plano de polarizao dado por:
[ ]
20
A constante
[ ] LC
20
D
(1)
o poder rotatrio tico especfico caracterstico da substncia (em
20,0C a rotao especfica da sacarose, sob luz de sdio, 66,53o e a da glicose 52,7o) e
depende do comprimento de onda do feixe de luz e da temperatura. definido como sendo o
ngulo-desvio (em graus angulares) apresentado por uma alquota de uma soluo cuja
concentrao de um quilograma (1000 g) de substncia oticamente ativa por metro cbico
(1000L) de soluo, colocada em um tubo polarimtrico de 1 metro (10 dm) de comprimento e
observada, a 20,0C, sob luz de sdio; L o comprimento, em dm, do tubo polarimtrico; C a
concentrao da soluo em g/cm3 e a rotao observada, em graus angulares. No Sistema
Internacional (SI), [
20
D
= m e sua unidade rad.m2/kg.
Pela expresso (1) v-se que o ngulo-desvio varia linearmente com a concentrao.
O desvio angular medido com um polarmetro, cujo esquema o seguinte:
Figura 1
A luz proveniente de uma fonte luminosa monocromtica (L), polarizada ao atravessar
um prisma de Nicol (P). Aps este prisma, o feixe luminoso atravessa o lquido contido no tubo
(T) e, em seguida, outro prisma de Nicol chamado analisador (A). O campo do instrumento
observado com a ocular (0). O analisador pode girar em torno do eixo longitudinal do
instrumento enquanto que o polarizador fixo. Quando o tubo (T) contm uma substncia que
no possui atividade tica (por exemplo, a gua) e o analisador est cruzado com o polarizador,
nenhuma luz passar e o campo do instrumento, portanto, se apresentar escuro. Esta situao
corresponde ao zero gravado no limbo do aparelho. Caso o tubo (T) contenha uma substncia
oticamente ativa, o raio luminoso sofrer uma rotao no seu plano de polarizao. Para que o
Fsico-Qumica Experimental - 2006/02
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
campo fique novamente escuro necessrio girar o analisador de certo ngulo, que ser
registrado no limbo e representa o desvio angular.
O polarmetro tem um dispositivo auxiliar, que torna a medida do desvio angular mais
precisa. Graas a ele o campo visual do instrumento fica dividido em trs partes (ver Figura 2).
Quando o analisador est um pouco antes da posio cruzada em relao ao polarizador a parte
central do campo visual torna-se escura e as partes laterais tornam-se claras (ver Figura 3).
Quando o analisador est um pouco alm da posio cruzada em relao ao polarizador, a
parte central do campo visual torna-se clara e as partes laterais tornam-se escuras (ver Figura 4).
Uma posio intermediria, em que as trs partes do campo esto totalmente sombreadas,
corresponde ao cruzamento dos dois prismas (ver Figura 5).
Caso o prisma analisador esteja na mesma posio que o prisma polarizador, o campo
apresenta-se totalmente iluminado (ver Figura 6).
Fig. 2 Campo visual
dividido em trs partes.
Fig.03 Analisador um
pouco antes da posio
cruzada em relao ao
polarizador
Fig. 05 Analisador na posio
cruzada em relao ao polarizador, com
o campo visual totalmente sombreado.
Fig.04 Analisador um
pouco alm da posio
cruzada em relao ao
polarizador.
Fig. 06 Analisador paralelo ao
polarizador com o campo visual
totalmente claro.
Leitura da escala
Sempre que se adicionar uma nova soluo no tubo
para uma leitura, antes de se fazer o ajuste do analisador
deve-se ajustar a escala (lateral ao visor) na posio 0,00,
conforme figura 7, ao lado. Alinhamento das marcaes do
ponto zero da escala de dentro (fixa) com a marcao do
ponto zero da escala de fora (mvel).
Escala fixa
Se a soluo no tubo no apresentar desvio da luz
plano-polarizada (desvio 0,00) o campo visual ser idntico
ao da figura 6, com a escala conforme figura ao lado.
No entanto, estando a escala ajustada na posio 0,00
e se for adicionada ao tubo uma soluo que apresente
desvio da luz plano-polarizada (desvio 0,00) o campo
visual ser idntico ao da figura 3 ou ao da figura 4. Uma
vez visto isso, deve-se procurar ajustar (lentamente) o
analisador de modo a se observar novamente a imagem da
figura 6. Para o caso de uma soluo de sacarose, que
apresenta desvio positivo, devemos girar o analisador no
Fsico-Qumica Experimental - 2006/02
Figura 7: Escala polarmetro.
10
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
sentido horrio. Aps encontrar-se a posio na qual se
observa a imagem da figura 6 faz-se a leitura do desvio
angular.
Supondo que para uma soluo hipottica o ajuste
tenha ficado conforme a figura 8, ao lado. O valor lido ser
de 6,15 graus.
O ponto de referncia a marcao do zero da escala
fixa. Como ele est entre 6 e 7 da escala mvel devemos
anotar 6,_ _. Os dois ltimos algarismos (os dois depois da
vrgula) so obtidos na escala fixa da seguinte maneira.
Procure a primeira marcao (risco) da escala fixa que
coincida exatamente com uma marcao (qualquer) da
escala mvel, o nmero correspondente a esta marcao
(fixa) lhe fornece os nmeros depois da vrgula. Neste caso
teremos 6,15 pois a quarta marcao da escala fixa est
alinhada com uma da mvel.
Obs.: Observe a diviso das escalas
Figura 8: Escala polarmetro.
A rotao especfica (tal como o ponto de fuso e o de ebulio) uma constante fsica
importante para a identificao de substncias.
A polarimetria, dentre outras aplicaes, utilizada na indstria alimentcia e na anlise
de produtos farmacuticos.
3. Procedimento Experimental:
Obs. Ateno para o item 9. A primeira leitura a ser feita deve ser da soluo mais
concentrada.
1. Prepare 100 ml de uma soluo contendo 0,15 g/mL de sacarose.
2. Por diluio prepare 50 mL de soluo de sacarose com as seguintes concetraes: 0,10, 0,05
e 0,02. Tenha o cuidado de restar ao menos 30 mL de cada soluo.
3. Ligue a lmpada de sdio.
4. Encha o tubo do polarmetro com gua destilada e coloque-o no instrumento. Tenha o
cuidado de no deixar bolhas de ar no interior do tubo e de limpar suas faces externamente.
5. Observe a ocular do instrumento de maneira a distinguir nitidamente as linhas que separam
as trs partes do campo visual do polarmetro. Gire a alavanca que comanda a posio do
analisador no sentido horrio ou anti-horrio, at observar que h uma inverso na
iluminao das partes central e lateral do campo visual. Em seguida, gire o analisador no
sentido que torne as trs partes igualmente iluminadas. Determine, cuidadosamente, este
ponto e anote o ngulo encontrado, que deve ser igual a zero (ou 90) grau(s). Caso isto no
ocorra o polarmetro necessita de um ajuste especial. Mesmo assim, anote a leitura (s).
6. Esvazie o tubo polarimtrico e lave-o com a soluo a ser analisada. Em seguida, encha-o
com a prpria soluo e elimine as bolhas de ar, caso existam. Por fim, feche o tubo e limpeo externamente. Repita as operaes do item 6 e anote o desvio angular (obs).
7. Operando de maneira anloga, determine o desvio angular para as demais solues.
8. Prepare a soluo da amostra problema (sacarose impura) e faa a leitura.
9. Depois de feita a leitura do desvio apresentado pela soluo mais concentrada, devolva a
mesma para seu frasco e em seguida adicione 0,5 mL de HCl concentrado e ao final da aula
repita a leitura da mesma.
Fsico-Qumica Experimental - 2006/02
11
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
4. Clculos e Resultados:
a) Organize seus dados sob a forma da seguinte tabela:
Desvio angular do solvente (H2O) = s =
Comprimento do tubo =
dm
Temperatura =
C
Soluo
Concentrao
C (g/cm3)
Desvio
angular Desvio angular final,
f = obs - s
observado (obs)
solvente
1
2
3
4
???
problema
OBS.: f o desvio angular final e obs o desvio angular observado.
b) Construa um grfico relacionando o desvio angular com a concentrao de sacarose e,
apartir deste, obtenha o valor do poder rotatrio tico especfico da sacarose.
c) Graficamente encontre o valor da concentrao de sacarose na soluo da amostra
problema, para em seguida determinar qual o teor de sacarose na mesma.
d) Discuta o resultado observado no item 10 do procedimento.
Fsico-Qumica Experimental - 2006/02
12
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
CONSTRUO DO DIAGRAMA TERNRIO DE COMPOSIO CIDO ACTICO
CLOROFRMIO GUA
1. Objetivos:
Construir um diagrama de fases de um sistema de trs componentes.
2. Introduo:
De acordo com a regra das fases, quando o nmero de componentes for igual a trs, o
nmero de graus de liberdade de um sistema monofsico deve ser igual a quatro (presso,
temperatura e numero de moles de dois componentes).
CH3COOH
L=C+2F=5F
0,0 1,0
Mantendo-se constantes a
temperatura e a presso, tem0,1
0,9
se 2 variveis independentes e
0,2
0,8
o
diagrama
pode
ser
construdo no plano.
0,3
0,7
L** = 3 F
0,4
0,6
O sistema em estudo
constitudo
por
dois
0,5
0,5
componentes
lquidos
0,6
0,4
parcialmente miscveis entre si
0,7
0,3
e um completamente miscvel
nos dois. O diagrama de fases
0,8
0,2
desses 3 componentes pode
0,9
0,1
ser apresentado na forma
triangular, onde cada vrtice
1,0
0,0
corresponde a um componente CHCl3 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0
H2O
puro (Figura ao lado).
Nessa figura, a curva dentro do diagrama representa a interface de separao entre duas
regies distintas: acima da curva a regio de uma fase, e abaixo a regio de duas fases.
Cada lado ir indicar sistemas binrios. As linhas que indicam uma concentrao
constante de um dado componente so paralelas ao lado oposto do vrtice representando este
componente. Por exemplo, considerando-se o componente B, a linha AC (o prprio lado oposto)
indica os pontos onde no h componente B, existindo apenas A e C (0% de B). As linhas
paralelas ao lado AC e em direo ao vrtice B indicam, sucessivamente, as concentraes
crescentes de B (10%, 20%, etc.). De modo similar podemos traar as linhas que definem as
concentraes de A e C.
Uma linha passando por um dos vrtices por exemplo, pelo vrtice C apresenta
proporo constante entre os dois outros componentes, no caso A e B. Isto , ao se deslocar o
ponto representativo do sistema ao longo desta linha, varia-se a quantidade de C, mantendo-se A
e B (As concentraes variam, mas o quociente das concentraes permanece constante).
Experimentalmente, o diagrama ternrio obtido preparando-se inicialmente misturas
conhecidas dos 2 lquidos parcialmente miscveis. Em seguida, com o auxlio de uma bureta, o
terceiro lquido adicionado at que a turbibez desaparea.
3. Procedimento Experimental
Parte A
1. Em um frasco erlenmeyer adicione 9,0 ml de clorofrmio.
2. Com o auxlio de uma bureta adicione 0,5 mL de H2O ao frasco. Titule ento com
CH3COOH at a formao de uma nica camada (1 fase). Nesse instante, assim que
Fsico-Qumica Experimental - 2006/02
13
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
perceber uma nica fase anote na tabela o volume de CH3COOH utilizado. (primeiro
ponto A).
3. Em seguida adicione 0,2 mL de H2O ao frasco de modo que no total tenha sido
adicionado 0,7 mL de H2O (anterior mais a presente). Titule ento com CH3COOH at a
formao de uma nica camada (1 fase). Nesse instante, assim que perceber a formao
de uma fase anote na tabela o volume de CH3COOH utilizado. (segundo ponto A).
4. Adicione novamente ao frasco, mais 0,9 mL de H2O e torne a titular com CH3COOH at
a formao de uma nica camada (1 fase). Nesse instante, assim que perceber a formao
de uma fase anote na tabela o volume de CH3COOH utilizado. (terceiro ponto A).
5. Obtenha mais dois pontos repetindo o procedimento anterior, porm com a adio de um
volume de H2O de modo a obter um total de 3,0 mL e depois mais uma quantia que
totalize 6,0 mL.
Obs.: Enquanto houver duas fases, sob agitao o sistema fica turvo.
Parte B
1. Em um frasco erlenmeyer adicione 14,0 ml de gua.
2. Com o auxlio de uma pipeta adicione 0,5 mL de CHCl3 na gua (observe a presena de
uma segunda camada). Titule ento com CH3COOH at a formao de uma nica
camada (1 fase). Nesse instante, assim que perceber a formao de uma fase anote na
tabela o volume de CH3COOH utilizado (primeiro ponto B).
3. Novamente com o auxlio de uma pipeta adicione mais 1,1 mL de CHCl3 no frasco
(observe a formao de uma segunda camada). Titule ento com CH3COOH at a
formao de uma nica camada (1 fase). Nesse instante, assim que perceber a formao
de uma fase anote na tabela o volume de CH3COOH utilizado. (segundo ponto B).
4. Obtenha mais trs pontos repetindo o procedimento anterior, porm com a adio de: 1,5,
3,2 e 3,2 mL de CHCl3 por vez. Sempre titulando com CH3COOH aps cada adio.
4. Tratamento dos Dados
Calcule as massas dos 3 componentes para cada ponto anotado.
Organize os resultados na tabela a seguir:
Obs.: Os valores de volume total de clorofrmio e gua de cada ponto anotados na tabela
Clorofrmio
gua
cido actico
Ponto
volume massa % m
volume massa % m
volume massa % m
9,0
0,5
1
9,0
0,7
2
9,0
1,6
3
9,0
3,0
4
9,0
6,0
5
0,5
14,0
6
1,6
14,0
7
3,1
14,0
8
6,2
14,0
9
9,4
14,0
10
Mostre todos os clculos.
Construa o diagrama ternrio utilizando as percentagens em massa de clorofrmio, gua e
cido actico das misturas monofsicas.
Determine experimentalmente o valor da massa especfica de cada componente. Caso
contrrio utilize os seguintes dados de massas especficas:
Clorofrmio 1,49 g/mL
gua 1,00 g/mL
cido actico 1,05 g/mL
Fsico-Qumica Experimental - 2006/02
14
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
CONSTRUO DO DIAGRAMA TERNRIO DE COMPOSIO GUA ETANOL
BENZENO
1. Objetivos:
Construir um diagrama de fases para um sistema de trs componentes lquidos
parcialmente miscveis, em T e P constantes.
2. Introduo:
(Mesmas consideraes gerais do roteiro anterior).
3. Procedimento Experimental
Parte A
Com auxlio de buretas ou de pipetas, em tubos de ensaio prepare as seguintes solues e
feche-as com papel alumnio.
gua
volume
4,0
4,0
4,0
2,7
1,5
0,5
0,3
Ponto
1
2
3
4
5
6
7
massa
%m
Etanol
volume
2,5
4,0
6,0
5,0
5,0
3,5
3,5
massa
%m
Benzeno
volume massa
%m
Obs.: Note que o etanol do frasco estoque no 100% puro.
Parte B
Com o auxlio de uma bureta titule com benzeno at que aparea uma turbidez. Nesse
instante, anote o volume.
Mostre todos os clculos.
Construa o diagrama ternrio utilizando as percentagens em massa de cada componente.
Fsico-Qumica Experimental - 2006/02
15
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
DETERMINAO DO VOLUME MOLAR PARCIAL NaCl/H2O
Estude PICNOMETRIA para realizar esta prtica.
1. Objetivos:
Calcular o volume molar parcial de solues de NaCl como uma funo da
concentrao a partir da massa especfica das solues (picnometria).
2. Introduo:
O volume molar parcial de particular interesse devido a sua coneco termodinmica
com outra propriedade molar parcial, a energia livre de Gibbs molar parcial, conhecida como
potencial qumico. Uma importante propriedade do potencial qumico que, quando em
equilbrio, para uma dada substncia ele possui o mesmo valor em todas as fases do sistema.
Considere um sistema contendo uma substncia slida pura (ex. NaCl) em equilbrio com uma
soluo saturada. O potencial qumico do soluto o mesmo em ambas as fases. Imagine agora
que a presso sobre o sistema seja mudada isotermicamente. O soluto tender a migrar de uma
fase para outra, refletindo em uma mudana na solubilidade? Para uma mudana de equilbrio
em temperatura constante envolvendo somente trabalho de expanso, a mudana na energia livre
de Gibbs (G) dada por
dG = VdP
(1)
Diferenciando relativamente a n2, o nmero de mols do soluto, obtemos
d G 2 = V 2 dP
(2)
Onde a energia livre de Gibbs molar parcial (potencial qumico) e o volume molar parcial
aparecem. Para a mudana de estado
NaCl (S) == NaCl (aq)
Podemos escrever
( G 2 )
d (G 2 ) = V 2 dP , ou
(3)
= V 2
P T
Ento, se o volume molar parcial do soluto em soluo for maior que o volume molar
parcial do soluto slido, um aumento na presso acrescer o potencial qumico do soluto em
soluo relativamente quele da fase slida; o soluto ento deixar a soluo at que um novo
equilbrio seja atingido. Por outro lado, se o volume molar parcial em soluo for menor que
aquele no slido, a solubilidade aumentar com a presso.
Volume molar parcial, e em particular seus desvios apresentados em relao aos valores
esperados para solues ideais, so de considervel interesse em conjunto com a teoria das
solues, especialmente quando aplicado a misturas binrias de componentes lquidos onde esto
relacionados aos calores de mistura e desvios da lei de Raoult.
O volume total (V) de uma mistura binria igual soma dos volumes de todos os
componentes na soluo; por sua vez, o volume de cada componente igual ao produto entre o
nmero de mols daquele componente presente na soluo e seu volume molar parcial. Assim,
V = n1.V1 + n2 .V2
(4)
A partir desta equao vemos que o volume total de uma quantidade de soluo contendo
1 kg (55,51 mol) de gua e m mol de soluto dado por
V = 55,51.V1 + m.V2
(5)
0
Onde o subscrito 1 e 2 refere-se ao solvente e ao soluto, respectivamente. Seja V 1 o
volume molar da gua pura (=18,016/0,997044 = 18,069 cm3/mol a 25,00 0C). Ento definimos o
volume molar aparente do soluto pela equao
Fsico-Qumica Experimental - 2006/02
16
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
0
V = n1 .V 1 + n2 . = 55,51.V 1 + m (6)
A qual pode ser rearranjada para dar
0
0
1
1
=
V n1 .V 1 = V 55,51.V 1
n2
m
Como:
1000 + mM 2
V =
(cm3)
) (
n1 .V 1 =
1000
(cm3)
(7)
(8)
(9)
onde a massa especfica da soluo e o a massa especfica do solvente puro, ambos
em g/cm3, e M2 a massa molecular do soluto em gramas. Substituindo as equaes 8 e 9 na 7,
obtemos
1
1000 w w0
, we = massa do picnometro vazio, w0 = massa do
.
= M 2
m w0 we
picnometro cheio de gua e w = massa do picnometro com a soluo.
Agora pela definio de volume molar parcial e pelo uso das equaes 5 e 6,
V
(10)
V2 =
= + n2
= +m
n2
m
n2 T , P ,n
1
0
0
1
m 2
= V 1
n1V 1 n22
(11)
n1
55,51 m
n 2
Podemos proceder graficando por m, obtendo uma curva suave com os pontos, e
posteriormente traando tangentes aos pontos requeridos de m na curva e obter os coeficientes
angulares.. No entanto, para solues de eletrlito simples, foi determinado que muitas
quantidade molar aparente tal como varia linearmente com m , mesmo em concentraes
moderadas. Este comportamento est de acordo com o previsto pela teoria de Debye-Hckel para
solues diludas. Como
d
d d m
d
1
=
=
(12)
dm d m dm
2 md m
A partir das equaes 10 e 11 obtemos
m d
m d
m d
V2 = +
= +
=0 +
(13)
2 d m
2 d m
2 md m
V1 =
m m d
(14)
55,51 2 d m
Onde 0 o volume molar aparente extrapolado para concentrao zero. Agora se pode
0
V1 =V1
plotar versus m e determinar a melhor reta entre os pontos. A partir do coeficiente angular
d
e do valor de 0, ambos V 1 e V 2 podem ser obtidos.
d m
3. Procedimento Experimental
1. Prepare 200 mL de uma soluo aquosa (de NaCl) de aproximadamente 3,2 m (3,0 M).
2. Por diluio da soluo estoque prepare 100 mL de solues com: 1/2, 1/4, 1/8 e 1/16 da
concentrao da soluo estoque.
Fsico-Qumica Experimental - 2006/02
17
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
3. Com o emprego de um picnmetro determine a massa especfica de cada soluo
preparada, inclusive a soluo estoque.
PICNMETRO: Utilize um picnmetro de 25 ou 50 ml para determinar a massa especfica de
cada lquido em temperatura constante.
COMO PROCEDER: Pese o picnmetro vazio e seco. Depois de pesado, encha o picnmetro
com o lquido-problema (faa primeiro para a gua) e seque-o bem para pesagem. Repita este
procedimento para todas as solues. Atravs da frmula ( = m / v) voc obtm o valor da
massa especfica do lquido naquela temperatura. (No esquea de descontar a massa do
picnmetro vazio).
OBS: Este procedimento feito para a gua pura para aferir o volume do picnmetro. O
valor da massa especfica da gua se encontra na tabela 1 dos anexos.
4. Clculos e Resultados
A molalidade (m, mol/kg) pode ser obtida da molaridade (M, mol/L) da soluo atravs
da seguinte equao:
1
, onde M2 = massa molar do soluto (58,45 g/mol), e = massa
m=
M 2
1000
M
especfica da soluo (g/cm3).
Calcule o para cada soluo.
Faa um grfico de versus m para cada soluo. Determine o coeficiente angular
d
) e o valor do coeficiente linear () atravs da reta que melhor correlaciona os pontos da
(
d m
figura.
Calcule V 1 e V 2 para m = 0.0, 0.5, 1.0, 1.5, 2.0 e 2.5. Construa um grfico de V 1 e V 2
versus m e trace as duas melhores curvas para estes pontos.
Para discusso:
A massa especfica do NaCl(S) 2,165 g/cm3 a 25C. Como a solubilidade do NaCl em
gua ser afetada por um acrscimo de presso?
Fsico-Qumica Experimental - 2006/02
18
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
DETERMINAO DA CONCENTRAO MICELAR CRTICA DE UM
SURFACTANTE
1. Objetivos:
Determinar, graficamente, a concentrao micelar crtica de um surfactante por
condutometria.
2. Introduo:
Os detergentes, tambm chamados surfactantes, apresentam em sua estrutura molecular
uma regio hidrofbica, que constituda por uma longa cadeia de hidrocarbonetos e uma
regio hidroflica, que um grupo polar ou inico. De acordo com a regio hidroflica os
surfactantes classificam-se em catinicos, aninicos e no inicos. Em solues diludas os
surfactantes existem na forma de monmeros, os quais atuam como eletrlitos fortes. medida
que a concentrao aumenta os monmeros formam agregados (MICELAS) e a concentrao
mnima de surfactante em que se inicia a formao de micelas denominada Concentrao
Micelar Crtica (C.M.C.). A C.M.C. de um surfactante uma propriedade fsica to importante
como os pontos de fuso e ebulio ou o ndice de refrao de substncias puras. As micelas
podem ser usadas como catalisadores ou inibidores no estudo cintico de reaes qumicas e tm
grande aplicao na rea farmacutica, em operaes industriais etc.
A C.M.C. de um surfactante determinada atravs do estudo da variao de propriedades
fsicas tais como tenso superficial, condutncia eltrica e outras, em funo da concentrao do
mesmo; graficamente, uma descontinuidade na curva obtida quando se loca condutncia eltrica,
medida em microsiemens (S), versus concentrao milimolar (mM) do detergente, indica o
valor da C.M.C.
Nesta experincia determina-se a C.M.C. de um surfactante aninico (dodecilsulfato de
sdio SDS) atravs da mudana no coeficiente angular da curva acima citada.
3. Procedimento Experimental
PARTE A
1.
Prepare 100mL de dodecilsulfato de
sdio (SDS) 40mM (surfactante aninico).
2. Monte um sistema, bureta com agitador
magntico e eletrodo do cundutivmetro,
similarmente a um sistema de titulao
potenciomtrica. Conforme figura ao lado
3.
Coloque na clula de condutncia
inicialmente 50mL de gua; mea a
condutmcia eltrica inicial da gua.
4.
Com auxlio de uma bureta adicione
a soluo estoque do surfactante de 1,5 em
1,5 mL at 25 mL sob agitao. Leia a
condutncia aps cada volume adicionado
da soluo estoque, calcule a concentrao
da soluo completando assim a tabela a
seguir.
Fsico-Qumica Experimental - 2006/02
19
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
Resultados
1. Preencha as lacunas e a tabela abaixo:
Temperatura =
C;
Volume inicial de gua =
V, ml
C, mM
mL;
Conc. da sol. Estoque de SDS =
mM;
Condut. inicial da gua (Li) =
S;
Lobs , S
Lf , S
V, ml Volume de surfactante adicionado, em mL; C, mM Conc. milimolar da soluo
resultante; Lobs , S Condut. eltrica observada da soluo resultante, em microsiemens;
Lf , S Condut. eltrica final da soluo resultante, em microsiemens
Lf = Lobs - Li
2. Construa o grfico da condutncia eltrica versus concentrao do surfactante e determine a
C.M.C. do surfactante empregado.
PARTE B
(Efeito da adio de etanol)
1. Coloque na clula de condutncia inicialmente 40mL de gua e mais 10 mL de etanol;
mea a condutmcia eltrica inicial da soluo.
2. Novamente com auxlio de uma bureta adicione a soluo estoque do surfactante de 1,5
em 1,5 mL at 40 mL sob agitao. Leia a condutncia aps cada volume adicionado da
soluo estoque, calcule a concentrao da soluo completando assim a tabela a seguir.
Fsico-Qumica Experimental - 2006/02
20
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
Resultados
1. Preencha as lacunas e a tabela abaixo:
Temperatura =
C;
Volume inicial de gua =
Volume inicial de etanol =
V, ml
C, mM
Conc. da sol. Estoque de SDS =
mM;
Condut. inicial da gua (Li) =
S;
mL;
mL;
Concentrao inicial de etanol =
Lobs , S
M;
Lf , S
V, ml Volume de surfactante adicionado, em mL; C, mM Conc. milimolar da soluo
resultante; Lobs , S Condut. eltrica observada da soluo resultante, em microsiemens;
Lf , S Condut. eltrica final da soluo resultante, em microsiemens
Lf = Lobs - Li
3. Construa o grfico da condutncia eltrica versus concentrao do surfactante e determine a
C.M.C. do surfactante empregado sob a influncia do etanol.
Fsico-Qumica Experimental - 2006/02
21
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
MEDIDA DA TENSO SUPERFICIAL: MTODO DA GOTA
1. Objetivos:
Determinar a influncia da concentrao de um surfactante na tenso superficial da gua.
2. Introduo:
As molculas da superfcie de um lquido so submetidas a foras intermoleculares
desiguais, resultando na tenso superficial. Esta tenso superficial expressa como a energia
livre de superfcie por unidade de rea e pode ser representada como uma fora que age no plano
da superfcie do lquido. Como consequncia, ao introduzir um tubo capilar em um lquido que o
molhe, o lquido eleva-se pelo capilar (Fig. 1).
Figura 1. Asceno de um lquido em um capilar.
A fora que sustenta a coluna lquida proporcional tenso superficial do lquido, fato
este que permite determin-la experimentalmente a partir da seguinte equao:
=r
g( ' )
r
L +
2. cos
3
(1)
Onde a tenso superficial do lquido, a sua massa especfica, ' a massa especfica do
sistema que faz a interface com o lquido-problema (gs ou lquido), g a acelerao da
gravidade, o ngulo de contato do menisco, L a altura da coluna lquida e r o raio do tubo
capilar.
Outro aparelho utilizado para a medida da tenso superficial o tensimetro de Noy, o
qual usa um anel de arame usualmente de platina com comprimento P= 4r, onde r o raio do
anel. Este anel suspenso por um brao semelhante ao de uma balana de pesagem. Num
extremo est o anel e no outro pode ser aplicada uma fora varivel (ver figura 2). O anel deve
tocar a superfcie lquida, a fora aplicada deve ser ento corrigida para representar a tenso
superficial do lquido atravs da equao. Na prtica o tensimetro fornece leitura diretamente
no dial (escala circular) a partir da toro aplicada sobre um cabo metlico conforme a figura 3.
Fsico-Qumica Experimental - 2006/02
22
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
(a)
(b)
Figura 2: a) disteno de uma pelcula superficial durante a medida de tenso superficial. b)
condio da pelcula de superfcie no ponto de ruptura.
Figura 3: Tensimetro de Nouy, aparelho utilizado para medir a tenso superficial de um
lquido.
Existem vrios mtodos de medida da tenso superficial; nesta experincia adota-se o
baseado na lei de Tates, em que se determina a massa (m) de uma gota do lquido que se
desprende, sob a ao do prprio peso, da extremidade de um tubo cilndrico, de raio R, mantido
na vertical. Nestas circunstancias se tem:
= mg/2R
Onde a tenso superficial e g a acelerao da gravidade.
A expresso anterior s vlida quando a gota se desprende integralmente da
extremidade do tubo, o que no ocorre na realidade. Utiliza-se por isso a frmula
= (mg/R)F`
Fsico-Qumica Experimental - 2006/02
23
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
Onde F` um fator determinado empiricamente, e que depende da razo entre o volume
V da gota e R3. Tabelas ou grficos apropriados possibilitam a sua estimativa.
Um aparelho simples que se pode utilizar para medir a massa m o esquematizado na
figura que segue. Na extremidade do tubo capilar forma-se a gota que, ao se desprender
recolhida no pesa filtro.
Mangueira
Pipeta graduada
Vlvula
Seringa
Tubo capilar
Pesa filtro
Tampa do pesa filtro
Figura 4: Sistema utilizado para determinar a tenso superficial de um lquido.
A velocidade de formao das gotas controlada por meio de uma vlvula colocada no
circuito.
A tenso superficial uma propriedade cujo valor sensvel modificao da
temperatura; conveniente medi-la em temperatura constante. Ela tambm influencivel pela
presena de diminutas quantidades de substncias adsorvida superfcie do liquido (cidos
graxos, por exemplo); indispensvel, por isso, que se tome escrupuloso cuidado para evitar a
contaminao da superfcie.
Neste experimento ser determinada a variao do valor da tenso superficial da gua
devido a diferentes concentraes de um surfactante.
3. Procedimento Experimental
1. Com base no experimento para a determinao da CMC de um surfactante prepare seis
(6) solues do mesmo surfactante, de modo a abranger todo o intervalo de concentrao
do experimento anterior. Concentraes no valor de: 0, 2, 4, 6, 8, 10 e 15 mM.
Fsico-Qumica Experimental - 2006/02
24
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
2. No instrumento, limpo, coloque um volume de gua suficiente para encher a pipeta. Este
procedimento efetuado com o auxlio de uma seringa do seguinte modo: O bquer
com o lquido deve ser colocado na base do suporte de modo que o capilar fique
mergulhado no mesmo (certifique-se de que a vlvula esteja aberta). Atravs da
seringa conectada a uma mangueira na extremidade superior da pipeta, faz-se
suco (lenta) do lquido at que o volume atinja um nvel pouco superior marca
do zero da pipeta (no permita que o lquido entre na mangueira). Aps ter enchido
a pipeta feche a vlvula e em seguida desconecte a seringa e ento ajuste o menisco
na marca da pipeta. Antes de iniciar as medidas, verifique o controle da velocidade de
formao e desprendimento das gotas. Ajuste o fluxo de modo que as gotas se formem
lentamente. Obs. Anote o volume inicial do lquido na pipeta bem como o valor da
massa do pesa filtro limpo e seco.
3. Conseguido o ajuste de velocidade, o frasco pesa filtro imediatamente abaixo do tubo
capilar e recolha 10 gotas, fechando-o logo em seguida. Retire o pesa filtro e determine
sua massa (m1) e, na pipeta, determine o volume (v1) das 10 gotas.
4. Retorne com o pesa filtro (com o lquido recolhido) e recolha mais 10 gotas; retire-o
novamente, tampe-o e determine novamente sua massa (m2) e o volume (v2). A diferena
entre as duas pesagens a massa de 10 gotas. Repita este procedimento 3 vezes para cada
soluo (conforme tabela).
5. O pesa filtro deve estar limpo e seco externamente, antes de se efetuar cada pesagem.
6. Mea e anote o raio externo do tubo, e anote a temperatura.
7. Ao terminar limpe o instrumento e a vidraria.
Obs. Aps ter recolhido as trinta gotas de cada soluo, no h a necessidade de efetuar a
lavagem do pesa filtro para o recolhimento das gotas da soluo seguinte.
4. Resultados
Preencha as lacunas e a tabela abaixo:
T (C) =
g = 979 cm/s2
Soluo
Massa do pesa filtro (g) =
R (cm) =
Massa de 10 gotas (g)
m1
m2
m3
Volume de 10 gotas
(cm3)
v1
v2
v3
Massa de 1
gota (g)
Vol de 1
gota (cm3)
F`
gua
fcil realizar o experimento e obter resultados com erros relativos menores que 1 a 2%.
Uma causa freqente de erro a contagem errnea do nmero de gotas.
Construa um grfico de tenso superficial em funo da concentrao e, outro grfico de
tenso superficial em funo do logaritmo decimal da concentrao.
Fsico-Qumica Experimental - 2006/02
25
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
ABAIXAMENTO DO PONTO DE FUSO
2. Objetivos:
Medir o decrscimo do ponto de fuso de um solvente devido a presena de um soluto.
Determinar a massa molar do soluto a partir da propriedade coligativa estudada.
3. Introduo:
Ver Propriedades Coligativas em livros de Fsico-Qumica.
4. Experimental:
Ponto de fuso do cicloexano.
1. Adicione 15 mL de cicloexano em um tubo de ensaio. Determine a massa desse
volume.
2. Monte o sistema conforme Figura abaixo.
termmetro
rolha
Fio para
agitao
Obs.: NO use o termmetro
como agitador
3. Mergulhe o tubo de ensaio com o termmetro em um banho de gelo.
4. Quando a temperatura atingir 10oC faa leituras (anotaes) a cada 30 segundos
duranto 15 minutos (agite com o fio), anotar o instante em que se forma o slido.
5. Retire o banho de gelo para que o sistema sofra fuso. Em seguida repita o
procedimento anterior.
6. Faa um grfico de temperatura pelo tempo e determine a temperatura de fuso do
cicloexano.
Ponto de fuso das solues.
1.
Pese 0,100 g de nafataleno e o dissolva no cicloexano do tubo.
2.
Repita o procedimento descrito anteriormente para verificao do ponto de fuso.
3.
Adicione mais 0,100 g de naftaleno e repita o processo anterior. Faa isso mais trs vezes.
4.
Determine a temperatura de fuso das solues, grficamente.
5.
Construa um grfico da variao de temperatura de fuso observada em funo da
concentrao do naftaleno, e determine o valor da constante crioscpica.
6.
Construa um grfico da temperatura inicial de formao do slido observada em funo da
concentrao do naftaleno.
7.
Estime a massa molar do soluto.
Fsico-Qumica Experimental - 2006/02
26
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
ANEXOS
Tab. 1: Massa especfica da gua em diferentes temperaturas.
Fsico-Qumica Experimental - 2006/02
27
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
Tab. 2: Valores de viscosidade da gua em diferentes temperaturas.
o
C
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
(cP)
1,787
1,728
1,671
1,618
1,567
1,519
1,472
1,428
1,386
1,346
1,307
1,271
1,235
1,202
1,169
1,139
1,109
1,081
1,053
1,027
1,002
0,9779
,9548
,9325
,9111
,8904
C
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
51
(cP)
0,8705
,8513
,8327
,8148
,7975
,7808
,7647
,7491
,7340
,7194
,7052
,6915
,6783
,6654
,6529
,6408
,6291
,6178
,6067
,5960
,5856
,5755
,5656
,5561
,5468
,5378
Fsico-Qumica Experimental - 2006/02
C
52
53
54
55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
75
76
77
(cP)
0,5290
,5204
,5121
,5040
,4961
,4884
,4809
,4736
,4665
,4596
,4528
,4402
,4398
,4335
,4273
,4213
,4155
,4098
,4042
,3987
,3934
,3882
,3831
,3781
,3732
,3684
C
78
79
80
81
82
83
84
85
86
87
88
89
90
91
92
93
94
95
96
97
98
99
100
(cP)
0,3638
,3592
,3547
,3503
,3460
,3418
,3377
,3337
,3297
,3259
,3221
,3184
,3147
,3111
,3076
,3042
,3008
,2975
,2942
,2911
,2879
,2848
,2818
28
Universidade Federal do Cear - Departamento de Qumica Analtica e Fsico-Qumica
Tab. 3: Fator F para o calcula da tenso superficial de um lquido a partir da massa de uma gota
do lquido.
Fsico-Qumica Experimental - 2006/02
29
Você também pode gostar
- Relatório 1. Viscosímetro CapilarDocumento32 páginasRelatório 1. Viscosímetro CapilarYasmin OliveiraAinda não há avaliações
- Relatorio de ReologiaDocumento32 páginasRelatorio de ReologiaLetícia RosaAinda não há avaliações
- Aula 1Documento24 páginasAula 1Jmassaneiro13Ainda não há avaliações
- ViscosidadeDocumento5 páginasViscosidadeJamile CastilhoAinda não há avaliações
- Ensaio 3 Massa EspecíficaDocumento5 páginasEnsaio 3 Massa EspecíficaMiguel ÂngeloAinda não há avaliações
- PRÁTICA 3 - Viscosimetro de Hoppler e OswaldDocumento10 páginasPRÁTICA 3 - Viscosimetro de Hoppler e OswaldAmanda CamillaAinda não há avaliações
- FPS Testado in VivoDocumento14 páginasFPS Testado in Vivochagas_83100% (1)
- Pratica 3 Viscosimetria UfcDocumento3 páginasPratica 3 Viscosimetria UfcMichael LimaAinda não há avaliações
- EXP 1 - ViscosidadeDocumento5 páginasEXP 1 - ViscosidadeNathalia RegesAinda não há avaliações
- Experiencia1 Viscosidade SacaroseDocumento4 páginasExperiencia1 Viscosidade SacaroseLucas MarcelinoAinda não há avaliações
- ViscosidadeDocumento6 páginasViscosidadeGeovanna LyssaAinda não há avaliações
- FQI ViscosidadeDocumento10 páginasFQI ViscosidadeJaqueline AlvesAinda não há avaliações
- Físico-Quimica - Viscosidade de LiquidosDocumento10 páginasFísico-Quimica - Viscosidade de LiquidosPablo VargasAinda não há avaliações
- Determinação Da Viscosidade de LíquidosDocumento4 páginasDeterminação Da Viscosidade de LíquidosBárbara LiviaAinda não há avaliações
- LEQ 1 - UFPE Roteiro Prática Instrumentação I 2023Documento12 páginasLEQ 1 - UFPE Roteiro Prática Instrumentação I 2023Alexandre HenriqueAinda não há avaliações
- Determinação Da Viscosidade Pelo Viscosímetro de OstwaldDocumento8 páginasDeterminação Da Viscosidade Pelo Viscosímetro de OstwaldLeonardo Andrade100% (3)
- FUNDAMENTAÇÃODocumento16 páginasFUNDAMENTAÇÃOJoão Víctor GarridoAinda não há avaliações
- InstrumentaçãoDocumento16 páginasInstrumentaçãoJosé Matheus RodriguesAinda não há avaliações
- Relatório FINAL Gabriel e MatheusDocumento16 páginasRelatório FINAL Gabriel e MatheusGabriel BrunAinda não há avaliações
- Experimento 4 - Viscosidade de LiquidosDocumento7 páginasExperimento 4 - Viscosidade de LiquidosCarlos Henrique BazoniAinda não há avaliações
- Relatorio - Experimento 3 - Viscosimetro de Stokes PDFDocumento7 páginasRelatorio - Experimento 3 - Viscosimetro de Stokes PDFGustavo Leal100% (1)
- EXP 5 - ViscosidadeDocumento12 páginasEXP 5 - ViscosidadeCARLOS BATISTAAinda não há avaliações
- Cannon FenskeDocumento16 páginasCannon FenskeHenrique Alves de OliveiraAinda não há avaliações
- Relatorio Reometro CompletoDocumento9 páginasRelatorio Reometro CompletoGisele ArrudaAinda não há avaliações
- Massa Específica e ViscosidadeDocumento4 páginasMassa Específica e ViscosidadePricila PereiraAinda não há avaliações
- PRÉ-RELATÓRIO #3 Coeficiente de ViscosidadeDocumento5 páginasPRÉ-RELATÓRIO #3 Coeficiente de ViscosidadeLarissa MarinhoAinda não há avaliações
- Determinação Da Viscosidade Pelo Método de Stokes - Método Da Velocidade TerminalDocumento8 páginasDeterminação Da Viscosidade Pelo Método de Stokes - Método Da Velocidade TerminalLeonardo Andrade100% (5)
- Viscosidade de Líquidos - RelatórioDocumento7 páginasViscosidade de Líquidos - RelatórioDe Paulo JoãoAinda não há avaliações
- Pratica 01 - ViscosimetriaDocumento5 páginasPratica 01 - ViscosimetriaJulia Lopes BragaAinda não há avaliações
- ViscosidadeDocumento4 páginasViscosidadesamucawinnerAinda não há avaliações
- Template - 2º Laboratório de Mecanica Dos FluidosDocumento5 páginasTemplate - 2º Laboratório de Mecanica Dos FluidosDarlan LucioAinda não há avaliações
- Determinação Da ViscosidadeDocumento17 páginasDeterminação Da ViscosidadePedro SiscatoAinda não há avaliações
- Relatório 4Documento4 páginasRelatório 4João Pedro Silva leiteAinda não há avaliações
- APRESENTAÇÃO MECANICA DOS FLUIDOS (Experimental)Documento10 páginasAPRESENTAÇÃO MECANICA DOS FLUIDOS (Experimental)Maximiliano MotaAinda não há avaliações
- Relatorio Mec-Flu Reinaults Eduardo - Marcelo - ViniciusDocumento9 páginasRelatorio Mec-Flu Reinaults Eduardo - Marcelo - ViniciusJoão MarcosAinda não há avaliações
- Leq 1Documento17 páginasLeq 1IvesAntônioAinda não há avaliações
- Prática 3 - Determinação Da Viscosidade de LíquidosDocumento4 páginasPrática 3 - Determinação Da Viscosidade de LíquidosLUCIANA SILVA MASCARENHASAinda não há avaliações
- Determinação Do Coeficiente de Descarga (CD) e Experiência de ReynoldsDocumento18 páginasDeterminação Do Coeficiente de Descarga (CD) e Experiência de ReynoldsPedro SiscatoAinda não há avaliações
- Relatório 2 QUI150Documento21 páginasRelatório 2 QUI150Nathalia ZuccolottoAinda não há avaliações
- Aula Pratica 02 PDFDocumento32 páginasAula Pratica 02 PDFWilson RibeiroAinda não há avaliações
- Aula Nº 2 - ViscosidadeDocumento23 páginasAula Nº 2 - ViscosidadeRômulo CastroAinda não há avaliações
- Aula ViscosidadeDocumento32 páginasAula ViscosidadeLuiz Gustavo CamargosAinda não há avaliações
- Fluid OsDocumento7 páginasFluid OsJohana Ascanio ArchilaAinda não há avaliações
- Experimento 3 - Propriedades Físico-Químicas - Densidade e Viscosidade (Adaptado)Documento5 páginasExperimento 3 - Propriedades Físico-Químicas - Densidade e Viscosidade (Adaptado)Lenon SilvaAinda não há avaliações
- Relatório de ViscosidadeDocumento18 páginasRelatório de ViscosidadeEduardo Da Costa Ilha100% (1)
- Relatório FT ViscosidadeDocumento11 páginasRelatório FT ViscosidadeGustavo Pinheiro0% (1)
- Aula 2 - ViscosidadeDocumento56 páginasAula 2 - ViscosidadeMatheus VieiraAinda não há avaliações
- Relat+ - Rio - ProjetoDocumento12 páginasRelat+ - Rio - ProjetoWanderson AlvesAinda não há avaliações
- Relatório Viscosidade - Hoeppler e SayboltDocumento23 páginasRelatório Viscosidade - Hoeppler e SayboltHenrique Fernandes100% (1)
- Apostila - Dimensionamento de TubulaçõesDocumento57 páginasApostila - Dimensionamento de Tubulaçõeskfrias100% (1)
- LEQ1 - Relatório 4Documento12 páginasLEQ1 - Relatório 4Douglas CavalcanteAinda não há avaliações
- Thiago FerreiraDocumento3 páginasThiago FerreiraThiago Ferreira Cândido Lima VerdeAinda não há avaliações
- Relatório ViscosidadeDocumento8 páginasRelatório ViscosidadeAna FlaviaAinda não há avaliações
- Drenagem de Obras ViariasDocumento62 páginasDrenagem de Obras ViariasIsabela PintoAinda não há avaliações
- Relatório 1 Lab Calor e Fluido IDocumento19 páginasRelatório 1 Lab Calor e Fluido IFábio BernalAinda não há avaliações
- Relatório Parcial - Mecânica Dos FluidosDocumento5 páginasRelatório Parcial - Mecânica Dos FluidosLeonardo IgaAinda não há avaliações
- Tempo de Esvaziamento - RELATORIODocumento13 páginasTempo de Esvaziamento - RELATORIOnatalialbuquerqueAinda não há avaliações
- INTRODUÇÃO A ReologiaDocumento5 páginasINTRODUÇÃO A ReologiaclaudioAinda não há avaliações
- Professor MineracaoDocumento8 páginasProfessor MineracaoRaulim GalvaoAinda não há avaliações
- Lista 7Documento2 páginasLista 7Ellyakin JesseAinda não há avaliações
- Lista 6Documento5 páginasLista 6MARIA EDUARDA BORDIGNON ENRICONIAinda não há avaliações
- Catálogo de Produtos Corneta - JBL SeleniumDocumento14 páginasCatálogo de Produtos Corneta - JBL SeleniumEdé di MacedoAinda não há avaliações
- Ae 3ceb Faq7 FT 6a Terra ForcasDocumento5 páginasAe 3ceb Faq7 FT 6a Terra ForcasMafalda Nicolau Alves MendesAinda não há avaliações
- Catálogo de Isolante - ExemploDocumento12 páginasCatálogo de Isolante - ExemploMayara BrandolisAinda não há avaliações
- Cinética QuímicaDocumento11 páginasCinética QuímicaJoão Pedro Araújo LimaAinda não há avaliações
- Raciocínio LógicoDocumento3 páginasRaciocínio LógicoRegis Silva SilvaAinda não há avaliações
- Relatório Ensaio Compressão de Barras de AçoDocumento8 páginasRelatório Ensaio Compressão de Barras de AçoMarlonArthurAinda não há avaliações
- Avaliação de Ciências - 9º Ano - 1º BDocumento5 páginasAvaliação de Ciências - 9º Ano - 1º BLucieudo NascimentoAinda não há avaliações
- 222 498 1 PBDocumento12 páginas222 498 1 PBIrisAinda não há avaliações
- Ficha Formativa FTS e Transporte Nas PlantasDocumento6 páginasFicha Formativa FTS e Transporte Nas PlantasBeatrizAinda não há avaliações
- Apostila VBA - Excel 2016Documento333 páginasApostila VBA - Excel 2016Edson NevesAinda não há avaliações
- O Espaço Existêncial e A ArquitecturaDocumento87 páginasO Espaço Existêncial e A ArquitecturanunofcsmpAinda não há avaliações
- Geradores de Corrente Continua SlidesDocumento70 páginasGeradores de Corrente Continua SlidesVinicius RonceteAinda não há avaliações
- Determinar Código CDOPDocumento22 páginasDeterminar Código CDOPFernando Jardim JuniorAinda não há avaliações
- Experimento 1 - Constante Elástica de MolasDocumento3 páginasExperimento 1 - Constante Elástica de MolasmilenyAinda não há avaliações
- Simulado - Atividade 04 de Matemática para 6º AnoDocumento5 páginasSimulado - Atividade 04 de Matemática para 6º AnoDesafios MatemáticosAinda não há avaliações
- Física 2 - FL 24 - Lentes Esféricas e Defeitos Da VisãoDocumento7 páginasFísica 2 - FL 24 - Lentes Esféricas e Defeitos Da VisãoGabriel CardosoAinda não há avaliações
- Dpa8 TesteDocumento4 páginasDpa8 TestexuxazeAinda não há avaliações
- Artigo - Teste de Hipotese - Bioestatistica - 22072020Documento13 páginasArtigo - Teste de Hipotese - Bioestatistica - 22072020Alexandre MacanzeAinda não há avaliações
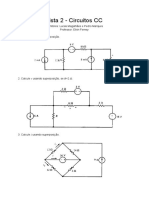
- Lista 2 - Circuitos CCDocumento12 páginasLista 2 - Circuitos CCMarcos Vinicios Lima dos SantosAinda não há avaliações
- Conformação É o Processo Mecânico Onde Se Obtém Peças Através Da Compressão de Metais Sólidos em MoldesDocumento4 páginasConformação É o Processo Mecânico Onde Se Obtém Peças Através Da Compressão de Metais Sólidos em MoldeschicotripsAinda não há avaliações
- Terra PlanaDocumento13 páginasTerra PlanaDieta 21 Emagrecer Usando a MenteAinda não há avaliações
- Livro C4 5a Reimpressao PDFDocumento221 páginasLivro C4 5a Reimpressao PDFnevvilleAinda não há avaliações
- Relações Massa Volume Dos GasesDocumento11 páginasRelações Massa Volume Dos GasesMagaly Stefania AlmeidaAinda não há avaliações
- Engenharia de ProduçãoDocumento5 páginasEngenharia de ProduçãoVitor AloiseAinda não há avaliações
- Introdução Aos Métodos EspectroquímicosDocumento4 páginasIntrodução Aos Métodos EspectroquímicosEzaú Pereira de MouraAinda não há avaliações