Escolar Documentos
Profissional Documentos
Cultura Documentos
Tarea 2 Preparacion de Halogenuros de Alquilo
Enviado por
Caro Villa MoraDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Tarea 2 Preparacion de Halogenuros de Alquilo
Enviado por
Caro Villa MoraDireitos autorais:
Formatos disponíveis
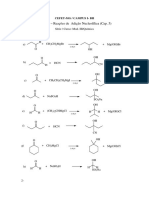
3.
- Prepare los derivados halogenados siguientes (escriba la reacción directa
de ser posible), por el método más adecuado, tratando de no repetir el método:
a).- Bromuro de secpentilo
CH3CH2CH2CH2 + Br2 CH3CH2CH2CH Br
CH3 CH3
b).- Cloruro de isobutilo
CH3 CH CH3 + Cl2 CH3 CH CH2 Cl
CH3 CH3
c).- 1-yodo, 2-buteno
CH3CH CHCH3 + I2 I CH2 CH CHCH3
d).- cloruro de secpentilo
e).- 2-bromo, 1-feniletano
O
CH2 CH3 CH2CH2 Br
+ N Br
f).- 2,2,3,3-tetraclorobutano
Cl Cl Cl
CCl4
CH3 C C CH3 + Cl2 CH3 C C CH3
Cl Cl Cl
g).- yoduro de isopentilo
CH3 CH CH CH2 + HI CH3 CH CH2CH2 I
CH3 CH3
h).- cloruro de vinilo
CH2 CH2 Cl2 calor CH2 CH Cl
+
600°C
i).- yoduro de alilo
CH2 CHCH3 + I2 CH2 CHCH2 I
4.- Prepare mediante síntesis a partir de alcoholes, indicando los pasos del
mecanismo correspondiente los derivados halogenados de alquilo que se solicitan.
(nota: será necesario no repetir el método utilizado)
a).- Cloro, metil ciclopentano
OH CH3 Cl CH3
+ eter
HCl
0°C
CH3 CH3
CH3 Cl (-)
eter + + H2 O
+ HCl +
OH 0°C OH
H
CH3 CH3
-
+ + Cl
Cl
b).- Bromuro de secpentilo
3 CH3CH2CH2 CH OH + PBr3 3 CH3CH2CH2 CH Br + H3PO3
CH3 CH3
1°era ETAPA
H
eter
CH3CH2CH2 CH OH + Br P Br CH3CH2CH2 CH O P Br + Br
CH3 35°C
Br CH3 Br
CH3CH2CH2 CH O P Br + H Br CH3CH2CH2 CH Br + HO P Br
CH3 Br CH3 Br
2°da ETAPA
H
CH3CH2CH2 CH OH + HO P Br CH3CH2CH2 CH O P Br + Br
CH3 Br CH3 OH
CH3CH2CH2 CH O P Br + H Br CH3CH2CH2 CH Br + HO P Br
CH3 OH CH3
OH
3° ETAPA
H
CH3CH2CH2 CH OH + HO P Br CH3CH2CH2 CH O P Br + Br
CH3 OH CH3 OH
CH3CH2CH2 CH O P OH + H Br CH3CH2CH2 CH Br + HO P OH
CH3 OH CH3
OH
c).- Cloruro de isobutilo
N
CH3 CH CH2 OH + SOCl2 CH3 CH CH2 Cl
eter, 0°C
CH3 CH3
O H O OH
H3C CH CH2 OH + N
Cl S Cl H3C CH CH2 O S Cl CH3 CH CH2 O S Cl
eter, 0°C +
CH3 CH3 Cl CH3 Cl
O H O
CH3 CH CH2 O S Cl CH3 CH CH2 O S + HCl CH3 CH CH2 Cl + SO2 + HCl
CH3 Cl CH3 Cl CH3
d).- Bromuro de isopentilo
Br Br
CH3 CH CH2 CH2 OH + P CH3 CH CH2 CH2 Br
Br Br
CH3 Br CH3
Br Br H Br Br Br Br
CH3 CH CH2 CH2 OH + eter
P CH3 CH CH2CH2 O P + Br CH3 CH CH2 CH2 O P
CH3 Br Br 0°C
Br CH3 Br Br CH3 Br Br
H Cl
Br Br O
CH3 CH CH2CH2 O P CH3 CH CH2 CH2 Br + Br P Br
CH3 Br Br
CH3 Br
e).- Cloruro de isopentilo
CH3 CH CH2 CH2 OH + HCl CH3 CH CH2 CH2 Cl
CH3 CH3
Zn Cl2 HCl Cl
CH3 CH CH2 CH2 OH + HCl CH3 CH CH2CH2 H+
CH3 CH CH2CH2 Cl +HO Zn CH3 CH CH2CH2 Cl +
CH3 CH3 OH CH3 Cl
CH3
Cl Zn Cl
+ H2O + ZnCl2
5.- Utilice el método de ácidos clorosulfónico, e indique su mecanismo
preparar:
a).- p-toluensulfonato de butilo
O O
N CH3 + HCl
CH3CH2CH2CH3 OH + Cl S CH3 CH3CH2CH2CH2 O S
O O
b).- p-toluensulfonato de isobutilo
O O
CH3CHCH2 OH + Cl N CH3 + HCl
S CH3 CH3CHCH2 O S
CH3 O CH3 O
6.- Realice las reacciones correspondientes con;
P-toluensulfonato de butilo y p-toluensulfonato de isobutilo y
a).- yoduro de sodio en acetona
O CH3 C CH3
O
CH3CH2CH2CH2 O S CH3 + NaI CH3CH2CH2CH2 I + CH3 SO3Na
O
O CH3 C CH3
CH3CHCH2 O S CH3 + NaI O
CH3CHCH2 I + CH3 SO3Na
CH3 O CH3
b).- bromuro de sodio en dimetilsulfóxido
O CH3 S CH3
O
CH3CH2CH2CH2 O S CH3 + NaBr CH3CH2CH2CH2 Br + CH3 SO3Na
O
O CH3 S CH3
CH3CHCH2 O S CH3 + NaBr O
CH3CHCH2 Br + CH3 SO3Na
CH3 O CH3
c).- cloruro de litio en dimetilsifóxido
O CH3 S CH3
O
CH3CH2CH2CH2 O S CH3 + LiCl CH3CH2CH2CH2 Cl + CH3 SO3Na
O
O CH3 S CH3
CH3CHCH2 O S CH3 + LiCl O
CH3CHCH2 Cl + CH3 SO3Na
CH3 O CH3
7.- Defina los siguientes conceptos:
a) nucleófilo: Especies ricas en electrones que pueden donar un par de
electrones para formar un enlace
b) electrófilo: Especies que pueden aceptar un par de electrones de un
nucleófilo, formando un enlace.
c) grupo saliente: Átomo o grupo de átomos que se desprenden durante una
sustitución o eliminación. El grupo saliente puede tener carga o ser neutro, pero se
desprende con el par de electrones con el que estaba enlazado inicialmente en la
molécula.
d) sustitución: Reacción en la que una especie atacante (nucleófilo, electrófilo
o radical libre) reemplaza a otro grupo.
e) reacción de SN2: Desplazamiento concertado de un nucleófilo por otro en
un átomo de carbono con hibridación sp3
f) reacción de SN1: Intercambio de nucleófilos en dos pasos, por ruptura de
enlace precediendo a la formación de enlace. El primer paso es la ionización para
formar un carbocatión; el segundo paso es la reacción del carbocatión con el
nucleófilo.
g) solvólisis: Sustitución nucleofílica donde el disolvente sirve como reactivo
atacante. La solvólisis literalmente significa “ruptura mediada por el disolvente”
h) eliminación: Reacción que lleva consigo la pérdida de dos átomos o grupos
del sustrato, generalmente para dar lugar a la formación de un enlace pi.
i) reacción E2: Eliminación concertada que implica un estado de transición
donde la base abstrae un protón a la vez que el grupo saliente se desprende.
Normalmente se produce un estado de transición anti-coplanar.
j) reacción E1: Eliminacion en varios pasos donde el grupo saliente se pierde
en un paso de ionización lento; a continuación se pierde un protón en un segundo
paso.
k) rearreglo:
l) base:
m) impedimento estérico: Interferencia entre dos grupos voluminosos que
están tan próximos que sus nubes de electrones experimentan una repulsión.
n) halogenuros de alquilo: Derivado de un alcano en el que uno (o más)
átomos de hidrogeno han sido sustituidos por un halógeno.
o) halogenuros de arilo: Compuesto aromático (derivado del benceno) en el
que un halógeno esta enlazado a uno de los átomos de carbono de un anillo
aromático.
p) halogenuros de vinilo: Derivado de un alqueno en el que uno (o mas) de
los átomos de hidrogeno de los átomos de carbono del doble enlace han siod
reemplazados por un halógeno.
q) halogenuro primario, secundario y terciario.estos términos especifican el
grado de sustitución del carbono al que esta unido el atomo de halógeno. Si el
carbono cabeza esta anlazado a otro atomo de carbono, es primario; si esta
enlazado a dos carbonos, es secundario, y si esta enlazado a tres carbonos, es
terciario
Você também pode gostar
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Actividad de Ácidos CarboxílicosDocumento7 páginasActividad de Ácidos Carboxílicosjorge severinoAinda não há avaliações
- Ejercicios de Alquenos y AlquinosDocumento2 páginasEjercicios de Alquenos y AlquinosMar LopeAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- 6a Lista ExerciciosDocumento6 páginas6a Lista Exercicioslucas henriqueAinda não há avaliações
- HalogenaçãoDocumento10 páginasHalogenaçãopedro.henrique2309Ainda não há avaliações
- Zzzhidrocarburos Alcanos Alquenos y Alquinos 2010Documento7 páginasZzzhidrocarburos Alcanos Alquenos y Alquinos 2010Jairo José Pinedo VargasAinda não há avaliações
- Exerc. 1 - Comp. Oxigenados. - Ácidos Carboxilico e Seus Derivados .VmixDocumento3 páginasExerc. 1 - Comp. Oxigenados. - Ácidos Carboxilico e Seus Derivados .Vmixnelito lamuceneAinda não há avaliações
- Exercicio Subst Elim 1Documento4 páginasExercicio Subst Elim 1Gabriela PaivaAinda não há avaliações
- Atividade 50 - AV1 QO IIDocumento1 páginaAtividade 50 - AV1 QO IIlaisouza225Ainda não há avaliações
- Capítulo 7Documento3 páginasCapítulo 7Selma MeloAinda não há avaliações
- Reações de OxidaçãoDocumento13 páginasReações de OxidaçãoPaulo Vitor SilvaAinda não há avaliações
- UntitledDocumento16 páginasUntitledNathalia AcuñaAinda não há avaliações
- Preparação de Um Aromatizante ArtificialDocumento6 páginasPreparação de Um Aromatizante ArtificialRafael Henrique Rodrigues AlvesAinda não há avaliações
- Química Orgânica - CASD - Aula14 Reações de Substituição II RespostasDocumento3 páginasQuímica Orgânica - CASD - Aula14 Reações de Substituição II RespostasQuímica Caderno de ResoluçõesAinda não há avaliações
- Manual de Quimica Organica IIDocumento261 páginasManual de Quimica Organica IItamele jrAinda não há avaliações
- Lista de Exercícios - Aldeídos e CetonasDocumento7 páginasLista de Exercícios - Aldeídos e CetonasBiancaBelo0% (1)
- Respostas Da Terceira Lista de Química Orgânica - UtfprDocumento2 páginasRespostas Da Terceira Lista de Química Orgânica - UtfprEstela RibasAinda não há avaliações
- Manual Org. 2 - AulaDocumento261 páginasManual Org. 2 - AulaAbdul Laura Condula100% (2)
- 7a Lista ExerciciosDocumento2 páginas7a Lista Exercicioslucas henriqueAinda não há avaliações
- Lista de Exercícios - Ácidos Carboxílicos e DerivadosDocumento6 páginasLista de Exercícios - Ácidos Carboxílicos e DerivadosBiancaBeloAinda não há avaliações
- GabaritoDocumento25 páginasGabaritowagnerAinda não há avaliações
- 05 Adicao Eletrofilica A DienosDocumento20 páginas05 Adicao Eletrofilica A Dienosaraquelsouza8723Ainda não há avaliações
- Lista de Exercicios 08 - Estereoisomeria BCTDocumento4 páginasLista de Exercicios 08 - Estereoisomeria BCTEdja TainaraAinda não há avaliações
- CQ94ExercCap 6Documento6 páginasCQ94ExercCap 6Edson OliveiraAinda não há avaliações
- Funções OxigenadasDocumento4 páginasFunções Oxigenadascharles costa100% (1)
- Reações de Aldeídos e CetonasDocumento26 páginasReações de Aldeídos e CetonasAlineMaira100% (4)
- Funções Orgânicas - TabelaDocumento1 páginaFunções Orgânicas - TabelaJonas SantosAinda não há avaliações
- Aula 23 - ExercíciosDocumento9 páginasAula 23 - ExercíciosWil BarbosaAinda não há avaliações
- Gabarito - Prova2 - Ácidos Carboxílicos e DerivadosDocumento10 páginasGabarito - Prova2 - Ácidos Carboxílicos e DerivadosFernanda MagalhaesAinda não há avaliações
- Reações de AlcenosDocumento41 páginasReações de AlcenosAna Paula LuzAinda não há avaliações
- 2 Lista Hidrocarbonetos 3°ano 2020Documento3 páginas2 Lista Hidrocarbonetos 3°ano 2020Nathan OliveiraAinda não há avaliações
- Ejercicios HidrocarburosDocumento6 páginasEjercicios HidrocarburosCarmenAinda não há avaliações
- Guia Q-Iii Reacciones P.1Documento7 páginasGuia Q-Iii Reacciones P.1Fabrizio2402 HernándezAinda não há avaliações
- Cátions Do Grupo III1 PDFDocumento5 páginasCátions Do Grupo III1 PDFRafael MonteiroAinda não há avaliações
- ÁLCOOL - Função Orgânica 1Documento15 páginasÁLCOOL - Função Orgânica 1teteeahAinda não há avaliações
- Exercícios Referentes Ao Capítulo 5 (Solomons)Documento3 páginasExercícios Referentes Ao Capítulo 5 (Solomons)rayssasoares3Ainda não há avaliações
- Guia de Ejercicios Nomenclatura de HidrocarburosDocumento5 páginasGuia de Ejercicios Nomenclatura de HidrocarburossergioAinda não há avaliações
- Acidez e Basicidade GABARITODocumento3 páginasAcidez e Basicidade GABARITOSandy RodriguesAinda não há avaliações
- Hidrocarburos Ii: Hidrocarburos No Saturados O InsaturadosDocumento6 páginasHidrocarburos Ii: Hidrocarburos No Saturados O InsaturadosSinapsis APAinda não há avaliações
- Aula 11-13 - Expe - 10 - Sintese Da P-NitroanilinaDocumento8 páginasAula 11-13 - Expe - 10 - Sintese Da P-NitroanilinaRaynne SousaAinda não há avaliações
- Chap12c Reactions of Alcoois, Eteres e SulfetosDocumento96 páginasChap12c Reactions of Alcoois, Eteres e Sulfetosrodrigo_0909Ainda não há avaliações
- QO Lista 01 HidrocarbonetosDocumento8 páginasQO Lista 01 HidrocarbonetosJoel CezarAinda não há avaliações
- Quimica2bach Exercicios OrganicaDocumento12 páginasQuimica2bach Exercicios OrganicaCristina ParrasAinda não há avaliações
- Reações de OxidaçãoDocumento11 páginasReações de OxidaçãoJaime VarelaAinda não há avaliações
- Ácidos Carboxilicos e DerivadosDocumento9 páginasÁcidos Carboxilicos e DerivadoswwAinda não há avaliações
- Problemas 1 QOIIDocumento3 páginasProblemas 1 QOIIEmanuel LopesAinda não há avaliações
- Nombres Comunes OrgánicaDocumento1 páginaNombres Comunes OrgánicahelenmrtnzAinda não há avaliações
- Aulas de Química - Anderson Dino - Hidrocarbonetos Parte 2 - Nomenclatura e Exercícios Com GabaritoDocumento9 páginasAulas de Química - Anderson Dino - Hidrocarbonetos Parte 2 - Nomenclatura e Exercícios Com GabaritoJean GreyAinda não há avaliações
- Lista de Exercícios. Nomenclatura Orgânica - Hidrocarbonetos Parte 2. Professor Anderson DinoDocumento9 páginasLista de Exercícios. Nomenclatura Orgânica - Hidrocarbonetos Parte 2. Professor Anderson DinoJulio NascimentoAinda não há avaliações
- 66 20rea C3 A7 C3 B5es 20org C3 A2nicas 20de 20adi C3 A7 C3 A3oDocumento23 páginas66 20rea C3 A7 C3 B5es 20org C3 A2nicas 20de 20adi C3 A7 C3 A3oEva FranciscoAinda não há avaliações
- Química Orgânica - CASD - Aula12 Reações Orgânicas - IntroduçãoDocumento2 páginasQuímica Orgânica - CASD - Aula12 Reações Orgânicas - IntroduçãoQuímica Caderno de Resoluções100% (1)
- FICHA 3 - EstereoquímicaDocumento1 páginaFICHA 3 - Estereoquímicalc788095Ainda não há avaliações
- 189157-Lista de Exercícios 2Documento2 páginas189157-Lista de Exercícios 2Roberto Sousa0% (1)
- 5a Lista ExerciciosDocumento3 páginas5a Lista Exercicioslucas henriqueAinda não há avaliações
- Solucionario 2.pdf Quimica OrganicaDocumento8 páginasSolucionario 2.pdf Quimica OrganicaÄlį PiZâ100% (2)
- Química 10Cl 2 Época2011 - Guiao PDFDocumento2 páginasQuímica 10Cl 2 Época2011 - Guiao PDFMauro Domingo's100% (1)
- Adição À Ligação DuplaDocumento46 páginasAdição À Ligação DuplaSergio Ricardo RibeiroAinda não há avaliações
- Apostila Quimica CEFET 1P TeoriaDocumento142 páginasApostila Quimica CEFET 1P TeoriaVitordarkshadow100% (1)
- Aula 3 - Pratica Curva de Titulacao Da Glicina PDFDocumento2 páginasAula 3 - Pratica Curva de Titulacao Da Glicina PDFAdriana Maria MeneghettiAinda não há avaliações
- Trabalho 2 Inorganica IIDocumento30 páginasTrabalho 2 Inorganica IICarmen PaulinoAinda não há avaliações
- Questões CalorimetriaDocumento12 páginasQuestões Calorimetriaanon-39544100% (1)
- Resumo Física A, 10º e 11º Ano.Documento61 páginasResumo Física A, 10º e 11º Ano.Tito CunhaAinda não há avaliações
- Teoria Da Ligação de ValênciaDocumento34 páginasTeoria Da Ligação de ValênciafctcrAinda não há avaliações
- Agrupamento de Escolas de Alcácer Do SalDocumento8 páginasAgrupamento de Escolas de Alcácer Do SalRuben FernandesAinda não há avaliações
- Aula 6 Metodos de Identificacao e PurezaDocumento13 páginasAula 6 Metodos de Identificacao e PurezaTeresa Helena PiauilinoAinda não há avaliações
- Relatório Da Velocidade Das Reações Químicas Muálua BaiãoDocumento4 páginasRelatório Da Velocidade Das Reações Químicas Muálua BaiãoSofia CoelhoAinda não há avaliações
- Relatório de Termodinâmica-7 PDFDocumento14 páginasRelatório de Termodinâmica-7 PDFJhonas KrugAinda não há avaliações
- Sebenta de Quimica Organica I FEUP 2011 2012 PDFDocumento98 páginasSebenta de Quimica Organica I FEUP 2011 2012 PDFAntónio AfonsoAinda não há avaliações
- Exercicios de Aprendizagem Funções QuimicasDocumento6 páginasExercicios de Aprendizagem Funções Quimicasjulia vitoriaAinda não há avaliações
- Revisão P1-T1 FísicaDocumento3 páginasRevisão P1-T1 FísicaNatáliaAinda não há avaliações
- Livro de Polímeros PDFDocumento34 páginasLivro de Polímeros PDFAriane Bronkow100% (2)
- Acetileno - White MartinsDocumento8 páginasAcetileno - White MartinsDiogotsc CardosoAinda não há avaliações
- Aula 1 QO II - Sistemas Insaturados ConjugadosDocumento69 páginasAula 1 QO II - Sistemas Insaturados ConjugadosPedro Morais100% (1)
- Resumo Ciencias Dos Materiais IiDocumento11 páginasResumo Ciencias Dos Materiais IiRodrigo CostenaroAinda não há avaliações
- Prova Ciências 4º Ano 1º BimestreDocumento5 páginasProva Ciências 4º Ano 1º BimestreSilvia Helena100% (2)
- Calorimetria Exercícios ResolvidosDocumento4 páginasCalorimetria Exercícios ResolvidosmarceloAinda não há avaliações
- ANÁLISE TÉRMICA DE VEÍCULOS ESPACIAIS - v02Documento112 páginasANÁLISE TÉRMICA DE VEÍCULOS ESPACIAIS - v02renanpacheco.randomAinda não há avaliações
- Exercíco de Avaliação 2023.1docxDocumento6 páginasExercíco de Avaliação 2023.1docxDaniel SantosAinda não há avaliações
- Sistema de Arrefecimento - 360Documento41 páginasSistema de Arrefecimento - 360leonardoAinda não há avaliações
- Teste 1 (2016)Documento5 páginasTeste 1 (2016)ana100% (1)
- Lista - Gás IdealDocumento6 páginasLista - Gás IdealJulia AquinoAinda não há avaliações
- ATIVIDADE PRATICA - Modulo CII - 2021 - Fisica Termodinamica e Ondas - Calor Especifico de SolidosDocumento5 páginasATIVIDADE PRATICA - Modulo CII - 2021 - Fisica Termodinamica e Ondas - Calor Especifico de SolidosFlavio PereiraAinda não há avaliações
- Procedimento Experimental e Tratamento de Resíduos - Polaridadde Molecular e Solubilidade de SubstânciasDocumento3 páginasProcedimento Experimental e Tratamento de Resíduos - Polaridadde Molecular e Solubilidade de SubstânciasLucia Noemi TakahashiAinda não há avaliações
- Aula 01 - 2 Série - B02 Termodinâmica I - SlidesDocumento15 páginasAula 01 - 2 Série - B02 Termodinâmica I - SlidesTúlio NaamãAinda não há avaliações
- Grupo 4 - MTH ApresentaçãoDocumento15 páginasGrupo 4 - MTH ApresentaçãoBruno BatistaAinda não há avaliações
- Transição VitreaDocumento14 páginasTransição VitreafredyrickAinda não há avaliações