Escolar Documentos
Profissional Documentos
Cultura Documentos
Lipideos 3
Enviado por
Diéssica Alves0 notas0% acharam este documento útil (0 voto)
1 visualizações42 páginasTítulo original
lipideos_3
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PPTX, PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
1 visualizações42 páginasLipideos 3
Enviado por
Diéssica AlvesDireitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PPTX, PDF, TXT ou leia online no Scribd
Você está na página 1de 42
6 – PAPEL DAS LIPOPROTEÍNAS NO
TRANSPORTE E METABOLISMO DOS AG
• SÃO COMPOSTOS DE TRIGLICERÍDEOS ABSORVIDOS DOS ALIMENTOS
E CONTÊM POUCA PROTEÍNA, FOSFOLIPÍDIOS E COLESTEROL.
TRANSPORTAM DO INTESTINO PARA O FÍGADO AS GORDURAS DA
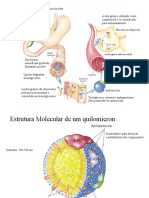
DIETA E OUTRAS CÉLULAS CORPORAIS. OS Qm são as lipoproteínas
menos densas e maiores.
• Os QM são formados no intestino, a partir da dieta, contendo TG e
APO B-48. Atingem, via sistema linfático, a circulação sanguínea. No
plasma, recebem das HDL as APO C-II e APO E. A APO C-II ativa a
enzima lipoproteína lipase, responsável pela hidrólise do TG em AG e
glicerol. Os AG, então, são capturados pelas células periféricas (tecido
adiposo e mm) e a APO C-II volta à HDL. As APO E e APO B-48
permitem o reconhecimento do QM remanescente por receptores
hepáticos. No fígado, o QM remanescente é oxidado ou metabolizado
a novos TG.
• SÃO produzidas e secretadas pelos hepatócitos. Contêm 50% de tg,
algum colesterol, fosfolipídios e proteína. As VLDL transportam os
lipídios sintetizados no fígado para os tecidos corporais. Perdem tg
para as células corporais E GANHAM COLESTEROL DE OUTROS
TECIDOS DO CORPO. QUANDO SUA CONCENTRAÇÃO É ALTA, AS vldl
AUMENTAM O RISCO DE ATEROSCLEROSE.
• A exportação dos TG produzidos endogenamente é feita
pela VLDL, sintetizada no fígado na presença da APO B-100.
Da mesma forma que o QM, a VLDL sofre a ação da enzima
lipoproteína lipase e libera os ácidos graxos para tecidos
periféricos, originando a IDL. Esta partícula pode ser captada
novamente por receptores hepáticos que reconhecem a IDL
através da APO B-100. A IDL também pode ser metabolizada
no plasma à LDL. Esta, por sua vez, contém a maior
quantidade do colesterol que é transportado aos tecidos
periféricos, podendo depositar o excedente de colesterol
nas artérias.
• PRINCIPAL FONTE DE COLESTEROL NO CORPO. CONTÊM 50% DE
COLESTEROL, MENOR QUANTIDADE DE PROTEÍNAS E FOSFOLIPÍDIOS
E POUCOS TRIGLICERÍDIOS. SÃO RESPONSÁVEIS PELO TRANSPORTE
DE COLESTEROL DO FÍGADO PARA OS TECIDOS. COMUMENTE
DENOMINADAS COLESTEROL “RUIM”, AS LDL SÃO UM FATOR
IMPORTANTE PARA O DESENVOLVIMENTO DE ATEROSCLEROSE.
• DENOMINADAS COLESTEROL “BOM”, AS HDL SÃO SINTETIZADAS NO
FÍGADO E CONTÊM 50% DE PROTEÍNAS, COM MENOR QUANTIDADE
DE COLESTEROL, FOSFOLIPÍDIOS E TRIGLICERÍDIOS. AS HDL
TRANSPORTAM COLESTEROL DOS TECIDOS CORPORAIS PARA O
FÍGADO, ONDE É RECICLADO OU DEGRADADO. NÍVEIS ALTOS DE HDL
DIMINUEM RISCO DE ATEROCLEROSE.
• A HDL, conhecida como fator protetor do excesso de
colesterol, capta o colesterol livre periférico,
esterificando-o por atuação da enzima lecitina
colesterol aciltrasnferase (LCAT). A transferência do
colesterol esterificado, da partícula de HDL para IDL e
novamente para o fígado, ocorre por atuação da
enzima de transferência do colesterol (CETP). Assim,
o colesterol excedente retorna ao fígado para ser
metabolizado.
7 – DEGRADAÇÃO DOS AG
• A degradação dos ácidos graxos consiste na retirada de duas
unidades de carbono, por vez, quebrando a molécula de
ácido graxo e produzindo acetil-coa. Este é oxidado no ciclo
do ácido tricarboxílico (ciclo de krebs), formando CO2 e
H2O.
• A degradação dos ácidos graxos ocorre principalmente no
fígado e no músculo. Não ocorre no cérebro, nas hemácias e
na medular da adrenal.
• De 90 a 95% da oxidação se dá na mitocôndria; o restante
ocorre no peroxissomo do rim e do fígado.
A obtenção de energia a partir dos triglicérides se dá em
quatro etapas:
• Lipólise: o triglicErÍdIO é hidrolizado em ácido graxo e
glicerol pela lipase, enzima presente no citossol do
adipócito. O glicerol é fosforilado no fígado, onde entra na
formação de outro triglicéride ou segue para a via glicolítica.
O AG cai na corrente sanguínea e é transportado junto com
a albumina para o fígado e o tecido muscular esquelético.
• Ativação do ácido graxo – através do acoplamento do grupo
coa para a formação do acil-coa no citossol.
• Transporte do acil-coa para a mitocôndria – nesta etapa, há
a participação fundamental da carnitina, presente na
membrana da mitocôndria responsável pela entrada do acil-
coa nesta organela. A carnitina recebe o grupo acil através
da enzima carnitina aciltranserase I (CAT I), presente no lado
citossólico da membrana mitocondrial interna. A
acilcarnitina, é transportada pela enzima translocase para a
matriz mitocondrial, onde volta a se transformar em
carnitina e acil-coa, agora através da carnitina
aciltrasnferase II (CAT II). A carnitina retorna ao citossol e o
acil-coa sofre β-oxidação.
• β-oxidação – ocorre na matriz mitocondrial. é uma
sequência de reações químicas em que há
encurtamento da cadeia de ácido graxo, com retirada
de dois carbonos, sob a forma de acetil-coa, por vez.
As reações de β-oxidação, em sequência, são: primeira
oxidação, hidratação, segunda oxidação e tiólise, que é
a etapa em que ocorre o encurtamento da molécula.
8 – REGULAÇÃO DO METABOLISMO DOS AG
• O controle do metabolismo dos AG ocorre durante a
lipólise, o transporte para a mitocôndria via carnitina e a β-
oxidação.
• Vários hormônios atuam na lipólise, a adrenalina, assim
como o glicogênio e o ACTH (hormônio
adrenocorticotrófico), ativam a lipase através da sua
fosforilação via AMP cíclico, estimulando a lipólise. Ao
mesmo tempo, a ativação da adenilciclase e o
consequente aumento do AMP cíclico intracelular inibem a
síntese de ácidos graxos. A insulina inibe a lipólise porque
desfosforila a lipase.
• Durante a síntese do ácido graxo, forma-se malonil-coa, que
inibe a CAT I, responsável pelo transporte do ácido graxo
para a mitocôndria. Essa inibição garante que o ácido graxo
que está sendo formado não seja logo oxidado na
mitocôndria, regulando assim, a sua degradação.
• A β-oxidação pode ser inibida com NADH e FADH2.
9 – CORPOS CETÔNICOS
• São substâncias equivalentes a ácidos graxos, mas
solúveis em águas derivadas do acetil-coa. Sua
produção basal aumenta em situações em que há a
necessidade de fonte de energia alternativa por falta ou
mau aproveitamento da glicose, como no caso do jejum
prolongado, diabetes descompensado e excesso de
exercício físico.
• Os corpos cetônicos são: ácido acetilacético, ácido 3-
hidroxibutírico e acetona.
• Os corpos cetônicos economizam a glicose obtida da
neoglicogênese (a partir de proteínas do músculo). Esse
mecanismo privilegia o gasto de gordura em relação às
proteínas do corpo.
• Os corpos cetônicos provêm da β-oxidação dos ácidos
graxos. A cetogênese (produção dos corpos cetônicos)
ocorre na mitocôndria dos hepatócitos. São carreados pelo
sangue a diversos órgãos capazes de aproveitá-los como
fonte de energia: coração, musculatura esquelética e
cérebro.
• Nos tecidos, ocorre a oxidação dos corpos cetônicos
também na mitocôndria, com produção de 26
moléculas de ATP por corpo cetônico oxidado, um
saldo de energia semelhante ao da glicose, que é de 32
atp.
• A utilização dos corpos cetônicos não é possível pelas
hemácias, que não possuem mitocôndrias, nem pelos
hepatócitos, por possuírem complexo enzimático que
impede sua oxidação.
10- LIPÍDEOS – Recomendações:
• De 15 a 30% do VET
• Gorduras trans: deve ser menor que 1%
do VET (no máximo 2g/dia para uma
dieta de 2000kcal)
• Atenção ao rótulos: “gordura
hidrogenada”, “gordura trans”, “óleo
hidrogenado”, “gordura vegetal”
Guia Alimentar para a população
Brasileira- MS- 2005
• 25 a 30% do VET
• Ácidos Graxos Saturados: < 10% (ex: gorduras carnes)
• Ácidos Graxos Poliinsaturados: > 10% (ex: óleos vegetais)
• Ácidos Graxos Monoinsaturados: > 20% (ex: azeite de
oliva)
• COLESTEROL: < 300mg/DIA
III Diretrizes Brasileiras Dislipidemias
Você também pode gostar
- Metabolismo dos LipídeosDocumento68 páginasMetabolismo dos LipídeosLetícia CabralAinda não há avaliações
- Resolução Lista BioquimicaDocumento16 páginasResolução Lista BioquimicaVitor SouzaAinda não há avaliações
- Metabolismo de Ácidos GraxosDocumento23 páginasMetabolismo de Ácidos Graxosfelipe parizotoAinda não há avaliações
- Aula 9 Metabolismo Dos LipídiosDocumento44 páginasAula 9 Metabolismo Dos Lipídiosaracnomarques100% (2)
- Metabolismo de carboidratos: glicólise, ciclo de Krebs e gliconeogêneseDocumento41 páginasMetabolismo de carboidratos: glicólise, ciclo de Krebs e gliconeogêneseRosiane Gomes Silva Oliveira100% (1)
- Metabolismo de lipídios e aminoácidos e integração metabólicaDocumento72 páginasMetabolismo de lipídios e aminoácidos e integração metabólicaAdriano MateusAinda não há avaliações
- Metabolismo de lipídeos: β-oxidação, corpos cetônicos e sínteseDocumento20 páginasMetabolismo de lipídeos: β-oxidação, corpos cetônicos e sínteseVanderval SIlva de OliveiraAinda não há avaliações
- 5 Metabolismo de Lipídios e Aminoácidos e Integração MetabólicaDocumento66 páginas5 Metabolismo de Lipídios e Aminoácidos e Integração MetabólicarilixgsimululadorAinda não há avaliações
- Lipídios: funções, classificação e metabolismoDocumento82 páginasLipídios: funções, classificação e metabolismokaline cardosoAinda não há avaliações
- Oxidação dos ácidos graxos: via central de geração de energiaDocumento7 páginasOxidação dos ácidos graxos: via central de geração de energiaDariê CruvinelAinda não há avaliações
- Módulo 6 - Oxidação de Ácidos GraxosDocumento17 páginasMódulo 6 - Oxidação de Ácidos GraxosBeatriz De Sousa CoelhoAinda não há avaliações
- Metabolismo dos carboidratos e lipídiosDocumento4 páginasMetabolismo dos carboidratos e lipídiosNetto LacerdaAinda não há avaliações
- Metabolismo de LipídiosDocumento16 páginasMetabolismo de LipídiosDanielle RodriguesAinda não há avaliações
- 2023 Exercícios - Degradação de Lipídios-Corpos Cetônicos GabaritoDocumento6 páginas2023 Exercícios - Degradação de Lipídios-Corpos Cetônicos GabaritoCybervetWandersonAinda não há avaliações
- Metabolismo Dos LipídiosDocumento5 páginasMetabolismo Dos LipídiosMariana BarbosaAinda não há avaliações
- Microsoft Word - Estudo Dirigido - Bloco LipídiosDocumento4 páginasMicrosoft Word - Estudo Dirigido - Bloco LipídiosFelipe MagalhaesAinda não há avaliações
- Catabolismo de Ácidos GraxosDocumento8 páginasCatabolismo de Ácidos Graxosjoão vitor fioratti de oliveiraAinda não há avaliações
- Metabolismo de Lipídeos Aula 2Documento26 páginasMetabolismo de Lipídeos Aula 2Brunno PinhoAinda não há avaliações
- Lipólise - Degradação dos Ácidos GraxosDocumento6 páginasLipólise - Degradação dos Ácidos GraxosIvone Pires PortoAinda não há avaliações
- Digestão, absorção e transporte de lipídiosDocumento11 páginasDigestão, absorção e transporte de lipídiosRicardo Junior100% (1)
- Oxidação Dos Ácidos GraxosDocumento5 páginasOxidação Dos Ácidos GraxosBruna NevesAinda não há avaliações
- Sessão 4Documento8 páginasSessão 4Gabriel PiresAinda não há avaliações
- BIOQUÍMICA II 11 - Lipolise (Arlindo Netto)Documento6 páginasBIOQUÍMICA II 11 - Lipolise (Arlindo Netto)bbruno5Ainda não há avaliações
- Roteiro Do Laboratório Morfofuncional: Curso de MedicinaDocumento32 páginasRoteiro Do Laboratório Morfofuncional: Curso de MedicinabluboarettoAinda não há avaliações
- Metabolismo de LipídeosDocumento5 páginasMetabolismo de LipídeosMarcela Lima de BritoAinda não há avaliações
- Metabolismo Do Colesterol - ResumidoDocumento5 páginasMetabolismo Do Colesterol - ResumidoDianaAinda não há avaliações
- Capitulo 9.4Documento44 páginasCapitulo 9.4Joana DiasAinda não há avaliações
- β-oxidação de lipídiosDocumento44 páginasβ-oxidação de lipídiosMaria Eduarda Frota100% (1)
- Mecanismos Insulina e GlucagonDocumento32 páginasMecanismos Insulina e GlucagonMichele MAinda não há avaliações
- Aula 9, 10, 11 - ATV3 (Metabolismo II)Documento30 páginasAula 9, 10, 11 - ATV3 (Metabolismo II)Mateus Mendes AlvesAinda não há avaliações
- No sistema digestório - Metabolismo dos LipidiosDocumento6 páginasNo sistema digestório - Metabolismo dos Lipidiosedson sordaneAinda não há avaliações
- 1740718 (2).pptDocumento20 páginas1740718 (2).pptAle Araujo100% (1)
- Catabolismo de LipídiosDocumento10 páginasCatabolismo de LipídiosIhury JhonsonAinda não há avaliações
- Capítulo 17Documento8 páginasCapítulo 17Davi SousaAinda não há avaliações
- Ed - Metabolismo de LipídiosDocumento3 páginasEd - Metabolismo de LipídiosMelanny PaixãoAinda não há avaliações
- Metabolismo de Lipídeos IQSC-USPDocumento53 páginasMetabolismo de Lipídeos IQSC-USPEvany Priscila100% (1)
- Bioquímica - Ciclo Alimentado e JejumDocumento9 páginasBioquímica - Ciclo Alimentado e JejumPedro CintraAinda não há avaliações
- Bioquimica Digestao e Absorcao Dos LipidiosDocumento5 páginasBioquimica Digestao e Absorcao Dos LipidiosdalilaAinda não há avaliações
- Transcrição Dos Áudios 2 Prova de Bioquímica Clínica IDocumento16 páginasTranscrição Dos Áudios 2 Prova de Bioquímica Clínica ICarol Fernandes de Assis100% (1)
- DislipidemiaDocumento14 páginasDislipidemiajoao bernacchiAinda não há avaliações
- LIPÍDIOS Fechamento UC IVDocumento8 páginasLIPÍDIOS Fechamento UC IVLuis Mateus Camelo França MartinsAinda não há avaliações
- Bioquímica 2 P2Documento14 páginasBioquímica 2 P2msouzaf89Ainda não há avaliações
- Aula Lipidios Partes II e IIIDocumento28 páginasAula Lipidios Partes II e IIIGabriel NobregaAinda não há avaliações
- Lipídeos e Seu MetabolismoDocumento31 páginasLipídeos e Seu Metabolismowesleyrs94Ainda não há avaliações
- Degradacao Dos Acidos Graxos 2020Documento60 páginasDegradacao Dos Acidos Graxos 2020Bio FontesAinda não há avaliações
- β-oxidação de lipídiosDocumento43 páginasβ-oxidação de lipídiosRique EmanuelAinda não há avaliações
- Anotações Conferencia Biocel 2Documento3 páginasAnotações Conferencia Biocel 2Ana Laura MartinsAinda não há avaliações
- Metabolismo Dos TriacilgliceroisDocumento32 páginasMetabolismo Dos Triacilgliceroismorena222Ainda não há avaliações
- Esteatose Hepática: Causas e Aspectos MorfológicosDocumento75 páginasEsteatose Hepática: Causas e Aspectos MorfológicosAna Cristina DuqueAinda não há avaliações
- Lipidos Aula de 3 Corte BioquimicaDocumento40 páginasLipidos Aula de 3 Corte BioquimicaLuis MartinezAinda não há avaliações
- Digestão e metabolismo de lipídeosDocumento34 páginasDigestão e metabolismo de lipídeosBRUNO MOREIRA DO SANTOS100% (1)
- LÍPIDOS Metabolismo 11Documento60 páginasLÍPIDOS Metabolismo 11Mirian NaimaAinda não há avaliações
- Bioquimica Prova 3Documento7 páginasBioquimica Prova 3LuanaAinda não há avaliações
- Introdução Bioquímica IIDocumento54 páginasIntrodução Bioquímica IILuis Henrique BarcellosAinda não há avaliações
- Dislipidemias e Aterosclerose: Aspectos GeraisDocumento74 páginasDislipidemias e Aterosclerose: Aspectos Geraispatricia torkaski100% (1)
- FicatDocumento8 páginasFicatEllena CristianaAinda não há avaliações
- 15 Metabolismo Dos TriacilgliceroisDocumento32 páginas15 Metabolismo Dos TriacilgliceroisMayara AlencarAinda não há avaliações
- Dieta Cetogénica: Recetas Rápidas Altas En Grasa Para Restablecer Su Cuerpo Y Vivir Una Vida SaludableNo EverandDieta Cetogénica: Recetas Rápidas Altas En Grasa Para Restablecer Su Cuerpo Y Vivir Una Vida SaludableNota: 5 de 5 estrelas5/5 (1)
- Soluções para Diabetes e Hipoglicemia (Traduzido): Como preveni-lo e livrar-se dele naturalmente, sem medicamentos, mas adotando um estilo de vida saudávelNo EverandSoluções para Diabetes e Hipoglicemia (Traduzido): Como preveni-lo e livrar-se dele naturalmente, sem medicamentos, mas adotando um estilo de vida saudávelAinda não há avaliações
- 2 Microscopia e Teoria CelularDocumento7 páginas2 Microscopia e Teoria Celularmaisacesso1Ainda não há avaliações
- Protocolos clínicos RECOVER fisioterapiaDocumento46 páginasProtocolos clínicos RECOVER fisioterapiaFelipe Mascarenhas OsteopatiaAinda não há avaliações
- Protocolos IM para saúdeDocumento38 páginasProtocolos IM para saúdeRafaella Queiroga100% (4)
- SimbioseDocumento2 páginasSimbiosedailtonddAinda não há avaliações
- QUESTAO Questoes Sobre CitologiaDocumento5 páginasQUESTAO Questoes Sobre Citologia'Samuel PereiraAinda não há avaliações
- Célula AnimalDocumento4 páginasCélula AnimalThiago Robert RoqueAinda não há avaliações
- Enem Biologia Exercícios Citoplasma MetabolismoDocumento146 páginasEnem Biologia Exercícios Citoplasma MetabolismoGisele MedeirosAinda não há avaliações
- Células e origem da vidaDocumento32 páginasCélulas e origem da vidaluciAinda não há avaliações
- Trabalho de Biologia CélulaDocumento16 páginasTrabalho de Biologia CélulaGustavo Baquião Dantas RochaAinda não há avaliações
- Beta OxidaçãoDocumento18 páginasBeta OxidaçãoErika BennaiaAinda não há avaliações
- Aula 1 Visão Geral Da CélulaDocumento33 páginasAula 1 Visão Geral Da Célulaapi-19738142Ainda não há avaliações
- Aula Capítulo 12Documento105 páginasAula Capítulo 12Antonio Carlos Cruz Da SilvaAinda não há avaliações
- A estrutura da célula eucariótica animal e vegetalDocumento23 páginasA estrutura da célula eucariótica animal e vegetalrafa100% (1)
- Exercícios sobre organelas celulares e suas funçõesDocumento1 páginaExercícios sobre organelas celulares e suas funçõesFabiana PereiraAinda não há avaliações
- Organelas citoplasmáticas e processo energéticoDocumento5 páginasOrganelas citoplasmáticas e processo energéticoISRAEL MARQUES DOS SANTOSAinda não há avaliações
- Cromossomas eucariontes e procarióticosDocumento12 páginasCromossomas eucariontes e procarióticosLuísa Carmo100% (2)
- CelulasDocumento2 páginasCelulasMaurim Olendino100% (1)
- Exerc Mitocondrias e CloroplastosDocumento5 páginasExerc Mitocondrias e CloroplastosromerkingAinda não há avaliações
- Fisiologia Da Nutrição e Bioquímica ApostilaDocumento37 páginasFisiologia Da Nutrição e Bioquímica ApostilaVanessa T100% (1)
- Bioquímica - Via das pentoses-fosfato e metabolismo de carboidratosDocumento11 páginasBioquímica - Via das pentoses-fosfato e metabolismo de carboidratosBoutique Dai SexyAinda não há avaliações
- Origem e Evolução Das CélulasDocumento3 páginasOrigem e Evolução Das CélulasAna Laura TeixeiraAinda não há avaliações
- Ficha de Avaliação Sumativa N.º1 Ciências 8º AnoDocumento6 páginasFicha de Avaliação Sumativa N.º1 Ciências 8º AnoSónia100% (1)
- Moléculas, Células e Tecidos - Muito FáceisDocumento7 páginasMoléculas, Células e Tecidos - Muito FáceisLuan Pablo Pereira Da CostaAinda não há avaliações
- Prova Unificada 8º Ano ALA - PDF ADocumento2 páginasProva Unificada 8º Ano ALA - PDF AElivando Silva MotaAinda não há avaliações
- Unidade e Multicelularidade. Mecanismos de EvoluçãoDocumento32 páginasUnidade e Multicelularidade. Mecanismos de EvoluçãoEmaAinda não há avaliações
- Leve DurasDocumento2 páginasLeve DurasTiago Sousa0% (1)
- Teste Seus Conhecimentos - Biologia CelularDocumento5 páginasTeste Seus Conhecimentos - Biologia CelularPaulo HenriqueAinda não há avaliações
- Célula - Atividade 02Documento4 páginasCélula - Atividade 02Pra Mari NascimentoAinda não há avaliações
- Transformação de Energia Na CélulaDocumento50 páginasTransformação de Energia Na Célulakamilla GarciaAinda não há avaliações
- Aula 1 2 e 3 - Etiopatogênese Geral Das LesõesDocumento21 páginasAula 1 2 e 3 - Etiopatogênese Geral Das Lesõescamilla fAinda não há avaliações