Escolar Documentos
Profissional Documentos
Cultura Documentos
Tristeza Parasitaria Bovina 1-16
Enviado por
Carla Janaina Rebouças0 notas0% acharam este documento útil (0 voto)
63 visualizações0 página1) O documento discute a tristeza parasitária bovina (TPB), causada principalmente por Babesia bovis, Babesia bigemina e Anaplasma marginale, transmitidos por carrapatos.
2) Detalha a biologia dos três agentes, incluindo seus ciclos de vida nos carrapatos e bovinos.
3) A TPB é uma das doenças mais importantes na pecuária bovina e limita o desenvolvimento de rebanhos em regiões tropicais e subtropicais.
Descrição original:
Título original
Tristeza parasitaria bovina 1-16
Direitos autorais
© Attribution Non-Commercial (BY-NC)
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documento1) O documento discute a tristeza parasitária bovina (TPB), causada principalmente por Babesia bovis, Babesia bigemina e Anaplasma marginale, transmitidos por carrapatos.
2) Detalha a biologia dos três agentes, incluindo seus ciclos de vida nos carrapatos e bovinos.
3) A TPB é uma das doenças mais importantes na pecuária bovina e limita o desenvolvimento de rebanhos em regiões tropicais e subtropicais.
Direitos autorais:
Attribution Non-Commercial (BY-NC)
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
63 visualizações0 páginaTristeza Parasitaria Bovina 1-16
Enviado por
Carla Janaina Rebouças1) O documento discute a tristeza parasitária bovina (TPB), causada principalmente por Babesia bovis, Babesia bigemina e Anaplasma marginale, transmitidos por carrapatos.
2) Detalha a biologia dos três agentes, incluindo seus ciclos de vida nos carrapatos e bovinos.
3) A TPB é uma das doenças mais importantes na pecuária bovina e limita o desenvolvimento de rebanhos em regiões tropicais e subtropicais.
Direitos autorais:
Attribution Non-Commercial (BY-NC)
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 0
TRISTEZA PARASITRIA BOVINA E PREMUNIO
Carlos Luiz Massard
1
Cleber Oliveira Soares
2
Jos Carlos Pereira de Souza
3
Adivaldo Henrique da Fonseca
4
1
Professor Titular, PhD., Dep. de Parasitologia Animal, Instituto de Biologia, Universidade Federal Rural do
Rio de Janeiro. Rod. Rio So Paulo, Km 47, Seropdica-RJ, 23851-970;
2
Mdico Veterinrio, MSc.,
Doutorando do Curso de Ps-Graduao em Medicina Veterinria - Parasitologia Veterinria, UFRRJ.
3
Mdico Veterinrio, MSc., Ministrio da Agricultura e do Abastecimento;
4
Professor Titular, PhD., Dep. de
Epidemiologia e Sade Pblica, Instituto de Veterinria, UFRRJ.
INTRODUO......................................................................................................................................................................................... 1
ETIOLOGIA.............................................................................................................................................................................................. 2
BIOLOGIA................................................................................................................................................................................................. 2
EPIZOOTIOLOGIA.................................................................................................................................................................................. 4
IMPORTNCIA........................................................................................................................................................................................ 5
PATOGENIA E SINTOMAS CLNICOS ............................................................................................................................................... 5
IMUNIDADE ............................................................................................................................................................................................. 7
DIAGNSTICO........................................................................................................................................................................................ 7
CONTROLE.............................................................................................................................................................................................. 8
TRATAMENTO........................................................................................................................................................................................ 9
PREMUNIO PARA A TRISTEZA PARASITRIA BOVINA.......................................................................................................... 9
PREMUNIO .................................................................................................................................................................................. 10
MTODOS DE PREMUNIO....................................................................................................................................................... 10
VACINAS............................................................................................................................................................................................ 12
IMUNGENOS NO VIVEIS........................................................................................................................................................ 12
REFERNCIAS BIBLIOGRFICAS ................................................................................................................................................... 13
INTRODUO
Tristeza Parasitria Bovina (TPB) a denominao associao dos agentes da
babesiose e anaplasmose dos bovinos. Esta enfermidade desencadeada pela massiva
destruio de eritrcitos, decorrente dos aspectos biolgicos dos agentes em realizarem
parte do seu ciclo no interior destas clulas.
O complexo TPB conhecido desde o final dos sculo XIX onde a enfermidade era
considerada como entidade nica. Em 1888, BABS descreveu um microrganismo
intraeritroctico em bovinos na Romnia, denominando-o Haematococcus bovis,
posteriormente classificado como Babesia bovis. No sudoeste dos Estados Unidos da
Amrica (EUA), em 1893, SMITH & KILBORNE identificaram o hematozorio Pyrosoma
bigeminum, classificado posteriormente como Babesia bigemina, causador de grandes
perdas econmicas no rebanho bovino texano, enfermidade ento denominada febre do
Texas. Neste mesmo trabalho, os autores identificaram o vetor (Boophilus annulatus) e o
modo de transmisso. Esta foi uma das mais importantes descobertas na histria da
Parasitologia, por ter sido a primeira demonstrao de que os carrapatos so hbeis
transmissores de patgenos. No incio do sculo XX, na frica do Sul, foi identificado o
terceiro agente etiolgico do "complexo TPB", o Anaplasma marginale, descrito como
agente do mal da bile (THEILER, 1910).
No Brasil, o primeiro registro da febre do Texas foi realizado por FAJARDO (1901),
ao examinar animais recm-importados e em fase de aclimatao. A anaplasmose, no
Brasil, foi primeiro relatada por CARINI (1910).
A distribuio da TPB tem relao estreita com a distribuio dos seus vetores;
ocorrendo nos pases de clima tropical e sub-tropical do globo. Esta uma das doenas
mais importantes na pecuria bovina, e considerada fator limitante no desenvolvimento e
melhoramento dos rebanhos bovinos (MC COSKER, 1981).
ETIOLOGIA
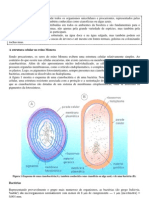
A TPB decorrente, principalmente, da associao de protozooses, determinadas
pela B. bigemina e pela B. bovis, associadas a rickettsiose causada pela A. marginale
(FONSECA & BRAGA, 1924; MASSARD & FREIRE, 1985). Estes agentes podem
apresentarem-se ainda em conjunto com outros hematozorios como a rickettsia Ehrlichia
bovis que parasita leuccitos (linfcitos e moncitos) (Fig. 1), levando ao agravamento da
TPB (MASSARD & MASSARD, 1982).
BIOLOGIA
O carrapato, B. microplus, durante o repasto sangneo, inocula no hospedeiro os
esporozotos, estas formas penetram nos eritrcitos, se diferenciam em trofozotos e
multiplicam-se dando origem aos merozotos. Estes rompem as hemcias e invadem novos
eritrcitos continuando o processo de diviso do tipo merognica.
Durante o hematofagismo, o carrapato ingere clulas sangneas e com estas os
eritrcitos que contm trofozotos. Na luz intestinal do carrapato ocorre o rompimento dos
eritrcitos com liberao dos zotos que evoluem para corpos raiados ("gametas"). Estes
corpos, contendo material gentico e sem dimorfismo sexual, se fusionam dois a dois
originando os zigotos. Esta fase representa a gametogonia dos babesiideos.
Os zigotos daro origem aos cinetos (formas mveis) que penetram em clulas do
epitlio intestinal do carrapato e realizam diviso multpla originando novos cinetos. Estes
so liberadas na hemolinfa e invadem clulas de vrios rgos, fazendo novas divises at
a morte do carrapato. Quando os ocitos so infectados haver a multiplicao no ovo, no
embrio e em diversos rgos da larva; caracterizando assim, a transmisso transovariana.
Quando os cinetos penetram nas clulas epiteliais das glndulas salivares, esses se
transformam em esporontes; os esporontes se rompem e liberam os esporozotos, formas
infectantes para o hospedeiro vertebrado. Esta multiplicao representa a fase de
esporogonia (FRIEDHOF, 1982; KAKOMA & MEHLHORN, 1994; MASSARD et al., 1998).
2
Babesia bovis: Esta espcie possui dimenses pequenas, atinge no mximo 3m e
apresenta morfologia, predominantemente, arredondada ou lanceolada que apareem
frequentemente aos pares (FONSECA & BRAGA, 1924). Apresenta colorao basoflica,
idntica tanto pelo corante de giemsa, leishman ou outros corantes derivados do
romanovski e apresenta pequena massa citoplasmtica e abundante massa nuclear. uma
espcie que possui acentuado tropismo pela circulao de rgos viscerais e centrais e
pouco tropismo pela circulao perifrica (Fig. 2). O carrapato B. microplus o vetor deste
agente; a infeco adquirida atravs das fmeas em ingurgitamento e, as larvas
infectadas, via transovariana, sero o nico nstar de B. microplus a transmitir a B. bovis ao
bovinos (MAHONEY & MIRRE, 1979).
Babesia bigemina: Este organismo possui tropismo pela circulao perifrica e
raramente encontrado no plasma ou superfcie eritroctica. muito pleomrfico, as
formas pequenas possui bordos irregulares, devido emisso de pseudpodes; as formas
piriformes podem aparecer isoladas, mas frequentemente esto bigeminadas com a
extremidade disposta em ngulo obtuso ou agudo (Fig. 3) (FONSECA & BRAGA, 1924).
Classificada como grande babsia, esta espcie possui dimenses de 3 a 5 m. As formas
arredondadas confundem-se com as formas de B. bovis. As formas amebides e ovaladas
tm sido relacionadas ao ciclo sexuado, o qual se completa no vetor, e as formas piriformes
relacionam-se ao ciclo assexuado. Apresenta colorao basoflica pelos corantes derivados
do romanovski. Na fase de convalescncia do hospedeiro, a morfologia deste babesdeo
pode estar alterada, podendo ainda encontrar elementos livres no plasma. As drogas
babesicidas tambm induzem modificaes morfolgicas (MASSARD & FREIRE, 1985).
Esta espcie tambm transmitida pelos carrapatos B. microplus, cuja infeco no
carrapato tambm ocorre no perodo de ingurgitamento da fmea; existe a transmisso
transovariana, porm, apenas os nstares de ninfa e adultos transmitem este agente para
os bovinos (MASSARD et al., 1998). Os machos de B. microplus, devido sua mobilidade
e longevidade podem transmitir a B. bigemina para diferentes bovinos (RIEK, 1964;
FRIEDHOF & SMITH, 1981).
Anaplasma marginale: uma rickettsia caracterizada morfologicamente como um
pequeno corpo arredondado ou ovalado, com caractersticas tintoriais basoflicas aos
corantes derivados do romanovski. Este organismo est localizado no eritrcito, em 80
a
90% das ocorrncias, perifrica/marginalmente (MOREL, 1989). Mais de um corpo podem
estar presentes no eritrcito. Corado pelo giemsa o A. marginale apresenta-se sob forma
arredondada, densa e homognea, com tonalidade purprea, e dimenses de 0,3 a 1,0 m
(Fig. 4). Cada corpo pode conter de um a oito subunidades (corpsculos iniciais) que so
as formas infectantes. Os corpsculos iniciais aderem-se s hemcias e sua entrada se d
por invaginao da membrana citoplasmtica, embolsamento do microrganismo e a
posterior formao do vacolo parasitforo. Logo aps a penetrao no eritrcito, o
corpsculo inicial se multiplica por diviso binria, sendo discutida a multiplicao por
brotamento, e forma o corpo elementar. A transmisso do A. marginale se d
mecanicamente, principalmente por dpteros hematfagos (tabandeos, culicdeos e
muscdeos), os carrapatos so importantes quanto transmisso transestadial e para o B.
microplus o macho tem papel relevante. A utilizao de agulhas, instrumentos cirrgicos e
outros objetos perfurantes contaminados so fontes de infeco (RIBEIRO, 1991;
MASSARD et al., 1998).
3
So descritas outras espcies da famlia Anaplasmataceae parasitando bovinos,
como o A. centrale THEILER, 1911 e Paranaplasma caudatum KREIER & RISTIC, 1963, a
segunda espcie ainda no descrita no Brasil. O A. centrale, nome dado pelo fato de 80 a
90% das formas estarem no centro do eritrcito (Fig. 5) (MOREL, 1989) o agente
etiolgico da anaplasmose bovina benigna; no entanto, esta rickettsia quando foi
diagnosticada pela primeira vez no Brasil, em bovinos da raa holandesa no municpio do
Rio de Janeiro, os animais desenvolveram doena aguda (MASSARD et al., 1980).
EPIZOOTIOLOGIA
Distribuio Geogrfica: A TPB encontra-se amplamente distribuda. As
babesioses determinadas pelas espcies B. bigemina e B. bovis ocorrem nas regies
tropicais e sub-tropicais do mundo, entre os paralelos 32
0
N e 32
o
S, regio onde encontra-
se o B. microplus (MC COSKER, 1981). E a anaplasmose ocorre tanto em regies tropicais
e sub-tropicais como em zonas temperadas (DALGLIESH et al, 1990; KESSLER et al.,
1992). A TPB possui diferentes situaes epizootiolgicas (MOREL, 1989):
Estabilidade enzotica: Nesta situao existe uma alta probabilidade de infeco
primria antes do desaparecimento da proteo passiva adquirida por anticorpos colostrais.
Neste estgio, a infeco ocorre em aproximadamente 100% dos bezerros com 3 a 4
meses e idade, embora a doena seja normalmente inaparente. A qualidade da proteo
passiva garantida pelo grau de premunio maternal.
Instabilidade enzotica: O risco da doena clnica nesta situao muito alto, pois
frequentes infeces primrias ocorrem aps a perda da proteo passiva, entre a idade de
4 meses a 3 anos. A situao pode vir a ser crtica quando o vetor comea a ficar escasso,
principalmente em casos de massivos tratamentos acaricidas, mesmo no erradicando-o.
Assim, os casos clnicos so raros, pois a maioria dos bovinos no so infectados e,
consequentemente premunidos; a regio pode tornar-se livre, o que desfavorvel no
momento da introduo e/ou proliferao dos carrapatos, pois os animais estaro
desprotegidos.
A epizootiologia da TPB est influenciada ainda pela relao hemoparasito-
hospedeiro, onde o fator primordial a imunidade, a qual dependente da especificidade
dos anticorpos. Entretanto, no existe uma correlao entre ttulo de anticorpos e o nvel de
proteo, exceto em animais jovens onde mesmo os baixos ttulos asseguram efetiva
proteo.
Relao hemoparasito-carrapato: Nesta relao est determinada a infeco do
carrapato pelo agente (Babesia sp) e a infectividade gerao seguinte. Em altas
parasitemias, as fmeas de B. microplus sofrem severas leses intestinais pelas
sucessivas multiplicaes da Babesia nas clulas do epitlio digestivo. Este processo pode
reduzir a oviposio do carrapato, mas as larvas tero uma relativa quantidade de B. bovis,
assim como as ninfas e adultos para B. bigemina (RIEK, 1966). Quanto ao A. marginale
sabido que este se multiplica nas clulas intestinais do carrapato, mas sua transmisso via
transovariana ainda discutvel (RIBEIRO, 1991; KESSLER et al., 1992).
4
Relao carrapato-hospedeiro: A variao sazonal, a biologia e a dinmica
populacional determinam os perodos de atividade do vetor no hospedeiro e,
consequentemente, o perodo de infeco ou reinfeco (MOREL, 1989). O
desenvolvimento da Babesia no vetor depende do ciclo de vida do carrapato e,
principalmente, da poca quando o carrapato infectado e da poca em que este
transmitir o piroplasmdeo ao hospedeiro. O risco de infeco est ainda relacionado ao
habitat do carrapato, e em muitas situaes o ixoddeo pode permanecer com o agente por
longos perodos (NEITZ, 1956; FRIEDHOF & SMITH, 1981; MOREL, 1989).
IMPORTNCIA
A TPB de grande importncia em todo o mundo devido s grandes perdas
econmicas. Segundo MC COSKER (1981), se o EUA no tivessem erradicado o B.
annulatus, as perdas decorrentes do carrapato e da TPB (babesioses) estariam prximo de
500 milhes de dlares anuais. Na Amrica Latina considera-se perdas em torno de 266
milhes de dlares/ano. A anaplasmose nos EUA responsvel por cerca de 100 milhes
de dlares anuais (MC CALLON, 1973).
No Brasil a associao de B. microplus e as doenas transmitidas por ele
determinam prejuzos estimados em mais de 1 bilho de dlares (Ministrio da Agricultura
do Brasil, 1985).
Esta importncia decorre do fato destes agentes serem responsveis por prejuzos
diretos e indiretos. A morbidade determinada pela TPB alta nos pases tropicais e sub-
tropicais, e em reas de instabilidade a taxa de mortalidade alta. Alm das
consequncias decorrentes da patogenia, deve-se levar em considerao a onerosidade do
tratamento, pois as drogas so especficas e de custo elevado.
PATOGENIA E SINTOMAS CLNICOS
A patogenia para o complexo TPB difere em relao aos agentes etiolgicos e,
consequentemente, expresso sintomatolgica. As principais aes so decorrentes de:
Ao hemoltica: Na TPB a eritrlise decorrente da multiplicao assexuada, dos
piroplasmdeos, de forma gradual e progressiva, levando a acentuada diminuio do
nmero de hemcias circulantes. A destruio de eritrcitos bem marcada pela B.
bigemina, enquanto a B. bovis considerada menos hemoltica (ARAGON, 1976). Na
anaplasmose no h hemlise intravascular, as hemcias parasitadas e/ou marcadas so
fagocitadas pelas clulas do sistema fagoctico mononuclear, a nvel de bao
principalmente; assim a anemia consequncia da remoo dos eritrcitos parasitados da
circulao. Entretanto na anaplasmose pode ocorrer um processo imuno-mediado,
determinado pela destruio de eritrcitos normais (BOERO, 1974).
5
Ao sobre o sistema digestivo: Nos casos graves de TPB frequente observar
alteraes digestivas como diarria ou coprostase e desidratao, associada ictercia e
anemia em funo da eritrlise. A nvel heptico, sobrevm a degenerao dos
hepatcitos, seguido de bilirrubinemia devido ao desdobramento de pigmentos hemticos.
Na babesiose encontra-se uma hemoglobinemia intensa, j na anaplasmose a
hemoglobina decomposta e os pigmentos biliares estaram em altas concentraes no
plasma e nas fezes (BOERO, 1974). Na babesiose a hemoglobina liberada passa ao
plasma para ento ser expelida pela urina ou acumular nas cavidades como no saco
pericrdico. Na anaplasmose a massiva destruio dos eritrcitos levar a excessiva
produo biliar, ficando a vescula aumentada com bile espessa e grumosa (mal da bile)
(MASSARD & FREIRE, 1985).
A insuficincia heptica permite a passagem de sais e cidos circulao, os quais
podem determinar uma toxemia. A grumosidade e o espessamento biliar favorece o
aparecimento das disfunes digestivas. A ao sobre o sistema digestivo ter como
consequncia a esplenomegalia, a hepatomegalia, a ictercia, a coprostase ou a diarria,
dentre outros distrbios.
Ao sobre a termorregulao: Existe uma relao, nas babesioses, entre a
eritrlise, hemoglobinria e hipertermia. Os primeiros sinais febris normalmente so
decorrentes da infeco pela B. bigemina, cuja parasitemia maior e a febre prxima de
40
o
C (MASSARD & FURLONG, 1994). Em relao a infeco pela B. bovis, a parasitemia
menor, pois esta tem caractersticas viscerotrpicas, no havendo intensa
hemoglobinemia, hemoglobinria e a febre pode ser menor que para a B. bigemina. A
anaplasmose, normalmente, caracteriza a segunda fase da TPB e o terceiro pico febril,
embora esta possa manifestar-se de forma isolada, e a febre acima de 40
o
C (FONSECA
& BRAGA, 1924).
Ao sobre a hematopoiese: A atividade da medula ssea pode ser caracterizada
pela presena de reticulcitos circulantes. A hemlise intravascular nas babesioses
associada a intensa funo esplnica quanto a hemocaterese (anaplasmose e babesiose),
determina uma parada de atividade esplnica quanto a sua funo frenadora. Assim a
medula ssea enviar grande nmero de clulas imaturas circulao (BOERO, 1974).
Estas clulas so ineficientes no transporte de oxignio.
A disfuno dos rgos hematopoiticos e do tecido sanguneo, quanto a eritrlise, a
diminuio da resistncia globular, a liberao de hemoglobina e a trombose capilar,
caracterizam a vitria do parasitismo sobre a barreira imunolgica do hospedeiro, o que
far o animal apresentar um quadro patolgico de gravidade varivel.
Ao viscerotrpica bloqueante: Enquanto a B. bigemina e o A. marginale
apresentam tropismo pela circulao perifrica, para a B. bovis esse comportamento raro.
Esta espcie possui tropismo por capilares de rgos centrais como crebro, cerebelo e
meninges, e rgos viscerais como rins, bao, pulmo, e corao. A B. bovis determina
uma patologia menos anemiante e menos ictergena com caracterstica viscerotrpica
aglutinante com bloqueio de vasos (MASSARD & FREIRE, 1985). A B. bovis, a nvel de
capilares do SNC, pode desencadear a sintomatologia nervosa decorrente de alteraes
devido a congesto da rede capilar, aglutinao de hemcias e trombose. Assim, o animal
apresentar sinais de incoordenao motora, sialorria, andar vacilante, cefelia,
culminando com encefalites e morte.
Ao sobre a funo renal: Na babesiose a hemoglobinria consequncia da
massiva eritrlise intravascular o que bem marcada na infeco pela B. bigemina. Na
anaplasmose, no entanto, no h hemoglobinria. comum ocorrer na babesiose
nefropatias devido deposio de pigmentos frricos e acmulo de cristais no glomrulo
renal (HILDEBRANDT, 1981).
Os sinais clnicos associados a toxemia hematgena, a leso renal, a desidratao,
a perda da viscosidade sangunea e a diminuio da tenso superficial do sangue,
determinam a morte do animal (MASSARD & FREIRE, 1985).
6
IMUNIDADE
A imunidade contra os agentes da TPB depende da especificidade dos anticorpos.
No entanto, no existe correlao entre o ttulo de anticorpos e o nvel de proteo, exceto
em animais jovens, onde mesmo ttulos baixos pode conferir proteo (MOREL, 1989).
Variaes antignicas podem ocorrer entre amostras de agentes provenientes de
diferentes regies geogrficas. Estas diferenas tambm so aplicveis quanto a
patogenicidade. Tais fenmenos so comuns entre as babsias, e no esto claramente
compreendidos.
As babsias possuem um mecanismo de variao antignica que aparece aps a
primeira expresso clnica/imunolgica do hospedeiro. Este fenmeno comum entre os
protozorios Apicomplexa (TAVERN & BRADLEY, 1997). Os antgenos permanecem
estveis durante a primo-infeco; entretanto, a recorrncia da enfermidade ocorre como
um resultado da produo de uma nova variao antignica no correspondendo aos
anticorpos pr-estabelecidos (MOREL, 1989).
Os agentes da TPB tm uma grande habilidade de evaso ao sistema imune do
hospedeiro seja no carter humoral ou celular. Pouco se conhece sobre a imunidade s
rickettsias, mas acredita-se que estas possuem mecanismos similares aos Apicomplexa.
Assim, a imunidade do tipo coinfecciosa de grande importncia, alm de ter papel
relevante quanto a epizootiologia da enfermidade.
DIAGNSTICO
O diagnstico da TPB pode ser dividido em:
Diagnstico clnico: As formas clnicas da TPB podem ser confundidas ou estarem
associadas a outros estados mrbidos (ARAGON, 1976). Em geral a babesiose a
primeira manifestao da TPB, onde a B. bigemina determina febre prxima de 40
o
C,
anemia, debilidade geral, prostao, inapetncia, perda de peso, desidratao e
hemoglobinria (ESTRADA PEA, 1984). Quanto a B. bovis raramente ocorre
hemoglobinria. A caracterstica viscerotrpica deste babesdeo levar ao bloqueio de
capilares e consequente congesto de rgos, e esta babsia no SNC desencadear o
quadro neurolgico de incoordenao, movimentos de pedalagem, salivao e opisttomo
(KESSLER et al., 1992). A babesiose visceral tem como diagnstico diferencial a raiva dos
bovinos e ainda intoxicao por plantas como a Cestrum laevigatum que determinam
sintomas neurolgicos.
A anaplasmose representa a segunda fase da TPB, onde ocorre febre muito alta
(acima de 40
o
C), palidez de mucosas, ictercia marcada, ausncia de hemoglobinria,
desidratao, perda do apetite, coprostase, fezes ressequidas e com estrias de sangue.
Pode ocorrer ainda aborto, esterilidade, alm da queda de produo.
A anamnese importante no diagnstico da TPB, pois o histrico relacionado com a
apresentao clnica da enfermidade constituem pontos importantes para o fechamento do
diagnstico.
7
Diagnstico laboratorial: O diagnstico laboratorial de grande valia para a
confirmao e identificao dos agentes da TPB. Esse pode ser direto atravs da
confeco de esfregaos sanguneos delgados, corados pelo mtodo de Giemsa, onde
pode-se observar o agente parasitrio. O exame direto pode ser auxiliado pela realizao
do hemograma (KESSLER et al., 1992) onde ter-se- determinada a concentrao de
hemoglobina, os nveis proticos sricos e plasmticos, o hematcrito e outros parmetros
sanguneos e bioqumicos. A urinlise tambm um procedimento, auxiliar, importante no
diagnstico.
Quanto ao diagnstico indireto, pode-se proceder os imunoensaios como a fixao
de complemento, a imunofluorescncia indireta, o ELISA indireto, a tcnica de aglutinao,
a conglutinao e ainda tcnicas mais modernas como a reao de polimerase em cadeia
e a hibridizao in situ.
Os exames anatomo-patolgicos so importantes no diagnstico da TPB. Pela
necropsia pode-se observar mucosas e serosas hipocoradas ou ictricas, hepatomegalia,
esplenomegalia. nefromegalia. congesto de diversos rgos como fgado, bao, rins,
crebro e cerebelo; linfonodos aumentados, bile espessa e grumosa, vescula biliar
distendida e bexiga urinria contendo urina escura.
Na suspeita de babesiose visceral importante proceder a confeco de impresses
de rgos, pelo mdico veterinrio, principalmente, a partir de fragmentos de crebro e
cerebelo, especialmente do hipocampo, onde pode-se encontrar a B. bovis, no interior dos
eritrcitos aglutinados ao capilar visceral.
CONTROLE
O controle da TPB baseia-se na adoo de medidas integradas, tais como:
Controle do vetor: Deve-se proceder o controle do carrapato de forma mais
adequada para a situao, tendo-se por opes: o manejo dos animais, o sistema de
rotao de pastagem, o controle qumico (MOREL, 1989), controle estratgico, controle
microbiolgico e o controle imunolgico que se baseia no uso de imungenos
recombinantes para o B. microplus, diminuindo assim a populao de carrapatos (DE LA
FUENTE, 1995). importante ressaltar a necessidade dos animais jovens entrarem em
contato com o carrapato, a fim de desenvolverem imunidade. A erradicao do carrapato
malfica quanto a imunidade para os agentes da TPB (MOREL, 1989). Para a
anaplasmose deve-se adotar medidas de higienizao dos intrumentos cirrgicos, e o
controle dos dpteros hematfagos.
Controle dos agentes da TPB: No incio do sculo iniciou-se o desenvolvimento da
tcnica de premunio dos bovinos aos agentes da TPB, estando esta tcnica hoje bem
aprimorada e amplamente utilizada com resultados satisfatrios.
O uso de vacinas no controle da TPB uma questo muito discutida. As vacinas
inativadas, sejam elas obtidas a partir de animais infectados ou de cultivo celular, garantem
uma imunidade temporria e/ou possuem um baixo poder imunognico, devido s
caractersticas regionais das cepas dos agentes (ESTRADA PEA, 1984). As vacinas
vivas, derivadas de sucessivas passagens dos agentes em bezerros esplenectomizados
tambm no garantem imunidade satisfatria, alm de levarem consigo o risco da reverso
de patogenicidade/variao na virulncia; embora sejam a melhor tecnologia disponvel.
Atualmente, acredita-se que uma vacina ideal seria obtida a partir de protenas produzidas
pelas organelas do complexo apical das babsias, como roptrias e micronemas. Estas
protenas esto associadas ao processo de invaso do agente ao eritrcito, sendo de
funo vital para a sobrevivncia das babsias (PERKINS, 1992).
8
TRATAMENTO
No tratamento teraputico e na profilaxia importante o acompanhamento pelo
profissional. O tratamento da TPB depende do diagnstico especfico quanto ao agente. As
babsias possuem diferentes nveis de sensibilidade s drogas. A B. bovis mais
resistente aos babesicidas que a B. bigemina. As drogas babesicidas mais encontradas no
mercado so os derivados das diamidinas e derivados do imidocarb. A dose teraputica
das diamidinas de 3,5 mg/Kg de peso, em dose nica, via intramuscular (IM), esta droga
muito eficiente para a B. bigemina. A dose teraputica dos derivados do imidocarb de
1,2 mg/Kg de peso, por via subcutnea, esta droga eficiente tanto para a B. bigemina
quanto para a B. bovis. O imidocarb alm de possuir longa ao, tem efetividade sobre as
rickettsias na dose de 2,4 mg/Kg de peso (ARAGON, 1976; ESTRADA PEA, 1984).
A droga de eleio para o A. marginale a tetraciclinas, principalmente sob a forma
de cloridrato de oxitetraciclina na dose de 2 a 4 mg/Kg de peso, via IM, fazendo aplicaes
dirias at o desaparecimento dos sintomas. Para as axitetraciclinas de longa ao a dose
de 20 mg/Kg de peso, via IM, em dose nica, podendo repetir esta dose, se necessrio,
aps trs dias, em casos severos (KESSLER et al., 1992). Todos estes quimioterpicos
apresentam efeitos colaterais srios, portanto, devem ser usados com precauo
(TODOROVIC et al., 1973b; PATARROYO et al., 1982 ).
PREMUNIO PARA A TRISTEZA PARASITRIA BOVINA
SERGENT et al. (1924) postularam que o termo premunir, de origem latnica,
significa pr (= antes) e munire (= mnia, igual a modo de defesa). Desta forma, premunir
nada mais significa do que fortalecer o sistema de defesa do animal contra um mal que
possa acontecer e, estando assim preparado, a doena ocorreria numa forma bengna.
Esclareciam ainda que premunir significa o ato, citando o seguinte exemplo: imunizar =
vacinar e premunio o ato da vacinao.
Concomitantemente a postulao do termo premunir, FONSECA & BRAGA (1924)
registraram, no Brasil, estudos detalhados sobre a TPB e seus agentes, enfocando
metodologia de controle pela premunio.
Vrias so as circunstncias que levam surtos de TPB. KESSLER et al. (1992)
relacionam como mais importantes:
Introduo de animais criados em reas livres de carrapatos em reas enzoticas;
introduo de animais parasitados por carrapatos em reas ou rebanhos livres;
reduo temporria da infestao de carrapatos, devido s condies climticas
desfavorveis sua multiplicao (reas de instabilidade enzotica) e,
reduo temporria de infestao de carrapatos por meios artificiais (controle intensivo
de carrapato atravs de banhos carrapaticidas, descanso de pastagens e criao de
raas mais resistentes).
Alm destes, a raa, a idade, a imunidade e o tempo de manifestao da doena
so fatores importantes relacionados ao animal que o predispe ao aparecimento da
enfermidade. O controle dos agentes da TPB foi inicialmente realizado, de forma emprica,
no final do sculo XIX, concomitante descrio da B. bigemina por SMITH & KILBORNE
em 1893, no extremo Sul dos EUA. Entretanto, os trabalhos precursores de premunio
foram realizados na frica do Sul por THEILER (1912), logo aps ter descrito o A.
marginale em 1910.
9
PREMUNIO
A tcnica de premunio foi utilizada, desde o incio do sculo, para imunizar
bovinos importados de reas indenes a serem introduzidos em reas enzoticas para
carrapatos, quando morriam cerca de 90 a 97% dos animais acometidos pela doena
(STEPHAN & SQUIBEL, 1929). A premunio um mtodo utilizado no Brasil, e quando
tecnicamente acompanhado, apresenta resultados satisfatrios. Este mtodo consiste em
induzir a imunidade coinfecciosa pela inoculao de sangue total, parasitado pelos agentes
da TPB, seguido de tratamento com quimioterpico quando se estabelece a doena na
fase aguda.
Hoje, alm da premunio clssica, tambm se utiliza a induo da imunidade
atravs do uso de vacinas atenuadas contra os hemoparasitos. As vacinas atenuadas por
passagem em animais esplenectomizados ou por passagem em outros hospedeiros tm
como principal fator desfavorvel, o risco de reverso da patogenicidade (virulncia),
embora estas sejam muito utilizadas (PERKINS, 1992). O insucesso das premunies
muitas das vezes esto relacionados com a no obervncia de fatores como raa, idade e
poca do ano que se procede a importao, o que poder acarretar prejuzos considerveis
(GRAA, 1996). Qualquer que seja o mtodo, a imunizao contra os patgenos da TPB
tem vantagens e desvantagens.
MTODOS DE PREMUNIO
Vrios tm sido os mtodos empregados no processo de premunio de animais
importados para adapt-los antes de serem introduzidos em reas enzoticas para
carrapatos e consequentemente TPB. A premunio segundo SERGENT et al. (1924) a
resistncia de um animal ao primeiro ataque da babesiose ou anaplasmose, estabelecendo
de certo modo uma simbiose somato-parasitria entre o hospedeiro e o parasita. Em
condies naturais de criao a campo esta simbiose ser mantida pelas sucessivas
reinfestaes de carrapatos, havendo, desta forma, um equilbrio entre a presena
constante do parasito e o organismo do hospedeiro.
Nas reas de estabilidade enzotica, os efeitos da TPB so minimizados pela
exposio precoce dos animais ao agente logo aps o nascimento, pela primo-infeco,
embora essa normalmente assegure apenas a uma imunidade temporria. Entretanto, nas
reas de instabilidade e em bovinos importados de reas indenes a doena ocorre sob
forma aguda causando altos ndices de mortalidade (CORRIER & GUZMAN, 1977; LIMA,
1991).
Os mtodos comumente empregados utilizam a inoculao de sangue parasitado,
desfibrinado e resfriado, colhido de animais portadores, seguido de acompanhamento e de
tratamento especfico quando aparece os sinais clnicos de babesiose e anaplasmose.
Contudo, deve-se ter o cuidado de no provocar uma quimioesterilizao com o uso
excessivo de drogas. Os principais mtodos de premunio so:
Mtodo natural: Foi o primeiro a ser utilizado e consiste em infestar o animal a
premunir com 20 a 50 larvas de carrapato. Este mtodo foi abandonado por apresentar
muitos inconvenientes, alm de no estabelecer o nmero de formas infectantes dos
hematozorios.
10
Mtodos artificiais:
Inoculao de carrapatos triturados: Consiste num processo emprico de
premunio, onde se usa carrapatos coletados em bovinos naturalmente infestados. Estes
so lavados em soluo de sulfato de cobre e posteriormente em gua destilada, aps
serem lavados, estes carrapatos so triturados em salina e preparado uma soluo para
ser inoculada nos bovinos a premunir. Esta tcnica consistia num tratamento emprico
apresentando mais desvantagens do que vantagens, como exemplo a formao de
abcessos, no local de inoculao, induzidos pela quitina do artrpode; outra desvantagem
o risco dos hematozorios estarem com virulncia exacerbada e a inoculao de outros
agentes (DALRYMPLE et al., citado por CORRA, 1973).
Mtodo de NUTHAL & THEILER: o mtodo mais utilizado. Consiste na
premunio propriamente dita, ou seja, um processo em que se utiliza sangue coletado
de um animal carrapateado, naturalmente portador dos trs agentes da TPB. Inocula-se o
sangue no animal a ser premunido, estabelecendo desta forma a infeco, a qual
controlada por quimioterpicos, e induz a imunidade coinfecciosa. Com a evoluo das
investigaes sobre a biologia dos agentes da TPB, este processo sofreu modificaes.
Mesmo assim, desde que usado com acompanhamento tcnico apresenta bons resultados
(SANTOS, 1950; KUTTLER, 1972; TODOROVIC et al., 1975; BANGEL Jr et al., 1987;
LIMA, 1991).
Mtodo de LIGINIRES: Neste mtodo usa-se o inculo de A. marginale obtido por
sucessivas passagens em ovinos, para atenuao da virulncia. Os ovinos, por serem
resistentes, ainda so usados como atenuadores do A. marginale com a finalidade da
produo de vacinas contra a anaplasmose do bovinos. Este processo foi confirmado por
OSORNO & SOLANA, (1975); VIZCAINO et al., (1978) e RISTIC & MONTENEGRO-
JAMES, (1988), os quais utilizaram bezerros holstein-friesian para testar a nvel de
laboratrio e a campo a vacina contra anaplasmose.
Mtodo de ROSEMBUSH: Os animais a serem premunidos so inicialmente
inoculados com Anaplasma a qual determina uma reao mais severa e de difcil
tratamento. Quando estiverem recuperados, os animais so ento inoculados com Babesia,
a qual acarretar uma reao mais branda com melhor resposta ao tratamento. Esta
tcnica foi recomendada por SANTOS (1950), este autor ressalvou que os melhores
resultados da premunio so obtidos em animais jovens e a tcnica deve ter
acompanhamento tcnico permanente.
Mtodo de SERGENT: Este era inicialmente a forma clssica de produo de
vacinas contra TPB, que consistia em colher sangue de um animal com doena em fase
crnica e passar em animal jovem como forma de atenuar a virulncia dos hematozorios.
Destes bezerros, coletava-se sangue para ser usado na premunio de outros animais.
Atualmente, esta tcnica foi modificada e a atenuao dos hematozorios feita por
passagens sucessivas em bezerros esplenectomizados (CALLOW & MELLORS, 1966;
KUTTLER, 1972; TODOROVIC et al., 1973a; KESSLER et al., 1992).
11
VACINAS
Visando minimizar os problemas decorrentes dos inculos utilizados nos mtodos de
premunio, pesquisadores da Austrlia, EUA, Argentina, Uruguai, Colmbia e Brasil, se
empenharam na obteno de um antgeno padro para imunizao contra os agentes da
TPB (KESSLER et al., 1992). Os principais tipos de imungenos so:
Vacinas vivas: So inculos que contm organismos viveis, purificados e
atenuados por passagens em bezerros esplenectomizados ou normais (CALLOW &
MELLORS, l966; VILAS NOVAS & VIANA, 1980).
Antgenos atenuados por irradiao: Este um mtodo pouco estudado. BISHOP
& ADANS (1974) testaram a infecciosidade e imunogenicidade de B. bovis submetida
vrias dosagens de irradiao por cobalto. Observaram que os hemoparasitos desta forma
atenuados e usados como vacina foram capazes de proteger bezerros contra a infeco ao
serem desafiados com cepas no atenuadas.
Amostras purificadas e no atenuadas: Neste processo utiliza-se doses mnimas
infectantes dos agentes da TPB para imunizar os animais (TODOROVIC et al., 1975;
BANGEL Jr et al., 1987; LIMA, 1991).
Amostras no purificadas nem atenuadas: Consiste no mtodo clssico de
premunio, onde se utiliza inculo proveniente de doadores naturalmente infectados. Este
processo confere bons resultados quando devidamente acompanhado (SANTOS, 1950;
BANGEL Jr. et al., 1987; LIMA, 1991; LOSS et al., 1992).
IMUNGENOS NO VIVEIS
Em virtude das vacinas contra a TPB conterem agentes ntegros que alm da
infeco podem veicular outros patgenos e provocarem sensibilizao dos eritrcitos,
podendo acarretar isoeritrlise neonatal; alguns pesquisadores investigaram a obteno de
uma vacina que induzisse a imunidade estril, isto , mesmo sem a presena dos agentes
ntegros, o hospedeiro estaria imune.
Plasma de animais enfermos e recentemente recuperados: Consiste na
transferncia de anticorpos para animais a serem premunidos. uma tcnica muito
discutida, pois esta no garante imunidade duradoura (CALLOW, 1967; MAHONEY &
GOODGER, l972).
Vacinas com o emprego da engenharia gentica, DNA recombinante: Os
estudos sobre a obteno de vacinas contra os agentes da TPB a partir da engenharia
gentica tiveram incio na dcada de 80. Entretanto, estas pesquisas tm utilizado
principalmente a B. bovis e, apesar dos resultados serem promissores, deve-se considerar
que uma boa vacina contra a TPB dever conter todos os agentes (B. bovis, B. bigemina e
A. marginale) (KESSLER et al., 1992).
12
A premunio, como ainda hoje feita no Brasil, desde que tecnicamente orientada
e acompanhada tem demonstrado ser eficiente. O que se deve tentar minimizar so fatores
como o excesso de medicao quimioterpica nos animais que apresentem a doena na
forma aguda, evitando uma quimioesterelizao. Este acontecimento acarretaria a
necessidade de reinoculaes com sangue parasitado, o que possivelmente exporia o
animal ao risco de uma sensibilizao para grupos sangneos, induzindo isoeritrlise,
conforme relato de CARSON et al. (1976). Outros riscos deste mtodo seria a veiculao
de doenas infecciosas como brucelose, leucose, tuberculose, diarria viral bovina,
rinotraqueite infecciosa bovina, lngua azul, febre aftosa, ehrlichiose, e outras; caso a
seleo do doador no seja rigorosa.
MAHONEY et al. (1981), define ser uma vacina de boa qualidade aquela que no
exponha o animal premunido aos riscos, ainda hoje, existentes e desta forma pudesse ser
recomendada na proteo de doenas hemotrpicas dos bovinos.
REFERNCIAS BIBLIOGRFICAS
ARAGON, R. S. 1976. Bovine babesiosis: A review. Vet. Bull., 46 (12): 903-917.
BABS, V. 1888. Sur l'hemoglobinurie bacterienne du boeuf. C. Hebd. Seances Acad. Sci.,
107: 692-694.
BANGEL Jr., J. J.; SCHEFFER, A. L. & DIAS, M. M. 1987. Premunio de bovinos segura e
sem perdas. Arq. Fac.Vet. UFRGS, Porto Alegre, 15/16: 5-9.
BISHOP, J. P. & ADANS, L. G. 1974. Babesia bigemina: Immune response of cattle
inoculated with irradiated parasites. Exp. Parasitol., 35: 35-40.
BOERO, J. J. 1974. Parasitosis animales: Piroplasmosis. Editorial Univ. Buenos Aires,
Tomo II. p. 201-226.
BRASIL, Ministrio da Agricultura, Secretaria Nacional de Defesa Agropecuria-Secretaria
de Defesa Sanitria Animal (Braslia, DF). 1985. Carrapato, berne e bicheira no Brasil.
Braslia, 153p.
CALLOW, L. L. & MELLORS, L. T. 1966: A new vaccine for Babesia argentina infection
prepared in splenectomised calves. Aust. Vet. J., 42: 464-465.
CALLOW, L. L. 1967. Sterili immunity, coinfectious immunity and strain differences in
Babesia bigemina infections. Parasitology, 57: 455-465.
CARINI, A. O. 1910. Anaplasma marginale em So Paulo. Rev. Med., So Paulo, 24.
CARSON, C. A.; SELLS, D. M. & RISTIC, M. 1976. Cell-mediated immunity in bovine
anaplasmosis and correlation with protection induced by vaccination (A review). Vet.
Parasitol., 2: 75-81.
CORRA, O. Doenas parasitrias dos animais domsticos. Ed. SULINA, 1973, 348p.
CORRIER, D. E. & GUZMAN, S. 1977. The effect of natural exposure to Anaplasma and
Babesia infections on native calves in an endemic are of Colombia. Trop. An. Hlth.
Prod., 9: 47-51.
DALGLIESH, R. J.; JORGENSEN, W. K. & DE VOS, A. J. 1990. Autralian froze vaccines for
the control of babesiosis and anaplasmosis in cattle- A review. Trop. An. Hlth. Prod., 22:
44-52.
DE LA FUENTE, J. 1995. Recombinant vaccines for the control of cattle tick. Elfos
Scientiae, La Habana, Cuba, 241p.
ESTRADA PEA, A. 1984. Babesiosis: Diagnstico, tratamiento, inmunizacin y
epizootiologia. Med. Vet., 1 (1): 7-16.
FAJARDO, F. A. 1901. A piroplasmose bovina no Rio de Janeiro. Rev. Med., 4: 18-30.
13
FONSECA, A. & BRAGA, A. 1924. Noes sobre a tristeza parasitria dos bovinos. Off.
Typog. do Ministrio da Agricultura, Rio de Janeiro. 216p.
FRIEDHOF, K. T. & SMITH, R. D. 1981. Transmission of Babesia by ticks. In: RISTIC, M. &
KREIER, J. P. Babesiosis. New York, Academic Press. p. 65-141.
FRIEDHOF, K. T. 1982. Morphology and development of Babesia species from domestics
animals: A review. In: VII Congresso Brasileiro de Parasitologia, Porto Alegre. 20p.
GRAA, F. A. S. 1996. Aspectos clnicos da premunio contra Babesia (Starcovici, 1893)
e Anaplasma (Theiler, l910) em bovinos (Bos taurus) da raa fleckvieh, no Municpio
de Aracruz, Estado do Esprito Santo. Tese de Mestrado, UFRRJ, 87P.
HILDEBRANDT, P. K. 1981. The organ and vascular pathology of babesiosis. In: RISTIC,
M. & KREIER, J. P. Babesiosis. New York, Academic Press. p 489-473.
KAKOMA, I. & MEHLHORN, H. 1994. Babesia of domestic animals. In: KREIER, J. P.
Parasitic protozoa. Second edition, Vol. 7. Academic Press. p. 141-216.
KESSLER, R. H.; SCHENK, M. A. M.; MADRUGA, C. R.; SACCO, A. M. S. & MIQUITA, M.
1992. Tristeza parasitria bovina. In: CHARLES, T. P. & FURLONG, J. Doenas
parasitrias dos bovinos de leite. EMBRAPA-CNPGL, Coronel Pacheco, 134p.
KREIER, J. P. & RISTIC, M. 1963. Anaplasmosis. X. Morphologic characteristics of
theparasitepresent in the blood of calves infected with the Oregon strain of Anaplasma
marginale. Am. J. Vet. Res., 24: 676.
KUTTLER, K. L. 1972. Cooperetive response to premunization using attenuated Anaplama
marginale, virulent Anaplasma marginale and Anaplasma centrale in different age
groups. Trop. An. Hlth. Prod., 4, (4): 197-20
LIMA, J. D. 1991. Premunio: Uma alternativa para controle da tristeza parasitria. Anais
do VII Seminrio Brasileiro de Parasitologia Veterinria, So Paulo, Brasil, p. 39-43.
LOSS, A. C.; LIMA, J. D. & BRAZ Jr.; C.J. 1992. Avaliao da resposta humoral para
anaplasmose em bovinos submetidos premunio. Arq. Bras. Med. Vet. Zoot., 44
(5):397-406.
MAHONEY, D. F. & GOODGER, B. V. 1972. Babesia argentina: Immunogenicity of plasma
from infected animals. Exp. Parasitol., 32:71-85
MAHONEY, D. F. & MIRRE, J. B. 1979. A note of the transmission of Babesia bovis (Syn.
B. argentina) by the one-host tick Boophilus microplus. Res. Vet. Sci., 26: 253-254.
MAHONEY, D. F.; WRIGHT, I. G. & GOODGER, B. V. 1981. Bovine babesiosis: The
immunization of cattle with fractions of erythrocytes infected with Babesia bovis (syn. B.
argentina). Vet. Immunol. Immunopathol., 2:145-156.
MASSARD, C. L.; MASSARD, C. A.; FONSECA, A. H. & LOSS, Z. G. 1980. Diagnstico de
Anaplasma centrale Theiler, 1911 em bovinos no Brasil. In: V Congresso Brasileiro de
Parasitologia. Rio de Janeiro, p. 178.
MASSARD, C. A. & MASSARD, C. L. 1982. Ehlichia bovis (Rickettsiales: Rickettsiaceae)
em gado de leite no Brasil. Arq. Univ. Fed. Rural Rio de Janeiro, 5(2): 237-239.
MASSARD, C. L. & FREIRE, R. B. 1985. Etiologia, manifestaes e diagnstico das
babesioses bovinas no Brasil. Hora Vet., 23: 53-56.
MASSARD, C. A. & FURLONG, J. 1994. Controle da tristeza parasitria dos bovinos. In:
FURLONG, J. Manejo sanitrio, preveno e controle de parasitoses e mamite em
rebanhos de leite. EMBRAPA-CNPGL, Coronel Pacheco-MG, p. 49-59.
MASSARD, C. L.; SOARES, C. O.; FONSECA, A. H. & MADRUGA, C. L. 1998. Tristeza
parasitria bovina: Histrico, biologia e modalidades de transmisso de Babesia bovis,
B. bigemina e Anaplasma marginale aos bovinos. In: Curso sobre controle de carrapato
em bovinos. EMBRAPA-CNPGC, Campo Grande-MS, p. 77-90.
14
MC CALLON, B. R. 1973. Prevalence and economic aspects of anaplasmosis. In: VI
National Anaplasmosis Conferences, Stillwater, Heritage, p.1.
MC COSKER. P. J. 1981. The global importance of babesiosis. In: RISTIC, M. & KREIER,
J. P. Babesiosis. New York, Academic Press. p. 1-24.
MOREL, P. C. 1989. Tick-borne disease of livestock in Africa. In: CAB International. Manual
of Tropical Veterirary Parasitology. Wallingford, UK. p. 301-459.
NEITZ, W. O. 1956. Classification, transmission, and biology of piroplasms of domestics
animals. Ann. New York Acad. Sci., 64 (2): 56-111.
OSORNO, M. B. & SOLANA, P. M. 1975. Study of an attenuated Anaplasma marginale
vaccine in Mexico natural challenge of immunity in na Enzootic area. Am. J. Vet. Res.,
36(5): 631-63.
PATARROYO, J. H.; RIBEIRO, M. F. & VARGAS, M. I. 1982. Effect of imidocarb
dipropionate in brazilian anaplasmosis and babesiosis. Trop. Anim. Hlth. Prod., 14:234.
PERKINS, M. E. 1992. Rhoptry organelas of apicomplexa parasites. Parasitol. Today, 8: 28-
32.
RIEK, R. F. 1964. The life cicle of Babesia bigemina (Smith & Kilborne, 1893) in the tick
vector Boophilus microplus (Canestrini). Aust. J. Agic. Res., 15: 802-821.
RIEK, R. F. 1966. The life cicle of Babesia argentina (Lignires, 1903) in the tick vector
Boophilus microplus (Canestrini). Aust. J. Agic. Res., 17: 247-254.
RIBEIRO, M. F. B. 1991. Morfologia, evoluo e reproduo do Anaplasma marginale
(Theiler, 1910) em clulas epiteliais intestinais de teleginas de Boophilus microplus
(Canestrini, 1887). Estudo ao microscpio ptico e eletrnico. Tese de Doutorado,
UFMG, 134p.
RISTIC, M. & MONTENEGRO-JAMES, S. 1988. Immunization againt Babesia. In: RISTIC,
M.. (ed.). Babesiosis of domestical animals and man. Boca Raton. CRC Press, 163p.
SANTOS, J. A. 1950. Normas prticas para premunio de bovinos contra a Tristeza
Parasitria (Piro e Anaplasmose). Instituto de Biologia Animal, 10p.
SERGENT, E.; PARROT, L. & DONATIEN, A. 1924: Une question de terminologie:
Immunizer et preminir. Bul. Soc. Pathol. Exot., 17:37-38.
SMITH, T. H. & KILBORNE, F. L. 1893. Investigation into the nature causation and
prevision of Texas or southern cattle fever. U. S. Dep. Agric. Bull. Anim. Ind., 1: 177-
304.
STEPHAN, O. & SQUIBEL, C. A. 1929. Mtodo de premunio contra a Tristeza, usado
no Posto Zootcnico de So Paulo. Arq. Inst. Biolgico, 2: 182-208
TAVERN, J. & BRADLEY, J. E. 1997. Imunidade aos protozorios e vermes. In: ROITT, I.;
BROSTOFF, J. & MALE, D. Imunologia. Editora Manole, So Paulo, p. 18.1-18.19.
THEILER, A. 1910. Anaplasma marginale (gen. and spec. nov.): A protozoon of cattle; a
cause of the called gall-sickness. Transv. Med. J., 5: 110-111.
THEILER, A. 1911. Futher investigations into anaplasmosis of south african cattle. In: First
Report of the Director of Veterinary Report. South African Dep. Agric., 1: 7-46.
THEILER, A. 1912. Gall-sickness of imported cattle and the protective inoculation against
disease. Agricul. J. Union South Africa, 3: 1-21.
TODOROVIC, R. A.; GONZALEZ, E. F. & ADANS, L. G. 1973a. Bovine babesiosis: Sterile
immunity to Babesia bigemina and Babesia argentina infection. Trop. An. Hlth. Prod., 5:
234-245.
TODOROVIC, R. A.; GONZALEZ, E, F. & ADANS, L. G. 1973b: Chemoprophylaxis
(imidocarb) against Babesia bigemina and Babesia argentina infections. Am. J. Vet.
Res., 34: 1153-1161.
15
TODOROVIC, R. A.; LOPEZ, A.G. & GONZALEZ, E. F. 1975. Bovine babesiosis and
anaplasmosis: Control by premunition and chemoprophylaxis. Exp. Parasitol., 37: 92-
104.
VILAS NOVAS, J. C. & VIANA, F. C. 1980. Avaliao a campo da vacina atenuada de
Anaplasma marginale na imunizao de bezerros. Arq. Esc. Vet. UFMG, 32(1): 57-62.
VIZCAINO, O.; CARSON, C. A.; LEE, A. J. & RISTIC, M. 1978. Efficacy of attenuated
Anaplasma marginale vaccine under laboratory and field conditions in Colombia. Am. J.
Vet. Res., 39(2): 229-233.
16
Você também pode gostar
- GUIA de Fórmulas SkinCare para Salvar No Celular e Computador PDFDocumento137 páginasGUIA de Fórmulas SkinCare para Salvar No Celular e Computador PDFrenata andrade100% (5)
- A Bandeira Do Elefante e Da Arara - Guia Do MestreDocumento475 páginasA Bandeira Do Elefante e Da Arara - Guia Do MestreI am Lucas Toon100% (3)
- Autismo - PDF Intervencao-Nutricional-No - (4699)Documento36 páginasAutismo - PDF Intervencao-Nutricional-No - (4699)Taiana Cardoso100% (1)
- Jaymin Eve - SuperNatural Prison Story 01 - Broken CompassDocumento295 páginasJaymin Eve - SuperNatural Prison Story 01 - Broken CompassRobson Magno100% (1)
- Ficha de Protozoários 1111Documento7 páginasFicha de Protozoários 1111Efraim Nobre SoaresAinda não há avaliações
- Apostila AQUIVET PDFDocumento39 páginasApostila AQUIVET PDFMarcos CamargoAinda não há avaliações
- Reino MoneraDocumento9 páginasReino MoneraJéssica QueirozAinda não há avaliações
- Roteiro PPDocumento25 páginasRoteiro PPLuana Lopes100% (4)
- Exercício Reino ProtistaDocumento4 páginasExercício Reino ProtistaEdvaldo Pereira da Silva Júnior100% (1)
- CEDERJ - MetabolismoDocumento324 páginasCEDERJ - MetabolismoKata FaradayAinda não há avaliações
- Inteligencia EmocionalDocumento460 páginasInteligencia EmocionalMárcia MartinsAinda não há avaliações
- Elementais Das Matas BrasileirasDocumento7 páginasElementais Das Matas BrasileirasVirgilio Luis Junior100% (2)
- Hemoparasitoses Med Vet03Documento33 páginasHemoparasitoses Med Vet03raphaeltnvAinda não há avaliações
- Babesiose CaninaDocumento10 páginasBabesiose CaninaThamirys SilveiraAinda não há avaliações
- Protozoa RiosDocumento6 páginasProtozoa RiosEfraim Nobre SoaresAinda não há avaliações
- A Criacao de ColeiroDocumento10 páginasA Criacao de ColeiroFelipe FestaAinda não há avaliações
- Tristeza Parasitaria BovinaDocumento9 páginasTristeza Parasitaria BovinaCazoo Ufmt RondonópolisAinda não há avaliações
- ArtigoDocumento20 páginasArtigoDammysanAinda não há avaliações
- Tristeza Parasitária Bovina - Revisão de LiteraturaDocumento21 páginasTristeza Parasitária Bovina - Revisão de LiteraturaThiago Augusto CasottiAinda não há avaliações
- Trab ParasitoDocumento16 páginasTrab Parasitothais.horanghaeAinda não há avaliações
- Balantidium ColiDocumento14 páginasBalantidium ColiViviane Maria100% (8)
- PARASITOLOGIA - Tópico 3Documento13 páginasPARASITOLOGIA - Tópico 3katrininovaesAinda não há avaliações
- Tuberculose PDFDocumento16 páginasTuberculose PDFmonique feitosaAinda não há avaliações
- Blue and White Professional Science Project PresentationDocumento10 páginasBlue and White Professional Science Project Presentationjuniorfreittas.gptAinda não há avaliações
- Barbosa 9788575414019Documento310 páginasBarbosa 9788575414019lagartojrAinda não há avaliações
- 09492909052012fundamentos de Parasitologia Aula 2 PDFDocumento23 páginas09492909052012fundamentos de Parasitologia Aula 2 PDFSalvatory ToméAinda não há avaliações
- PBL LeishmanioseDocumento11 páginasPBL LeishmanioseMARIA GRAÇASAinda não há avaliações
- Aspectos Clínicos Da Toxoplasmose Como Zoonose.Documento21 páginasAspectos Clínicos Da Toxoplasmose Como Zoonose.Pietra Nunes BergerAinda não há avaliações
- Capitulo 12 A Interacao Do Protozoario Leishmania Com Seus Insetos VetoresDocumento45 páginasCapitulo 12 A Interacao Do Protozoario Leishmania Com Seus Insetos VetoresGabriel LopesAinda não há avaliações
- Grupos de Bergey - Apontamentos 2Documento14 páginasGrupos de Bergey - Apontamentos 2SMOC94Ainda não há avaliações
- Leishmaniose Tegumentar AmericanaDocumento10 páginasLeishmaniose Tegumentar AmericanaJuliana Coutinho MachadoAinda não há avaliações
- Atividade de Revisão Microbiologia e ParasitologiaDocumento4 páginasAtividade de Revisão Microbiologia e ParasitologiaLuma ChristinaAinda não há avaliações
- Introdução A Botanica SistemáticaDocumento7 páginasIntrodução A Botanica SistemáticaIsabel Matunha MatunhaAinda não há avaliações
- Atividade 2 - Far - Fundamentos Da Microbiologia e Imunologia - 51-2023Documento3 páginasAtividade 2 - Far - Fundamentos Da Microbiologia e Imunologia - 51-2023Cavalini Assessoria AcadêmicaAinda não há avaliações
- PARASITOLOGIA - Tópico 4Documento12 páginasPARASITOLOGIA - Tópico 4katrininovaesAinda não há avaliações
- Artigo MaláriaDocumento12 páginasArtigo MaláriaOctávio Augusto Cruz BritoAinda não há avaliações
- LeishmanioseDocumento7 páginasLeishmanioseGiovanna MirandaAinda não há avaliações
- ABBASDocumento11 páginasABBASLeti BullaAinda não há avaliações
- Os Fungos Do BrasilDocumento7 páginasOs Fungos Do BrasilPamelaAinda não há avaliações
- Parasitologia 3Documento13 páginasParasitologia 3valAinda não há avaliações
- ParasitologiaDocumento11 páginasParasitologiaeduardaAinda não há avaliações
- 11 Doença de Chagas Medresumo 2016 Parasitologia - 37724166 PDFDocumento8 páginas11 Doença de Chagas Medresumo 2016 Parasitologia - 37724166 PDFGabriela LuzAinda não há avaliações
- Introdução Toxoplasmose Arq 3Documento22 páginasIntrodução Toxoplasmose Arq 3Sílvia ScabinAinda não há avaliações
- Protozoários FitopatogênicosDocumento17 páginasProtozoários FitopatogênicosAlison K. Picinin100% (1)
- Atividade de ParasitologiaDocumento7 páginasAtividade de ParasitologiaLaricien DelonghiAinda não há avaliações
- Gabarito 2 Ano - PET4Documento17 páginasGabarito 2 Ano - PET4Carolina FernandesAinda não há avaliações
- 4 Unid - 4Documento51 páginas4 Unid - 4giselemiranda800Ainda não há avaliações
- O Gênero Leishmania e As LeishmaniosesDocumento9 páginasO Gênero Leishmania e As Leishmaniosesvanusalima3555Ainda não há avaliações
- CryptosporidiumDocumento4 páginasCryptosporidiumJonas JuniorAinda não há avaliações
- Ciclo BiologicoDocumento8 páginasCiclo BiologicoAylle KellyAinda não há avaliações
- Trabalho de BioDocumento8 páginasTrabalho de Biogabriel borges kienerAinda não há avaliações
- FungosprotistasDocumento62 páginasFungosprotistasLUCIANAAinda não há avaliações
- Isso Explicaria Seus Sintomas?: Entendendo os Riscos de Uma Epidemia Oculta da Doença de Lyme no BrasilNo EverandIsso Explicaria Seus Sintomas?: Entendendo os Riscos de Uma Epidemia Oculta da Doença de Lyme no BrasilAinda não há avaliações
- Ordem UredinalesDocumento20 páginasOrdem UredinalesRaul CoutinhoAinda não há avaliações
- Livro-Texto - Unidade IIIDocumento50 páginasLivro-Texto - Unidade IIIRafael CedroAinda não há avaliações
- Microbiologia - Fungos e Os AlimentosDocumento12 páginasMicrobiologia - Fungos e Os AlimentosAline CamurçaAinda não há avaliações
- Bovin Alim Brach AndropDocumento13 páginasBovin Alim Brach AndropJessica Costa LeiteAinda não há avaliações
- Doença de Jorge LoboDocumento14 páginasDoença de Jorge LoboJulia AbreuAinda não há avaliações
- Artigo-Uma Abordagem Histórica Da Tragetória Da ParasitologiaDocumento6 páginasArtigo-Uma Abordagem Histórica Da Tragetória Da ParasitologiaLooh MarquesAinda não há avaliações
- Leishmaniose (Úlcera-de-Bauru) PDFDocumento10 páginasLeishmaniose (Úlcera-de-Bauru) PDFjkmilfont860Ainda não há avaliações
- TricomonosebovinaDocumento43 páginasTricomonosebovinaJuliana Lira AlvesAinda não há avaliações
- Rodococcus PotroDocumento13 páginasRodococcus Potrohugoh2cnAinda não há avaliações
- Microbiologia e Biologia Dos FungosDocumento85 páginasMicrobiologia e Biologia Dos FungosFardilha Catarina100% (1)
- Parasitologia Humana - Filariose LinfáticaDocumento21 páginasParasitologia Humana - Filariose Linfáticapedronunes100% (32)
- Artigo Histoplasma CapsulatumDocumento17 páginasArtigo Histoplasma CapsulatumDAMedVeterináriaUpfAinda não há avaliações
- Aula de Parasitologia Basica 1Documento36 páginasAula de Parasitologia Basica 1crisAinda não há avaliações
- FungosDocumento10 páginasFungosLeandro FernandesAinda não há avaliações
- Atlas ParasitologiaDocumento9 páginasAtlas ParasitologiaSarah Diniz MeloAinda não há avaliações
- Praga Hospitalar: Formicídeos como potenciais transmissores de bactérias em hospitaisNo EverandPraga Hospitalar: Formicídeos como potenciais transmissores de bactérias em hospitaisAinda não há avaliações
- EcoempreendedorismoDocumento13 páginasEcoempreendedorismoVictor Almeida PereiraAinda não há avaliações
- Descritores de Língua Portuguesa D7Documento5 páginasDescritores de Língua Portuguesa D7Flávia M. Malaquias Piccini0% (2)
- Conservação Pós Colheita MaçãsDocumento16 páginasConservação Pós Colheita MaçãsJerson ZontaAinda não há avaliações
- Como Aprimorar o SexoDocumento27 páginasComo Aprimorar o SexoIsadora InacioAinda não há avaliações
- DesenvolvimentoDocumento3 páginasDesenvolvimentoJose LicucoAinda não há avaliações
- 15 Dicas Infalíveis para Desanuviar A Sua Mente - Estado ZenDocumento3 páginas15 Dicas Infalíveis para Desanuviar A Sua Mente - Estado ZenArnaldo GomesAinda não há avaliações
- Administração de Medicamentos REGIDocumento106 páginasAdministração de Medicamentos REGIkeslei.soares.alvesAinda não há avaliações
- O Estresse Causado Pela Aceleração Dos PensamentosDocumento3 páginasO Estresse Causado Pela Aceleração Dos PensamentosCelia GevartoskiAinda não há avaliações
- Legendas MargareteDocumento3 páginasLegendas Margareterenato diasAinda não há avaliações
- E.E. Haydée Maria Imculada Schittini Ensino Religioso - Projeto Meio Ambiente Meio Ambiente - E Eu Com Isso?Documento4 páginasE.E. Haydée Maria Imculada Schittini Ensino Religioso - Projeto Meio Ambiente Meio Ambiente - E Eu Com Isso?Romilda Dores Brito100% (1)
- Aula BiodiversidadeDocumento18 páginasAula BiodiversidadeCiências Profe AnelizeAinda não há avaliações
- A Missão Dos EspíritasDocumento4 páginasA Missão Dos EspíritasJennifer JonesAinda não há avaliações
- Fundamentos Da-AnatomiDocumento37 páginasFundamentos Da-AnatomiLucas De FreitasAinda não há avaliações
- RapéDocumento15 páginasRapéNatalia ConcolattoAinda não há avaliações
- 7 Grupo QF 1Documento56 páginas7 Grupo QF 1Gildo Salai MacalaneAinda não há avaliações
- Blades in The DarkDocumento59 páginasBlades in The DarkJamesAinda não há avaliações
- Cultura Da Moranga HíbridaDocumento6 páginasCultura Da Moranga HíbridaCauã AraújoAinda não há avaliações
- 36 - Insuficiência Renal Crônica (IRC)Documento12 páginas36 - Insuficiência Renal Crônica (IRC)tycaetanoAinda não há avaliações
- Avam 2020 Caderno 8º Ano FinalDocumento25 páginasAvam 2020 Caderno 8º Ano FinalMariane CastroAinda não há avaliações
- LICOPENODocumento4 páginasLICOPENOFrancine SallaAinda não há avaliações
- FeridasDocumento164 páginasFeridasPediatria FMU 2019Ainda não há avaliações