Escolar Documentos
Profissional Documentos
Cultura Documentos
FAVET 4.carbonilicos 2018
Enviado por
Adriano Jaime RafaelDescrição original:
Título original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
FAVET 4.carbonilicos 2018
Enviado por
Adriano Jaime RafaelDireitos autorais:
Formatos disponíveis
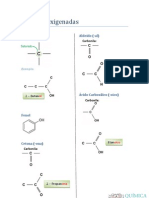
Compostos carbonílicos
São compostos orgânicos contém um ou mais grupos
carbonilos, ou seja grupos caracterizados pela ligação
dupla entre átomos de oxigénio e cabono. A ligação
C=O é característica de várias familias, contudo refere
especialmente os aldeídos e cetonas.
Aldeídos Cetonas
Cloretos de ácidos Ácidos carboxílicos
Amidas Ésteres
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 1
Aldeídos e cetonas
São compostos carbonílicos cujo grupo carbonilo terminal
(em aldeídos) e entre átomos de carbono (em cetonas).
O O O O
H C H H3C C H H3C CH2 C H H3C (CH2)2 C H
metanal ou etanal ou propanal ou butanal ou
formaldeído acetaldeído propionaldeído butiraldeído
O O O
H3C C CH3 H3C CH2 C CH3 H3C CH2 C CH2 CH3
propanona butanona ou pentanona-3
ou acetona etilmetilcetona ou dietilcetona
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 2
Carbonílicos casos na nomenclatura
O O O
CHO
H CH3
benzaldeído acetofenona benzofenona ciclohexanocarbaldeído
CHO O O O
H3C CH2 CH CH2 COH H3C CH2 C CH2 C CH3
ácido 3-formilpentanóico hexano-2,4-diona
O O O
H3C CH2 C CH2 CH H3C CH CH CH2 C CH3
3-oxopentanal hex-4-en-2-ona
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 3
Formaldeído: aldeído mais simples
É um gás incolor, carcinogénico, de odor pungente, com
vapores irritantes aos olhos, vias respiratórias, à pele e
causa de tonturas, dores de cabeça e fadiga.
Na industria, é um reagente na síntese de polímeros para
fazer tecidos, materiais de isolamento, forragem com
tapetes, madeira prensada e plásticos para balcões de
cozinha, etc.
A sua solução aquosa de 37 a 40%, chamada formalina ou
formol, é usada como uma germicida e para preservar
espécimes biológicas.
O formaldeído tem o p. e. -21 oC.
O formol é um gem-diol.
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 4
Acetona: cetona mais simples
É um líquido incolor cujo p. e. 56 oC, de odor suave e
que tem ampla utilização como solvente de limpeza,
em preparações que removem tintas, vernizes e
cimento de borracha.
É extremamente inflamável e deve-se ter cuidado ao
usa-lo.
No corpo, a acetona pode ser produzida em diabetes
não controladas, jejum e dietas ricas em proteínas e
quando grandes quantidades de gorduras são
metabolizadas para a energia.
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 5
Carbonílicos Exemplos na natureza
Muscona
(perfume de almíscar/musk) Carvona
(fragrância de hortelã)
Benzaldeído Vanilina Cinamaldeído
(em amêndoas) (no feijão baunilha/vanilla) (essência de canela)
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 6
Carbonílicos métodos de obtenção
Revisão da oxidação de álcoois – slide 14:
álcoois 1rios formam aldeídos e, depois, ácidos;
álcoois 2rios formam cetonas.
Revisão da ozonólise de alcenos – slide 26:
carbonos 1rios e 2rios formam aldeídos;
carbonos 3rios de formam cetonas.
Revisão de hidratação de alcinos – slide 33:
hidratação indirecta (BH3/H2O2) forma aldeídos;
hidratação directa (H2O/Hg2+) forma cetonas.
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 7
Carbonílicos métodos de obtenção
Revisão da acilação de aromáticos – slide 18:
Acilação de Friedel-Crafts forma cetonas;
O
O H
AlCl3
+
Cl HCl
cloreto de
3-metilbutanoilo 1-fenil-3-metilbutan-1-ona
Método de Gutterman-Koch
Preparacao de benzaldeído a partir de CO, HCl e benzeno:
O
CO AlCl3/CuCl
+ HCl + H
benzaldeído
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 8
Carbonílicos métodos de obtenção
Sínteses a partir de organometálicos:
nitrilos com reagente de Grignard ou com organolítios:
O
N MgBr
C N C C
CH3CH2MgBr H3O+ CH2CH3
CH2CH3
éter
Cloretos de acilos com redutor suave para evitar a
redução para álcoois primários – exemplo:
O O
LiAlH(O-t-Bu)3
CH3CH2CH2 C Cl CH3CH2CH2 C H
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 9
Carbonílicos propriedades físicas
O grupo carbonilo/acilo é um dipolo, com as cargas
parciais, negativa e positiva, sobre oxigénio e carbono,
respectivamente:
Esta característica confere a este grupo de compostos
propriedades singulares:
Formam pontes de hidrogénio, portanto, têm pontos de ebulição
mais altos que os hidrocarbonetos e éteres, sendo mais baixos
que dos álcoois;
A ligacao C=O é mais curta, mais forte e mais polar que a C=C em
alcenos;
São misciveis em compostos polares (agua, álcoois).
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 10
Carbonílicos propriedades químicas
Devido ao caracter bipolar do grupo carbonilo, aldeídos e
cetonas sofrem reacções de adição nucleofílica:
partículas polarizadas negativamente atacam o grupo carbonilo
do lado do carbono, polarizado positivamente.
partículas polarizadas positivamente atacam o grupo carbonilo
do lado do oxigénio, polarizado negativamente.
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 11
Carbonílicos adição nucleofílica
Sob condições neutras a adição nucleofílica é lenta,
sendo a velocidade relativamente alta quando a
reacção ocorre activada, em meio ácido ou básico.
Ataque nucleofílico protonação desidratação/desidrogenação
aldeído
ou
cetona
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 12
Carbonílicos adição nucleofílica
Ex: hidratação de formaldeído formação de formalina
Em meio ácido:
Em meio básico:
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 13
Carbonílicos adição nucleofílica
Ex. reacção com álcoois formação de acetais
protonação ataque nucleofílico desprotonação
hemiacetal protonação
hemiacetal acetal
desidratação
desprotonação ataque nucleofílico
acetal
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 14
Carbonílicos adição nucleofílica
Ex: com reagente de Grignard formação de álcoois
formaldeído álcool 1rio
aldeídos
álcool 2rio
cetonas
álcool 3rio
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 15
Carbonílicos condensação aldólica
Sob influência de ácidos ou alcalis em solução diluída,
duas moléculas de aldeídos (ou cetonas) adicionam-se de
modo que o carbono de um fique ligado carbonilo do
outro, formando um -aldol (-hidroxialdeido) ou -cetol
(-hidroxialdeido).
Por exemplo, a condensação aldólica de acetaldeído:
O O OH
H
OH O
CH3 CH + CH2 CH CH3 CH CH2 CH
-hidroxibutiraldeído
ou 3-hidroxibutanal
Em aldeídos ou cetonas sem de H no -carbono (tal como PhCHO, HCHO,
PhCOPh, PhCOCR3, CR3CHO, etc.) não se observa esta condensação.
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 16
Carbonílicos -halogenação
Os aldeídos e as cetonas podem ser α-halogenados,
simplesmente tratando-os com o halogénio (X2) em meio
ácido ou básico. Para que a substituição tenha lugar é
necessário que haja hidrogénios no α-carbono.
Por exemplo:
A eliminação de -halogénio conduz a formação de compostos
carbonílicos (aldeídos ou cetonas) ,-insaturados.
O O
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 17
Carbonílicos testes de oxidação
Ex: reagente de Tollens solução Ag+ (AgNO3) e amónio
oxida aldeídos, mas não as cetonas;
O ião de prata é reduzido e forma um "espelho de prata".
espelho
Ex: reagente de Benedict solução Cu2+ (CuSO4)
oxida aldeídos α-hidoxilados, mas não as cetonas.
Vermelho
tijolo
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 18
Carbonílicos testes de oxidação
reagente de Benedict teste positivo para açúcares
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 19
Carbonílicos reacções de redução
Na redução de compostos oxigenados, há uma diminuição
no número de ligações carbono–oxigénio pela adição de
hidrogénio e/ou perda de oxigénio.
São usados hidretos como NaBH4 ou H2/Pt (Pd ou Ni)
Os aldeídos são reduzidos a álcoois 1rios
As cetonas são reduzidas a álcoois 2rios
O OH
H2/Pt
H3C C CH3 H3C CH CH3
Cetona álcool 2rio
O OH
H2/Pt
H3C CH2 CH H3C CH2 CH2
aldeído álcool 1rio
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 20
Carbonílicos resumo de reacções
oxidação de aldeídos
23/04/2018 Química Orgânica I - Dr. Miguel Mussa 21
Você também pode gostar
- EQ 5.carbonilicos 2019Documento21 páginasEQ 5.carbonilicos 2019nelito lamuceneAinda não há avaliações
- Aula 18 Organica Carbonilas CarboxilasDocumento71 páginasAula 18 Organica Carbonilas CarboxilasLizzy DarcyAinda não há avaliações
- 7 AlcenosDocumento24 páginas7 Alcenosapi-27441481100% (4)
- Ácidos Carboxílicos e DerivadosDocumento16 páginasÁcidos Carboxílicos e Derivadoseduamaria147Ainda não há avaliações
- Aldeídos e CetonasDocumento5 páginasAldeídos e CetonasGhislaine TakashimaAinda não há avaliações
- Fascículo de QUÍMICA - 12 ClasseDocumento11 páginasFascículo de QUÍMICA - 12 ClasseFrancis EliasAinda não há avaliações
- Química 3Documento21 páginasQuímica 3Guilherme PereiraAinda não há avaliações
- Aldeídos e CetonasDocumento31 páginasAldeídos e CetonasshirleyfernandapAinda não há avaliações
- Química Orgânica - CetonasDocumento18 páginasQuímica Orgânica - CetonasJerciany KetellyAinda não há avaliações
- Funções OxigenadasDocumento4 páginasFunções Oxigenadascharles costa100% (1)
- Slides QuimDocumento16 páginasSlides QuimLucas JalesAinda não há avaliações
- QuimicaDocumento87 páginasQuimicasah grigahcineAinda não há avaliações
- IFSC - Química Orgânica I 2021.2 - Aula 04 Funções OrgânicasDocumento37 páginasIFSC - Química Orgânica I 2021.2 - Aula 04 Funções OrgânicasEduardo Bechara FilhoAinda não há avaliações
- Ricelly - Aula 04Documento6 páginasRicelly - Aula 04camilly britoAinda não há avaliações
- Funcao HidrocabornetoDocumento107 páginasFuncao Hidrocaborneto90NEI 23Ainda não há avaliações
- Funções Orgânicas OxigenadasDocumento72 páginasFunções Orgânicas OxigenadasNicolasAinda não há avaliações
- Tutorial Nomenclatura de Compostos OrgânicosDocumento18 páginasTutorial Nomenclatura de Compostos OrgânicosEva FranciscoAinda não há avaliações
- Testo de Apoio III Trimestre 10classeDocumento19 páginasTesto de Apoio III Trimestre 10classeJorge Pedro ArmandoAinda não há avaliações
- Reações de OxidaçãoDocumento13 páginasReações de OxidaçãoPaulo Vitor SilvaAinda não há avaliações
- Aula 03. 1 AlcanosDocumento26 páginasAula 03. 1 AlcanosJoel SamuelAinda não há avaliações
- Oxigenadas CM 2022 AlunosDocumento33 páginasOxigenadas CM 2022 AlunosLetícia M. VieiraAinda não há avaliações
- Quimica Trabalho Tif1 1Documento15 páginasQuimica Trabalho Tif1 1Armin ArlertAinda não há avaliações
- Funções Oxigenadas e Nitrogenadas - Prof° Agamenon RobertoDocumento12 páginasFunções Oxigenadas e Nitrogenadas - Prof° Agamenon Robertocb_penatrujillo33% (3)
- Reações de OxidaçãoDocumento11 páginasReações de OxidaçãoJaime VarelaAinda não há avaliações
- Funcao Oxigenadas NitrogenadasDocumento55 páginasFuncao Oxigenadas NitrogenadasTchau GorduraAinda não há avaliações
- 3 Funcao Oxigenadas NitrogenadasDocumento65 páginas3 Funcao Oxigenadas NitrogenadasGleison Paulino GonçalvesAinda não há avaliações
- Quimica OrganicaDocumento31 páginasQuimica OrganicaGaius Cassius Longinus100% (1)
- Funcao Oxigenadas Nitrogenadas - PpsDocumento87 páginasFuncao Oxigenadas Nitrogenadas - Ppsgabriel antonio fernandes messiasAinda não há avaliações
- Funcao Oxigenadas Nitrogenadas 230907 223802Documento34 páginasFuncao Oxigenadas Nitrogenadas 230907 223802gabycosta2511Ainda não há avaliações
- Alcinos. 3º Grupo. Turma DD BiologiaDocumento11 páginasAlcinos. 3º Grupo. Turma DD BiologiaAlbino Sande FrançaAinda não há avaliações
- Classificação - Carbonos e Cadeias Carbônicas - 57 QuestõesDocumento24 páginasClassificação - Carbonos e Cadeias Carbônicas - 57 QuestõesCamila Barreiros100% (1)
- Alquenos e Alquinos em PDFDocumento26 páginasAlquenos e Alquinos em PDFfotografiaarthurAinda não há avaliações
- Acidos Carboxilicos-Esteres-Aminas e Amidas QA.2012Documento46 páginasAcidos Carboxilicos-Esteres-Aminas e Amidas QA.2012Margarida MirandaAinda não há avaliações
- Docsity Resumo 10a Aula de Quimica Hidrocarbonetos Alcanos e CiclanosDocumento4 páginasDocsity Resumo 10a Aula de Quimica Hidrocarbonetos Alcanos e CiclanosMarcella MagaldiAinda não há avaliações
- Compostos OrgânicosDocumento4 páginasCompostos OrgânicosBeatriz Pereira GonçalvesAinda não há avaliações
- Alcool Enol FenolDocumento26 páginasAlcool Enol FenolPatrícia SilvaAinda não há avaliações
- 3 Ano - Hidrocarbonetos BomDocumento85 páginas3 Ano - Hidrocarbonetos BomdanzootecAinda não há avaliações
- Química Orgânica - FundamentosDocumento8 páginasQuímica Orgânica - FundamentosEduardo KüllAinda não há avaliações
- Química OrgânicaDocumento76 páginasQuímica OrgânicaLiceAinda não há avaliações
- Hidrocarboneto Alcino, AlcadienoDocumento26 páginasHidrocarboneto Alcino, AlcadienoBianca N C BasilioAinda não há avaliações
- Hidrocarboneto Alcino, AlcadienoDocumento26 páginasHidrocarboneto Alcino, AlcadienoGiovanna GomesAinda não há avaliações
- 004 Nomenclaturas OrgânicasDocumento19 páginas004 Nomenclaturas OrgânicasTúlio BotegaAinda não há avaliações
- Cetonas, Acidos Carboxilicos e AldeidosDocumento9 páginasCetonas, Acidos Carboxilicos e AldeidosAlfredo Zacarias Feduca AzcAinda não há avaliações
- Ficha 6 - Reações de AdiçãoDocumento5 páginasFicha 6 - Reações de AdiçãoMatheus LucasAinda não há avaliações
- Aula 10 - ExercíciosDocumento7 páginasAula 10 - ExercíciosWil BarbosaAinda não há avaliações
- 2 Aula - InTRODUÇÃO HidrocarbonetosDocumento29 páginas2 Aula - InTRODUÇÃO HidrocarbonetospatriciamartinsAinda não há avaliações
- Funções Orgânicas: @negomauro - QuimicaDocumento63 páginasFunções Orgânicas: @negomauro - QuimicaVinicius AndradeAinda não há avaliações
- Funçoes Organicas PDFDocumento17 páginasFunçoes Organicas PDFEliel MárioAinda não há avaliações
- Extensivoenem-Química-Hidrocarbonetos - Alcanos, Alcenos e Alcinos-30-08-2019 PDFDocumento10 páginasExtensivoenem-Química-Hidrocarbonetos - Alcanos, Alcenos e Alcinos-30-08-2019 PDFNatel AmaralAinda não há avaliações
- Reações Orgânicas 246 QuestõesDocumento81 páginasReações Orgânicas 246 QuestõesMyriloAinda não há avaliações
- Funções Organicas1Documento70 páginasFunções Organicas1Vicente ReboucasAinda não há avaliações
- Aula de EstereoquímicaDocumento29 páginasAula de EstereoquímicagelsonrsAinda não há avaliações
- ÁLCOOL - Função Orgânica 1Documento15 páginasÁLCOOL - Função Orgânica 1teteeahAinda não há avaliações
- Apostila Química Orgânica: Terpenos E Rotas De SínteseNo EverandApostila Química Orgânica: Terpenos E Rotas De SínteseAinda não há avaliações
- Apostila Química Orgânica: Carbono, Dienos E AromáticosNo EverandApostila Química Orgânica: Carbono, Dienos E AromáticosAinda não há avaliações
- Conselho Segurança10 tcm310-25936Documento3 páginasConselho Segurança10 tcm310-25936João de Deus MemoAinda não há avaliações
- AviaçãoDocumento15 páginasAviaçãocefgaAinda não há avaliações
- ENVIRONMENTAL APPLICATIONS - Soxhlet Extraction - En.ptDocumento9 páginasENVIRONMENTAL APPLICATIONS - Soxhlet Extraction - En.ptCarol SilvaAinda não há avaliações
- Compostos Oxigenados (II)Documento27 páginasCompostos Oxigenados (II)GleisonAinda não há avaliações
- III Lista Geral de Funções OrgânicasDocumento11 páginasIII Lista Geral de Funções OrgânicasWalber Araujo100% (1)
- Grupos Funcionais PDFDocumento69 páginasGrupos Funcionais PDFJunior DuarteAinda não há avaliações
- Exercícios OrgânicaDocumento4 páginasExercícios OrgânicaDanielly CostaAinda não há avaliações
- Prática 7. Derivados CristalinosDocumento7 páginasPrática 7. Derivados Cristalinosvitorlima.sAinda não há avaliações
- Ciclo HexanonaDocumento10 páginasCiclo HexanonaCarlos AdrianoAinda não há avaliações
- Ômega - Módulo 30Documento17 páginasÔmega - Módulo 30maclaudioAinda não há avaliações
- Grupos FuncionaisDocumento36 páginasGrupos FuncionaisRenata SeixasAinda não há avaliações
- Aldeídos e CetonasDocumento5 páginasAldeídos e CetonasJOSEILA BERGAMOAinda não há avaliações
- Cge 2176 PDFDocumento24 páginasCge 2176 PDFmybassAinda não há avaliações
- Lista de Exercícios 6Documento5 páginasLista de Exercícios 6Alan StampiniAinda não há avaliações
- Por Que A Farmoquímica Utiliza Solventes em Seu Processo IndustrialDocumento3 páginasPor Que A Farmoquímica Utiliza Solventes em Seu Processo Industriallilian leyveAinda não há avaliações
- Super Color Uso Geral Tek BondDocumento7 páginasSuper Color Uso Geral Tek BondAndré VictorAinda não há avaliações
- 568Documento56 páginas568Francinete Alves100% (1)
- QuimicaDocumento12 páginasQuimicaAna Margarida DavideAinda não há avaliações
- FS - Prego Liquido Special PECOL - Revisão 0Documento11 páginasFS - Prego Liquido Special PECOL - Revisão 0Tiago oliveiraAinda não há avaliações
- Zanussi Fa522 PDocumento24 páginasZanussi Fa522 Pricardovaz102100% (1)
- FISPQ Solvente 90 So 044 V05Documento10 páginasFISPQ Solvente 90 So 044 V05WT Estamparia100% (1)
- Acetileno PDFDocumento9 páginasAcetileno PDFFerreira SouzaAinda não há avaliações
- Trabalho de QuímicaDocumento16 páginasTrabalho de QuímicaGustavo de MesquitaAinda não há avaliações
- Diluente 364Documento16 páginasDiluente 364Marcos AntonioAinda não há avaliações
- Amanco Manual Ultratemp CPVC 2013 FINALDocumento0 páginaAmanco Manual Ultratemp CPVC 2013 FINALFabFabFabFabAinda não há avaliações
- Aldeídos e CetonasDocumento8 páginasAldeídos e CetonasJovana MarianoAinda não há avaliações
- Relatorio Sint. AcetonaDocumento9 páginasRelatorio Sint. AcetonaAndre FernandesAinda não há avaliações
- Inventario de Riscos - Nossa EscolaDocumento32 páginasInventario de Riscos - Nossa Escolaricardo costaAinda não há avaliações
- ABNT NBR 13610-1996 - Resinas de PVC - Determinação Do Valor K PDFDocumento8 páginasABNT NBR 13610-1996 - Resinas de PVC - Determinação Do Valor K PDFVanderley SousaAinda não há avaliações
- AcetilenoDocumento14 páginasAcetilenoTHALLESPS5749Ainda não há avaliações