UNIVERSIDADE FEDERAL DE SERGIPE
CENTRO DE CINCIAS EXATAS E TECNOLOGIA
DEPARTAMENTO DE ENGENHARIA QUMICA
LABORATRIO FENMENOS DE TRANSPORTE
ANGELINA MARIA ALVES ARCIERI - 201010009522
DANIEL DE OLIVEIRA VENCESLAU - 201010009478
ROSA DANYELLE LIMA DOS SANTOS - 201120012138
SABRINA ARAJO DE OLIVEIRA - 201120012102
VIVIANA MAURA DOS SANTOS - 201010009946
DETERMINAO DO COEFICIENTE DE
DIFUSO MSSICO (D
AB
)
SO CRISTVO
2014
ANGELINA MARIA ALVES ARCIERI - 201010009522
DANIEL DE OLIVEIRA VENCESLAU - 201010009478
ROSA DANYELLE LIMA DOS SANTOS - 201120012138
SABRINA ARAJO DE OLIVEIRA - 201120012102
VIVIANA MAURA DOS SANTOS - 201010009946
DETERMINAO DO COEFICIENTE DE
DIFUSO MSSICO (D
AB
)
Relatrio solicitado para avaliao
parcial da disciplina de Laboratrio de
Fenmenos de Transporte (EQUI0097) da
turma T01, ministrada pelo Professor
Manoel Marcelo Padro. Para o curso de
Engenharia de Produo.
SO CRISTVO
2014
3
Sumrio
1. Resumo ..................................................................................................................... 4
2. Fundamentao Terica ......................................................................................... 5
2.1. Introduo .................................................................................................................... 5
2.2. Lei de Fick da Difuso ................................................................................................ 5
2.3. Difusividade Mssica................................................................................................... 6
2.4. Clula de Stefan ......................................................................................................... 10
2.5. Correlaes para a Estimativa do Coeficiente de Difuso em Gases Apolares ... 12
2.5.1. Parmetros para Clculos para Mistura Apolar/Apolar ............................ 12
2.5.2. Parmetros para Clculos para Mistura Polar/Apolar .............................. 13
2.5.3. Correlao Chapmann-Enskog ................................................................. 14
2.5.4. Correlao Wilke e Lee ............................................................................ 14
2.5.5. Correlao Fuller et al. ............................................................................. 15
2.6. lcool Etlico .............................................................................................................. 15
3. Objetivos ................................................................................................................ 16
3.1. Objetivo Geral ........................................................................................................... 16
3.2. Objetivo Especfico .................................................................................................... 16
4. Materiais e Mtodos .............................................................................................. 17
4.1. Materiais .................................................................................................................... 17
4.2. Procedimento Experimental ..................................................................................... 17
5. Anlise de Resultados e Discusses ...................................................................... 18
5.1. Clculo da Presso de Vapor .................................................................................... 19
5.2. Correo do Terico ........................................................................................ 20
5.3. Determinao do Experimental ...................................................................... 20
5.3.1. Determinao do Desvio Relativo ............................................................ 20
5.4. Determinao do por Correlaes .................................................................. 21
5.4.1. Parmetros para Clculos para Mistura Apolar/Apolar ............................ 21
5.4.2. Parmetros para Clculos para Mistura Polar/Apolar .............................. 22
5.4.3. Correlao de Chapmann-Enskog ............................................................ 23
5.4.4. Correlao de Wilke e Lee ....................................................................... 24
5.4.5. Correlao de Fuller et al.......................................................................... 25
6. Concluso ............................................................................................................... 27
7. Referncias ............................................................................................................. 28
4
1. Resumo
A transferncia de massa refere-se ao movimento de uma substncia devido ao
gradiente de concentrao. Esse movimento de uma espcie qumica a partir de uma
regio de concentrao elevada em direo a uma regio de menor concentrao ocorre
por difuso.
O coeficiente de difuso (D
AB
) um valor que representa a facilidade com que
cada soluto em particular se move em um solvente determinado. uma proporcionalidade
constante entre o fluxo molar devido a difuso molecular e o gradiente na concentrao
de espcies.
5
2. Fundamentao Terica
2.1. Introduo
A transferncia de massa pode ser compreendida como a transferncia de um
componente especfico, denominado soluto, devido a um gradiente de concentrao
existente. O sentido em que essa transferncia se d anlogo ao da transferncia de calor
(ocorre do meio em que h maior temperatura para o meio de menor temperatura), isto ,
passa do meio mais concentrado para o de menor concentrao. Essa transferncia se d
por meio da difuso molecular, que, segundo Treybal (1968), est relacionada ao
movimento de molculas individuais atravs de uma substncia devido sua energia
trmica.
observada a ocorrncia desse fenmeno tanto em atividades industriais como
absoro, secagem, destilao, entres outros, como em atividades cotidianas como
infuso de um ch, solubilizao do sal em gua, evaporao de gua na superfcie de
uma piscina, etc.
Geankoplis (2006) afirma que os fenmenos de transporte seguem o tipo geral de
equao que escrita na forma: Taxa de Transferncia =
Fora Motriz
Resistncia
, sendo a fora
motriz da transferncia de massa, o gradiente de concentrao.
2.2. Lei de Fick da Difuso
De acordo com engel (2009) a lei de Fick da difuso afirma que a taxa de difuso
de uma espcie qumica em um local, em uma mistura de gases, ou soluo de lquido ou
slido proporcional ao gradiente de concentrao desta espcie nesse local, onde:
Fluxo de Massa = Constante de Proporcionalidade Gradiente de Concentrao
Para a difuso de uma espcie A em uma mistura binria de A e B a taxa de difuso
escrita pelas equaes (1) e (2):
Base Mssica:
J
dif,A
=
m
dif,A
S
= D
AB
d(
)
dz
(
kg
s m
2
)
(1)
Base Molar:
J
dif,A
=
N
dif,A
S
= D
AB
d(
C
A
C
)
dz
(
kmol
s m
2
)
(2)
6
Onde j
dif,A
o fluxo de massa difusivo da espcie A, j
dif,A
o fluxo molar e S a
rea da seo reta.
engel ainda acrescenta que o fluxo mssico de uma espcie em um local proporcional
a densidade da mistura nesse local, sendo que =
A
+
B
, ou seja, a densidade pode
variar na mistura assim como a concentrao C = C
A
+C
B
mas, para os casos onde a
densidade da mistura ou concentrao molar sejam constantes as equaes (1) e (2)
podem ser simplificadas e representadas pelas equaes (3) e (4):
Base Mssica:
J
dif,A
= D
AB
d
A
dz
(
kg
s m
2
)
(3)
Base Molar:
J
dif,A
= D
AB
dC
A
dz
(
kmol
s m
2
)
(4)
Ou simplesmente representa-se a 1 Lei de Fick pela equao (5):
J
A
= D
AB
dc
A
dz
(5)
Essa relao segundo engel apropriada para solues de slidos e lquidos
diludos, porm no o caso onde se tem misturas de gs ou solues de lquidos
concentrados. A literatura contempla vrios mtodos de obteno do D
AB
para misturas
gasosas dentre eles experimento da clula de Stefan e por meio de correlaes empricas.
2.3. Difusividade Mssica
Para anlise da difuso de um vapor atravs de um gs quase estacionrio
caracterstico da clula de Stefan adota-se as seguintes hipteses para clculo da
difusividade mssica ou coeficiente de difuso de A no meio B:
Sistema binrio composto de dois gases considerados ideais;
Regime pseudo-permanente;
Fluxo mssico unidirecional;
7
Meio no-reacional;
Gs B pouco insolvel em A;
Temperatura e presso constantes;
Manipulando-se as hipteses e empregando no balano de massa para o volume
de controle, temos:
|
Taxa molar
de entrada
de A no VC
| +|
Taxa molar
de sada
de A no VC
| |
Taxa molar de
produo/consumo
de A por reao
| = |
Taxa molar
de acmulo
de A no VC
|
Desta forma, para um volume de controle de espessura z da coluna estabelece que
a massa de A que entra no plano z igual massa de A que sai do plano z +z, como
expresso na equao (6):
SN
AZ
|
z
SN
AZ
|
z+z
= 0 (6)
Dividindo ambos os membros da equao por Sz e tomando-se o limite quando
z 0, tem-se a equao (7) que a equao da continuidade para o componente A:
dN
AZ
dz
= 0
(7)
Portanto, conclui-se que o fluxo molar do componente A na direo z constante e
diferente de zero. Assim, a 1 Lei de Fick pode ser escrita conforme a equao (8):
J
A
= cD
AB
z
A
(8)
A partir da anlise da primeira lei de Fick possvel definir o coeficiente de difuso
de um soluto em um meio gasoso, objeto deste experimento, sendo assim:
J
A
= c
A
(v
A
v
) , sendo que, (v
A
v
) a velocidade de difuso.
Sabendo-se que o fluxo de massa de A proporcional ao gradiente de concentrao
do prprio A no local onde se avalia o J
A
, temos que o fluxo molar de A N
A
:
N
A
= J
A
+c
A
v
(9)
8
Onde: N
A
= c
A
v
A
o fluxo de molar de A em relao ao referencial fixo
cv
= N
j
n
j1
(10)
A partir das equaes (8), (9) e (10) a lei de Fick apresentada como:
N
A
= y
A
(N
A
+N
B
) cD
AB
z
A
(11)
Onde a frao molar y
A
=
c
A
c
e y
A
(N
A
+ N
B
) equivale a parcela de A no fluxo de
massa total do fludo e cD
AB
z
A
equivale a parcela de A referente ao gradiente de
concentrao, considerando que o componente B sendo insolvel em A, no caso o
componente B o ar considera-se o fluxo de B(N
B
= 0), simplificando a equao (11)
para:
N
A
(1 y
A
) = cD
AB
dy
A
dz
(12)
Integrando para os limites y
A
[y
A1
, y
A2
] e z [z
1
, z
2
], temos:
N
A,z
dz = cD
AB
1
1 y
A
dy
A
N
A,z
dz
z
2
z
1
= cD
AB
1
1 y
A
dy
A
y
2
y
1
N
A,z
=
cD
AB
z
2
z
1
ln
1 y
A2
1 y
A1
(13)
Que o fluxo molar de A em funo da sua concentrao na fase gasosa e da mistura
gasosa AB. Sabendo-se que:
y
A1
+y
B1
= 1 y
A1
= 1 y
B1
(14)
y
A2
+y
B2
= 1 y
A2
= 1 y
B2
(15)
Assim:
y
A1
+y
A2
y
B2
+y
B1
= 1 (16)
9
A partir da substituio de (14) em (15) e da multiplicao de (16) em (13) obtemos:
N
A,z
=
cD
AB
z
2
z
1
ln (
y
B2
y
B1
) (
y
A1
+y
A2
y
B2
+y
B1
) (17)
No tempo t, z(t) ocupa um volume de lquido no interior da clula igual a V(t).
Para o tempo t +t, temos que z(t +t) ocupa um volume igual a V(t +t). Ao
relacionarmos o fluxo molar com a diminuio do lquido em funo do tempo atravs da
hiptese do regime estacionrio tem-se a seguinte relao:
S [L(t +t) L(t)] = [V(t +t) V(t)], onde S a rea da seo reta da clula,
considerando o limite t 0 obtemos a relao?
S
dL
dt
=
dV
dt
(18)
Substituindo pela densidade do lquido,
A,liq
=
m
V
tem-se:
S
dL
dt
=
1
A,liq
m
dt
(19)
Ao igualarmos as equaes (17) e (19) obtemos:
dL
dt
=
1
A,liq
N
A,z
(20)
Continuando com os ajustes,
A,liq
dL
dt
=
cD
AB
(z
2
z
1
) y
B,lm
(y
A1
y
A2
) (21)
Para y
B,lm
=
y
B1
y
B2
ln(
y
B2
y
B1
)
e z
2
z
1
= L, temos:
A,liq
dL
dt
=
cD
AB
L y
B,lm
(y
A1
y
A2
) (22)
Ao efetuarmos a integrao da equao (16) para t{t
0
, t) e para L{L
0
, L) obtemos:
A,liq
L dL =
cD
AB
y
B,lm
(y
A1
y
A2
)dt (23)
10
dz
L
L
0
=
cD
AB
A,liq
y
B,lm
(y
A1
y
A2
) dt
t
0
(L
g
2
L
g0
2
)
2
=
cD
AB
(y
A1
y
A2
)
A,liq
y
B,lm
(t t
0
) (24)
Agora recorremos a teoria termodinmica do gs ideal e considerando que o vapor
do lquido se comporte como tal, calculamos a concentrao deste pela relao c =
P
RT
onde
A,liq
=
A,
M
A
e obtemos
1
y
B,lm
= ln
y
B2
y
B1
(y
B2
y
B1
)
=
y
A1
ln(
1
1y
A1
)
Relacionando as leis de Dalton onde y
A1
P
A
P
e a lei de Roult onde x
A1
P
A
vap
P
A
obtemos que y
A1
P
A
vap
P
e consequentemente:
y
B,lm
=
y
A1
ln(
1
1
P
A
vap
P
)
ln (
1
1
P
A
vap
P
) =
y
A1
y
B,lm
(25)
Considerando y
A2
0 obtemos a equao para determinar experimentalmente o
coeficiente de difuso:
L
2
L
0
2
=
2cD
AB
(y
A1
y
A2
)t
A
y
B,ml
L
g
2
L
g0
2
=
2D
AB
M
A
P
A
RT
ln (
1
1
P
A
vap
P
)t
(26)
2.4. Clula de Stefan
A clula de Stefan utilizada para a determinao experimental do coeficiente de
difuso em misturas gasosas binrias (compostas por duas substncias A e B), onde um
dos componentes provm da evaporao de uma substncia lquida pura. Para a
simplificao das tarefas experimentais, foram adotadas as seguintes hipteses:
Sistema binrio: composto de suas substncias denotadas por A e B;
11
Sistema no-reacional: as substncias A e B no se decompem e nem reagem;
Uniformidade de algumas propriedades: densidade e coeficiente de difuso (D
AB
);
Fluxo mssico unidirecional: apenas na direo z;
Regime pseudo-permanente (quase-estacionrio): no depende do tempo de
exposio ao processo de transferncia de massa.
A estrutura da clula para o experimento mostrada na Figura 1 - Clula de Stefan.
Figura 1 - Clula de Stefan
Aps a evaporao da substncia A na superfcie, que nesse caso o lcool etlico
(etanol), ela desloca-se com um fluxo constante e diferente de zero na direo x. Sendo a
substncia B o ar, que praticamente insolvel em A e que no se move relativamente
aos eixos fixos, o fluxo de B zero (N
B
= 0). Tendo em vista essas e outras
consideraes sobre o comportamento do sistema da clula de Stefan possvel
determinar uma equao para o clculo do coeficiente de difuso mssico experimental,
sendo a equao (26) do coeficiente de difuso experimental para a clula de Stefan.
Atravs da equao citada, determinado o coeficiente de difuso mssica D
AB
,
atravs dos dados coletados uma presso (P) constante e temperatura dada.
12
Sendo: P e T, presso e temperatura total do sistema, respectivamente, P
Vap
presso
de vapor do lquido A (etanol), R a constante universal dos gases e M
A
o peso molecular
de A.
2.5. Correlaes para a Estimativa do Coeficiente de Difuso em Gases Apolares
Para os clculos do coeficiente de difuso so feitas algumas correlaes onde cada
uma ter em sua formulao o incremento de termos diferentes a serem calculados para
devidas comparaes com valores dados na literatura.
2.5.1. Parmetros para Clculos para Mistura Apolar/Apolar
[Link]. Dimetro de Coliso da Espcie
A
= 1,18
V
b
A
3
(27)
[Link]. Dimetro de Coliso da Mistura
AB
=
A
+
B
2
(28)
[Link]. Energia Mxima de Atrao da Espcie
A
k
= 1,15 T
b
A
(29)
[Link]. Energia Mxima de Atrao da Mistura
AB
k
=
A
k
B
k
(30)
[Link]. Temperatura Reduzida
T
=
T
AB
k
(40)
13
[Link]. Integral de Coliso
D
= (
A
T
B
+
C
exp(DT
)
+
E
exp(FT
)
+
G
exp(HT
)
) (50)
2.5.2. Parmetros para Clculos para Mistura Polar/Apolar
Segundo Cremasco, estimativa a proposta de Brokaw recomendada do coeficiente
de difuso tanto para o par polar/polar quanto para o par polar/apolar.
[Link]. Parmetro de Polaridade
A
=
1,94 10
3
p
i
2
V
b
A
T
b
A
(51)
[Link]. Dimetro de Coliso da Espcie
A
=
1,585 V
b
A
1 +(1,3
A
2
)
3
(52)
[Link]. Dimetro de Coliso da Mistura
AB
=
A
B
(53)
[Link]. Energia Mxima de Atrao da Espcie
A
k
= 1,18 (1 +1,38
A
2
) T
b
A
(54)
[Link]. Energia Mxima de Atrao da Mistura
AB
k
=
A
k
B
k
(55)
[Link]. Temperatura Reduzida
T
=
T
AB
k
(56)
14
[Link]. Integral de Coliso Reduzida
= (
A
T
B
+
C
exp(DT
)
+
E
exp(FT
)
+
G
exp(HT
)
) (57)
[Link]. Integral de Coliso
D
=
D
+(0,196
AB
2
T
) (58)
2.5.3. Correlao Chapmann-Enskog
Essa correlao foi obtida baseando-se em uma rigorosa teoria cintica dos gases,
onde foram obtidos coeficientes de transporte por intermdio da energia potencial.
D
AB
=
b 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
(59)
Para Chapmann-Enskov b = 1,858, logo temos:
D
AB
=
1,858 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
(60)
2.5.4. Correlao Wilke e Lee
A correlao de Wilke e Lee se comparada com a correlao de Chapmann-Enskov,
nota-se que a diferena nas duas est no valor do b, onde para o qual foi proposta a
seguinte expresso:
b = 2,17 (
1
2
1
M
A
+
1
M
B
) (61)
Substituindo (61) em (59), temos:
D
AB
= [2,17 (
1
2
1
M
A
+
1
M
B
)] 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
(62)
15
2.5.5. Correlao Fuller et al.
A correlao de Fuller et al. se baseia na formulao original do coeficiente de
difuso, porem feita uma correo da mesma em termos de temperatura, onde T est em
(K) e P em (atm) e o resultado DAB expresso em (cm
2
/s). Com isso temos:
D
AB
=
1 10
3
T
1,75
1
M
A
+
1
M
B
P d
AB
2
(63)
d
AB
= (v)
A
3
+ (v)
B
3
(64)
Onde: (v)
i
o volume de molar de difuso de Fuller, Schetter e Giddings, que so
tabelados.
2.6. lcool Etlico
O lcool etlico, popularmente conhecido como Etanol se tornou um principal
bicombustvel justamente pela caracterstica de ser uma fonte de energia renovvel.
composto por dois tomos de carbono, cinco de hidrognio e uma hidroxila (C2H5OH),
devido a existncia da hidroxila, OH, tal composto mantem permanncia na classe dos
lcoois e um carter polar, mesmo que sua estrutura possua uma parte apolar. Segundo
PERRY (1999), a difusividade da lcool etlico no ar a 0C e 1 atm de 0,102 cm
2
/s.
O etanol pode ser produzido a partir da cana-de-acar, gros (milho e soja),
beterraba, mandioca, batata, eucalipto, etc.
Dados para o lcool etlico:
R = 8314,472 (cm
3
kPa)/(K mol)
M
A
(C
2
H
6
O)
= 46,069 g/mol
A
(C
2
H
6
O)
= 0,787 g/cm
3
a 25C
(1)
16
3. Objetivos
3.1. Objetivo Geral
O objetivo geral a aplicao de conceitos da Transferncia de massa em
laboratrio, contribuindo com a formao do conhecimento dos alunos ao longo das
etapas do experimento.
3.2. Objetivo Especfico
O objetivo especfico o clculo do coeficiente de difuso do lcool etlico no ar
utilizando-se a clula de Stefan. Alm disso, busca-se comparar o resultado obtido com o
valor terico da literatura, incluindo a comparao com os valores estimados das
correlaes de Fuller et al. e Chapmann-Enskog.
17
4. Materiais e Mtodos
4.1. Materiais
Os seguintes materiais foram utilizados para a execuo do experimento:
Clula de Stefan
Rgua
Termmetro
lcool Etlico
4.2. Procedimento Experimental
Com o uso do lcool etlico, preenche-se o tubo de ensaio que est fixo clula de
Stefan. Assim, possvel medir a diferena de altura entre a coluna de lquido e a de ar,
diferena essa necessria para o clculo do coeficiente de difuso. A etapa seguinte a
medio das variaes das alturas das colunas, sendo tambm registrados o horrio e a
temperatura do ambiente. Considerando a volatilidade do lcool etlico, foram necessrios
quatro dias para a realizao das medies, sendo registrado um total de onze medidas.
18
5. Anlise de Resultados e Discusses
Durante os quatro dias de realizao do experimento foram coletados dados da
altura do etanol e consequentemente calculado o diferena de comprimento de gs ao
quadrado como descritos na Tabela 3 Volumes molares de difuso, abaixo:
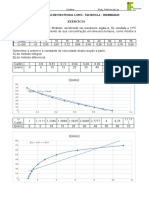
Tabela 1 Dados obtidos experimentalmente
Tempo
(s)
Comp. Lquido
Ll (cm)
Comp. Gs
Lg (cm)
Lg
2
Lg0
2
(cm)
Temperatura
T (C)
0 21,7 7,4 0,0 28,0
19800 21,6 7,5 1,5 28,0
32400 21,6 7,5 1,5 26,5
85500 21,4 7,7 4,5 26,5
107700 21,4 7,8 5,3 24,5
117900 21,3 7,8 6,1 24,5
174000 21,2 7,9 7,7 23,0
192900 21,1 8,0 9,2 22,0
203400 21,1 8,0 9,2 23,0
345000 20,9 8,2 12,5 25,5
369960 20,8 8,3 14,1 23,0
A partir dos dados experimentais construiu-se o grfico da diferena de
comprimento de gs ao quadrado(L
g
2
L
g
0
2
) versus o tempo (t) conforme a Figura 2 -
Grfico da diferena de comprimento ao quadrado (Lg - Lg0) versus Tempo (t):
19
Figura 2 - Grfico da diferena de comprimento ao quadrado (Lg - Lg0) versus Tempo (t)
O grfico apresenta o comportamento esperado, no caso, linear. Por meio dos
ajustes do coeficiente angular pode-se obter a reta da diferena de comprimento de gs
ao quadrado:
L
g
2
L
g
0
2
= 4,07991 10
5
t (65)
Essas equaes e condies de contorno do experimento da Clula de Stefan permitiram
determinar efetivamente o coeficiente de difusividade (D
AB
) experimental, sabendo-se
que P = 101,325 kPa, R = 8314,472 (cm
3
kPa)/(K mol) e que a temperatura
mdia experimental T = 25C = 298,15 K.
5.1. Clculo da Presso de Vapor
Para as condies experimentais necessrio o clculo da presso de vapor por
meio da equao (66) de Antonie com base nos dados Tabela 2 Constantes da equao
de Antoine.
ln P
vap
(mmHg) = A
B
T(C) +C
(66)
20
Tabela 2 Constantes da equao de Antoine
Composto Intervalo (C) A B C
lcool Etlico 19,6 a 93,4 8,1122 1592,864 226,184
Fonte: Felder (2011)
ln P
vap
(mmHg) = A
B
T(C) +C
P
vap
= 10
8,1122
1592,864
25+226,184
= 58,99 mmHg
P
vap
(kPa) = 0,133322 P
vap
(mmHg) = 0,133322 58,99 = 7,865 kPa
5.2. Correo do
Terico
D
AB2
= D
AB1
P
1
P
2
(
T
2
T
1
)
1,75
D
AB2
= 0,102
1
1
(
298,15
273,15
)
1,75
D
AB2
= 0,119 cm
2
/s
5.3. Determinao do
Experimental
D
AB
=
(L
g
2
L
g0
2
) RT
A
2M
A
P ln(
1
1
P
A
vap
P
)
D
AB
=
4,07991 10
5
cm
2
s
8314,472
cm
3
kPa
Kmol
298,15K 0,787
g
cm
3
2 46,069
g
mol
101,325 kPa ln(
1
1
7,865 kPa
101,325 kPa
)
D
AB
= 0,106 cm
2
/s
5.3.1. Determinao do Desvio Relativo
DR =
(exp teo)
teo
100% =
(0,106 0,119)
0,119
100% = 11,25%
21
5.4. Determinao do
por Correlaes
As tabelas 4, 5 e 6 contm os dados utilizados nos clculos da correlaes.
Tabela 3 Volumes molares de difuso
Molculas C H O Ar
()
(/) 16,5 1,98 5,48 20,1
Fonte: Cremasco (2002)
Tabela 4 Propriedade dos gases
Espcie
Frmula
Molecular
Massa
Molecular
(g/gmol)
(K)
(cm/gmol)
(debyes)
()
Etanol (A) C
2
H
6
O 46,069 351,5 60,8 1,7 - -
Ar (B) - 28,85 - - - 3,711 78,6
Fonte: Cremasco (2002)
Tabela 5 Constantes para clculo da integral de coliso
A = 1,06036 C = 0,19300 E = 1,03587 G = 1,76474
B = 0,15610 D = 0,47635 F = 1,52996 H = 3,89411
Fonte: Cremasco (2002)
5.4.1. Parmetros para Clculos para Mistura Apolar/Apolar
[Link]. Dimetro de Coliso da Espcie
A
= 1,18
V
b
A
3
= 1,18 60,8
3
= 4,640
[Link]. Dimetro de Coliso da Mistura
AB
=
A
+
B
2
=
4,640 +3,711
2
= 4,175
22
[Link]. Energia Mxima de Atrao da Espcie
A
k
= 1,15 T
b
A
= 1,15 351,5 = 404,225
[Link]. Energia Mxima de Atrao da Mistura
AB
k
=
A
k
B
k
= 404,225 78,600 = 178,247
[Link]. Temperatura Reduzida
T
=
T
AB
k
=
298,150
178,247
= 1,673
[Link]. Integral de Coliso
D
= (
A
T
B
+
C
exp(DT
)
+
E
exp(FT
)
+
G
exp(HT
)
)
D
= (
1,06036
1,673
0,1561
+
0,19300
exp(0,476351,673)
+
1,03587
exp(1,529961,673)
+
1,76474
exp(3,894111,673)
)
D
= 1,148
5.4.2. Parmetros para Clculos para Mistura Polar/Apolar
[Link]. Parmetro de Polaridade
A
=
1,94 10
3
p
i
2
V
b
A
T
b
A
=
1,94 10
3
1,70
2
60,80 351,50
= 0,262
[Link]. Dimetro de Coliso da Espcie
A
=
1,585 V
b
A
1 +(1,3
A
2
)
3
=
1,585 60,8
1 +(1,3 0,262)
3
= 4,456
[Link]. Dimetro de Coliso da Mistura
AB
=
A
B
= 4,456 3,711 = 4,066
23
[Link]. Energia Mxima de Atrao da Espcie
A
k
= 1,18 (1 +1,38
A
2
) T
b
A
= 1,18 (1 + 1,38 0,262
2
) 351,5
= 454,164
[Link]. Energia Mxima de Atrao da Mistura
AB
k
=
A
k
B
k
= 454,164 78,600 = 188,937
[Link]. Temperatura Reduzida
T
=
T
AB
k
=
298,150
188,937
= 1,578
[Link]. Integral de Coliso Reduzida
= (
A
T
B
+
C
exp(DT
)
+
E
exp(FT
)
+
G
exp(HT
)
)
= (
1,06036
1,578
0,1561
+
0,19300
exp(0,476351,578)
+
1,03587
exp(1,529961,578)
+
1,76474
exp(3,894111,578)
)
= 1,175
[Link]. Integral de Coliso
D
=
D
+(0,196
AB
2
T
) = 1,175 +(0,196
0,262
1,578
) = 1,207
5.4.3. Correlao de Chapmann-Enskog
[Link]. Clculos para Mistura Apolar/Apolar
[Link].1. Determinao do
D
AB
=
b 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
24
D
AB
=
1,858 10
3
298,15
1,5
1
46,069
+
1
28,850
1 4,175
2
1,148
D
AB
= 0,113 cm
2
/s
[Link].2. Determinao do Desvio Relativo
DR =
(cal exp)
exp
100% =
(0,113 0,106)
0,106
100% = 6,60%
[Link]. Clculos para Mistura Polar/Apolar
[Link].1. Determinao do
D
AB
=
b 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
D
AB
=
1,858 10
3
298,15
1,5
1
46,069
+
1
28,850
1 4,066
2
1,207
D
AB
= 0,114 cm
2
/s
[Link].2. Determinao do Desvio Relativo
DR =
(cal exp)
exp
100% =
(0,114 0,106)
0,106
100% = 7,55%
5.4.4. Correlao de Wilke e Lee
[Link]. Clculos para Mistura Apolar/Apolar
[Link].1. Determinao do
D
AB
=
b 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
b = 2,17 (
1
2
1
M
A
+
1
M
B
) = 2,17 (
1
2
1
46,069
+
1
28,850
) = 2,051
25
D
AB
=
2,951 10
3
298,15
1,5
1
46,069
+
1
28,850
1 4,175
2
1,148
D
AB
= 0,125 cm
2
/s
[Link].2. Determinao do Desvio Relativo
DR =
(cal exp)
exp
100% =
(0,125 0,106)
0,106
100% = 17,92%
[Link]. Clculos para Mistura Polar/Apolar
[Link].1. Determinao do
D
AB
=
b 10
3
T
1,5
1
M
A
+
1
M
B
P
AB
2
D
D
AB
=
2,951 10
3
298,15
1,5
1
46,069
+
1
28,850
1 4,066
2
1,207
D
AB
= 0,126 cm
2
/s
[Link].2. Determinao do Desvio Relativo
DR =
(cal exp)
exp
100% =
(0,126 0,106)
0,106
100% = 18,87%
5.4.5. Correlao de Fuller et al.
[Link]. Determinao do
D
AB
=
1 10
3
T
1,75
1
M
A
+
1
M
B
P d
AB
2
d
AB
= V
A
3
+ V
B
3
= 50,36
A
3
+ 28,85
B
3
= 6,412
D
AB
=
1 10
3
298,15
1,75
1
46,069
+
1
28,850
1 6,412
2
26
D
AB
= 0,124 cm
2
/s
[Link]. Determinao do Desvio Relativo
DR =
(cal exp)
exp
100% =
(0,124 0,106)
0,106
100% = 16,98%
Tabela 6 Coeficientes de Difusividade para cada correlao e o desvio relativo
Correlao Polaridade DAB (cm
2
/s) Erro relativo (%)
Terico (Perry) - 0,119 -
Experimental - 0,106 -10,92
Chapman-Enskog
Apolar 0,113 6,60
Polar 0,114 7,55
Wilke & Lee
Apolar 0,125 17,92
Polar 0,126 18,87
Fuller et al. - 0,124 16,98
Percebe-se que todas as correlaes apresentaram um pequeno desvio relativo, por
isso, pode-se dizer que h uma boa relao entre o valor terico e o obtido
experimentalmente.
27
6. Concluso
Deparar-se com o fenmeno de transferncia de massa um fato do cotidiano de
muitas operaes industriais, por isso, utiliza-se o coeficiente de difuso para a avaliar a
taxa dessa transferncia. Dessa forma, experimentalmente objetivou-se a determinao
do coeficiente de difuso D
AB
do vapor proveniente da mistura lcool etlico e ar
aplicados no instrumento denominado por Clula de Stefan.
Na literatura encontra-se o valor de D
AB
= 0,119 cm
2
/s para o coeficiente de
difuso para a mistura lcool etlico e ar em comparao com valor experimental do
coeficiente de difuso obtido D
AB
= 0,106 cm
2
/s , para a temperatura mdia de T =
298,15K, obteve-se um erro relativo de DR = 10,92%.
Avaliou-se os coeficiente de difuso encontrados pelas correlaes empricas
Chapmann-Enskog, Wilke e Lee e Fuller et al. Sabendo que o lcool etlico pode ter
comportamento polar ou apolar, foram feitos os clculos de correlao empricas de
Chapmann-Enskog, Wilke e Lee para ambos os casos. Constatou-se a equao de
Chapmann-Enskog resultou no menor erro relativo de coeficiente de difuso em relao
ao experimental.
Assim, mesmo com simplificaes e adoes de hipteses, o modelo utilizado para
determinao do coeficiente de difusividade mssica do etanol no ar mostrou-se eficiente.
28
7. Referncias
ENGEL, Y. A.. 2009. Transferncia de Calor e Massa: uma abordagem prtica.
3. So Paulo : McGrw-Hill, 2009
CREMASCO, M. A.. Fundamentos de transferncia de massa. 2. ed. rev.
Campinas, SP: UNICAMP, 2002.
FELDER, M. F.; RONALD, W. R.; Princpios Elementares dos Processos
Qumicos; [Reimpr.] Rio de Janiero, 2011.
GEANKOPLIS, C. J.. Transport processes and separation process principles.
[Link]. New Delhi: Prentice Hall, 2006.
PERRY, R. H.; GREEN, D. W. (Ed.) Perrys Chemical Engineers Handbook. New
York: McGraw-Hill, 1999.
TREYBAL, R. E. Mass transfer operations. 2nd. ed. New York: McGraw-Hill, 1968.