0% acharam este documento útil (0 voto)
77 visualizações145 páginasFundamentos de Química Orgânica I
1) O documento apresenta as informações sobre a disciplina de Química Orgânica I ministrada pelo professor Samir Cavalcante na Universidade Castelo Branco no ano de 2018.
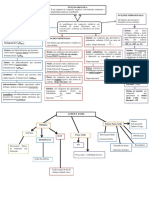
2) São listados os principais tópicos que serão abordados ao longo do curso, incluindo definições de química orgânica, hibridização de carbono, ligação sigma e pi, e nomenclatura de compostos orgânicos.
3) As funções orgânicas principais como hidrocarbonetos, haletos, alcoó
Enviado por
LUCIANEDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato PDF, TXT ou leia on-line no Scribd
0% acharam este documento útil (0 voto)
77 visualizações145 páginasFundamentos de Química Orgânica I
1) O documento apresenta as informações sobre a disciplina de Química Orgânica I ministrada pelo professor Samir Cavalcante na Universidade Castelo Branco no ano de 2018.
2) São listados os principais tópicos que serão abordados ao longo do curso, incluindo definições de química orgânica, hibridização de carbono, ligação sigma e pi, e nomenclatura de compostos orgânicos.
3) As funções orgânicas principais como hidrocarbonetos, haletos, alcoó
Enviado por
LUCIANEDireitos autorais
© © All Rights Reserved
Levamos muito a sério os direitos de conteúdo. Se você suspeita que este conteúdo é seu, reivindique-o aqui.
Formatos disponíveis
Baixe no formato PDF, TXT ou leia on-line no Scribd