Escolar Documentos
Profissional Documentos
Cultura Documentos
Biologi A
Biologi A
Enviado por
tatamluzTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Biologi A
Biologi A
Enviado por
tatamluzDireitos autorais:
Formatos disponíveis
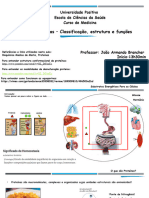
Biologia 1
Proteinas
AMINOÁCIDOS
Monômeros das proteínas com caráter
amina básico.
Desnaturação proteíca
Ác. Carboxílico + Ag. Amina + grupo
Alteração da proteína terciária
radical que varia de aminoácido para
aminoácido Temperatura, ph, contato com outras
substãncias
Ligação peptídica: amina – Gp.
Carboxílico Rompe ligações dissulfeto
Síntese por desidratação Reversível: alisamento temporário do
cabelo (queratina)
As plantas produzem os 20 que existem
Irreversível: cozimento do ovo (albumina)
Naturais: sintetizados pelo corpo
Essenciais: obtidos apenas pela
alimentação Enzimas
Proteínas Biocatalizadores, alta velocidade das
reações químicas, baixa energia de
Simples: formadas apenas por aminoácidos ativação
Conjugadas: contém grupo protéstico, Estrutura terciária proteíca
como o femo da hemoglobina Específica para um substrato só
Mecanismo chave-fechadura
Funções desempenhadas pelas proteínas: Não são consumidos na reação
Estrutural: membrana plasmática, fibras
colágenas, hemoglobina Fatores que não influenciam
Hormonal: insulina (ajuda na glicemia) Temperatura:
Defesa: imunoglobinas (anticorpos) Varia de espécie para espécie. Para os
Contração Muscular: actina e miosina humanos T. ótima: 36 graus celsius,
Coagulação Sanguínea: tromboplastina, temperaturas inferiores ou superiores
protrombina e fibrinogênio podem causar desnaturação
Impermeabilização: queratina Ph ideal:
Enzimática: a maioria das enzimas são O ph varia nas partes do corpo humano
proteínas Ph ótimo para a pepsina: 2
Ph ótimo para a ptialina: 6,8
Estrutura das proteínas: Concentração do substrato:
Primária: simples sequência de Quanto mais [substrato], maior sua chance
aminoácidos de encontro com as enzimas, aumentando
Secundária: os aminoácidos se interagem a eficiência enzimática
(espirais ou zig-zag) formando ligações Proenzimas: Hcl (ativador enzimático)
dissulfato entre seus radicais R Inibidores enzimáticos: íon cianeto
Terciária: forma da proteína como um todo
Quartenária: combinação das terciárias. É
o caso da hemoglobina
Você também pode gostar
- Controle Da RaivaDocumento34 páginasControle Da RaivaAbel Silva100% (1)
- O Fim Da Prospecção Amadora FinalDocumento63 páginasO Fim Da Prospecção Amadora Finalisrael De Souza Soares100% (1)
- Aula 5 - 2 SDocumento24 páginasAula 5 - 2 SPatricia aparecida calisto de oliveiraAinda não há avaliações
- Aula ProteínasDocumento31 páginasAula ProteínasZezinho Henrique100% (1)
- Resumo ProteínasDocumento2 páginasResumo Proteínasproedibio100% (2)
- Fvs 01 Compactação de AterroDocumento1 páginaFvs 01 Compactação de AterroDaiane IzaAinda não há avaliações
- A Metodologia 8 Ps Do Marketing DigitalDocumento2 páginasA Metodologia 8 Ps Do Marketing Digitaltakezo_akiraAinda não há avaliações
- EF11 - Teste - Avaliaçao 1 20 - 21 - EnunciadoDocumento10 páginasEF11 - Teste - Avaliaçao 1 20 - 21 - EnunciadoSara Pereira100% (1)
- EnzimasDocumento45 páginasEnzimasdaviAinda não há avaliações
- Aula 11 Plano de Aula Bioquímica ProteínasDocumento7 páginasAula 11 Plano de Aula Bioquímica ProteínasLorena B100% (1)
- Caderno de BioquímicaDocumento8 páginasCaderno de BioquímicaGIOVANNA ASSONI RODRIGUES SOARESAinda não há avaliações
- Memorial Descritivo Do Mapa de RiscosDocumento4 páginasMemorial Descritivo Do Mapa de RiscosNadine MarinoAinda não há avaliações
- As Proteínas Composição, Estrutura e FunçõesDocumento27 páginasAs Proteínas Composição, Estrutura e FunçõesDayrlaPerairaAinda não há avaliações
- As Proteínas Composição, Estrutura e Funções - 3º AnoDocumento26 páginasAs Proteínas Composição, Estrutura e Funções - 3º AnoIgor CajatyAinda não há avaliações
- Ava Univirtus PDFDocumento4 páginasAva Univirtus PDFDimas Guerreiro100% (2)
- Bioquímica ProteínasDocumento3 páginasBioquímica ProteínasNereida LopesAinda não há avaliações
- Aula4 Enzimas.Documento34 páginasAula4 Enzimas.Adenomar Neves de CarvalhoAinda não há avaliações
- Macro Nutrient EsDocumento26 páginasMacro Nutrient EsVICTORIA'S HAIRAinda não há avaliações
- Aminoácidos, Proteínas e EnzimasDocumento1 páginaAminoácidos, Proteínas e EnzimasCarolina Viana LimaAinda não há avaliações
- ProteínasDocumento3 páginasProteínasaku anitterAinda não há avaliações
- Cap 05 - Proteínas - 9º AnoDocumento11 páginasCap 05 - Proteínas - 9º Anoemily camposAinda não há avaliações
- Proteínas e Ácidos NucleicosDocumento3 páginasProteínas e Ácidos NucleicosLara MaricatoAinda não há avaliações
- Aula 8 - Aminoácidos e Proteà - Nas D PDFDocumento34 páginasAula 8 - Aminoácidos e Proteà - Nas D PDFJuliana EvelinAinda não há avaliações
- Proteínas 2023Documento40 páginasProteínas 2023NeidelayAinda não há avaliações
- Aminoacidos e Proteinas. Generalidades Isptec 2018Documento42 páginasAminoacidos e Proteinas. Generalidades Isptec 2018Gime PitraAinda não há avaliações
- Aula 3 Estrutura e Funções de Proteínas2Documento56 páginasAula 3 Estrutura e Funções de Proteínas2api-19738190100% (1)
- Aminoacidos e Proteinas Resumo GabyDocumento3 páginasAminoacidos e Proteinas Resumo GabyLeticia ComunelloAinda não há avaliações
- Biovisão - Revisão AD (Caps. 3, 4 e 5)Documento20 páginasBiovisão - Revisão AD (Caps. 3, 4 e 5)enzoscarmoAinda não há avaliações
- BioquimicaDocumento6 páginasBioquimicaLara Beatriz MoraisAinda não há avaliações
- Proteínas e Enzimas - 1C - 8° CicloDocumento20 páginasProteínas e Enzimas - 1C - 8° CicloEdson Pereira de LimaAinda não há avaliações
- ResoluçõesDocumento9 páginasResoluçõesVinícius FariasAinda não há avaliações
- Enzimas e Cinética EnzimáticaDocumento84 páginasEnzimas e Cinética EnzimáticaHenriqueAinda não há avaliações
- Aula de ProteínasDocumento22 páginasAula de ProteínasMarcos Marzano100% (1)
- ProteínasDocumento3 páginasProteínasMyllena CoelhoAinda não há avaliações
- ProteínasDocumento3 páginasProteínasrhuanna csAinda não há avaliações
- Aula2 - Aminoácidos, Peptídeos e ProteínasDocumento32 páginasAula2 - Aminoácidos, Peptídeos e ProteínasAnderson CostaAinda não há avaliações
- Aula ProteínasDocumento30 páginasAula ProteínasAgência OxygenAinda não há avaliações
- 2022 Proteínas MEDDocumento21 páginas2022 Proteínas MEDRafaella AranhaAinda não há avaliações
- Aula 10 Aminoacidos Proteinas Estrutura MetabolismoDocumento52 páginasAula 10 Aminoacidos Proteinas Estrutura Metabolismogiovanaao88Ainda não há avaliações
- 3 Serie PROTEINASDocumento19 páginas3 Serie PROTEINASDrielly MoraisAinda não há avaliações
- Proteinas - Insulina HormoniosDocumento14 páginasProteinas - Insulina Hormoniosthany souzaAinda não há avaliações
- ProteínasDocumento1 páginaProteínasLeonardo MirandaAinda não há avaliações
- AULA 4 Proteínas FundamentosDocumento63 páginasAULA 4 Proteínas FundamentosJairelda Sousa RodriguesAinda não há avaliações
- ProteínasDocumento10 páginasProteínasisabela.castro825Ainda não há avaliações
- ProteinaDocumento13 páginasProteinaAnderson pantolfi moraes100% (1)
- En ZimasDocumento53 páginasEn ZimasLuma Gabrielli Gomes NunesAinda não há avaliações
- Producao de ProteinasDocumento29 páginasProducao de ProteinasDavi AbrantesAinda não há avaliações
- Aula - Proteínas - e - Enzimas - 2024Documento38 páginasAula - Proteínas - e - Enzimas - 2024David Aragão de SousaAinda não há avaliações
- Semana 6.0 PDFDocumento11 páginasSemana 6.0 PDFBerga PlaysAinda não há avaliações
- Bactérias MetabolismoDocumento3 páginasBactérias MetabolismoMarlon MaiaAinda não há avaliações
- Semienem-Biologia1-Proteínas, Ácidos Nucleicos e Vitaminas-25-05-2020Documento8 páginasSemienem-Biologia1-Proteínas, Ácidos Nucleicos e Vitaminas-25-05-2020Ana Luíza RibeiroAinda não há avaliações
- Resumo BioquímicaDocumento3 páginasResumo BioquímicaguingiAinda não há avaliações
- As Proteínas Composição, Estrutura e FunçõesDocumento28 páginasAs Proteínas Composição, Estrutura e FunçõesJosé Wilson RibasAinda não há avaliações
- PROTEÍNASDocumento32 páginasPROTEÍNASMatheus Bellini FiorinAinda não há avaliações
- Trabalho BioquimicaDocumento2 páginasTrabalho BioquimicaizidroAinda não há avaliações
- Metabolismo ProteínasDocumento61 páginasMetabolismo Proteínasiara.cavalcanteAinda não há avaliações
- AULA 3 - Aminoácidos e ProteínasDocumento63 páginasAULA 3 - Aminoácidos e ProteínasMateus LealAinda não há avaliações
- Aminoácidos 1Documento16 páginasAminoácidos 1Renan OliveiraAinda não há avaliações
- Digestão, Absorção e Transporte Das ProteínasDocumento33 páginasDigestão, Absorção e Transporte Das ProteínasAndréa Moura100% (1)
- 04 ProteinasDocumento5 páginas04 ProteinasSamuelSamuelAinda não há avaliações
- Proteinas e EnzimasDocumento20 páginasProteinas e EnzimasJoão MinervinoAinda não há avaliações
- Aula 3 (EM1) - Módulo 3 - Proteínas, Ácidos Nucleicos e VitaminasDocumento22 páginasAula 3 (EM1) - Módulo 3 - Proteínas, Ácidos Nucleicos e Vitaminaslucasrdantas788Ainda não há avaliações
- Proteínas TrabalhoDocumento22 páginasProteínas TrabalhoManu de Andrade Di palmaAinda não há avaliações
- Enzimas - Conceito, Função e RegulaçãoDocumento5 páginasEnzimas - Conceito, Função e RegulaçãoAna Carolina FernandesAinda não há avaliações
- A Teologia Do Ger No Antigo Testamento - Doaldo BelémDocumento201 páginasA Teologia Do Ger No Antigo Testamento - Doaldo BelémDiego SerraAinda não há avaliações
- Casos Praticos Simples NacionalDocumento69 páginasCasos Praticos Simples NacionalAntonio QuirinoAinda não há avaliações
- Guia de Boas Práticas de TIC - v1Documento31 páginasGuia de Boas Práticas de TIC - v1Sidney LuzAinda não há avaliações
- Introducao Ao Estudo Dos TimerDocumento17 páginasIntroducao Ao Estudo Dos TimerThiago MeirelesAinda não há avaliações
- Psicologia de DesenvolvimentoDocumento12 páginasPsicologia de DesenvolvimentoZeca NoaAinda não há avaliações
- ORTOPEDIADocumento6 páginasORTOPEDIALarissa WelterAinda não há avaliações
- MatematicaDocumento14 páginasMatematicaTainá OliveiraAinda não há avaliações
- Centro de Atenção Psicossocial InfantilDocumento31 páginasCentro de Atenção Psicossocial InfantillegobaAinda não há avaliações
- Guia TP - Artigos, Preposições e ContraçõesDocumento3 páginasGuia TP - Artigos, Preposições e ContraçõesB.RAinda não há avaliações
- ANEXO 1 Manual SR 3 EIXOSDocumento35 páginasANEXO 1 Manual SR 3 EIXOSCaroline RochaAinda não há avaliações
- Termos Da OraçãoDocumento6 páginasTermos Da OraçãoCarlos HenriqueAinda não há avaliações
- Caixa Termoplástica CESAN HIDRÔMETRODocumento4 páginasCaixa Termoplástica CESAN HIDRÔMETRORodrigo FonsecaAinda não há avaliações
- Anamnese - Amp - Amf TXT PucDocumento15 páginasAnamnese - Amp - Amf TXT PucdrpropeAinda não há avaliações
- Dissertação Final - RosárioDocumento180 páginasDissertação Final - RosárioHeltonMoraesAinda não há avaliações
- Advpl IDocumento78 páginasAdvpl IFábio Ribeiro Magalhães100% (1)
- Apostila Processo de SaúdeDocumento102 páginasApostila Processo de SaúdeRaphaela SantosAinda não há avaliações
- Analise de Confiabilidade em Selos Mecanicos de Bombas CentrífugasDocumento10 páginasAnalise de Confiabilidade em Selos Mecanicos de Bombas CentrífugasCesar SampaioAinda não há avaliações
- Noções de Geografia - CACDDocumento23 páginasNoções de Geografia - CACDTalysson KelvenAinda não há avaliações
- Antisol Pav - Msds-397-01Documento9 páginasAntisol Pav - Msds-397-01Klarc CamachoAinda não há avaliações
- O Jus Postulandi e o Acesso A Justiça No Processo Do TrabalhoDocumento30 páginasO Jus Postulandi e o Acesso A Justiça No Processo Do TrabalhoedimargsAinda não há avaliações
- Zotero - TutorialDocumento4 páginasZotero - TutorialnataliacnAinda não há avaliações
- Tutoriais Passo A Passo App Banrisul DigitalDocumento19 páginasTutoriais Passo A Passo App Banrisul DigitalcrislaineschepaAinda não há avaliações