Escolar Documentos
Profissional Documentos
Cultura Documentos
06 Renal
Enviado por
juliareis23070 notas0% acharam este documento útil (0 voto)
3 visualizações6 páginasestudo sistema renal
Título original
06.Renal
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoestudo sistema renal
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
3 visualizações6 páginas06 Renal
Enviado por
juliareis2307estudo sistema renal
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 6
6.
FUNÇÃO RENAL
6.1 Anatomia e Fisiologia renal
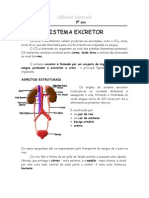
O sistema urinário é formado anatomicamente por quatro componentes
principais: (1) os rins, onde a urina é formada a partir da filtração do sangue, reabsorção
(reciclagem) de substâncias essenciais, incluindo a água, e secreção tubular de
substâncias que não foram filtradas; (2) os ureteres que conduzem a urina dos rins até a
bexiga; (3) a bexiga que armazena a urina produzida e (4) a uretra que conduz a urina
para excreção.
Os rins são órgãos pares localizados na região dorsolombar e são responsáveis
pela manutenção da homeostase, da composição dos líquidos corporais, osmolalidade e
volume do liquido extracelular e também controlam o equilíbrio ácido-base, excreção
de produtos finais do metabolismo e regulação da composição de eletrólitos e outros
solutos no plasma. Adicionalmente, os rins também têm funções endócrinas, como na
produção de eritropoetina e da forma ativa da vitamina D, e da manutenção da pressão
sanguínea pelo eixo renina-angiotensina-aldosterona.
O rim é um órgão em formato de feijão e sua borda medial contém uma
indentação, chamada hilo, a partir do qual a artéria renal chega ao rim e a veia renal e o
ureter deixam o rim. Cada rim é encoberto por uma cápsula formada por tecido
conjuntivo e encimado pela glândula endócrina adrenal. A estrutura interna do rim
consiste em três regiões: córtex, medula e pelve renal. O córtex, mais externo, está
localizado logo abaixo da cápsula; regiões do córtex, chamadas colunas renais se
estendem até a medula, região mais interna. Também no interior da medula, encontram-
se as pirâmides renais, triangulares, cujas pontas projetam-se para os cálices, formando
a pelve que consiste numa expansão do ureter.
Microscopicamente, o néfron é a unidade funcional renal, cada rim possui
cerca de um milhão de néfrons. Cada néfron é composto por um glomérulo e uma rede
de túbulos localizados no córtex e na medula.
Os rins recebem cerca de 25% do sangue que é bombeado pelo ventrículo
esquerdo via artérias renais. No interior do rim, a artéria renal se ramifica em ramos
cada vez menores, chamados arteríolas aferentes que se enovelam formando os
glomérulos (também chamados corpúsculos renais), que consistem em uma rede
capilares enovelados, formando tufos arteriolares de epitélio fenestrado recobertos por
uma cápsula de Bowmann composta por epitélio escamoso. A camada interna (visceral)
da cápsula é composta por podócitos, que são células especializadas que possuem
processos de extensão que formam fendas de filtração.
Nesse contexto, o líquido que extravasa para o espaço de Bowmann é chamado
de ultrafiltrado, o qual passará por processos de reabsorção e secreção dentro dos
túbulos renais, formado, ao final, a urina. O sangue filtrado rico em células e moléculas
não filtradas sai do glomérulo pela arteríola eferente e alcança uma rede de capilares
secundária denominada capilares peritubulares, que envolve também os túbulos.
Os túbulos renais consistem em uma extensão da cápsula de Bowmann. Os
túbulos renais subdividem-se em túbulo contorcido proximal, alça de Henle e túbulo
contorcido distal. Cada néfron desemboca em um ducto coletor ao qual outros néfrons
estão conectados. A urina é então coletada na pelve renal e desemboca no ureter.
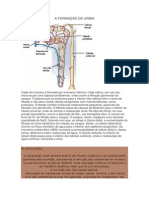
6.2. Formação da urina
Os principais componentes da urina normal são água, ureia, ácido úrico,
creatinina, sódio, potássio, cloreto, cálcio, magnésio, fosfatos, sulfatos e amônia. Em 24
horas o corpo excreta 60g de materiais dissolvidos, cuja metade corresponde à uréia. A
urina também pode ter estruturas como cilindros, cristais, células sanguíneas e células
epiteliais.
O sangue transportado pela arteríola aferente chega até os glomérulos onde é
filtrado por pressão hidrostática. A estrutura dos capilares fenestrados glomerulares,
bem como sua carga negativa não permite a filtração de substâncias com carga negativa
e/ou com alto peso molecular. Assim, o conteúdo filtrado pelos glomérulos, conhecido
como ultrafiltrado, possui a mesma composição do plasma sanguíneo, exceto por
proteínas e outras moléculas de maior peso molecular que excedam 15 kDa. A taxa de
filtração glomerular é proporcional ao tamanho do corpo e varia de acordo com a idade
e com o sexo. A estimativa taxa de filtração glomerular é um indicador importante da
função renal, usada para monitorar a progressão de algumas doenças.
Nos túbulos, a concentração de solutos no ultrafiltrado é alterada por processos
de reabsorção e secreção. A medida que o ultrafiltrado sai do espaço de Bowmann e vai
para o túbulo contorcido proximal, uma grande quantidade de água, cloreto de sódio,
bicarbonato, potássio, cálcio, aminoácidos, fosfato, proteínas de baixo peso molecular,
glicose e outras substâncias são reabsorvidas em proporções variadas e retornam para a
corrente sanguínea por transporte ativo ou passivo.
Mais de 80% do ultrafiltrado é reabsorvido nos túbulos proximais, pois as
células apresentam borda em escova com microvilosidades, aumentando a superfície de
contato para reabsorção e secreção. Nos túbulos proximais, os íons hidrogênio são
trocados pelo sódio do bicarbonato de sódio. Hidrogênio e bicarbonato se combinam,
formando ácido carbônico, o qual, pela ação da enzima anidrase carbônica, é clivado em
CO2 e água. O CO2 se difunde em direção ao interstício e, portanto, tanto sódio quanto
bicarbonato são reabsorvidos.
Após o túbulo proximal, temos a alça de Henle onde acontece a reabsorção por
multiplicação em contracorrente. O ramo descendente da alça é bastante permeável à
água. O ramo ascendente, por sua vez, é praticamente impermeável à água, porém há a
reabsorção ativa de sódio, cloreto, cálcio e magnésio, fazendo com que o fluido que
deixa a alça de Henle tenha osmolaridade menor que a do plasma. Esse processo é
importante para a manutenção do interstício medular hipertônico, favorecendo a
reabsorção de água a nível de ramo descendente e pelo ducto coletor.
Nos túbulos distais e ductos coletores acontece a reabsorção substancial de
água, mediada principalmente pelo hormônio antidiurético. Nos túbulos distais,
acontece também a secreção ativa de ânions orgânicos, potássio e íons hidrogênio, bem
como a reabsorção de bicarbonato, permitindo a manutenção do equilíbrio ácido-base.
O processo de secreção tubular acontece quando substâncias não previamente
filtradas são adicionadas na luz tubular por transporte ativo. Sulfatos, glicuronídeos,
hipuratos, hidrogênio e fármacos, como a penicilina, são exemplos de substâncias
secretadas no túbulo proximal. A secreção tubular (1) remove produtos finais exógenos
indesejáveis, como medicamentos e toxinas e (2) promove a secreção do íon hidrogênio
e outros íons, auxiliando no equilíbrio ácido-base e hidroeletrolítico.
Cada néfron produz aproximadamente 100 uL de ultrafiltrado por dia. Dos 120
ml/min filtrados nos glomérulos, apenas cerca de 1 ml/min é excretado na forma de
urina. No adulto, o volume diário normal de urina é de 600 a 2000 ml/dia. O termo
poliúria é usado para definir o aumento anormal da urina (>2500 ml/24h), como
observado no diabetes mellitus e insípido; oligúria representa uma redução do volume
urinário (<500 mL/24h), como ocorre no choque e na nefrite aguda; e o termo anúria
refere-se à completa ausência da formação de urina, embora seja sugerido com <100
mL/24h durante 2 a 3 dias consecutivos.
6.3. Funções endócrinas do rim
Os rins podem possuir ação endócrina primária, produzindo hormônios, ou
secundária, funcionando como alvo de hormônios produzidos em outro local. Em sua
função endócrina, os rins produzem eritropoetina, prostaglandinas e tromboxanas,
renina e 1,25(OH)vitamina D.
A eritropoetina age nas células da medula óssea estimulando a eritropoese, ou
seja, a produção e amadurecimento de células vermelhas (eritrócitos). A produção de
eritropoetina é mediada pela redução da pO2 detectada pelos rins.
As prostaglandinas e tromboxanas são sintetizadas nos rins pelas enzimas
ciclooxigenases, usando o ácido araquidônico como substrato. Esses compostos,
principalmente PGI2 e PGE2 possuem um papel importante na regulação de processos
biológicos, na contratilidade da vasculatura renal, no tônus mesangial e no
processamento tubular de água e sal.
Os rins exercem papel importante na regulação da PA, não só através da
filtração sanguínea e regulação da volemia, mas também a partir de sua função
endócrina. No córtex renal, as células da arteríola aferente estabelecem contato com as
células da mácula densa do túbulo distal no mesmo néfron, formando o aparato
justaglomerular, mantendo a pressão sanguínea numa taxa relativamente constante. As
células justaglomerulares contém renina, enzima que converte angiotensinogênio em
angiotensina I que, por ação da ECA é convertida em angiotensina II, promovendo
vasoconstrição sistêmica, estímulo da reabsorção de sódio no túbulo contorcido
proximal e desencadeamento da liberação de aldosterona pelas glândulas adrenais e do
hormônio antidiurético (ou vasopressina) pela adenohipófise.
Os rins são responsáveis pela produção da forma ativa da vitamina D. A
vitamina D é um hormônio regulador do metabolismo do cálcio. Esta é sintetizada na
pele por ação da radiação UV sobre a molécula do 7-desidrocolesterol. No fígado, a
vitamina D sofre uma hidroxilação na posição 25, gerando sua principal forma de
armazenamento. O metabólito ativo, 1,25-diidroxi-vitamina D, o calcitriol, é formado
por hidroxilação principalmente por enzimas presentes nos túbulos renais, por estímulo
do PTH.
6.4. Marcadores de função renal
a) Taxa de filtração glomerular (TFG)
A TFG é considerada uma medida segura da capacidade funcional dos rins e
funciona como uma estimativa do número de néfrons funcionantes. A formação do
filtrado glomerular depende de forças hidrostáticas e oncóticas ao longo da arteríola
aferente e no próprio glomérulo a fim de impulsionar a passagem dos ultrafiltrado pelos
túbulos. Na ausência do equilíbrio entre essas forças, os lumens dos túbulos entrarão em
colapso.
Diversas técnicas são usadas para estimar a TFG em doença estabelecida a fim
de objetivar o tratamento, monitorar a progressão e prever a terapia de reposição
(hemodiálise). As mensurações de TFG podem ser determinadas pela depuração, ou
clearance, de determinada substância. O clearance renal de uma substância pode ser
definido como “o volume de plasma do qual a substância é completamente eliminada
dos rins por unidade de tempo” desde que a substância esteja em concentração estável
no plasma, fisiologicamente inerte, livremente filtrada nos glomérulos, não seja
excretada, reabsorvida, sintetizada ou metabolizada pelo rim. Logo, a totalidade da
substância presente no plasma é totalmente excretada na urina, então:
Ps GFR = Us V à GFR = (Us V)/Ps
Vários marcadores exógenos e endógenos são usados para estimar o clearance,
o qual requer medidas precisas do marcador em amostras plasmáticas e urinárias. Para
isso, recomenda-se a coleta de urina de 24 horas, pois a excreção dos marcadores pode
apresentar flutuações. Dentre os marcadores exógenos da TFG destaca-se o clearance de
inulina, além do uso de radiofármacos. A inulina é um polímero de frutose que satisfaz
os critérios de um bom biomarcador. A infusão constante de inulina é realizada no
paciente e este teste é considerado padrão ouro. Esta abordagem possui como
desvantagens o fato de ser invasiva e as metodologias analíticas laboratoriais não são
simples.
Na prática clínica o clearance de cretinina é o marcador da TFG mais
amplamente utilizado. A creatinina é um composto endógeno gerado a partir da
degradação da creatina proveniente do metabolismo muscular e é livremente filtrada nos
glomérulos e produzida a uma taxa relativamente constante. No entanto, a creatinina
sofre influência de fatores como sexo, idade, etnia, massa muscular, uso de fármacos e
consumo de carne, ainda assim existe uma pequena proporção que sofre secreção e
reabsorção tubular.
Contudo, a determinação da creatinina plasmática é de grande valia, visando
avaliar que, sua acumulação na circulação consiste provavelmente em disfunções na
filtração glomerular. Além disso, como a produção de creatinina é proporcional à
atividade muscular, sugere-se correção dos valores com relação à área de superfície
corporal.
Visando a realização de testes de estimativa da TFG se faz necessária, muitas
vezes, a coleta de urina de 24 horas, fator que pode agregar um erro aos resultados
quando esta coleta não é realizada de forma adequada ou quando não for possível.
Assim, existem mais de 25 fórmulas matemáticas que visam estimar a TFG com base
nas dosagens de creatinina plasmática, buscando corrigir os fatores interferentes. Dentre
as principais, destacam-se a estimava de Cockcroft-Gault e a MDRD (Modification of
Diet in Renal Disease).
Segundo Cockcroft-Gault, a TFG é estimada pela fórmula:
Esta estimativa reduz a influência da diferença de massa muscular associada a
sexo e idade. Entretanto, tende a superestimar os valores de TFG, por não considerar
variações na massa muscular causadas por estados patológicos ou eliminação extra renal
e secreção tubular.
Já a fórmula padronizada pelo estudo MDRD é:
Existindo variações simplificadas desta. Em comparação com a fórmula de
Cockcroft-Gault esta fórmula não considera a área de superfície corporal.
Muitas proteínas com baixo peso molecular são filtradas nos glomérulos, como
as alfa1 e alfa2microglobulina e a cistatina C. A cistatina C é uma proteína sintetizada
em todas as células nucleadas a uma taxa constante e tem função inibidora da protease,
é completamente filtrada no glomérulo e metabolizada nos túbulos, possuindo pouca
interferência extrarrenal nas suas concentrações. A dosagem sérica tem sido descrita
com um bom marcador para a estimativa da TFG, no entanto, possui limitações como a
variação da produção em estados patológicos/inflamatórios e as metodologias analíticas
são mais complexas e mais caras.
Outro marcador referente à taxa de filtração glomerular é a ureia plasmática. A
uréia é um composto orgânico resultante do catabolismo de grupamento amino de
aminoácidos e proteínas que é transformado em amônia e é detoxificado em ureia a
partir da reação da amônia com a ornitina no ciclo da ureia. A ureia é eliminada
predominantemente pelos rins através de filtração glomerular. Entretanto,
aproximadamente metade da ureia filtrada é reabsorvida, além de esta sofrer influência
da dieta, hemorragia gastrintestinal, catabolismo proteico e desidratação.
O aumento da excreção urinaria de proteínas (proteinúria) pode ser glomerular,
de excesso e tubular. O acumulo de proteínas no lúmen tubular pode causar lesão
intersticial. A proteinúria acima de 300 mg/dia é patológica. A presença de proteínas de
alto peso molecular na urina pode indicar um dano na barreira de filtração glomerular,
supondo que proteínas plasmáticas estão chegando até os túbulos, dentre essas
proteínas, a principal é a albumina.
A albumina é uma proteína globular, pesando cerca de 66 kDa, sendo a mais
abundante no plasma sanguíneo. Produzida no fígado, esta é eliminada através de
fagocitose em diversos tecidos, não estando presente na urina. Condições de
microalbuminúria (30 a 300 mg/dia na urina) ou proteinúria maciça (>300 mg/dia na
urina) podem indicar instalação de lesão glomerular, como a que acontece na nefropatia
diabética.
b) Reabsorção tubular
A avaliação da reabsorção tubular é feita a partir de alguns testes como a
medida da osmolaridade urinária, a dosagem da glicose urinaria (glicosúria) e dosagem
de eletrólitos eliminados na urina.
A osmolaridade de uma solução pode ser definida como a medida da
quantidade de solutos presentes em um determinado volume de solução. Assim, é usado
para avaliar a capacidade renal de concentração urinária. Alterações na reabsorção de
água ou eletrólitos, por exemplo, pode gerar uma urina diluída ou hipertônica.
A avaliação da capacidade dos túbulos renais em reabsorver a glicose presente
no ultrafiltrado configura a glicosúria. Existem substâncias de transporte máximo, que
são completamente removidas do ultrafiltrado quando estão em concentrações
adequadas na corrente sanguínea, como é o caso da glicose. Em geral, não há glicose na
urina até que as concentrações plasmáticas excedam de 160 a 180 mg/dL, o que
ultrapassa o limiar de reabsorção da glicose pelos túbulos. Portanto, glicosúria pode
indicar um excesso de glicose plasmática ou um dano tubular que impeça a sua
reabsorção, o uso da glicosúria como marcado renal tem uma limitação em pacientes
diabéticos.
Os túbulos renais, bem como a alça de Henle, possuem uma ampla capacidade
de reabsorver eletrólitos essenciais para a homeostase, como o sódio, potássio, cálcio e
magnésio. Existem estratégias das células tubulares para manter um equilíbrio
eletrolítico, como as trocas ne Na+/K+ e K+/H+, correlacionando o equilíbrio
hidroeletrolítico também com o ácido-base. Disfunções tubulares de reabsorção
refletem em alterações na composição de eletrólitos na urina, como a osteopenia por
perda de cálcio na insuficiência renal crônica e a acidose tubular renal causada por
alteração na reabsorção de bicarbonato.
c) Secreção tubular
Diversos compostos são secretados na urina, principalmente aqueles que por
conta de sua forma, cargas ou tamanho não passaram pela barreira de filtração
glomerular. Uma dessas substâncias é o ácido úrico, o qual é secretado pela bomba
secretora de ácidos orgânicos presente nas células tubulares proximais. O ácido úrico é
o produto final do catabolismo de nucleosídeos purínicos (adenosina e guanosina).
Alterações na secreção tubular podem levar ao seu acúmulo na corrente sanguínea,
condição esta que em mamíferos pode ser manifestada como uma doença chamada gota.
O aumento do ácido úrico na corrente sanguínea, condição chamada de hipeuricemia,
pode ser idiopática, ou causada por quimioterapia, distúrbios metabólicos herdados,
álcool, psoríase e hipóxia tecidual.
6.5. Abordagem laboratorial
a) Dosagem de creatinina: A dosagem de creatinina é feita preferencialmente
em amostras de soro. Existem metodologias analíticas baseadas em métodos químicos e
enzimáticos.
O método químico utiliza a reação de Jaffe (picrato alcalino) no qual a
creatinina reage com o íon picrato em meio alcalino gerando produto laranja-
avermelhado o qual é avaliado espectrofotometricamente (500 nm). Este método pode
apresentar baixa especificidade, possuindo como interferentes o ácido ascórbico, corpos
cetônicos e altas concentrações de proteínas. A bilirrubina é um interferente negativo,
no entanto, em alguns kits comerciais é adicionado o ferricianeto, o qual oxida a
bilirrubina em biliverdina, a qual não interfere na leitura da reação.
Os métodos enzimáticos para dosagem de creatinina consistem em métodos
com múltiplas reações, as quais, são avaliadas, normalmente pela formação de um
produto por espectrofotometria. Dois métodos de química seca utilizados são o que
usam as enzimas creatininase e creatinina desaminase. Esses métodos são cinéticos que
avaliam a transformação de substrato por unidade de tempo.
b) Dosagem de ureia: A análise pode ser realizada por métodos químicos
utilizando cromógenos ou por métodos enzimáticos. O método enzimático mais
amplamente difundido é o método que utiliza a urease, enzima que cliva a ureia em
amônio. Uma reação acoplada catalisada pela glutamato desidrogenasse consome o
NH4+ e as concentrações da coenzima NADH são acompanhadas por absorção UV a
340 nm.
NH4+ + 2oxoglutarato (glutamato desidrogenase) à Glutamato + H2O
c) Dosagem de ácido úrico: A análise comumente é feita usando o ácido
fosfotúngstico que em reação com o ácido úrico forma um cromógeno azul. Outro
método utiliza a enzima uricase, o qual analisa a utilização de ácido úrico para formação
de alantoína. Segundo a reação:
Urato + O2 (Uricase) à Alantoína + H2O2 + CO2
Técnicas de HPLC também são descritas para identificação e quantificação de
ácido úrico em amostras biológicas.
d) Dosagem de proteínas: Proteinúria pode ser identificada e quantificada
através da precipitação com ácido sulfossalicílico e analise por turbidimetria.
Proteinemia e albuminemia – Biureto e Verde de Bromocresol.
e) Uranálise: Esta é uma ferramenta válida e prática, bastante utilizada em
laboratórios clínicos para análise da composição urinária. A partir da uranálise é
possível determinar características e alterações físicas (densidade, cor, aspecto),
químicas (pH, proteínas, cetonas, bilirrubina, urobilinogênio, esterase leucocitária,
nitrito, hemoglobina, glicose) e microscópicas (presença de bactérias, fungos, hemácias,
leucócitos, parasitas) em amostras urinárias.
6.6 Doenças renais
a) Lesão renal aguda: Diminuição abrupta do ritmo de filtração pelos rins,
determinando aumento no sangue de uréia e creatinina e resultando na incapacidade do
rim em regular homeostase de fluidos, eletrólitos e equilíbrio ácido-básico. A perda
súbita da função renal pode resultar de inadequada perfusão renal associada a
diminuição na circulação sanguínea efetiva (IRA pré-renal) como acontece em estados
de hipovolemia e desidratação; lesão celular renal por insulto isquêmico, tóxico,
imunológico ou infeccioso (IRA renal), como as que acontecem na hepatite tóxica e
infecciosa e obstrução do fluxo urinário (IRA pós-renal) causada, por exemplo, por
cálculos ou tumores. O tratamento da doença de base é a estratégia utilizada para
prevenir a evolução para a doença renal crônica.
b) Doença renal crônica: é definida como uma lesão no rim ou redução
permanente e progressiva da taxa de filtração glomerular, da função tubular e endócrina.
A taxa de progressão da doença depende de fatores como idade, raça, sexo, tabagismo,
nível de proteinúria, pressão sanguínea. Hipertensão arterial sistêmica e Diabetes
mellitus são as duas principais causas.
c) Síndrome urêmica: é considerada a manifestação clínica final da
insuficiência renal e resulta da insuficiência dos rins para manter as funções excretora,
reguladora e endócrina. Os sinais e sintomas incluem fraqueza, tontura, náuseas e
vômitos, perda muscular e acidose metabólica. Os achados laboratoriais clássicos
incluem aumento das concentrações plasmáticas de compostos nitrogenados como a
ureia e a creatinina resultantes da TFG diminuída.
d) Síndrome nefrítica: Geralmente é causada por processo proliferativo
consequente de glomerulonefrite, seja autoimune ou infecciosa, causando manifestação
da inflamação glomerular. De início rápido, apresenta hematúria, proteinúria, TFG
reduzida, retenção de sódio e água causando edema e oligúria. Pode ser aguda ou
crônica.
e) Síndrome nefrótica: Ou nefrose, é caracterizada por mudanças na
permeabilidade glomerular. Apresenta proteinúria (3,5 g/dia) sem hematúria devido à
redução nas propriedades carga-seletivas da barreira de filtração. Hipoproteinemia,
hipercolesterolemia, edema e ascite são encontrados. Pode acontecer como complicação
do diabetes e do lúpus, bem como na glomeruloescleose segmentar. Deve-se tratar a
doença de base.
Além disso, outras patologias são apresentadas, como a nefropatia diabética, a
nefropatia hipertensiva, nefropatia toxica, cálculos renais e a presença de cadeias leves
monoclonais (proteínas de bence Jones) no mieloma múltiplo.
Você também pode gostar
- BELZONA 1111 Solidifier TradDocumento13 páginasBELZONA 1111 Solidifier TradAlvaro Pereira NetoAinda não há avaliações
- Como Fazer Extratos Glicólicos de PlantasDocumento4 páginasComo Fazer Extratos Glicólicos de PlantasFatima Silva100% (1)
- BiologiaDocumento19 páginasBiologiaFox Prevenções100% (1)
- FUNÇÃO RENAL e EQUILÍBRIO ÁCIDO BASEDocumento26 páginasFUNÇÃO RENAL e EQUILÍBRIO ÁCIDO BASEGabriela Emi ImanoboAinda não há avaliações
- 4 - Sistema UrinárioDocumento17 páginas4 - Sistema UrinárioMatheus LanzaAinda não há avaliações
- Resumo 1 FrequênciaDocumento106 páginasResumo 1 FrequênciaÉrica CoutinhoAinda não há avaliações
- Aulas Anatomia e Fisiologia - Parte 5 - S. Urinário e S. ReprodutoresDocumento86 páginasAulas Anatomia e Fisiologia - Parte 5 - S. Urinário e S. ReprodutoresGladisson RamosAinda não há avaliações
- Aula 07 - SISTEMA EXCRETORDocumento6 páginasAula 07 - SISTEMA EXCRETORprote.lauraAinda não há avaliações
- Fisiologia renal: Funções e estruturas do rimDocumento16 páginasFisiologia renal: Funções e estruturas do rimAnaltina VictóriaAinda não há avaliações
- Sistema Renal e Produção de UrinaDocumento17 páginasSistema Renal e Produção de UrinaDébora CarvalhoAinda não há avaliações
- Sistema UrinarioDocumento18 páginasSistema UrinarioMichelle Soares PereiraAinda não há avaliações
- Questionário de FisiologiaDocumento3 páginasQuestionário de FisiologiaMarla Abalem100% (1)
- Capitulo 9 Regulação Do Corpo HumanoDocumento42 páginasCapitulo 9 Regulação Do Corpo HumanogabriellyAinda não há avaliações
- 05 - Anatomofisiologia Do Sistema RenalDocumento15 páginas05 - Anatomofisiologia Do Sistema RenalCristiano PereiraAinda não há avaliações
- Apostila Urinalise.2008Documento61 páginasApostila Urinalise.2008Tamara AlvesAinda não há avaliações
- 4 Urografia Parte2Documento8 páginas4 Urografia Parte2Rodrigo RibeiroAinda não há avaliações
- Sistema urinário e evolução dos sistemas excretoresDocumento7 páginasSistema urinário e evolução dos sistemas excretoresLili RibeiroAinda não há avaliações
- Resumo RenalDocumento6 páginasResumo RenalGabriella TeixeiraAinda não há avaliações
- Fisiologia RenalDocumento7 páginasFisiologia RenalNatália OiringAinda não há avaliações
- 20222sistemaurinario1 20231116185541Documento79 páginas20222sistemaurinario1 20231116185541wilton.alvaresxdAinda não há avaliações
- Função RenalDocumento7 páginasFunção RenalLetícia Guadálupe Santana GomesAinda não há avaliações
- Sistema urinário e formação da urinaDocumento82 páginasSistema urinário e formação da urinaZERO43MEIAAinda não há avaliações
- Filtração Glomerular e Hemodinâmica Renal e Mecanismos de Transporte - CompletoDocumento61 páginasFiltração Glomerular e Hemodinâmica Renal e Mecanismos de Transporte - CompletoFernanda Somera100% (2)
- Funções do sistema urinárioDocumento44 páginasFunções do sistema urinárioMarquinhos GomesAinda não há avaliações
- Biologia - Pré-Vestibular Vetor - Bio1 Fisiologia - Sistema UrinárioDocumento3 páginasBiologia - Pré-Vestibular Vetor - Bio1 Fisiologia - Sistema UrinárioBiologia Concurso Vestibular100% (2)
- Fisiologia RenalDocumento16 páginasFisiologia RenalSaraAinda não há avaliações
- Apostila Psicoterapias Módulo 6 FinalDocumento51 páginasApostila Psicoterapias Módulo 6 FinalBrunoAinda não há avaliações
- Sistema excretor e formação da urinaDocumento9 páginasSistema excretor e formação da urinacatarisabel100% (1)
- Resumo SP 1.5Documento16 páginasResumo SP 1.5Arthur VianaAinda não há avaliações
- Introdução A Fisiologia RenalDocumento4 páginasIntrodução A Fisiologia RenalrodrigocamargovetAinda não há avaliações
- Excreção Comparada e HumanaDocumento5 páginasExcreção Comparada e HumanaiamnnegAinda não há avaliações
- Nutrição e Doenças RenaisDocumento106 páginasNutrição e Doenças RenaisLogain ExcluiAinda não há avaliações
- Sistema UrinárioDocumento2 páginasSistema Urináriopqfnqkf5tqAinda não há avaliações
- Fisiologia e Patologia Dasdoencas RenaisDocumento26 páginasFisiologia e Patologia Dasdoencas RenaisJuliana Guedes Ferreira LemosAinda não há avaliações
- A Formação Da UrinaDocumento3 páginasA Formação Da UrinaPedro SantosAinda não há avaliações
- Apresentação Caso Clinico DRCDocumento9 páginasApresentação Caso Clinico DRCIvete GonçalvesAinda não há avaliações
- Sistema Urinário: Funções Renais e Formação da UrinaDocumento32 páginasSistema Urinário: Funções Renais e Formação da UrinaKarolainy KetlynAinda não há avaliações
- Fisiologia renal - Reabsorção e excreçãoDocumento5 páginasFisiologia renal - Reabsorção e excreçãofenixcyberlanAinda não há avaliações
- Patologia Veterinaria - 2 Ed - Santos E Alessi-460-530Documento71 páginasPatologia Veterinaria - 2 Ed - Santos E Alessi-460-530Herick PassosAinda não há avaliações
- Sistema Excretor RenalDocumento60 páginasSistema Excretor RenalMárcia NP100% (1)
- Aula 09Documento20 páginasAula 09Paulo sousaAinda não há avaliações
- Nefro 01 (Conceitos, GNDA, GNRP)Documento7 páginasNefro 01 (Conceitos, GNDA, GNRP)Francisco FreireAinda não há avaliações
- Relatório de FechamentoDocumento5 páginasRelatório de FechamentoGeisa Maritsa WippelAinda não há avaliações
- Sistema ExcretorDocumento25 páginasSistema ExcretorMichelle Stefani Guimarães100% (1)
- Sistema excretor e regulação renalDocumento56 páginasSistema excretor e regulação renalCristiane Santos100% (1)
- Fisiologa Renal PDFDocumento37 páginasFisiologa Renal PDFGrebyMontalvánRoblesAinda não há avaliações
- Trabalho Escrito Sistema UrinárioDocumento12 páginasTrabalho Escrito Sistema UrinárioCassia Tavares TavaresAinda não há avaliações
- TeoricoDocumento35 páginasTeoricoMariana AdeoAinda não há avaliações
- Indicadores bioquímicos da função renalDocumento17 páginasIndicadores bioquímicos da função renalalexalmeida19Ainda não há avaliações
- 1 Avaliação Laboratorial Do Sistema UrinárioDocumento58 páginas1 Avaliação Laboratorial Do Sistema UrináriorilixgsimululadorAinda não há avaliações
- Ua 04Documento26 páginasUa 04bioalbuquerque@gmail.comAinda não há avaliações
- Capitulo Livro PDFDocumento64 páginasCapitulo Livro PDFSr. Winston (e-Denúncias)Ainda não há avaliações
- Apostila Do Sistema UrinárioDocumento7 páginasApostila Do Sistema UrinárioRodrigo NascimentoAinda não há avaliações
- 4265-Urinálise e Espermograma - ApostilaDocumento50 páginas4265-Urinálise e Espermograma - ApostilaMayara NascimentoAinda não há avaliações
- Anatomia, fisiologia e fisiopatologia renalDocumento61 páginasAnatomia, fisiologia e fisiopatologia renalSauloThiagoAinda não há avaliações
- A urinálise no diagnóstico de doenças renaisDocumento14 páginasA urinálise no diagnóstico de doenças renaisBruna BarrosoAinda não há avaliações
- Funções dos rins e processo de filtração renalDocumento13 páginasFunções dos rins e processo de filtração renalvivianeAinda não há avaliações
- HistologiaDocumento2 páginasHistologiaFabio DonatoAinda não há avaliações
- Apostila - Doenas RenaisDocumento26 páginasApostila - Doenas RenaiseldesouzaAinda não há avaliações
- Sistema UrinárioDocumento7 páginasSistema UrinárioGuilherme NascimentoAinda não há avaliações
- Análise do pH de substâncias com indicador de repolho roxoDocumento19 páginasAnálise do pH de substâncias com indicador de repolho roxoMariana MartinsAinda não há avaliações
- PoçõesDocumento106 páginasPoçõesKalyson Juan Azevedo Da SilvaAinda não há avaliações
- Aula Prática Estendida - Montando Uma Coluna de Winogradsky - Aula Na PráticaDocumento4 páginasAula Prática Estendida - Montando Uma Coluna de Winogradsky - Aula Na PráticaMaria João S. Nascimento100% (1)
- Liga de AlumínioDocumento6 páginasLiga de AlumínioEngenharia ProduçãoAinda não há avaliações
- Apresentação GeralDocumento23 páginasApresentação GeralNoelle SantosAinda não há avaliações
- Fispq 710733 Colorsteel Epxi Cinza M N8 V01Documento11 páginasFispq 710733 Colorsteel Epxi Cinza M N8 V01Amarildo CanaliAinda não há avaliações
- Preparação e Diluição de Soluções Aquosas de NaOH e HClDocumento4 páginasPreparação e Diluição de Soluções Aquosas de NaOH e HClMarcia Pimentel BarcellosAinda não há avaliações
- Lista de atividades - números de oxidaçãoDocumento4 páginasLista de atividades - números de oxidaçãoAndréa Marli Dos SantosAinda não há avaliações
- Fispq - B-821 - Detergente DesoxidanteDocumento7 páginasFispq - B-821 - Detergente DesoxidanteJacqueline NascimentoAinda não há avaliações
- 01 Sistema Vulkem Circulação de VeículosDocumento13 páginas01 Sistema Vulkem Circulação de VeículosEduardo LeslãoAinda não há avaliações
- Acetato de ISO Amila Ficha de SegurançaDocumento4 páginasAcetato de ISO Amila Ficha de SegurançaThiago Alves Barroso MadalenaAinda não há avaliações
- Texto de Apoio 12a Classe Fisiologia Vegetal-1Documento17 páginasTexto de Apoio 12a Classe Fisiologia Vegetal-1Álvaro António SortaneAinda não há avaliações
- Questionário Ii - Química GeralDocumento4 páginasQuestionário Ii - Química GeralTalita Miguel ProfissionalAinda não há avaliações
- Farmacologia veterináriaDocumento45 páginasFarmacologia veterináriaIsaias JuniorAinda não há avaliações
- Relatório 7 - Reações QuímicasDocumento5 páginasRelatório 7 - Reações QuímicasLarissa RamosAinda não há avaliações
- Éter e ÉsterDocumento9 páginasÉter e ÉsterAmélie Slater100% (1)
- Indústria Brasileira de Papel e Celulose: Processos, Impactos e CompetitividadeDocumento51 páginasIndústria Brasileira de Papel e Celulose: Processos, Impactos e CompetitividadeTathianne Valeska Reis FerreiraAinda não há avaliações
- Tecnologia de Mel e DerivadosDocumento226 páginasTecnologia de Mel e DerivadosÁlvaro PedrosaAinda não há avaliações
- Algumas Forrageiras Recomendadas para Ensilar 2022Documento24 páginasAlgumas Forrageiras Recomendadas para Ensilar 2022Pedro Batista da Silva JúniorAinda não há avaliações
- ÁCIDOS E BASES - PHDocumento15 páginasÁCIDOS E BASES - PHNicolle GabrielleAinda não há avaliações
- Teste 2 de Quimica 12 ClasseDocumento3 páginasTeste 2 de Quimica 12 ClasseJaime Ernesto NaeneAinda não há avaliações
- Aprendendo A Química Do Vinho - PDF Download GrátisDocumento15 páginasAprendendo A Química Do Vinho - PDF Download GrátisLeticia SilvaAinda não há avaliações
- Acetato de EtilaDocumento3 páginasAcetato de EtilaandrewolinskiAinda não há avaliações
- Tabela1.1 Difusividade Dos GasesDocumento1 páginaTabela1.1 Difusividade Dos GasesengailsonAinda não há avaliações
- Universidade Católica de Moçambique: PedogeografiaDocumento10 páginasUniversidade Católica de Moçambique: PedogeografiaRachid MussaAinda não há avaliações
- Química Orgânica ExperimentalDocumento40 páginasQuímica Orgânica ExperimentalDouglas José MeierAinda não há avaliações
- Tecnologias PLPHDocumento38 páginasTecnologias PLPHJosila Fagundes - Gama GmailAinda não há avaliações