Escolar Documentos
Profissional Documentos
Cultura Documentos
Relatório de Aula Prática - Determinação de Parâmetros Cinéticos de Reações Homogêneas
Enviado por
Ricardo Engenharia RibeirãoTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Relatório de Aula Prática - Determinação de Parâmetros Cinéticos de Reações Homogêneas
Enviado por
Ricardo Engenharia RibeirãoDireitos autorais:
Formatos disponíveis
LABORATORIO DE ENGENHARIA QUMICA I RELATRIO DE AULA PRTICA DETERMINAO DE PARMETROS CINTICOS DE REAES HOMOGNEAS GRUPO II
Ribeiro Preto 2011
SUMRIO
1. 2. 3. 4.
INTRODUO ................................................................................................................. 3 OBJETIVO ........................................................................................................................ 4 PROCEDIMENTO EXPERIMENTAL .......................................................................... 5 RESULTADOS E DISCUSSES .................................................................................... 7
4.1. 4.2. 4.3. Mtodo integral de anlise de dados ....................................................................................... 9 Mtodo diferencial de anlise de dados ................................................................................ 13 Discusso............................................................................................................................... 15
5.
CONCLUSO ................................................................................................................. 19
APNDICE A TABELAS DOS DADOS EXPERIMENTAIS COLETADOS POR GRUPO .................................................................................................................................... 20 APNDICE B PERFIL DE CONCENTRAO EXPERIMENTAL E CURVAS DE AJUSTE ................................................................................................................................... 24 APNDICE C PERFIL DE CONCENTRAO TERICO E EXPERIMENTAL ... 28 REFERNCIAS ..................................................................................................................... 32
1.
INTRODUO
Ao se estudar uma reao qumica leva-se em considerao, alm da espontaneidade
da mesma (estudo termodinmico), a rapidez com que ela ocorre (estudo cintico). Atravs de estudos experimentais possvel determinar esses parmetros. A velocidade com que a reao acontece definida por uma funo determinada como o produto de um termo dependente da temperatura por um termo de concentrao. Com a equao da velocidade pode-se determinar a ordem de uma reao, fator importante que foi analisado neste experimento. A ordem global de uma reao definida pela soma dos expoentes dos termos de concentrao na expresso da velocidade. As reaes presentes na natureza apresentam ordens globais diferenciadas, que nem sempre so diretamente relacionadas com sua estequiometria, ou seja, reaes no elementares, cujo expoente de um ou mais termos da funo concentrao, diferem do seu respectivo coeficiente estequiomtrico. Uma reao pode ter ordem global com nmeros inteiros, fracionados e, at mesmo, ser nula. Por isso, a importncia de se obter esses valores atravs de experimentos. A reao entre o violeta de metila, de colorao violeta intensa, e o hidrxido de sdio (Figura 1), composto alcalino incolor, bastante vlida para ser estudada por mtodos colorimtricos, pois o violeta de metila, tambm chamado de violeta cristal, perde sua cor na presena de ons OH-, o que resulta em um produto totalmente sem cor. Atravs da perda de sua colorao, possvel verificar o consumo desse reagente, usando a lei de Lambert-Beer, que correlaciona a concentrao de uma substncia com sua absorbncia.
Figura 1 Reao entre o violeta de metila e o hidrxido de sdio
2.
OBJETIVO
Obter os parmetros cinticos da reao de descolorao do violeta de metila, tais
como ordem da reao em relao a cada um dos componentes e, tambm, a ordem global da reao juntamente com a constante de velocidade para as condies experimentais.
3.
PROCEDIMENTO EXPERIMENTAL
Inicialmente, fez-se a calibrao do colormetro (Figura 2), adicionando-se gua
destilada em uma cubeta seca e limpa, para que o aparelho fosse devidamente zerado a um comprimento de onda de 590 nm.
Figura 2 Colormetro Em seguida, adicionou-se 90 mL de soluo de violeta de metila ,
-
M e 10 mL
de soluo de hidrxido de sdio 0,05 M em um Erlenmeyer de 100 mL (Figura 3).
Figura 3 Mistura reacional em constante agitao Ao adicionar-se a soluo de hidrxido de sdio, o cronmetro foi acionado marcando o incio da reao, e colocaram-se os reagentes em constante agitao em um agitador magntico. Para dados experimentais, mediu-se a temperatura do meio reacional.
Transferiu-se uma alquota de 4 mL da mistura reacional (Figura 4) para uma cubeta plstica, devidamente limpa. Introduziu-se a cubeta no colormetro e foi feita a leitura da absorbncia no comprimento de onda de 590 nm. Em seguida, o contedo da cubeta foi descartado.
Figura 4 Retirada da alquota do meio reacional O procedimento de retirada da alquota do meio reacional para ser medida sua absorbncia no colormetro, foi repetido nos tempos de aproximadamente 1, 3, 6, 9, 12, 15, 18, 21, 24, 27, 30, 35, 40, 45, 50, 60, 70, 80 e 90 minutos com o cronmetro acionado desde a mistura inicial dos reagentes. A cada medio, a cubeta foi devidamente limpa e seca, a fim de no ocasionar erros durante o experimento. Ao trmino das medies, retirou-se uma alquota de 4 mL da soluo de violeta de metila ,
-
M pura, para obteno da curva de calibrao do colormetro.
Anotaram-se os dados de absorbncia medida e tempo obtidos em formato de tabela para facilitar o manuseio e tratamento dos mesmos.
4.
RESULTADOS E DISCUSSES
A reao do violeta de metila com hidrxido de sdio pode ser escrita genericamente:
A concentrao inicial dos reagentes adicionados no Erlenmeyer foi calculada pelas Equaes 1 e 2.
(1) (2)
Sendo desse reagente e desse reagente.
a concentrao da soluo de violeta de metila e a concentrao de hidrxido de sdio e
o volume adicionado o volume adicionado
Calculou-se a concentrao do violeta de metila medida que a reao estava acontecendo atravs da Equao 3, que foi obtida pela curva de calibrao para o violeta de metila (Figura 5).
(3)
Sendo C a concentrao do violeta de metila a ser medida e A a absorbncia desse reagente dada pelo colormetro.
1,600E-05 1,400E-05 y = 1,803E-05x R = 1,000E+00
Concentrao (mol/L)
1,200E-05
1,000E-05 8,000E-06
6,000E-06
4,000E-06 2,000E-06 0,000E+00 0,000 0,200 0,400 0,600 0,800 1,000
Absorbncia (-)
Figura 5 Curva de calibrao do violeta de metila para a temperatura de 27C
A concentrao do reagente B (hidrxido de sdio) foi obtida atravs da Regra do nmero de equivalentes, que representa o quanto um reagente foi consumido ou o quanto um produto foi formado durante uma reao. Atravs desse conceito, conhecendo as quantidades de um dos componentes possvel calcular para os outros componentes da reao conforme descrito na obra de Martin Schmal (2010). A concentrao do hidrxido de sdio foi obtida pela Equao 4.
(4)
Os dados obtidos experimentalmente juntamente com os respectivos valores de concentrao do violeta de metila e hidrxido de sdio para os grupos 2 e 5 so mostrados na Tabela 1. O APNDICE A mostra os dados experimentais coletados para os outros grupos que realizaram o mesmo experimento. Tabela 1 Dados experimentais obtidos pelos grupos 2 e 5 Absorbncia (-) 0,548 0,503
t(s) 0 140 226
CA (mol/L) , , ,
CB (mol/L) , , ,
456 814 1183 1542 1800 2157 2470 2769 3047 3359 3600 3914 4529
0,392 0,279 0,194 0,133 0,113 0,092 0,080 0,072 0,065 0,066 0,061 0,065 0,063
, , , , , , , , , , , , ,
, , , , , , , , , , , , ,
Para facilitar os clculos, o reagente B (hidrxido de sdio) foi adicionado em excesso com relao ao reagente A (violeta de metila) podendo ser considerada sua concentrao constante durante o decorrer da reao.
4.1. Mtodo integral de anlise de dados
O mtodo integral de anlise sempre tem uma equao particular de taxa, integrando e comparando a curva estimada de C versus t com os respectivos dados experimentais (LEVENSPIEL, 2000, p. 34). Como mencionado no item 4, a concentrao do reagente B est em grande excesso em relao ao reagente A. Sendo assim, a constante k representa o produto da constante de velocidade k pela concentrao de B conforme a Equao 5.
(5)
As Equaes do reator e da reao so, respectivamente, 6 e 7.
( (
) )
quao do reator S quao da reao
(6) (7)
10
Substituindo-se pelas ordens 0, 1, 2 e 3, igualando as Equaes 6 e 7 e integrando, obtivemos, respectivamente, as Equaes 8, 9, 10 e 11 que propiciam o clculo da concentrao do reagente A (violeta de metila) em funo do tempo.
(8)
( )
(9) (10)
(11)
Calculou-se a constante
para reaes de ordem 0, 1, 2 e 3 utilizando todos os
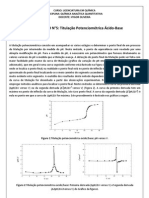
valores de concentrao obtidos experimentalmente. Depois, foram calculadas as concentraes do violeta de metila para cada tempo e cada ordem de reao proposta utilizando o valor da constante ajustado pelo grfico no Microsoft Excel e as Equaes de 8 a 11. O melhor ajuste encontrado foi obtido para reaes de ordem 2 para todos os dados analisados. A Figura 6 representa a comparao feita entre a curva experimental e as curvas obtidas pelos ajustes feitos atravs do mtodo integral para as ordens 0, 1, 2 e 3. Os ajustes feitos para os outros grupos encontram-se no APNDICE B deste relatrio.
1,60E-05
1,40E-05 1,20E-05
Concentrao (mol/L)
1,00E-05
8,00E-06 6,00E-06
Experimental Ordem 0 Ordem 1 Ordem 2
4,00E-06
2,00E-06 0,00E+00
-2,00E-06
-4,00E-06 -6,00E-06 0 1000 2000 3000 4000 5000 Tempo (s)
Figura 6 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 1,2 e 3, grupos 2 e 5.
11
A Tabela 2 mostra os valores de
e k para cada grupo.
Tabela 2 Parmetros obtidos em cada ensaio reacional Grupo 1 2e5 3 4 6 7 8 9 ( ) k 156,9 218,6 213,0 582,1 105,2 143,9 281,2 457,2
Temperatura 27C 0,0025 0,0050 0,0075 0,0100 Temperatura 25C 0,0025 0,0050 0,0075 0,0100
Como k representa o produto da constante de velocidade pela concentrao do reagente B o valor da constante k e do coeficiente da reao foram obtidos pelo ajuste linear feito no Microsoft Excel atravs da substituio das incgnitas da Equao 12 pelos valores da Tabela 2. ( ) ( ) ( )
(12)
Para a temperatura de 27C: ( ( ( { ( ( ) ) ) ) ) ( ) ( ) ( ) ( ) ( ( ( ( ) ) ) )
Para a temperatura de 25C: ( ( ( { ( ) ) ) ) ( ( ( ( ) ) ) ) ( ( ( ( ) ) ) )
12
( ) mostra os valores das ordens e obtidos experimentalmente e a
A Tabela
constante de velocidade k para os experimentos em temperaturas diferentes.
13
Tabela 3 Valores de e e constante de velocidade k obtido pelo mtodo integral de anlise de dados Grupo 1 2e5 3 4 6 7 8 9 2 2 2 2 2 2 2 2 Temperatura 27C 0,8582 ,
,
mol
Temperatura 25C 0,8669 ,
,
mol
As expresses de velocidade para as duas temperaturas de 27C e 25C so dadas, respectivamente, pelas Equaes 13 e 14. ( ( ) )
(13) (14)
4.2. Mtodo diferencial de anlise de dados
O mtodo diferencial de anlise de dados lida diretamente com a equao diferencial de taxa a ser testada, avaliando todos os termos na equao, inclusive a derivada ,e
testando a qualidade do ajuste da equao com os dados experimentais (LEVENSPIEL, 2000, p. 52). Traaram-se tangentes no ponto que representava a concentrao inicial do reagente A (violeta de metila) para todos os grupos como mostrado na Figura 7. Os dados do Grupo 1 no possibilitaram a utilizao desse mtodo, portanto foram desprezados.
14
1,40E-05 1,20E-05
Concentrao (mol/L)
Concentrao de violeta de metila
1,00E-05 8,00E-06
6,00E-06 4,00E-06 2,00E-06 0,00E+00
Tangente
1000
2000 Tempo (s)
3000
4000
Figura 7 Grfico para obteno dos parmetros cinticos pelo mtodo diferencial
Calcularam-se as velocidades iniciais da reao para cada grupo pela Equao 15.
(15)
A partir da linearizao da equao que representa a velocidade de reao entre o violeta de metila e hidrxido de sdio (Equao 16), obteve-se a Equao 17. ( ( ) ) ( ) ( ) ( )
(16) (17)
Substituem-se os valores das velocidades iniciais encontrados pelo ajuste grfico da Figura 7 para cada grupo e as concentraes iniciais dos reagentes A e B calculadas pelas Equaes 1 e 2. Foram utilizados os valores da Tabela 4 para o clculo da constante de velocidade e das ordens e . Tabela 4 Dados obtidos pelo mtodo diferencial Grupo 2e5 , CA0 (M) CB0 (M) (-rA0) ( ) Ln (CA0) Ln (CB0) -5,298 Ln (-rA0) -17,042
Temperatura de 27C 0,0050 -11,213 ,
15
3 4 6 7 8 9
, , , , , ,
0,0075 0,0100 0,0025 0,0050 0,0075 0,0100
-11,266 , -11,331 , Temperatura de 25C -11,155 , -11,213 , -11,266 , -11,331 ,
-4,893 -4,605 -5,991 -5,298 -4,893 -4,605
-16,032 -15,895 -17,424 -16,060 -16,199 -15,498
Os valores da constante de velocidade e das ordens e so mostrados na abela . Tabela 5 Resultados obtidos a partir do mtodo diferencial Grupo 2 3 4 6 7 8 9 k Temperatura de 27C 21,281 , 21,281 , 21,281 , Temperatura de 25C 421,63 3,266 421,63 3,266 421,63 3,266 421,63 3,266 5,279 5,279 5,279 1,666 1,666 1,666 1,666
As expresses de velocidade para as temperaturas de 27C e 25C so dadas, respectivamente, pelas Equaes 18 e 19. ( ( ) )
(18) (19)
4.3. Discusso
O fator pr-exponencial (k0) e a energia de ativao (EA) para a reao entre o violeta de metila e hidrxido de sdio valem, respectivamente, , , mol- se
mol- (MADEIRA; MENDES e MAGALHES, 2006, p. 193).
(20)
16
Com auxlio dessas informaes e da Lei de Arrhenius (Equao 20) calculou-se o perfil de concentrao do violeta metila terico para cada grupo e comparou-se com o perfil de concentrao experimental. Verificou-se para todos os grupos que a curva experimental no coincidia com a curva terica construda atravs das informaes da literatura. A Figura 8 mostra a comparao entre as duas curvas. Os perfis comparativos para os outros grupos que realizaram o mesmo experimento encontram-se no APNDICE C deste relatrio.
1,60E-05
1,40E-05
Concentrao (mol/L)
1,20E-05
1,00E-05
Terico Experimental
8,00E-06
6,00E-06 4,00E-06 2,00E-06 0,00E+00 0 1000 2000 3000 4000 5000 Tempo (s)
Figura 8 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupos 2 e 5.
Pela observao dos grficos comparativos de todos os grupos verificou-se que na maioria deles h um padro sistemtico para a curva experimental. O incio da reao se processa mais rpido do que deveria acontecer na teoria, o que explica o fato de os pontos estarem abaixo da curva terica. Prximo ao fim da reao, quando a reao est mais lenta, a concentrao do violeta de metila fica acima da concentrao terica. Como o Erlenmeyer onde a reao estava acontecendo permaneceu aberto durante todo o experimento o dixido de carbono (CO2) presente na atmosfera poderia ter se dissolvido na gua ocupando os espaos entre as molculas, j que a soluo estava sob agitao. Uma pequena parte do dixido de carbono dissolvido acaba formando o cido carbnico, um cido fraco. H uma mudana de cor causada pelo armazenamento do gs na gua presente no meio reacional. Essa mudana de cor caracterizada pelo clareamento caracterstico da colorao violeta do violeta de metila.
17
Como o clculo da concentrao do reagente se baseou na mudana de colorao que ocorre durante o desempenho da reao, pode ter havido, alm do clareamento normal esperado pelo consumo do reagente violeta cristal, um aclaramento provocado pelo acmulo de dixido de carbono na gua tornando a soluo ainda mais clara. Isso gerou um valor de absorbncia menor do que deveria acontecer e, consequentemente, a reao pareceu acontecer mais rpido, o que explica o mostrado na Figura 8. Como o dixido de carbono dissolvido tambm forma cido carbnico, este ltimo acabaria reagindo com o hidrxido de sdio, criando uma reao em paralelo reao principal, consumindo parte do reagente B que teoricamente estava constante. Embora a concentrao desse reagente seja muito maior do que a concentrao do violeta de metila (cerca de 1000 vezes maior), ento o cido no suficiente para neutralizar todo o hidrxido de sdio presente na reao, entretanto, como a velocidade da reao uma funo da concentrao e da temperatura, com a diminuio da concentrao de um dos reagentes a reao teve sua velocidade alterada tornando-a mais lenta. Discutiu-se tambm a hiptese de que a concentrao da soluo de violeta de metila utilizada poderia ser diferente da concentrao indicada no rtulo do recipiente. Isso tambm poderia influenciar a velocidade da reao forando um decaimento da curva terica que se aproximaria mais dos resultados experimentais como mostrado na Figura 9 considerando uma concentrao inicial hipottica do reagente A de ,
-
M.
18
1,40E-05
1,20E-05
Concentrao (mol/L)
Terico 1,00E-05 Experimental
8,00E-06
6,00E-06 4,00E-06
2,00E-06
0,00E+00 0 1000 2000 3000 4000 5000 Tempo (s)
Figura 9 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente para concentrao inicial hipottica do reagente A de ,
-
Nesse caso, o ajuste se tornou melhor do que com a concentrao indicada no recipiente. Os valores de absorbncia encontrados tambm podem ter tido desvios, pois no fim do experimento verificou-se que ao inserir a cubeta com gua destilada no colormetro esse no estava zerado mostrando um valor de absorbncia prximo de , , o que somado ao valor
real de absorbncia da soluo medida indicaria um valor de absorbncia maior e, consequentemente, causaria uma falsa impresso de que a concentrao do reagente A seria maior do que o valor real. Esse fato poderia explicar a maior concentrao do violeta de metila mais prxima ao fim da reao.
19
5.
CONCLUSO
Os parmetros cinticos obtidos pelos mtodos integral (Tabela 3, item 4.1) e
diferencial (Tabela 4, item 4.2) atravs do tratamento dos dados experimentais, no correspondem aos valores encontrados na literatura em que a reao de hidrlise do violeta de metila de ordem global 2, sendo de primeira ordem em relao a cada reagente. O mtodo diferencial apresentou valores bem divergentes do mtodo integral, mostrando-se inadequado para anlise dos dados desse experimento. As hipteses levantadas para explicar os desvios que comprometeram o resultado final do experimento so: Interferncia do dixido de carbono atmosfrico (CO2) na reao; A concentrao da soluo de violeta de metila utilizada no experimento seria diferente da indicada no rtulo do recipiente; Formao do cido carbnico devido absoro do gs carbnico da atmosfera, o que neutralizaria parte do reagente hidrxido de sdio diminuindo a velocidade da reao; Valores de absorbncia com desvio devido perda de calibrao do colormetro durante a execuo do experimento. Para alcanar melhores resultados na execuo desse experimento sugeriu-se manter o Erlenmeyer onde a reao foi feita tampado, verificar a concentrao real dos reagentes por meio de padres e zerar o colormetro a cada retirada de alquota evitando a perda de calibrao do equipamento e o comprometimento dos resultados.
20
APNDICE A TABELAS DOS DADOS EXPERIMENTAIS COLETADOS POR GRUPO
Tabela A1 Dados experimentais obtidos pelo grupo 1 Absorbncia (-) 0,417 0,404 0,342 0,307 0,281 0,264 0,234 0,196 0,180 0,152 0,139 0,123 0,109 0,104 0,092 0,067 0,066 0,066
t(s) 0 60 180 360 540 720 900 1080 1260 1440 1620 1800 2100 2400 2700 3000 3600 4200 4800 5400
CA (mol/L) , , , , , , , , , , , , , , , , , , , ,
CB (mol/L) , , , , , , , , , , , , , , , , , , , ,
Tabela A2 Dados experimentais obtidos pelo grupo 3 Absorbncia (-) 0,392 0,323 0,252 0,192 0,143 0,119 0,101 0,089 0,080
t(s) 0 59 179 355 536 717 899 1080 1258 1441
CA (mol/L) , , , , , , , , , ,
CB (mol/L) , , , , , , , , , ,
21
1620 1799 2399 3000 3301 3600 3898 4198 4497 4794
0,071 0,068 0,054 0,047 0,045 0,042 0,041 0,040 0,039 0,038
, , , , , , , , , ,
, , , , , , , , , ,
Tabela A3 Dados experimentais obtidos pelo grupo 4 t(s) 0 60 123 181 240 300 360 420 480 540 660 780 960 1200 1440 1680 1980 2280 2880 3480 4080 Absorbncia (-) 0,473 0,410 0,363 0,321 0,283 0,244 0,217 0,189 0,166 0,133 0,111 0,087 0,070 0,054 0,048 0,047 0,044 0,031 0,031 0,031 CA (mol/L) , , , , , , , , , , , , , , , , , , , , , CB (mol/L) , , , , , , , , , , , , , , , , , , , , ,
Tabela A4 Dados experimentais obtidos pelo grupo 6 t(s) 0 180 300 Absorbncia (-) 0,626 0,573 CA (mol/L) , , , CB (mol/L) , , ,
22
480 720 1200 1680 2040 2460 2820 3540 4230 4980 5580
0,497 0,426 0,314 0,247 0,210 0,183 0,154 0,127 0,110 0,101 0,105
, , , , , , , , , , ,
, , , , , , , , , , ,
Tabela A5 Dados experimentais obtidos pelo grupo 7 Absorbncia (-) 0,548 0,503 0,392 0,279 0,194 0,133 0,113 0,092 0,080 0,072 0,065 0,066 0,061
t(s) 0 50 132 226 348 614 905 1210 1680 2260 3090 4090 5020 5900
CA (mol/L) , , , , , , , , , , , , ,
CB (mol/L) , , , , , , , , , , , , , ,
Tabela A6 Dados experimentais obtidos pelo grupo 8 t(s) 0 95 195 314 435 613 791 976 Absorbncia (-) 0,538 0,469 0,413 0,355 0,288 0,218 0,178 CA (mol/L) , , , , , , , , CB (mol/L) , , , , , , , ,
23
1212 1511 1810 2412 3075 4214 4815
0,148 0,115 0,106 0,088 0,084 0,079 0,069
, , , , , , ,
, , , , , , ,
Tabela A7 Dados experimentais obtidos pelo grupo 9 t(s) 0 40 60 80 150 200 300 498 600 900 1500 1800 2820 3600 4800 Absorbncia (-) 0,377 0,360 0,355 0,349 0,328 0,272 0,153 0,136 0,099 0,061 0,053 0,046 0,025 0,015 CA (mol/L) , , , , , , , , , , , , , , , CB (mol/L) , , , , , , , , , , , , , , ,
24
APNDICE B PERFIL DE CONCENTRAO EXPERIMENTAL E CURVAS DE AJUSTE
2,00E-05 1,50E-05
Concentrao (mol/L)
1,00E-05 5,00E-06
Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
0,00E+00
-5,00E-06 -1,00E-05 0 1000 2000 3000 Tempo (s) 4000 5000 6000
Figura B1 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 1.
1,40E-05
1,20E-05 1,00E-05 8,00E-06 6,00E-06 Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
Concentrao (mol/L)
4,00E-06
2,00E-06
0,00E+00
-2,00E-06 -4,00E-06 -6,00E-06 0 1000 2000 3000 Tempo (s) 4000 5000 6000
Figura B2 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 3.
25
1,50E-05
1,00E-05 5,00E-06 0,00E+00 -5,00E-06 -1,00E-05 0 1000 2000 Tempo (s) 3000 4000 Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
Figura B3 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 4.
Concentrao (mol/L)
1,60E-05
1,40E-05 1,20E-05 Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
Concentrao (mol/L)
1,00E-05
8,00E-06 6,00E-06
4,00E-06
2,00E-06 0,00E+00
-2,00E-06
-4,00E-06 -6,00E-06 0 1000 2000 3000 Tempo (s) 4000 5000 6000
Figura B4 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 6.
26
1,60E-05
1,40E-05 1,20E-05 Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
Concentrao (mol/L)
1,00E-05
8,00E-06 6,00E-06
4,00E-06
2,00E-06 0,00E+00
-2,00E-06
-4,00E-06 -6,00E-06 0 1000 2000 3000 4000 5000 6000 7000 Tempo (s)
Figura B5 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 7.
1,40E-05 1,20E-05
1,00E-05
Concentrao (mol/L)
8,00E-06 6,00E-06
Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
4,00E-06
2,00E-06 0,00E+00
-2,00E-06
-4,00E-06 -6,00E-06
-8,00E-06 0 1000 2000 3000
Tempo (s)
4000
5000
6000
Figura B6 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 8.
27
1,40E-05 1,20E-05 1,00E-05 8,00E-06 6,00E-06 4,00E-06 2,00E-06 0,00E+00 -2,00E-06 -4,00E-06 -6,00E-06 -8,00E-06 0 1000 2000 3000 Tempo (s)
Concentrao (mol/L)
Experimental Ordem 0 Ordem 1 Ordem 2 Ordem 3
4000
5000
6000
Figura B7 Variao da concentrao do violeta de metila experimental e ajustes feitos para ordem 0, 1, 2 e 3, grupo 9.
28
APNDICE C PERFIL DE CONCENTRAO TERICO E EXPERIMENTAL
0,000016
0,000014
Concentrao (mol/L)
0,000012
0,00001
Terico
Experimental
0,000008
0,000006 0,000004 0,000002 0 0 1000 2000 3000 4000 5000 Tempo (s)
Figura C1 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 1.
1,40E-05 1,20E-05
Concentrao (mol/L)
1,00E-05 8,00E-06 6,00E-06 4,00E-06 2,00E-06 0,00E+00 0 1000
Terico
Experimental
2000
3000 Tempo (s)
4000
5000
6000
Figura C2 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 3.
29
1,40E-05
1,20E-05
Concentrao (mol/L)
1,00E-05 8,00E-06
Terico
Experimental
6,00E-06
4,00E-06 2,00E-06
0,00E+00 0 1000 2000
Tempo (s)
3000
4000
Figura C3 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 4.
1,60E-05
1,40E-05
Concentrao (mol/L)
1,20E-05
1,00E-05
Terico
Experimental
8,00E-06
6,00E-06 4,00E-06 2,00E-06 0,00E+00 0 1000 2000 3000 Tempo (s) 4000 5000 6000
Figura C4 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 6.
30
1,60E-05
1,40E-05
Concentrao (mol/L)
1,20E-05
Terico
Experimental
1,00E-05
8,00E-06 6,00E-06 4,00E-06 2,00E-06 0,00E+00 0 1000 2000 3000 4000 5000 6000 7000 Tempo (s)
Figura C5 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 7.
1,60E-05
1,40E-05
Concentrao (mol/L)
1,20E-05
1,00E-05
Terico
Experimental
8,00E-06
6,00E-06 4,00E-06 2,00E-06 0,00E+00 0 1000 2000 3000 Tempo (s) 4000 5000 6000
Figura C6 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 8.
31
1,40E-05
1,20E-05
Terico Experimental
Concentrao (mol/L)
1,00E-05 8,00E-06
6,00E-06
4,00E-06 2,00E-06
0,00E+00 0 1000 2000 3000
Tempo (s)
4000
5000
6000
Figura C7 Comparao do perfil de concentrao terico do violeta de metila com o perfil obtido experimentalmente, grupo 9.
32
REFERNCIAS
ABSORO de CO2. Cincia da Terra. [S.l. s.n.], [200-?], No paginado. Disponvel em: < http://planetseed.com/pt-br/node/27577>. Acesso em: 4 set. 2011.
DETERMINAO da ordem de uma reao e da constante de velocidade, por anlise colorimtrica. Anlise Colorimtrica. [S.l. s.n.], [2009?], No paginado. Disponvel em: < http://www2.iq.usp.br/docente/hvlinner/QFL2426/>. Acesso em: 13 set. 2011.
GELDER, John I.; GETTYS, Nancy S.; EUBANKS, Dwaine I. Kinetics of the Decolorization of Crystal Violet by Sodium Hydroxide. In: _______. AP Chemistry by Satellite Laboratory Manual. Student Edition. Stillwater: Oklahoma State University. cap. 12, pg. 12-15. Disponvel em: < http://intro.chem.okstate.edu/html/S1LIX.HTM>. Acesso em: 13 set. 2011.
LEVENSPIEL, Octave. Interpretao dos Dados de Reatores Descontnuos. In: ________. Engenharia das Reaes Qumicas. 3 ed. So Paulo: Edgard Blcher Ltda, 2000, cap. 3, pg. 34-52.
MADEIRA, Luis M.; MENDES, Adlio.; MAGALHES, Ferno D. Teaching Laminar-Flow Reactors: From Experimentation To CFD Simulation. In: _______. Int. J. Engng. GrBretanha: TEMPUS, 2006. vol. 22, pg. 188-196.
SCHMAL, Martin. Cintica. In: _______. Cintica e Reatores: Aplicao na Engenharia Qumica. 1 ed. Rio de Janeiro: Synergia, 2010. cap. 1, pg. 6-7.
SKOOG, Douglas A. Spectrochemical Methods. In: _______. Fundamentals of Analytical Chemistry. 8 ed. Canada: Thomson Brooks/Cole, 2004. cap. 24, Parte V, pg. 718-724.
Você também pode gostar
- Resumo Doug LemovDocumento12 páginasResumo Doug LemovKarla Mascarenhas100% (4)
- Preparo de Solução e PadronizaçãoDocumento9 páginasPreparo de Solução e PadronizaçãoNeimar RodriguesAinda não há avaliações
- Rubens Muzio - O DNA Da Liderança Cristã PDFDocumento17 páginasRubens Muzio - O DNA Da Liderança Cristã PDFArlei Veloso50% (2)
- UFCD 8622 Ficha de Trabalho Nº2Documento2 páginasUFCD 8622 Ficha de Trabalho Nº2Margarida Rodrigues0% (1)
- Experimento - Método de MohrDocumento26 páginasExperimento - Método de MohrAlessandro OliveiraAinda não há avaliações
- Determinação Da Entalpia de Vaporização de LíquidosDocumento7 páginasDeterminação Da Entalpia de Vaporização de LíquidosPedro Kortstee SimõesAinda não há avaliações
- Eletroanálises: aspectos teóricos e práticosNo EverandEletroanálises: aspectos teóricos e práticosAinda não há avaliações
- Nietzsche - Volume 1 (Martin Heidegger)Documento531 páginasNietzsche - Volume 1 (Martin Heidegger)MatheusAinda não há avaliações
- Teste de Portugues 7 Ano - LadinoDocumento8 páginasTeste de Portugues 7 Ano - LadinoCubo Mágico100% (2)
- Folhas XangoDocumento3 páginasFolhas XangoSANTA CRUZ LOGISTICAAinda não há avaliações
- Pratica 1 - Gravimetria Niquel PDFDocumento4 páginasPratica 1 - Gravimetria Niquel PDFJoão PauloAinda não há avaliações
- Geometria Analitica e Algebra Linear para IniciantesDocumento172 páginasGeometria Analitica e Algebra Linear para IniciantesAnonymous fdZ815WAinda não há avaliações
- Relatório de Físico Química - Calor de VaporizaçãoDocumento8 páginasRelatório de Físico Química - Calor de VaporizaçãoKarine SilvaAinda não há avaliações
- Experimento 03 - Determinação Da Condutividade de Solução Aquosa de Ácido Acético Com Diferentes ConcentraçõesDocumento11 páginasExperimento 03 - Determinação Da Condutividade de Solução Aquosa de Ácido Acético Com Diferentes ConcentraçõesFelipe Marcassa100% (1)
- Ainda Estou A Aprender - Ribeiro Et Al. 2016 PDFDocumento482 páginasAinda Estou A Aprender - Ribeiro Et Al. 2016 PDFsusetevieira7193Ainda não há avaliações
- Projeto de Peneiras IndustriaisDocumento26 páginasProjeto de Peneiras IndustriaisRicardo Engenharia Ribeirão100% (4)
- Reação Com Violeta de MetilaDocumento32 páginasReação Com Violeta de MetilaRicardo Engenharia Ribeirão100% (1)
- Reação Com Violeta de MetilaDocumento32 páginasReação Com Violeta de MetilaRicardo Engenharia Ribeirão100% (1)
- PR Tica 12 Caracteriza o de Complexos Via An Lise Condutom TricaDocumento5 páginasPR Tica 12 Caracteriza o de Complexos Via An Lise Condutom TricaBeatriz ViannaAinda não há avaliações
- Cristal Violata e NaOHDocumento7 páginasCristal Violata e NaOHAndré MarchiAinda não há avaliações
- Cinética Química - Reação Relógio Iodeto/iodoDocumento11 páginasCinética Química - Reação Relógio Iodeto/iodoRafael Araújo Borges100% (1)
- Universidade Estadual de Feira de SantanaDocumento12 páginasUniversidade Estadual de Feira de SantanaEduardo ChavesAinda não há avaliações
- Relatório 2: EFEITO DA CONCENTRAÇÃO E TEMPERATURA NA VELOCIDADE DE REAÇÃODocumento9 páginasRelatório 2: EFEITO DA CONCENTRAÇÃO E TEMPERATURA NA VELOCIDADE DE REAÇÃOVinicius MaquiavelAinda não há avaliações
- Calorímetro e A Determinação Da Entalpia Do Peróxido de HidrogênioDocumento15 páginasCalorímetro e A Determinação Da Entalpia Do Peróxido de HidrogênioDanieleAinda não há avaliações
- Cátions Do Grupo VDocumento26 páginasCátions Do Grupo VEduardo Da Silva SousaAinda não há avaliações
- Relatório Quimica Inorgânica I - Energia de DissoluçãoDocumento12 páginasRelatório Quimica Inorgânica I - Energia de DissoluçãoGabriel BritoAinda não há avaliações
- ISO 8859 1QAdsor E7 E3o I 2edocxDocumento8 páginasISO 8859 1QAdsor E7 E3o I 2edocxWillian BoulosAinda não há avaliações
- Relatório 04 - Volumetria Por PrecipitaçãoDocumento9 páginasRelatório 04 - Volumetria Por PrecipitaçãoLucas ManuelAinda não há avaliações
- Estudo DirigidoDocumento25 páginasEstudo DirigidoCarlos SilvaAinda não há avaliações
- Relatório 1 Titulação Ácido-BaseDocumento9 páginasRelatório 1 Titulação Ácido-BasepolyengquimicaAinda não há avaliações
- Relatório Físico-Química (Prática 4)Documento8 páginasRelatório Físico-Química (Prática 4)Pedro Lucas Ferreira RodriguesAinda não há avaliações
- Lista Volumetria Complexação e Oxido-Redução1Documento2 páginasLista Volumetria Complexação e Oxido-Redução1Mariana GarciaAinda não há avaliações
- Analítica - Relatório Padronização Do KMnO4Documento10 páginasAnalítica - Relatório Padronização Do KMnO4Maria ValentinAinda não há avaliações
- Relatorio QGEDocumento9 páginasRelatorio QGEoliverAinda não há avaliações
- Relatorio Experimental - Equilibrio QuimicoDocumento7 páginasRelatorio Experimental - Equilibrio QuimicoSandra FagundesAinda não há avaliações
- RELATÓRIO CAA - Thaynara CoutinhoDocumento42 páginasRELATÓRIO CAA - Thaynara CoutinhoThaynara CoutinhoAinda não há avaliações
- Relat+ Rio de Sistema Tern+írio - AdemirDocumento9 páginasRelat+ Rio de Sistema Tern+írio - AdemirPamela ChristineAinda não há avaliações
- Prática - 2 - Determinação Dos Parâmetros Cinéticos de ReaçãoDocumento20 páginasPrática - 2 - Determinação Dos Parâmetros Cinéticos de ReaçãoChrystiano CaladoAinda não há avaliações
- Relatório Prática 4Documento6 páginasRelatório Prática 4Milena LimaAinda não há avaliações
- Pós Laboratório - Cinética Química - Erissom, Luan, Pedro, Ricardo e Victor PDFDocumento2 páginasPós Laboratório - Cinética Química - Erissom, Luan, Pedro, Ricardo e Victor PDFAlter EgoAinda não há avaliações
- Condutividade Elétrica e Solubilidade de Compostos QuímicosDocumento23 páginasCondutividade Elétrica e Solubilidade de Compostos QuímicosJuliana v.Ainda não há avaliações
- Aula 2 Titulação Ácido BaseDocumento54 páginasAula 2 Titulação Ácido BaseGabi PessoaAinda não há avaliações
- Cap 27 Tensão SuperficialDocumento18 páginasCap 27 Tensão SuperficialTelmanm100% (1)
- Experimento 3: Determinação Experimental Da Massa Molar Do Gás ButanoDocumento10 páginasExperimento 3: Determinação Experimental Da Massa Molar Do Gás ButanoJoelson Kalil Coelho100% (1)
- F.I.S.P.Q. Sulfeto de Amonio SolDocumento4 páginasF.I.S.P.Q. Sulfeto de Amonio SolJuliana GilAinda não há avaliações
- Lista Cap07 20231o - GabaritoDocumento7 páginasLista Cap07 20231o - GabaritoPedro Henrique100% (1)
- Cinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesDocumento72 páginasCinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesrafelAinda não há avaliações
- Padronização de SoluçõesDocumento4 páginasPadronização de SoluçõesFrederico De Barros Moraes100% (1)
- Equivalente em Água de Um CalorímetroDocumento16 páginasEquivalente em Água de Um CalorímetroNatalia GomezAinda não há avaliações
- Hidrólise Catalisada Por Um ÉsterDocumento11 páginasHidrólise Catalisada Por Um ÉsterHenrique Fernandes100% (2)
- Equilíbrio Entre Fases - Entalpia Molar de VaporizaçãoDocumento35 páginasEquilíbrio Entre Fases - Entalpia Molar de VaporizaçãoPaulo MachadoAinda não há avaliações
- Experimento 5 Titulação Potenciometrica Ácido BaseDocumento2 páginasExperimento 5 Titulação Potenciometrica Ácido BaseGeilson SilvaAinda não há avaliações
- Relatório Volumetria Acidez Do VinagreDocumento7 páginasRelatório Volumetria Acidez Do VinagreKelly RochaAinda não há avaliações
- Analises Química Por Via ÚmidaDocumento38 páginasAnalises Química Por Via ÚmidaJunior FariasAinda não há avaliações
- Relatório Iodo - Química Geral (UFMG)Documento6 páginasRelatório Iodo - Química Geral (UFMG)Júlia SoaresAinda não há avaliações
- Relatório - Perda de Massa e TafelDocumento4 páginasRelatório - Perda de Massa e TafelElisa CunhaAinda não há avaliações
- Lista 3 Unidade-2020.2docxDocumento4 páginasLista 3 Unidade-2020.2docxcontasAinda não há avaliações
- Condutimetria e Titulações CondutimétricasDocumento40 páginasCondutimetria e Titulações CondutimétricasNatacha CacitaAinda não há avaliações
- Violeta de Cristal II 17-03-2010Documento19 páginasVioleta de Cristal II 17-03-2010Francisco Patrocinio100% (2)
- Pré-Relatório 03 CineticaDocumento4 páginasPré-Relatório 03 CineticaGabriel AquinoAinda não há avaliações
- Relatorio 9Documento7 páginasRelatorio 9Flavio SousaAinda não há avaliações
- 2 Lei de Velocidade e Ordem de Reação CINÉTICADocumento13 páginas2 Lei de Velocidade e Ordem de Reação CINÉTICAclauber_dalmas100% (1)
- Exercicio Físico Química 2 2017 1Documento5 páginasExercicio Físico Química 2 2017 1Vitor LimaAinda não há avaliações
- Relatorio11 - Hidrólise Da SacaroseDocumento11 páginasRelatorio11 - Hidrólise Da SacaroseRyan ThairykAinda não há avaliações
- Leis Dos Gases IdeaisDocumento7 páginasLeis Dos Gases IdeaishorbiteAinda não há avaliações
- Relatório Experimento 5 Reagente LimitanteDocumento9 páginasRelatório Experimento 5 Reagente LimitanteJunior DuarteAinda não há avaliações
- Modelagem Matemática e Simulação de Processos FermentativosDocumento14 páginasModelagem Matemática e Simulação de Processos FermentativosYuslyJulianiAinda não há avaliações
- Hidrólise Ácida de Um ÉsterDocumento9 páginasHidrólise Ácida de Um Ésteranny_rodrigues_1Ainda não há avaliações
- Relatório 1 - VersãoDocumento7 páginasRelatório 1 - VersãoNatalia NevesAinda não há avaliações
- Riscos BiológicosDocumento114 páginasRiscos BiológicosRicardo Engenharia Ribeirão100% (1)
- Higiene III - Ambiente Térmico e Ventilação (Jan-Fev.2017)Documento172 páginasHigiene III - Ambiente Térmico e Ventilação (Jan-Fev.2017)Ricardo Engenharia RibeirãoAinda não há avaliações
- Trabalho de Conclusão de Curso de Especialização em Gestão de ProduçãoDocumento44 páginasTrabalho de Conclusão de Curso de Especialização em Gestão de ProduçãoRicardo Engenharia RibeirãoAinda não há avaliações
- NHO06Documento0 páginaNHO06Ed Carlo Rosa PaivaAinda não há avaliações
- Sensores CapacitivosDocumento7 páginasSensores CapacitivosFarofino99Ainda não há avaliações
- CEP Aplicado Ao Monitoramento de Envase Da Tintura de IodoDocumento8 páginasCEP Aplicado Ao Monitoramento de Envase Da Tintura de IodoRicardo Engenharia RibeirãoAinda não há avaliações
- NBR 10898-99 - Sistema de Iluminação de EmergênciaDocumento24 páginasNBR 10898-99 - Sistema de Iluminação de EmergênciaErnani E BrunaAinda não há avaliações
- NBR 17025Documento4 páginasNBR 17025raquelkasAinda não há avaliações
- Aula Componentes CaldeiraDocumento47 páginasAula Componentes CaldeiraRicardo Engenharia RibeirãoAinda não há avaliações
- Trocador de PlacasDocumento42 páginasTrocador de PlacasRicardo Engenharia RibeirãoAinda não há avaliações
- Tipos CaldeirasDocumento13 páginasTipos CaldeirasRicardo Engenharia RibeirãoAinda não há avaliações
- Tensão SuperficialDocumento10 páginasTensão SuperficialRicardo Engenharia RibeirãoAinda não há avaliações
- A Segunda Guerra MundialDocumento4 páginasA Segunda Guerra MundialRicardo Engenharia RibeirãoAinda não há avaliações
- FichamentoDocumento3 páginasFichamentoJadson CostaAinda não há avaliações
- Tópicos Do Review - Projeto Pedagógicos Curriculo e Trilhas de AprendizagemDocumento5 páginasTópicos Do Review - Projeto Pedagógicos Curriculo e Trilhas de AprendizagemVitoria Carvalho100% (1)
- Design de Exposicao e Experiencia EsteticaDocumento20 páginasDesign de Exposicao e Experiencia EsteticaRômulo GonzalesAinda não há avaliações
- Cifras Axe e Pagode 90 para EdiçãoDocumento23 páginasCifras Axe e Pagode 90 para EdiçãoFábio RecordssAinda não há avaliações
- Apostila Contratos Imobiliários e AtualizaçõesDocumento73 páginasApostila Contratos Imobiliários e AtualizaçõesLuany NunesAinda não há avaliações
- Orixas - 3 - Umbanda Cristica - Os Sagrados Orixas PDFDocumento10 páginasOrixas - 3 - Umbanda Cristica - Os Sagrados Orixas PDFHanna de BuenoAinda não há avaliações
- Tese 163 PDFDocumento507 páginasTese 163 PDFRodrigo de Melo MachadoAinda não há avaliações
- Prospecção Por LuminescênciaDocumento17 páginasProspecção Por LuminescênciaMiguel UchihaAinda não há avaliações
- CERVO, Amado Luiz. Uma Historia Da Cooperação Tecnica Internacional Do BrasilDocumento225 páginasCERVO, Amado Luiz. Uma Historia Da Cooperação Tecnica Internacional Do BrasilCamilla Alanis de OliveiraAinda não há avaliações
- Exercícios+-+Dia+da+Feira+de+Profissões PDFDocumento9 páginasExercícios+-+Dia+da+Feira+de+Profissões PDFLourencoCalegarioCelinAinda não há avaliações
- Recrutamento Online Uma RealidadeDocumento2 páginasRecrutamento Online Uma RealidadeRafael IasiAinda não há avaliações
- Materialdeapoioextensivo Literatura Exercicios o CorticoDocumento3 páginasMaterialdeapoioextensivo Literatura Exercicios o CorticoSara SchiavinatoAinda não há avaliações
- Resolucao Do PROFMAT Pet Matematica UFCG 2012Documento38 páginasResolucao Do PROFMAT Pet Matematica UFCG 2012Willians GavioliAinda não há avaliações
- Escola, Curriculo e Cultura - Unidades I e IIDocumento138 páginasEscola, Curriculo e Cultura - Unidades I e IIjudhyeAinda não há avaliações
- 1Documento1 página1Chris RedfieldAinda não há avaliações
- Giovanna Carranza Administração e Gestão de PessoasDocumento13 páginasGiovanna Carranza Administração e Gestão de PessoasNelson PinheiroAinda não há avaliações
- AULAT3 - Mecanismos Gerais de Acção Dos FármacosDocumento51 páginasAULAT3 - Mecanismos Gerais de Acção Dos FármacosJoão DomingosAinda não há avaliações
- A Influencia Do Positivismo No Ensino de QuimicaDocumento13 páginasA Influencia Do Positivismo No Ensino de QuimicaAlmirAinda não há avaliações
- Lista de Exercicios 20 - Fisica 2 IntegradoDocumento5 páginasLista de Exercicios 20 - Fisica 2 Integradoدانيال دينيزAinda não há avaliações
- Plano Ensino UrologiaDocumento7 páginasPlano Ensino UrologiaCamila Farah PissaiaAinda não há avaliações
- Preconceito RacialDocumento3 páginasPreconceito RacialRicky RochaAinda não há avaliações
- Os Lusíadas Canto IIDocumento11 páginasOs Lusíadas Canto IIvitinhousaAinda não há avaliações