Escolar Documentos
Profissional Documentos
Cultura Documentos
Estudo Dirigido - P1 - Neurobiologia Molceular
Enviado por
gabi.amota3Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Estudo Dirigido - P1 - Neurobiologia Molceular
Enviado por
gabi.amota3Direitos autorais:
Formatos disponíveis
Estudo Dirigido - P1
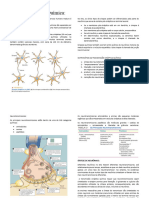
1. O slide apresenta a morfologia dos neurônios piramidais que possuem o soma, em
formato de pirâmide, um dendrito apical longo e arborizado e os outros dendritos. Os
neurônios piramidais são encontrados no córtex e no hipocampo. No córtex, os neurônios
piramidais estão posicionados de forma que o dendrito apical esteja para cima/fora, ou seja,
mais próximos ao crânio. Por isso, quando pensamos em medições ou tratamento por
estimulação transcraniana, por exemplo, os dendritos apicais são os primeiros a serem
alcançados. Diferente do neurônios piramidais do hipocampo que tem o dendrito apical
posicionado para dentro. Além disso, o neurônio piramidal, que é um neurônio
glutamatérgico e, portanto, excitatório, recebe sinapses GABAérgicas (inibitórias) de
interneurônios em diferentes regiões do neurônio. Os interneurônios chamados de células
de basket são parvalbumina positivos e fazem sinapses inibitórias no soma e cone axonal
de neurônios piramidais. Os interneurônios chamados de células de Martinotti são
somatostatina positivos e fazem sinapses inibitórias no dendrito apical da célula piramidal.
2. O dendrito apical piramidal possui a maior quantidade de espinhas dendríticas. As
espinhas dendríticas possuem uma cabeça e um pescoço. Como estão no dendrito apical,
essas espinhas recebem as modulações de somatostatina das células de Martinotti. Casa
região das espinhas dendríticas recebe entradas de diferentes neurotransmissores. A
cabeça recebe glutamato, o pescoço recebe dopamina e serotonina e o espaço entre as
espinhas recebe serotonina e acetilcolina. O pescoço modula a informação da cabeça e a
informação entre as espinhas modula cabeça e pescoço.
3. A sinapse é tripartida, ou seja, possui três elementos: neurônio pré-sináptico, neurônio
pós-sináptico e astrócitos. Os astrócitos, células gliais, são de extrema importância para a
sinapse pois eles cumprem com diversas funções essenciais ao funcionamento da sinapse.
Entre elas estão: recaptação do glutamato na fenda sináptica, metabolismo energético da
glicose em ATP para os neurônios, regulação do pH e dos íons, produção da matriz
extracelular que participa na movimentação dos canais de cálcio até a fenda sináptica.
4. O potencial de membrana do neurônio é determinado pelo equilíbrio de Nernst dos íons
que atravessam a sua membrana, principalmente Na+, K+, Ca+2 e Cl-, além de proteínas
que estão do lado de dentro da célula. Sódio, cálcio e cloro estão mais concentrados no
meio extracelular e potássio está mais concentrado no meio intracelular. Por conta de suas
concentrações e suas cargas, esses íons possuem duas forças impulsoras: a química e a
elétrica. Sódio e cálcio estão na mesma situação: as duas forças cooperam para que o íon
entre na célula que é mais negativa internamente. Potássio e cloro têm as duas forças
opostas, uma impulsionando para fora e a outra para dentro. O potencial e condutibilidade
de cada um desses íons determina o valor do potencial de membrana no repouso. O
potássio, que tem potencial negativo, e cloro, que é apenas um pouco menos negativo, são
os íons mais importantes para o potencial de repouso da membrana que está entre -50 e -
100mV. O potássio especialmente porque possui 90% da condutividade na membrana. A
bomba de sódio e potássio tem o importante papel de manter o gradiente de concentrações
desses dois íons bombeando sódio de volta para fora e potássio de volta para dentro da
célula.
5. O potencial de ação começa pela chegada de um PEPS que aumenta o potencial de
membrana o suficiente para passar o limiar. Quando isso acontece, canais de sódio e
potássio dependentes de voltagem são abertos. Os canais de sódio tem cinética mais
rápida de forma que eles abrem mais rápido, liberando a entrada de sódio que causa a
despolarização. Quando os canais de sódio começam a ser inativados, os canais de
potássio já terminaram de se abrir e começa o efluxo de potássio causando a repolarização
do potencial de membrana. O potencial de membrana é hiperpolarizado pela ação desses
canais de potássio dependentes de voltagem (que logo se fecham) e, principalmente, pelos
canais de potássio vazantes. A volta do potencial de membrana até o valor de repouso é
feito pelo cálcio. Os canais dependentes de voltagem primeiro se inativam e quando há a
hiperpolarização, eles se fecham se preparando para abrir de novo. A inativação é causada
pela comporta bola que impede a passagem dos íons.
6. O metabolismo energético neuronal está intimamente relacionado à manutenção do
potencial de membrana devido ao seu papel de produzir ATPs. O potencial de membrana é
mantido pela distribuição dos íons formando um gradiente de concentrações. Esse
gradiente é mantido por diversas bombas que bombeiam os íons contra o seu gradiente
natural e, portanto, gastam energia para isso. A bomba de Na+/K+, por exemplo, é
essencial para o gradiente de concentrações que mantém o potencial de repouso da
membrana. Uma falha na bioenergética afeta diretamente a produção de energia das
células e, consequentemente, a capacidade da célula de manter esses gradientes e o
potencial de membrana.
7. Para que o astrócito mande lactato para o neurônio, onde ele será transformado em
piruvato e passará pela fosforilação oxidativa que produzirá ATP, o neurônio precisa
sinalizar para o astrócito que precisa de produção rápida de energia. Essa sinalização é
feita pelo glutamato, liberado na fenda sináptica em uma sinapse excitatória. Esse
glutamato é captado por meio de transportadores EAATs (transportadores de aminoácidos
excitatórios). Esses transportadores levam o glutamato para dentro da célula junto com Na+
e H+. O glutamato que entra é transformado em glutamina por meio da enzima glutamina
sintase e então levado para o neurônio por outros transportadores. No neurônio, a
glutamina é transformada em glutamato e pode ser liberada na fenda sináptica novamente.
O sódio que entra na célula junto com o glutamato é bombeado para fora por uma bomba
de Na+/K+ que também precisa de ATP para funcionar - esse ATP é gerado pela glicose
que passa na glicólise dentro do astrócito.
8. A doença de Alzheimer está associada à falta de transportadores GLUT3. Os
transportadores GLUT3 são os transportadores de glicose mais presentes nos neurônios.
São eles os responsáveis por levar a glicose dos astrócitos, barreira hematoencefálica e
vasos sanguíneos para dentro dos neurônios. A ausência desses transportadores causa
uma diminuição na captação de glicose e, consequentemente, na produção de energia para
o neurônio. Em casos em que o GLUT3 falha, os astrócitos ajudam no aporte energético do
neurônio mas, ainda assim, a produção de ATPs é prejudicada. Nesse aporte energético, os
astrócitos transformam o piruvato em lactato que é transportado para os neurônios. No
neurônio, o lactato é transformado em piruvato novamente e passa pelo ciclo do TCA e
fosforilação oxidativa para produção de ATP.
9. O slide apresenta os dois caminhos percorridos pelo cálcio quando entra na célula pré-
sináptica por meio dos canais dependentes de voltagem do tipo L. A primeira proteína
importante é a CaM-quinase do tipo II. Essa é uma proteína sensora, ou seja, quando ela
percebe a presença do cálcio dentro da célula, ativa a proteína sinapsina que leva a
vesícula com os neurotransmissores para a readesão na zona ativa (membrana no terminal
pré-sináptico). A sinapsina está acoplada à vesícula e quando é fosforilada pelo CaM-
quinase II, se desacopla da vesícula permitindo sua translocação para a membrana. A outra
proteína sensora é a sinaptotagmina, que ao perceber a presença de cálcio, se associa a
ele ativando as proteínas do complexo SNARE (sintaxina e SNAP25 na membrana
sináptica) e ligando-as a sinaptobrevina na membrana pré-sináptica. Aqui, as outras
proteínas do complexo zíper vão se associar permitindo a exocitose.
10. O zíper complexo descreve o complexo de proteínas presentes tanto na membrana da
vesícula como na membrana do neurônio pré-sináptico que se associam formando algo
parecido com um zíper que abre e fecha permitindo a exocitose dos neurotransmissores. Na
membrana da vesícula temos a sinaptotagmina e sinaptobrevina que se associam a
sintaxina e SNAP-25 na membrana pré-sináptica. Mas, para essas proteínas interagirem é
necessário a presença das proteínas do Scaffold que são Munc 13 (que tem formato circular
e se abre para se ligar a outras proteínas), RIM e RIM-BP (que junto com o canal de cálcio
fazem o tethering), Rab3 (que permite o acople da sinaptotagmina ao cálcio), ELKS e liprin.
Além disso, todas essas proteínas se associam a Basson e Piccolo que por meio da profilin
se conectam a uma actina. Essas ligações formam um complexo de proteínas com formato
parecido ao de pirâmide de forma que é denominado de pirâmide densa.
Você também pode gostar
- Genética Médica para Médicos e Estudantes de Medicina: OncologiaNo EverandGenética Médica para Médicos e Estudantes de Medicina: OncologiaAinda não há avaliações
- Sistema Nervoso - Potenciais de membrana, sinapses e receptoresDocumento6 páginasSistema Nervoso - Potenciais de membrana, sinapses e receptoresnetim69Ainda não há avaliações
- Biossíntese de neurotransmissores no SNCDocumento12 páginasBiossíntese de neurotransmissores no SNCIsadora RenóAinda não há avaliações
- Bioeletrogênese e Sinapses Dra. Ana Paula Peña DiasDocumento6 páginasBioeletrogênese e Sinapses Dra. Ana Paula Peña DiasarthurAinda não há avaliações
- Fisiologia Humana Geral I - Parte 1Documento39 páginasFisiologia Humana Geral I - Parte 1douglas.diasAinda não há avaliações
- Sem Título 1Documento2 páginasSem Título 1Vitor SilvaAinda não há avaliações
- Captação de Glicose Pelo MúsculoDocumento15 páginasCaptação de Glicose Pelo Músculovictorallan2005Ainda não há avaliações
- Bases Biológicas 3Documento11 páginasBases Biológicas 3victorallan2005Ainda não há avaliações
- Estudo Dirigido de Membranas A NeurotransmissoresDocumento4 páginasEstudo Dirigido de Membranas A Neurotransmissoreskarina garzAinda não há avaliações
- Sinapses: a transmissão da informação neuronalDocumento13 páginasSinapses: a transmissão da informação neuronalNoemi SantosAinda não há avaliações
- Exercicio Sinapse e NeurotransmissoresDocumento4 páginasExercicio Sinapse e NeurotransmissoresRaphael Gripp RibeiroAinda não há avaliações
- Potencial de Ação e SinapsesDocumento9 páginasPotencial de Ação e SinapsesAmanda Francisquini100% (1)
- Potencial de Membrana, Potencial de Ação e SN - MonitoriaDocumento8 páginasPotencial de Membrana, Potencial de Ação e SN - MonitoriaIASMIN VALESCA SANTA CLARAAinda não há avaliações
- Potenciais elétricos e neurotransmissores no SNCDocumento3 páginasPotenciais elétricos e neurotransmissores no SNCLucas LiberatoAinda não há avaliações
- Fisiologia Humana 2Documento7 páginasFisiologia Humana 2Alessandro PedrettiAinda não há avaliações
- Questionário De. FisiologiaDocumento4 páginasQuestionário De. FisiologiaVielceketlin FrancoAinda não há avaliações
- Potencial de ação e propagação do impulso nervosoDocumento6 páginasPotencial de ação e propagação do impulso nervosoRafaela SpertineAinda não há avaliações
- Resumo PsicofármacoDocumento7 páginasResumo PsicofármacoRianne GomesAinda não há avaliações
- Receptores Ionotrópicos e Canais IônicosDocumento2 páginasReceptores Ionotrópicos e Canais Iônicosanon_104459440Ainda não há avaliações
- Bioeletrogênese e sinapsesDocumento9 páginasBioeletrogênese e sinapsesJéssica MartiellyAinda não há avaliações
- Neurotransmissão 40Documento2 páginasNeurotransmissão 40Rogério TavaresAinda não há avaliações
- Neurociências LivroDocumento4 páginasNeurociências LivroKarina LimaAinda não há avaliações
- FISIOLOGIA EstudoDocumento5 páginasFISIOLOGIA Estudoaylafonseca39Ainda não há avaliações
- Pricipais NeurotransmissoresDocumento9 páginasPricipais NeurotransmissoresTarssila Rafaela Santos88% (8)
- CélulaDocumento9 páginasCélulaMariana RochaAinda não há avaliações
- Neurotransmissores e ReceptoresDocumento9 páginasNeurotransmissores e ReceptoresJennifer Fontenelle100% (1)
- O transporte entre citosol e núcleoDocumento12 páginasO transporte entre citosol e núcleoMatheus Correa0% (1)
- Biologia Celular: Estruturas e FunçõesDocumento11 páginasBiologia Celular: Estruturas e FunçõesDiogo RibasAinda não há avaliações
- Estudos Dirigidos I, II, III - Bases (1)Documento17 páginasEstudos Dirigidos I, II, III - Bases (1)vbruno640Ainda não há avaliações
- BiocelDocumento10 páginasBiocelPatriciaAinda não há avaliações
- Estudo Fisiologia Humana Atividade FísicaDocumento6 páginasEstudo Fisiologia Humana Atividade FísicaAMANDA SILVAAinda não há avaliações
- Transmissão sináptica químicaDocumento14 páginasTransmissão sináptica químicaMakiesse António100% (1)
- cola para M1 neuro TaineDocumento2 páginascola para M1 neuro TainetaineborgesfreitasAinda não há avaliações
- O Papel Do Calcio Na Contração MuscularDocumento9 páginasO Papel Do Calcio Na Contração MuscularalmaformaAinda não há avaliações
- Potencial de Ação - Contração MuscularDocumento9 páginasPotencial de Ação - Contração MuscularRodrigo SousaAinda não há avaliações
- Fisiologia Do Impulso NervosoDocumento2 páginasFisiologia Do Impulso NervosoSuellen Nobre100% (2)
- Mapa Mental Sistema Nervoso - SNC e SNPDocumento18 páginasMapa Mental Sistema Nervoso - SNC e SNPsuzanna cassarAinda não há avaliações
- As propriedades elétricas de neurôniosDocumento4 páginasAs propriedades elétricas de neurôniosJoseval PoloAinda não há avaliações
- Resistência de pragas a pesticidas: principais mecanismos de ação de inseticidasDocumento6 páginasResistência de pragas a pesticidas: principais mecanismos de ação de inseticidasLuiz Eduardo AbreuAinda não há avaliações
- Condução do estímulo nervoso na sinapse químicaDocumento21 páginasCondução do estímulo nervoso na sinapse químicaYasmin MattosAinda não há avaliações
- Comunicação SinápticaDocumento4 páginasComunicação SinápticaMAdAinda não há avaliações
- 01.resumo ÁcNucleicos SíntProteíca 2022Documento4 páginas01.resumo ÁcNucleicos SíntProteíca 2022yuki sanAinda não há avaliações
- Fisiologia TrabalhoDocumento2 páginasFisiologia Trabalhoemilycovolo1Ainda não há avaliações
- Sinapse e NeurotransmissoresDocumento1 páginaSinapse e NeurotransmissoresJulia Cenci do CarmoAinda não há avaliações
- RESUMO prova biocelularDocumento20 páginasRESUMO prova biocelularguiarensoAinda não há avaliações
- Potencial de Ação e Unidade Motora 2016 PDFDocumento69 páginasPotencial de Ação e Unidade Motora 2016 PDFAna Luiza MenezesAinda não há avaliações
- Fisiologia Do Sistema Musculo EsqueleticoDocumento18 páginasFisiologia Do Sistema Musculo Esqueleticogeojac2112Ainda não há avaliações
- Ribossomos RER REL tradução proteínasDocumento8 páginasRibossomos RER REL tradução proteínasAndre Luiz do NascimentoAinda não há avaliações
- Aula 5 - BiocelDocumento13 páginasAula 5 - Biocelliz de andradeAinda não há avaliações
- Transporte de Proteínas para Organelas por Sinais de DistribuiçãoDocumento5 páginasTransporte de Proteínas para Organelas por Sinais de DistribuiçãoMacklecio OliveiraAinda não há avaliações
- Processo de contração muscularDocumento1 páginaProcesso de contração muscularMarina BeltrameAinda não há avaliações
- Açao NeuromuscularDocumento53 páginasAçao Neuromuscularanon_736807922Ainda não há avaliações
- Comunicação célula-célula no SNCDocumento2 páginasComunicação célula-célula no SNCJean Carlo FlamiaAinda não há avaliações
- Sinapses e Junção NeuromuscularDocumento23 páginasSinapses e Junção NeuromuscularCamila MendesAinda não há avaliações
- Assunto: Fisiologia Dos Neurônios Assunto Da Próxima Semana: Medula Espinhal e NervosDocumento5 páginasAssunto: Fisiologia Dos Neurônios Assunto Da Próxima Semana: Medula Espinhal e NervosMarina Clemente100% (1)
- Neuroanatomia: Neurônios, Sinapses e NeurotransmissoresDocumento17 páginasNeuroanatomia: Neurônios, Sinapses e NeurotransmissoresIsabela BertoncelloAinda não há avaliações
- Aula 4 - Farmacologia Do Sistema Nervoso Autônomo e Motor SomáticoDocumento69 páginasAula 4 - Farmacologia Do Sistema Nervoso Autônomo e Motor SomáticoFisio BooksAinda não há avaliações
- Neurofisiologia celular: potencial de ação e membrana celularDocumento2 páginasNeurofisiologia celular: potencial de ação e membrana celularIvone Pires PortoAinda não há avaliações
- Princípios de Neurociência - Kandel 5a EdDocumento40 páginasPrincípios de Neurociência - Kandel 5a EdcarlosAinda não há avaliações
- GABARITODocumento6 páginasGABARITOMarcio CastroAinda não há avaliações
- Aula JNMDocumento47 páginasAula JNMLarissa DuarteAinda não há avaliações
- Codigo Tuss Infiltração Ponto Gatilho - Pesquisa GoogleDocumento1 páginaCodigo Tuss Infiltração Ponto Gatilho - Pesquisa Googledamary.floresAinda não há avaliações
- Cerebelo Fisioterapia - 2018Documento42 páginasCerebelo Fisioterapia - 2018Johnathan QuariguasíAinda não há avaliações
- Caso Clínico (Aula 3 - Parte 1) - AlunosDocumento6 páginasCaso Clínico (Aula 3 - Parte 1) - AlunoslaoftupAinda não há avaliações
- Vias Piramidais e ExtrapiramidaisDocumento22 páginasVias Piramidais e ExtrapiramidaisJunio Alves de LimaAinda não há avaliações
- Mapasmentais NeuroDocumento199 páginasMapasmentais NeuroDante FilhoAinda não há avaliações
- Resumo Geriatria p2 - Sistema NervosoDocumento16 páginasResumo Geriatria p2 - Sistema NervosoNeillyan CarvalhoAinda não há avaliações
- Atividade SISTEMA NERVOSODocumento5 páginasAtividade SISTEMA NERVOSOwillian silvaAinda não há avaliações
- Aula Sistema Nervoso Sensorial I NickDocumento22 páginasAula Sistema Nervoso Sensorial I NickCarlos Eduardo Silva pimentaAinda não há avaliações
- Transmissão Sináptica-Abreu Dias Felino SombeDocumento18 páginasTransmissão Sináptica-Abreu Dias Felino SombeAbreuAinda não há avaliações
- Slide Tronco EncefálicoDocumento17 páginasSlide Tronco EncefálicoCamille LanesAinda não há avaliações
- Exercicio de Fixação - Sistema NervorsoDocumento5 páginasExercicio de Fixação - Sistema NervorsoYuri Jivago RibeiroAinda não há avaliações
- Psi Co Farm Acolo GiaDocumento113 páginasPsi Co Farm Acolo GiaHabilita SKY SE - ALAinda não há avaliações
- PLANO DE AULA Sistema NervosoDocumento2 páginasPLANO DE AULA Sistema NervosoElisa Caroline da S. Santos IkegamiAinda não há avaliações
- Mecanismos de Busca de Referências Bibliográficas UC1Documento3 páginasMecanismos de Busca de Referências Bibliográficas UC1Amanda Paganini LourenciniAinda não há avaliações
- Neurofisiologia - ResumoDocumento78 páginasNeurofisiologia - Resumofejare2171Ainda não há avaliações
- Fisiologia Do Sistema Nervoso Central Vet 2023Documento3 páginasFisiologia Do Sistema Nervoso Central Vet 2023Beatriz DaruishAinda não há avaliações
- Fisiologia ResumoDocumento7 páginasFisiologia ResumoBianca SartiAinda não há avaliações
- 2.1 Estruturas e Divisão Anatômica Da MedulaDocumento42 páginas2.1 Estruturas e Divisão Anatômica Da MedulacarolinamarinhoguiAinda não há avaliações
- Aula 01 - Sistema Nervoso (SNC)Documento76 páginasAula 01 - Sistema Nervoso (SNC)rossafakaellane0Ainda não há avaliações
- Caderno Anestesio FinalDocumento36 páginasCaderno Anestesio FinalFati ZapataAinda não há avaliações
- Neural - Engineering-Neurofisiologia - TraduçãoDocumento59 páginasNeural - Engineering-Neurofisiologia - TraduçãohienkaiAinda não há avaliações
- Procedimentos ICD 10Documento2.925 páginasProcedimentos ICD 10Susana CoutoAinda não há avaliações
- Jose Carlos Dos Santos - 18 - 10 - 33Documento7 páginasJose Carlos Dos Santos - 18 - 10 - 33fernanzildaAinda não há avaliações
- Sistema Nervoso Autônomo FarmacologiaDocumento7 páginasSistema Nervoso Autônomo Farmacologiaisis.emc01Ainda não há avaliações
- Estudo Dirigido SIstema NervosoDocumento5 páginasEstudo Dirigido SIstema NervosoFrancisco AlessandroAinda não há avaliações
- Exercicio Prã©-Prova AB 2S.2023 BioeletrDocumento4 páginasExercicio Prã©-Prova AB 2S.2023 BioeletrbrenojunkmailAinda não há avaliações
- Sistema NervosoDocumento2 páginasSistema NervosoMarcelo OliveiraAinda não há avaliações
- NervosoDocumento31 páginasNervosoMagly SilvaAinda não há avaliações
- Neurônio e SinapseDocumento4 páginasNeurônio e SinapseMaria LuizaAinda não há avaliações
- Simetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaNo EverandSimetria Molecular III: Série Didática para o apoio a formação de professores de QuímicaAinda não há avaliações
- Práticas de Genética, Biologia Molecular, Biotecnologia e EvoluçãoNo EverandPráticas de Genética, Biologia Molecular, Biotecnologia e EvoluçãoNota: 4 de 5 estrelas4/5 (1)
- Uma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNo EverandUma viagem pelo cérebro: A via rápida para entender neurociência: 1ª edição revisada e atualizadaNota: 4 de 5 estrelas4/5 (13)
- Química da Cerveja: Uma Abordagem Química e Bioquímica das Matérias-Primas, Processo de Produção e da Composição dos Compostos de Sabores da CervejaNo EverandQuímica da Cerveja: Uma Abordagem Química e Bioquímica das Matérias-Primas, Processo de Produção e da Composição dos Compostos de Sabores da CervejaAinda não há avaliações
- Para Gostar de Química: Introdução à Química GeralNo EverandPara Gostar de Química: Introdução à Química GeralAinda não há avaliações
- Equilíbrio iônico: aplicações em química analíticaNo EverandEquilíbrio iônico: aplicações em química analíticaAinda não há avaliações
- Uma breve história da química: Da alquimia às ciências moleculares modernasNo EverandUma breve história da química: Da alquimia às ciências moleculares modernasAinda não há avaliações
- Detetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseNo EverandDetetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseAinda não há avaliações
- Série Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNo EverandSérie Didática para o Apoio a Formação de Professores de Química: Volume 2: MoléculasNota: 5 de 5 estrelas5/5 (1)
- Uso do Policloreto de Alumínio (PAC): vantagens sobre o Sulfato de Alumínio em sistema de tratamento de águaNo EverandUso do Policloreto de Alumínio (PAC): vantagens sobre o Sulfato de Alumínio em sistema de tratamento de águaAinda não há avaliações
- Problemas de Cinética e Reatores Químicos: 100 Problemas Resolvidos, 500 Problemas Propostos (Com Respostas)No EverandProblemas de Cinética e Reatores Químicos: 100 Problemas Resolvidos, 500 Problemas Propostos (Com Respostas)Ainda não há avaliações
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNo EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteAinda não há avaliações
- Química na Educação Básica: Ferramentas teóricas e práticasNo EverandQuímica na Educação Básica: Ferramentas teóricas e práticasNota: 4 de 5 estrelas4/5 (1)
- Princípios de química analítica: Abordagem teórica qualitativa e quantitativaNo EverandPrincípios de química analítica: Abordagem teórica qualitativa e quantitativaNota: 5 de 5 estrelas5/5 (1)
- Reatores Químicos em Leito Fluidizado: modelagem e simulaçãoNo EverandReatores Químicos em Leito Fluidizado: modelagem e simulaçãoAinda não há avaliações
- Reologia do Concreto: Fatores influentes para previsão da retração e fluênciaNo EverandReologia do Concreto: Fatores influentes para previsão da retração e fluênciaAinda não há avaliações
- Química em tubos de ensaio: uma abordagem para principiantesNo EverandQuímica em tubos de ensaio: uma abordagem para principiantesAinda não há avaliações