Escolar Documentos
Profissional Documentos
Cultura Documentos
Unidade 5 - Evaporadores Parte 3
Enviado por
Daniel Nóbrega0 notas0% acharam este documento útil (0 voto)
33 visualizações11 páginasEste documento discute operações unitárias relacionadas a evaporadores. Explica como a presença de solutos eleva o ponto de ebulição de uma solução em comparação com o solvente puro, requerendo uma temperatura maior para ebulição. Também apresenta o diagrama de Düring como uma ferramenta para calcular a temperatura de ebulição de soluções a diferentes concentrações.
Descrição original:
Título original
Unidade_5_-_Evaporadores_parte_3
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoEste documento discute operações unitárias relacionadas a evaporadores. Explica como a presença de solutos eleva o ponto de ebulição de uma solução em comparação com o solvente puro, requerendo uma temperatura maior para ebulição. Também apresenta o diagrama de Düring como uma ferramenta para calcular a temperatura de ebulição de soluções a diferentes concentrações.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
33 visualizações11 páginasUnidade 5 - Evaporadores Parte 3
Enviado por
Daniel NóbregaEste documento discute operações unitárias relacionadas a evaporadores. Explica como a presença de solutos eleva o ponto de ebulição de uma solução em comparação com o solvente puro, requerendo uma temperatura maior para ebulição. Também apresenta o diagrama de Düring como uma ferramenta para calcular a temperatura de ebulição de soluções a diferentes concentrações.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 11
OPERAÇÕES UNITÁRIAS II
UNIDADE 4 - EVAPORADORES
Professora responsável: MA. Anna Letícia
ELEVAÇÃO DO PONTO DE EBULIÇÃO
• A P vap de uma solução é menor que a do solvente puro na mesma
temperatura.
• Para certa pressão de operação, a Te da solução é MAIOR que a
do solvente puro.
• A solução dentro do evaporador, com o passar do tempo, tem-se a
concentração de sólidos e consequentemente tem o AUMENTO
DO PONTO DE EBULIÇÃO (EPE).
ELEVAÇÃO DO PONTO DE EBULIÇÃO
Aparecem em processos como:
Produção de açúcar durante a concentração do caldo p/
posterior cristalização;
Caldo de cana Melaço Açúcar
ELEVAÇÃO DO PONTO DE EBULIÇÃO
• EPE é função da concentração e do tipo do soluto.
• EPE ↓: soluções diluídas ou de material orgânico;
• EPE ↑: soluções de compostos inorgânicos (podendo atingir até
80°C).
• Regra para o cálculo de evaporadores: Duhring
A Teb de uma dada solução a dada concentração é
uma função linear da Teb do solvente puro na mesma
pressão
ELEVAÇÃO DO PONTO DE EBULIÇÃO
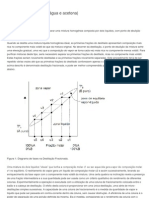
Diagrama de fases para substância pura.
Adiciona SOLUTO não volátil ao SOLVENTE líquido, 𝑃𝑣𝑎𝑝. ↓ 𝑎 → 𝑏
aumentando a temperatura de ebulição da solução.
𝐸𝑃𝐸 = (𝑇𝑏′ − 𝑇𝑏 )
DIAGRAMA DE DÜRING,
• Para se utilizar o Diagrama de Düring, procede-se da seguinte
maneira:
• Determinar a pressão de funcionamento do evaporador;
• Entrar numa tabela de vapor d’água SATURADO e determinar a
temperatura de ebulição da água pura, correspondente a esta
pressão;
• Entrar com esta temperatura no diagrama e, usando a curva
correspondente à concentração da solução que sai do evaporador,
determinar a temperatura de ebulição da solução .
ELEVAÇÃO DO PONTO DE EBULIÇÃO
REGRA DE DUHRING.
𝐸𝑃𝐸 = (𝑇𝑏′ − 𝑇𝑏 )
Diagrama de During para suco de uva.
REGRA DE DUHRING.
Elevação da temperatura de ebulição (EPE) de soluções de sacarose
EFEITO DA ALTURA DE LÍQUIDO
(CARGA HIDROSTÁTICA)
• Denomina-se EH — EPE por efeito hidrostático — ao fato de a
Te em um ponto situado abaixo da superfície do líquido ser maior
do que aquele da superfície. Esse efeito será mais pronunciado
quanto maior a profundidade e quanto maior a velocidade no
tubo. Dessa maneira, tem-se a diminuição da diferença de
temperatura entre o vapor e a solução, reduzindo assim a
capacidade de evaporação.
REFERÊNCIAS BIBLIOGRÁFICAS
TADINI, C.C.; TELIS, V.R.N.; MEIRELLES, A.J.D.; FILHO, P.A.P. OPERAÇÕES UNITÁRIAS NA
INDÚSTRIA DE ALIMENTOS. VOL. 01. LTC- LIVROS TÉCNICOS E CIENTÍFICOS EDITORA S.A.
RIO DE JANEIRO RJ, 2018. Capítulo 11. Disponível em:
https://integrada.minhabiblioteca.com.br/#/books/978-85-216-3034-
0/cfi/6/2!/4/2/2@0:0
MEIRELLES, M.A.A; PEREIRA, C. G. FUNDAMENTOS DE ENGENHARIA DE
ALIMENTOS. VOL. 06. ATHENEU. SÃO PAULO SP, 2013. Capítulo 17.
Você também pode gostar
- Evaporadores Aulas 2014Documento76 páginasEvaporadores Aulas 2014Joana Cordeiro100% (1)
- Evaporadores Aulas 2014Documento76 páginasEvaporadores Aulas 2014Alan Icaro100% (7)
- Plant AsDocumento24 páginasPlant AsSabrina GonçalvesAinda não há avaliações
- FQExpServ P6 Ebuliometria PDFDocumento4 páginasFQExpServ P6 Ebuliometria PDFAntonio Roque CardosoAinda não há avaliações
- Evaporação SeminarioDocumento36 páginasEvaporação SeminarioJoana CordeiroAinda não há avaliações
- Prática IV - Propriedades ColigativasDocumento4 páginasPrática IV - Propriedades ColigativasRafael ConceiçãoAinda não há avaliações
- Aula 2 - Propriedades ColigativasDocumento44 páginasAula 2 - Propriedades ColigativasBeatriz NunesAinda não há avaliações
- 5-Solucoes e SeparacaoDocumento6 páginas5-Solucoes e SeparacaoAdriano FuriniAinda não há avaliações
- Aula 03. Propriedades ColigativasDocumento58 páginasAula 03. Propriedades ColigativasPaulo WagnnerAinda não há avaliações
- Resumo Das Propriedades Coligativas Das SoluçõesDocumento10 páginasResumo Das Propriedades Coligativas Das SoluçõesJEFERSON SILVESTREAinda não há avaliações
- EvaporacaoDocumento17 páginasEvaporacaoThiago LuchetaAinda não há avaliações
- Evaporadores - Engenharia QuímicaDocumento34 páginasEvaporadores - Engenharia QuímicaFernanda DiasAinda não há avaliações
- Propriedades Coligativas 3serie PDFDocumento9 páginasPropriedades Coligativas 3serie PDFSthefany Raniery Costa SilvaAinda não há avaliações
- Aula 39 e 40 - 11 Classe - 2022 - Cópia - CópiaDocumento5 páginasAula 39 e 40 - 11 Classe - 2022 - Cópia - CópiaJosemarAinda não há avaliações
- Propriedades ColigativasDocumento28 páginasPropriedades Coligativasmatson0806Ainda não há avaliações
- DESTILAÇÃO1Documento10 páginasDESTILAÇÃO1Roberta BelazAinda não há avaliações
- EvaporadorDocumento6 páginasEvaporadorWilliam Ricardo RosaAinda não há avaliações
- Aula de Propriedades Coligativas em Power Point Pronta 23.08.2023Documento26 páginasAula de Propriedades Coligativas em Power Point Pronta 23.08.2023BrunodsAinda não há avaliações
- Relatório 3 - PressãoDocumento11 páginasRelatório 3 - PressãoMatheus RossiniAinda não há avaliações
- Destilação Fracionada e Destilação Por Arraste de VaporDocumento13 páginasDestilação Fracionada e Destilação Por Arraste de VaporNatáliaCabralAinda não há avaliações
- Propriedades ColigativasDocumento40 páginasPropriedades ColigativasKarina Vitti KleinAinda não há avaliações
- Relatório Inorganica I (Vinho)Documento8 páginasRelatório Inorganica I (Vinho)mauricelioaraujoAinda não há avaliações
- Aula 1 - Pré Evaporação e Evaporação Do Caldo em Usinas de AçúcarDocumento30 páginasAula 1 - Pré Evaporação e Evaporação Do Caldo em Usinas de AçúcardiegoceccatoAinda não há avaliações
- Propriedades ColigativasDocumento2 páginasPropriedades ColigativasIzabela OliveiraAinda não há avaliações
- Recuperação de Etanol Por Destilação Com RefluxoDocumento15 páginasRecuperação de Etanol Por Destilação Com Refluxoclaudia PozzerAinda não há avaliações
- Relatorio Destilação Simples e FracionadaDocumento11 páginasRelatorio Destilação Simples e FracionadaVictor MarquesAinda não há avaliações
- 7898-2 - PROPRIEDADES COLIGATIVAS - Propriedades ColigativasDocumento9 páginas7898-2 - PROPRIEDADES COLIGATIVAS - Propriedades ColigativasMarcelo GfteamAinda não há avaliações
- Exercícios Sobre Propriedades ColigativasDocumento8 páginasExercícios Sobre Propriedades ColigativasCarlos LiraAinda não há avaliações
- PropriedadescoligativasDocumento33 páginasPropriedadescoligativasRonielson DamascenoAinda não há avaliações
- Relatório de Química 12º - Destilação SimplesDocumento5 páginasRelatório de Química 12º - Destilação SimplesLinteloth0% (1)
- Apostila Química 3 - Propriedades ColigativasDocumento7 páginasApostila Química 3 - Propriedades ColigativasGeilson SilvaAinda não há avaliações
- Aula Experimental Coeficiente de SolubilidadeDocumento2 páginasAula Experimental Coeficiente de SolubilidadeAstronáuta AstroAinda não há avaliações
- EBULIOSCOPIA Turma 305Documento1 páginaEBULIOSCOPIA Turma 305Isadora Camporese Schuster100% (1)
- Propriedas Cognitivas - Química - 4 UnidadeDocumento28 páginasPropriedas Cognitivas - Química - 4 Unidadegab alvesAinda não há avaliações
- Relatório DestilaçãoDocumento13 páginasRelatório DestilaçãoerickiyotaAinda não há avaliações
- Apresentação DestilaçãoDocumento29 páginasApresentação DestilaçãoRuiGonçalvesAinda não há avaliações
- Química Lista 02 - Propriedades ColigativasDocumento14 páginasQuímica Lista 02 - Propriedades ColigativasHugo CimehrioAinda não há avaliações
- Capítulo - 11 - Propriedades - Coligativas 2Documento16 páginasCapítulo - 11 - Propriedades - Coligativas 2Amanda TravassoAinda não há avaliações
- Artigo EbuliometriaDocumento4 páginasArtigo EbuliometriaRaquel NamiAinda não há avaliações
- Destilação Simples - Victor GuedesDocumento6 páginasDestilação Simples - Victor GuedesVictor GuedesAinda não há avaliações
- Trabalho de Des ColigativasDocumento10 páginasTrabalho de Des ColigativasJorgenilson SandraAinda não há avaliações
- Relatório Propriedades ColigativasDocumento9 páginasRelatório Propriedades ColigativasBruna Avelar100% (1)
- Destilaçao Por Arraste de VaporDocumento14 páginasDestilaçao Por Arraste de VaporMary DegoAinda não há avaliações
- Propriedades ColigativasDocumento19 páginasPropriedades ColigativasJuliano SmaAinda não há avaliações
- FQ Cap1Documento10 páginasFQ Cap1filipelima.graveAinda não há avaliações
- 1 - Propriedades Das Soluções Ou Propriedades ColigativasDocumento22 páginas1 - Propriedades Das Soluções Ou Propriedades ColigativasAdriana SilvaAinda não há avaliações
- Relatório 12 Ponto de EbuliçãoDocumento7 páginasRelatório 12 Ponto de EbuliçãojosiedoliAinda não há avaliações
- Destilação FracionadaDocumento5 páginasDestilação FracionadaEdu AntunesAinda não há avaliações
- Aula 11-12Documento34 páginasAula 11-12Bruna GarciaAinda não há avaliações
- Aula Propriedades ColigativasDocumento16 páginasAula Propriedades ColigativasDudaAinda não há avaliações
- Extração Com Solventes Reinaldo - CópiaDocumento15 páginasExtração Com Solventes Reinaldo - CópiaLucimara MagalhaesAinda não há avaliações
- Propriedades Coligativas - IfrnDocumento42 páginasPropriedades Coligativas - Ifrnvictor.costa1Ainda não há avaliações
- Destilação FlashDocumento47 páginasDestilação FlashMichael Lima100% (1)
- Determinação Da Capacidade Tamponante de Soluções TampõesDocumento3 páginasDeterminação Da Capacidade Tamponante de Soluções TampõesGeovane SouzaAinda não há avaliações
- Curso DestilaçãoDocumento118 páginasCurso DestilaçãoLino Cleber GregorioAinda não há avaliações
- Projetos Em Clp Ladder Baseado No Twidosuite Parte XiiNo EverandProjetos Em Clp Ladder Baseado No Twidosuite Parte XiiAinda não há avaliações
- Projetos Com Esp8266 Programado Em Lua - Parte XxiNo EverandProjetos Com Esp8266 Programado Em Lua - Parte XxiAinda não há avaliações
- Prova AP1Documento1 páginaProva AP1Daniel NóbregaAinda não há avaliações
- Lista-2 OP1 2018-2Documento8 páginasLista-2 OP1 2018-2Daniel NóbregaAinda não há avaliações
- OP1 CapítuloV Agita e MisturaDocumento129 páginasOP1 CapítuloV Agita e MisturaDaniel NóbregaAinda não há avaliações
- Lista 1 - OP1 - 2019 2Documento6 páginasLista 1 - OP1 - 2019 2Daniel NóbregaAinda não há avaliações
- OP1 CapítuloX SedimentaçãoDocumento27 páginasOP1 CapítuloX SedimentaçãoDaniel NóbregaAinda não há avaliações
- OP1 - Capítulo II - Caracterização de PartículasDocumento63 páginasOP1 - Capítulo II - Caracterização de PartículasDaniel NóbregaAinda não há avaliações
- OP1 CapítuloVI SeparaçãoCampoGravitacional CâmarasDocumento26 páginasOP1 CapítuloVI SeparaçãoCampoGravitacional CâmarasDaniel NóbregaAinda não há avaliações
- OP1 Cap - VII Separação-ForçaCentrífuga 2019-2Documento81 páginasOP1 Cap - VII Separação-ForçaCentrífuga 2019-2Daniel NóbregaAinda não há avaliações
- OP1 CapítuloIII Dinâmica Da Partícula 2020-1Documento36 páginasOP1 CapítuloIII Dinâmica Da Partícula 2020-1Daniel NóbregaAinda não há avaliações
- OP1 CapítuloIX Teoria e Prática Da FiltraçãoDocumento79 páginasOP1 CapítuloIX Teoria e Prática Da FiltraçãoDaniel NóbregaAinda não há avaliações
- Unidade 4 - Condensadores EXEMPLO 8.2 Refrigerao IndustrialDocumento11 páginasUnidade 4 - Condensadores EXEMPLO 8.2 Refrigerao IndustrialDaniel NóbregaAinda não há avaliações
- 229 661 1 PBDocumento23 páginas229 661 1 PBDaniel NóbregaAinda não há avaliações
- Analisador de GasesDocumento2 páginasAnalisador de GasesDaniel NóbregaAinda não há avaliações
- Analisador de Gases - ConforDocumento2 páginasAnalisador de Gases - ConforDaniel NóbregaAinda não há avaliações
- Unidade 5 - Evaporadores Parte 2 - EXEMPLO CORRIGIDODocumento38 páginasUnidade 5 - Evaporadores Parte 2 - EXEMPLO CORRIGIDODaniel Nóbrega100% (1)
- Técnicas de ExtraçãoDocumento92 páginasTécnicas de ExtraçãoTiago RafaelAinda não há avaliações
- Relatorio Síntese e Purificação Da AcetanilidaDocumento10 páginasRelatorio Síntese e Purificação Da AcetanilidaDavi Alex NogueiraAinda não há avaliações
- Soluto e SolventeDocumento8 páginasSoluto e SolventeDanielle ToscanoAinda não há avaliações
- Simulado 1ano - QuimicaDocumento3 páginasSimulado 1ano - QuimicaedsonAinda não há avaliações
- Vidrarias e Segurança No LaboratórioDocumento14 páginasVidrarias e Segurança No LaboratórioLeticia ClementeAinda não há avaliações
- Fispq Mobil Super 1000 20W-50Documento10 páginasFispq Mobil Super 1000 20W-50edison juniorAinda não há avaliações
- Química - FGVDocumento6 páginasQuímica - FGVLucas FaeddaAinda não há avaliações
- 2-Substituição Nucleofílica Alifática - Clayton - 2Documento86 páginas2-Substituição Nucleofílica Alifática - Clayton - 2Mateus Ramos100% (1)
- Especificação Técnica - Solbrax ECO 230-260Documento1 páginaEspecificação Técnica - Solbrax ECO 230-260Junior MalheiroAinda não há avaliações
- Apostila QO1Documento47 páginasApostila QO1JubsAinda não há avaliações
- Análise de Alcalinidade em PercloroetilenoDocumento2 páginasAnálise de Alcalinidade em PercloroetilenoAlessandra FerreiraAinda não há avaliações
- As Técnicas - 1. Segurança No Laboratorio-MescladoDocumento146 páginasAs Técnicas - 1. Segurança No Laboratorio-MescladoPietra MatosAinda não há avaliações
- 16-Manual Enquip IDocumento34 páginas16-Manual Enquip IMarcus Vinicius Ribeiro GomesAinda não há avaliações
- 03-Novas TecnologiasDocumento63 páginas03-Novas TecnologiasezequieltoniAinda não há avaliações
- Propriedades ColigativasDocumento29 páginasPropriedades ColigativasGleisonAinda não há avaliações
- Aula Reacao Substituicao SN1 e SN2Documento53 páginasAula Reacao Substituicao SN1 e SN2Matheus SilvaAinda não há avaliações
- Apostila - Análise Química Qualitativa e QuantitativaDocumento29 páginasApostila - Análise Química Qualitativa e QuantitativaLourisvan CostaAinda não há avaliações
- Relatório SolubilidadeDocumento13 páginasRelatório SolubilidadeInaiara CasapulaAinda não há avaliações
- 04 PE - Extração Da CafeínaDocumento6 páginas04 PE - Extração Da CafeínaVitória MedeirosAinda não há avaliações
- (Lista de Exercícios 4) Balanços de Massa em Processos Com Múltiplas UnidadesDocumento8 páginas(Lista de Exercícios 4) Balanços de Massa em Processos Com Múltiplas UnidadesDiniz SilvaAinda não há avaliações
- Nbr14598 - Ponto de FulgorDocumento26 páginasNbr14598 - Ponto de FulgorDanilo Kronka100% (1)
- Metodos de Determinacao Da Massa MolarDocumento28 páginasMetodos de Determinacao Da Massa MolarCaio CésarAinda não há avaliações
- Lab IIDocumento4 páginasLab IIRayssa Alves BadaroAinda não há avaliações
- Densidade e SolubilidadeDocumento7 páginasDensidade e SolubilidadeThayane WilmsenAinda não há avaliações
- 09 Importancia Da Agua e Suas Propriedades para A Vida 1Documento11 páginas09 Importancia Da Agua e Suas Propriedades para A Vida 1Fabio RiemannAinda não há avaliações
- Cuidado em Uma Analise de HPLCDocumento19 páginasCuidado em Uma Analise de HPLCMatheus Dal CimAinda não há avaliações
- XIRTEC 24 Laranja Cimento de Baixo VOC para Tubulações Plásticas CPVCDocumento2 páginasXIRTEC 24 Laranja Cimento de Baixo VOC para Tubulações Plásticas CPVCKaka PoerschkeAinda não há avaliações
- Pré Lab - Extração AtivaDocumento3 páginasPré Lab - Extração AtivaMelina FernandesAinda não há avaliações
- Propriedades em Compostos OrgânicosDocumento21 páginasPropriedades em Compostos Orgânicoschristiane camposAinda não há avaliações
- Relatórios Das Aulas Práticas de FarmacognosiaDocumento4 páginasRelatórios Das Aulas Práticas de FarmacognosiamarianaAinda não há avaliações