Escolar Documentos
Profissional Documentos
Cultura Documentos
Módulo 08 Apli Lei Eq Qui Sist Homog
Enviado por
Daniel SantosDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Módulo 08 Apli Lei Eq Qui Sist Homog
Enviado por
Daniel SantosDireitos autorais:
Formatos disponíveis
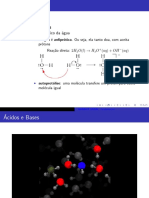
ÁCIDOS E BASES FRACOS:
Cálculo do pH de um ácido fraco:
Sabendo a concentração formal (F) do ácido HA, e o Ka,
temos:
* Concentração formal é o número de moles de um composto em um
litro. A concentração formal de um ácido refere-se a quantidade total
de HA colocada na solução, independente do fato de algumas
moléculas terem se transformado em A-.
Ka
HA H+ + A-
da água
BALANÇO DE CARGA: [H+] = [A-] + [OH-]
BALANÇO DE MASSA: F = [A-] + [HA]
[H+] . [A-]
EQUILÍBRIOS: Ka =
[HA]
e
Kw = [H+] . [OH-]
MÓDULO:08 pg:01 (Prof. Dr. Jean Karlo Acosta Mendonça)
Existe quatro equações e quatro incógnitas (A-, HA, H+,
OH-), isso resulta em uma equação cúbica, mas nós químicos sabemos
que a concentração de A- é bem maior do que a concentração de OH-
oriunda da dissociação da água. Sendo assim:
[H+] [A-]
Desse modo:
Ka
HA + H2O H+ + A-
início F - -
equilíbrio F-x x x
[H+] . [A-]
Ka =
[HA]
x.x x2
Ka = Ka =
F-x F-x
x = [H+]
MÓDULO:08 pg:02 (Prof. Dr. Jean Karlo Acosta Mendonça)
-
Ka
+ H 2O + H 3 O+
Exemplo 1) Para o ácido -hidroxibenzoico, F = 0,05 M e Ka=1,07 .
10-3,o pH fica:
x2
= 1,07 . 10-3
0,05 - x
x2 + (1,07 . 10-3)x – 5,35 . 10-5 = 0
x = 6,80 . 10-3 (raiz negativa rejeitada)
[H+] = [A-] = x = 6,80 . 10-3 M
[HA] = F – x = 0,0432 M
E o pH: pH = -log 6,8 . 10-3
pH = 2,17
MÓDULO:08 pg:03 (Prof. Dr. Jean Karlo Acosta Mendonça)
A aproximação de [H+] [A-] é justificável?
Kw 1,0 . 10-14
Lembrando que [OH-] = 1,47 . 10-12
[H+] 6,8 . 10-3
Temos então:
[A-] (da dissociação do HA) = 6,8 . 10-3 M
[H+] (da dissociação do HA) = 6,8 . 10-3 M
[OH-] (da dissociação da H2O) = 1,47 . 10-12 M
[H+] (da dissociação do H2O) = 1.47 . 10-12 M
A suposição de que H+ é derivado principalmente de HA é excelente.
FRAÇÃO DE DISSOCIAÇÃO :
nº de moléculas ionizadas
=
nº total de moléculas em solução
Fração de [A-] x x
dissociação = = =
-
[A ] + [HA] F
de um ácido x + (F-x)
Para o exemplo 1 do ácido -hidroxibenzoico:
x 6,8 x 10-3
= = = 0,136
F 0,05
Isto é, o ácido está 13,6% dissociado numa mesma
concentração formal de 0,05
MÓDULO:08 pg:04 (Prof. Dr. Jean Karlo Acosta Mendonça)
EQUILÍBRIO DE BASE FRACA : (mesmo raciocínio)
Kb [BH+] . [OH-]
B + H2O BH+ + OH- Kb =
[B]
Supondo que todos os [OH-] são provenientes da reação de
B + H2O, e poucos são resultantes da dissociação da H2O. Então [OH-]
= [BH+] = x e F= [B] + [BH+]
[BH+] . [OH-] x.x x2
Kb = = Kb =
[B] F-x F-x
x = [OH-]
Exemplo 2) A base fraca cocaína tem Kb= 2,6 . 10-6 e concentração formal
de 0,037 M, qual o seu pH?
CH3 O CH3 O
:N +
OCCH3 H N OCCH3
H H
+ H2 O + OH-
O O
OCC6H5 OCC6H5
H H
B + H2 O BH+ + OH-
MÓDULO:08 pg:05 (Prof. Dr. Jean Karlo Acosta Mendonça)
Sendo assim:
B + H2 O BH+ + OH-
0,037 – x x x
x2
= 2,6 . 10-6 x = 3,1 . 10-4
0,037 – x
Como x = [OH-]
Kw 1,0 . 10-14
[H+] = 3,22 . 10-11
-
[OH ] 3,1 . 10-4
pH = -log [H+] = 10,49
Fração de [BH+] x 3,1 . 10-4
associação = = = 0,0083
de uma base
+
[B] + [BH ] F 0,037
Então, somente 0,83 % da base reagiu.
MÓDULO:08 pg:06 (Prof. Dr. Jean Karlo Acosta Mendonça)
ÁCIDOS E BASES CONJUGADOS:
A base conjugada de um ácido fraco é uma base fraca, e o ácido
conjugado de uma base fraca é um ácido fraco.
Ka . Kb = Kw
Exemplo 3) Encontre o pH de uma solução de amônia 0,1 M
Kb
NH3 + H2O NH4+ + OH-
Ka
amônia amônio
F–x x x
O pKa para o amônio é 9,244 portanto Kb para NH3 é:
Kw 1,0 . 10-14
Kb = = = 1,75 . 10-5
Ka 10-9,244
O pH da amônia:
[NH4+] . [OH-] x2
Kb =
[NH3] 0,1 - x
x = [OH-] = 1,31 . 10-3 M
Kw 1,0 . 10-14
[H+] = = = 7,61 . 10-12
[OH-] 1,31 . 10-3
pH = -log [H+] = 11,12
MÓDULO:08 pg:07 (Prof. Dr. Jean Karlo Acosta Mendonça)
Você também pode gostar
- Módulo 09 Equações de Comp FracionadaDocumento9 páginasMódulo 09 Equações de Comp FracionadaDaniel SantosAinda não há avaliações
- Equilíbrio de Bases e Ácidos Fracos: Flávia MarquesDocumento25 páginasEquilíbrio de Bases e Ácidos Fracos: Flávia MarquesLuany Souza CoelhoAinda não há avaliações
- Ácido BaseDocumento9 páginasÁcido BaseJuhrosaAinda não há avaliações
- AULA 2 PH e TampõesDocumento21 páginasAULA 2 PH e TampõesBeni QuímicoAinda não há avaliações
- Equilíbrio IônicoDocumento28 páginasEquilíbrio IônicoakafsAinda não há avaliações
- CAPitulo 10 - EQUILBRIO INICODocumento18 páginasCAPitulo 10 - EQUILBRIO INICOnayane mendesAinda não há avaliações
- Lista Equilibrio Acido Base FINALDocumento14 páginasLista Equilibrio Acido Base FINALgabihsabaAinda não há avaliações
- Aula Soluções (PH e pOH) ..EXCELENTE - Professor Rikardo CoimbraDocumento3 páginasAula Soluções (PH e pOH) ..EXCELENTE - Professor Rikardo CoimbraRicardo Coimbra100% (2)
- Aula Phmetria Retomada 2020.1Documento25 páginasAula Phmetria Retomada 2020.1JOSE ROBERTO DA CRUZAinda não há avaliações
- Atividade PHDocumento3 páginasAtividade PHERIK CESARAinda não há avaliações
- POLIPRÓTICOSDocumento22 páginasPOLIPRÓTICOSJoãoAinda não há avaliações
- Slide2 - Equilíbrio Ácido-Base em Solução Aquosa - Aula - 2Documento33 páginasSlide2 - Equilíbrio Ácido-Base em Solução Aquosa - Aula - 2Luana Silva FerreiraAinda não há avaliações
- Quimica EngAmb-05acidosebasesDocumento23 páginasQuimica EngAmb-05acidosebasesJoão PauloAinda não há avaliações
- Equilíbrio Iônico AquosoDocumento136 páginasEquilíbrio Iônico AquosoThiago Brito de Almeida PROFESSORAinda não há avaliações
- Equilíbrio Ácido-Base - PARTE 1Documento26 páginasEquilíbrio Ácido-Base - PARTE 1JoãoAinda não há avaliações
- Aula 4 05 - 12 - 23Documento9 páginasAula 4 05 - 12 - 23ANIBAL MIGUEZ DOS SANTOSAinda não há avaliações
- Equilíbrio Ácido BaseDocumento21 páginasEquilíbrio Ácido BaseDouglas SantosAinda não há avaliações
- Aula Solução TampãoDocumento19 páginasAula Solução TampãoClaudia MachadoAinda não há avaliações
- Exercícios Ácido-Base - SoluçõesDocumento11 páginasExercícios Ácido-Base - Soluçõessimon diaz scharffAinda não há avaliações
- Equilíbrio Químico - 2023 - Equilíbrio Iônico ExercíciosDocumento6 páginasEquilíbrio Químico - 2023 - Equilíbrio Iônico ExercícioscradogodAinda não há avaliações
- Slide Equilibrio Acido BaseDocumento44 páginasSlide Equilibrio Acido BaseÍcaro MychelAinda não há avaliações
- Aula Nº 14 e 15 Acido-Base Semana 7 Nov A 11 NovDocumento16 páginasAula Nº 14 e 15 Acido-Base Semana 7 Nov A 11 NovJohn KilyanAinda não há avaliações
- Equilíbrio IônicoDocumento7 páginasEquilíbrio IônicoWellingtonAinda não há avaliações
- Revisao Metodos Numericos IterativosDocumento1 páginaRevisao Metodos Numericos IterativosAna CarolinaAinda não há avaliações
- Ácido Base 1Documento48 páginasÁcido Base 1fctcrAinda não há avaliações
- 3-Ph e Solução Tampão - Samuel - 2018Documento41 páginas3-Ph e Solução Tampão - Samuel - 2018Carlos Eduardo100% (1)
- VOLUMETRIA DE NEUTRALIZAÇÃO (Modo de Compatibilidade)Documento11 páginasVOLUMETRIA DE NEUTRALIZAÇÃO (Modo de Compatibilidade)Viviane SilvaAinda não há avaliações
- PH e Tampões 1Documento8 páginasPH e Tampões 1Luiz TabordaAinda não há avaliações
- 3 Calculo - de - PH e pOH EQUILIBRIO QUÍMICADocumento12 páginas3 Calculo - de - PH e pOH EQUILIBRIO QUÍMICAOrlando FirmezaAinda não há avaliações
- Aula Hidrólise Parte 1Documento22 páginasAula Hidrólise Parte 1Barteloide Ricardo ErnestoAinda não há avaliações
- Aula de Quarta1Documento27 páginasAula de Quarta1Sabrina sampaioAinda não há avaliações
- Conferencia 2 Port Equilibrio IónicoDocumento43 páginasConferencia 2 Port Equilibrio IónicoMango lavoAinda não há avaliações
- Testo de Apoio Equilibrio QuimicoDocumento18 páginasTesto de Apoio Equilibrio QuimicoMira Luis BasilioAinda não há avaliações
- Exercicios PH e Sistema TampaoDocumento9 páginasExercicios PH e Sistema TampaoAluana Santana CarlosAinda não há avaliações
- Exercicios Resolvidos PH, TampãoDocumento15 páginasExercicios Resolvidos PH, TampãoLucas LeoncioAinda não há avaliações
- Formulario Quimica AnaliticaDocumento2 páginasFormulario Quimica AnaliticaCéliaKaterinaVossosAinda não há avaliações
- Exercicios Sobre Agua e PHDocumento16 páginasExercicios Sobre Agua e PHTed JuniorAinda não há avaliações
- Equilíbrio. Continuação. Prof A Alessandra Smaniotto. QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102BDocumento39 páginasEquilíbrio. Continuação. Prof A Alessandra Smaniotto. QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102BHevertonJonnysAinda não há avaliações
- Problemas de Equilíbrio Químico - Passei Direto3Documento10 páginasProblemas de Equilíbrio Químico - Passei Direto3Vanessa CorreiaAinda não há avaliações
- Aula 7 - Equilíbrio Ácido-BaseDocumento33 páginasAula 7 - Equilíbrio Ácido-BaseAfonso VasconcelosAinda não há avaliações
- Ácido Base 2 e SolubilidadeDocumento40 páginasÁcido Base 2 e SolubilidadefctcrAinda não há avaliações
- Aula 5 Titulação Ácido Base QUI 094 2018 2 NUPISDocumento16 páginasAula 5 Titulação Ácido Base QUI 094 2018 2 NUPISEricson Andre MonteiroAinda não há avaliações
- ResultadosDocumento1 páginaResultadosAlexander CruzAinda não há avaliações
- Resolução Simulado Enem 2023 - 2ºdiaDocumento12 páginasResolução Simulado Enem 2023 - 2ºdiachw8rh4z7bAinda não há avaliações
- Questões 5º Prova FQDocumento8 páginasQuestões 5º Prova FQÍtalo SantosAinda não há avaliações
- Módulo 16 - PH e POH - 3º Bimestre - 2º Ano EMDocumento28 páginasMódulo 16 - PH e POH - 3º Bimestre - 2º Ano EMGabriela LimaAinda não há avaliações
- Atividade Equilibrio IIDocumento6 páginasAtividade Equilibrio IIademairmoreiraAinda não há avaliações
- Chico & Parada Chico & Parada Chico & Parada: R E Q IDocumento17 páginasChico & Parada Chico & Parada Chico & Parada: R E Q ICristiane Soares CardosoAinda não há avaliações
- Ácidos e BasesDocumento13 páginasÁcidos e BasesmiquaiattiAinda não há avaliações
- Captura de Tela 2023-09-01 À(s) 07.25.19Documento20 páginasCaptura de Tela 2023-09-01 À(s) 07.25.19Kamilly SalesAinda não há avaliações
- TemaIV (Aula 2) - Equilibrio Ionico e SolubilidadeDocumento46 páginasTemaIV (Aula 2) - Equilibrio Ionico e SolubilidadeFernando BanzeAinda não há avaliações
- Ácido BaseDocumento8 páginasÁcido BasempedroleesilvaAinda não há avaliações
- Reações Ácido-Base ApresentaçãoDocumento26 páginasReações Ácido-Base ApresentaçãoanaclaudiarosaAinda não há avaliações
- 2024-1 Assunto 01 (PH e Tampoes) APOSTILADocumento22 páginas2024-1 Assunto 01 (PH e Tampoes) APOSTILAGuilherme SpamAinda não há avaliações
- Ácido-Base - Parte 1Documento11 páginasÁcido-Base - Parte 1Maria cunhaAinda não há avaliações
- Ficha Avaliação Moduloq4Documento4 páginasFicha Avaliação Moduloq4daires73Ainda não há avaliações
- Aula 5 07 - 12 - 23Documento9 páginasAula 5 07 - 12 - 23ANIBAL MIGUEZ DOS SANTOSAinda não há avaliações
- Aula Equilibrio Acido Base 1Documento23 páginasAula Equilibrio Acido Base 1placreAinda não há avaliações
- LISTA DE EXERCÍCIOS Ondas - 2 PROVADocumento5 páginasLISTA DE EXERCÍCIOS Ondas - 2 PROVADaniel SantosAinda não há avaliações
- Determina o de PH de Diversas Subst NciaDocumento4 páginasDetermina o de PH de Diversas Subst NciaDaniel SantosAinda não há avaliações
- Gabarito OficialDocumento15 páginasGabarito OficialDaniel SantosAinda não há avaliações
- Elementos Do Grupo 15 e 16Documento5 páginasElementos Do Grupo 15 e 16Daniel SantosAinda não há avaliações
- Ministério Da Educação Secretaria de Educação Profissional E Tecnológica Instituto Federal de Educação, Ciência E Tecnologia de Minas GeraisDocumento5 páginasMinistério Da Educação Secretaria de Educação Profissional E Tecnológica Instituto Federal de Educação, Ciência E Tecnologia de Minas GeraisDaniel SantosAinda não há avaliações
- Prova QUIMICADocumento25 páginasProva QUIMICAELCIO MARINHEIRO DA SILVAAinda não há avaliações
- LISTA DE EXERCÍCIOS - 3 PROVA ADocumento7 páginasLISTA DE EXERCÍCIOS - 3 PROVA ADaniel SantosAinda não há avaliações
- Professor de Educacao Basica QuimicaDocumento13 páginasProfessor de Educacao Basica QuimicaDaniel SantosAinda não há avaliações
- Perguntas Do Artigo - InGLÊSDocumento1 páginaPerguntas Do Artigo - InGLÊSDaniel SantosAinda não há avaliações
- Estatística Aplicada À Química - Aula 1Documento22 páginasEstatística Aplicada À Química - Aula 1Daniel SantosAinda não há avaliações
- 1Documento1 página1Evelyn Alves Nunes SimonettiAinda não há avaliações
- Edital de Gabarito Sme Derh1 PublicadoDocumento15 páginasEdital de Gabarito Sme Derh1 PublicadoDaniel SantosAinda não há avaliações
- Lista de Exercícios 1 - Química de CoordenaçãoDocumento3 páginasLista de Exercícios 1 - Química de CoordenaçãoJ Carlos Junior0% (1)
- QG Aula 5 QuímicaDocumento67 páginasQG Aula 5 QuímicaDaniel SantosAinda não há avaliações
- QG Estrutura Atômico Material ApoioDocumento24 páginasQG Estrutura Atômico Material ApoioDaniel SantosAinda não há avaliações
- Aula 11 Reações SubstituiçãoDocumento54 páginasAula 11 Reações SubstituiçãoDaniel SantosAinda não há avaliações
- Compostos de Coordenação Definições GeraisDocumento8 páginasCompostos de Coordenação Definições GeraisDaniel SantosAinda não há avaliações
- Estatística Aplicada À Química - Aula 4Documento31 páginasEstatística Aplicada À Química - Aula 4Daniel SantosAinda não há avaliações
- Lista de Exercícios Sobre TLVDocumento3 páginasLista de Exercícios Sobre TLVDeivison Santiago0% (1)
- Horario Quimica 2023 2Documento5 páginasHorario Quimica 2023 2Daniel SantosAinda não há avaliações
- Química Inorgânica DescritivaDocumento38 páginasQuímica Inorgânica DescritivaDaniel SantosAinda não há avaliações
- Exercícios Equilíbrio Ácido-BaseDocumento2 páginasExercícios Equilíbrio Ácido-BaseFabio WuAinda não há avaliações
- QG Aula 7 QuímicaDocumento46 páginasQG Aula 7 QuímicaDaniel SantosAinda não há avaliações
- Lista 3 MHS e Ondas - 2020Documento6 páginasLista 3 MHS e Ondas - 2020Daniel SantosAinda não há avaliações
- Fisica Fundamental CompletoDocumento21 páginasFisica Fundamental CompletoDaniel SantosAinda não há avaliações
- Avaliação 2 - EstatisticaDocumento1 páginaAvaliação 2 - EstatisticaDaniel SantosAinda não há avaliações
- Lista de Exercícios 3 - EAQDocumento3 páginasLista de Exercícios 3 - EAQDaniel SantosAinda não há avaliações
- Apostila Ingles Instrumental IIDocumento106 páginasApostila Ingles Instrumental IIRicardo PortoAinda não há avaliações
- Aula 4 - SinteseDocumento1 páginaAula 4 - SinteseDaniel SantosAinda não há avaliações
- Batista 7 14Documento9 páginasBatista 7 14Nicolas BenedictoAinda não há avaliações
- Derivadas ADocumento19 páginasDerivadas ADiego Fernandes do NascimentoAinda não há avaliações
- Ficha de Exploração AL 3.1 - Paineis FotovoltaicosDocumento2 páginasFicha de Exploração AL 3.1 - Paineis Fotovoltaicosandreooos PTAinda não há avaliações
- O Grande Segredo e As Leis Da Atração e Da RepulsãoDocumento18 páginasO Grande Segredo e As Leis Da Atração e Da RepulsãoPaulo Cesar Pfaltzgraff FerreiraAinda não há avaliações
- Cimento Portland (Consistência Normal e Tempo de Início e Fim de Pega)Documento3 páginasCimento Portland (Consistência Normal e Tempo de Início e Fim de Pega)Willian SilvaAinda não há avaliações
- Metodo TabularDocumento20 páginasMetodo TabularKlarc CamachoAinda não há avaliações
- Avaliação de Matemática Geometria Analitica 3º EjaDocumento3 páginasAvaliação de Matemática Geometria Analitica 3º EjaJanio SoaresAinda não há avaliações
- Estruturas de Concreto Armado - ApostilaDocumento240 páginasEstruturas de Concreto Armado - ApostilaGustavo BaggioAinda não há avaliações
- YCON Fissuras 2008 PDFDocumento120 páginasYCON Fissuras 2008 PDFjmariros7903Ainda não há avaliações
- Apostila Elementos de MáquinasDocumento156 páginasApostila Elementos de MáquinasRenan GonçalvesAinda não há avaliações
- Aula 5 - Tópico 3 - Materiais Betuminosos e Revestimentos Betuminosos NoiteDocumento38 páginasAula 5 - Tópico 3 - Materiais Betuminosos e Revestimentos Betuminosos Noitegabriel.san1010Ainda não há avaliações
- Dissertação de Mestrado - ÍtaloMGonçalves - VERSÃO FINALDocumento85 páginasDissertação de Mestrado - ÍtaloMGonçalves - VERSÃO FINALÍtalo Macêdo GonçalvesAinda não há avaliações
- Questionário Da Aula 2: eST-202 - Higiene Do Trabalho (Parte B)Documento2 páginasQuestionário Da Aula 2: eST-202 - Higiene Do Trabalho (Parte B)Nelson Baptista da CruzAinda não há avaliações
- Militarmy Ofilizzola PDFDocumento8 páginasMilitarmy Ofilizzola PDFTeste 01Ainda não há avaliações
- Lista 2 - Resistência ElétricaDocumento2 páginasLista 2 - Resistência Elétricavaldielio6534Ainda não há avaliações
- Laboratorio de Matematica e Fisica - Movimento Retilíneo Uniforme - Mru - Relatório - Unid 1Documento3 páginasLaboratorio de Matematica e Fisica - Movimento Retilíneo Uniforme - Mru - Relatório - Unid 1Kenny RalphAinda não há avaliações
- Treinamentolubrificacaobasicaerolamentos 2005 Modul 091202151156 Phpapp02Documento106 páginasTreinamentolubrificacaobasicaerolamentos 2005 Modul 091202151156 Phpapp02Ronaldo Batista100% (1)
- Ficha N3 Equacoes e Inequacoes ExponenciaisDocumento6 páginasFicha N3 Equacoes e Inequacoes ExponenciaisNelson100% (1)
- Paper Motor Elétrico IIDocumento13 páginasPaper Motor Elétrico IIThiago Camargo100% (1)
- 2022 Cap13 InstabilidadeDocumento85 páginas2022 Cap13 InstabilidadeRafael DiasAinda não há avaliações
- LISTA 4 DE FISICA Leis de Newton PDFDocumento4 páginasLISTA 4 DE FISICA Leis de Newton PDFZandrimAinda não há avaliações
- Atividade AvaliativaDocumento2 páginasAtividade AvaliativaAndre Francisco Alves LemosAinda não há avaliações
- NR 05 - Mapa de RiscosDocumento7 páginasNR 05 - Mapa de RiscosCPSSTAinda não há avaliações
- J.S. Owen - The Influence of Member Orientation On The Resistance of Cross Joints in Square RHS Construction PTDocumento31 páginasJ.S. Owen - The Influence of Member Orientation On The Resistance of Cross Joints in Square RHS Construction PTCaio SantosAinda não há avaliações
- Github LaserDocumento5 páginasGithub LaserJair ArmandoAinda não há avaliações
- Geografia UrbanaDocumento17 páginasGeografia UrbanaUssene AmandeAinda não há avaliações
- EP 5029 R0 FundaçõesDocumento51 páginasEP 5029 R0 FundaçõesLeoLamegoCruelAinda não há avaliações
- Documento 2Documento46 páginasDocumento 2MárcioAinda não há avaliações
- Aula 6 - Geometria SolarDocumento74 páginasAula 6 - Geometria SolarAnthony CavalcanteAinda não há avaliações
- Coeficientes de Recalque Horizontal e Vertical Do SoloDocumento8 páginasCoeficientes de Recalque Horizontal e Vertical Do SoloHenrique Furia SilvaAinda não há avaliações