Escolar Documentos
Profissional Documentos
Cultura Documentos
Flavonoides Protocolo
Enviado por
Matheus Almeida0 notas0% acharam este documento útil (0 voto)
18 visualizações2 páginasEste documento descreve um protocolo para quantificar flavonoides, especificamente quercetina, em brácteas secas de cebola usando espectrofotometria. A metodologia envolve extrair a quercetina com etanol, reagir com nitrito de sódio e cloreto de alumínio, e medir a absorvância. Padrões de quercetina são usados para construir uma curva de calibração e quantificar a quercetina nas amostras.
Descrição original:
Título original
Flavonoides-Protocolo
Direitos autorais
© © All Rights Reserved
Formatos disponíveis
PDF, TXT ou leia online no Scribd
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoEste documento descreve um protocolo para quantificar flavonoides, especificamente quercetina, em brácteas secas de cebola usando espectrofotometria. A metodologia envolve extrair a quercetina com etanol, reagir com nitrito de sódio e cloreto de alumínio, e medir a absorvância. Padrões de quercetina são usados para construir uma curva de calibração e quantificar a quercetina nas amostras.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
0 notas0% acharam este documento útil (0 voto)
18 visualizações2 páginasFlavonoides Protocolo
Enviado por
Matheus AlmeidaEste documento descreve um protocolo para quantificar flavonoides, especificamente quercetina, em brácteas secas de cebola usando espectrofotometria. A metodologia envolve extrair a quercetina com etanol, reagir com nitrito de sódio e cloreto de alumínio, e medir a absorvância. Padrões de quercetina são usados para construir uma curva de calibração e quantificar a quercetina nas amostras.
Direitos autorais:
© All Rights Reserved
Formatos disponíveis
Baixe no formato PDF, TXT ou leia online no Scribd
Você está na página 1de 2
Prática laboratorial: Determinação de
flavonoides na cebola (Allium cepa)
Introdução
Os flavonóides são moléculas
polifenólicas solúveis em água,
contendo 15 átomos de carbono. Os
flavonóides pertencem à família dos
polifenóis. Os flavonóides são
constituídos por dois anéis de benzeno
unidos por uma cadeia com 3C. Um dos
átomos de carbono de cadeia curta está
sempre ligado a um carbono de um dos
anéis de benzeno, quer diretamente ou
através de uma ponte de oxigénio,
formando deste modo um terceiro anel
no meio, que pode ser de cinco ou seis
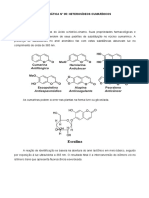
membros. Os flavonóides incluem 6 Figura 1: Estrutura de alguns dos principais subgrupos dos flavonoides.
subgrupos principais: calconas,
flavonas, flavonois, flavanonas,
antocianinas e isoflavonóides (figura
1).
A quercetina é um flavonóide
natural que possui propriedades
farmacológicas (antinflamatória, anti-
carcinogénica, antiviral, anti-histamí-
nica, cardiovascular). Tem massa molar
de 302,236 g/mol e forma complexos
com alumínio (figura 2).
A quercetina apresenta uma
forte banda de absorção a 372 nm. A
adição de Al (III) à solução mostra que
o pico de absorção a 372 nm diminui,
enquanto uma banda centrada em 428
nm aumenta com a quantidade de
metal adicionado até que a proporção
Figura 2: Estrutura molecular da quercetina e dos seus complexos (I e II) com
molar [AICI3]/[Q] seja <0.5 alumínio.
(correspondente ao complexo I). Para
proporções [AICI3]/[Q] ≥ 2.5 a banda de
absorção passa para 456 nm
(correspondente ao complexo II)
(figuras 2 e 3).
A ação antioxidante da quercetina
parece ser uma combinação de reação
com radicais livres e da complexação
com iões metálicos. A quercetina liga
diferentes iões metálicos (Fe2+, Fe3+,
Al3+, Cu2+) e elimina de radicais peroxil
(H2O2) enquanto o seu efeito na
eliminação de radicais OH. é muito
menos importante.
Figura 3: Espectros de absorção da quercetina em metanol na ausência e na
presença de Al (III). As proporções molares [AICI3] / [Q] são indicadas em cada
espectro (Cornard e Merlin, 2002).
Metodologia
A- Quantificação de flavonoides (quercetina)
Preparação do extrato
1. Pesar 0.1g de material vegetal (brácteas secas de cebola roxa ou amarela) e
macerar em almofariz com 10 ml de etanol a 85%. O procedimento deverá ser
realizado na escuridão para evitar a degradação dos flavonoides.
2. Colocar o homogenado em tubo de centrífuga tapado com papel de alumínio e
centrifugar a 10000x g durante 10 minutos a 4ºC.
3. Acertar o sobrenadante para 10 ml com etanol a 85%, adicionar 150 µl 5% NaNO2
e incubar 5 min a 50ºC.
4. Dividir o sobrenadante equitativamente (5 ml) por 2 tubos falcon tapados (A e B)
com papel de alumínio.
5. Ao tubo falcon B adicionar respetivamente 100 µl de 10% AlCl3 e incubar 5 min a
50ºC.
6. Fazer duas séries de padrões (A e B). Na série A pipetar para microtubos 5000 µl
de soluções padrão de quercetina (0, 0.01, 0.02, 0.03 e 0.05 mg/ml) em etanol 85%
adicionar 75 ul NaNO2 e incubar 5 min a 50ºC. Na série B pipetar para microtubos
5000 µl de soluções padrão de quercetina (0, 0.01, 0.05, 0.1 e 0.5 mg/ml) em
etanol 85% adicionar 75 ul NaNO2 e incubar 5 min a 50ºC. Adicionar 100ul
10%AlCl3 e incubar mais 5 minutos.
7. Arrefecer todos os tubos em gelo antes de passar as soluções para cuvetes PMMA
(UV).
Obtenção dos espectros de absorção dos flavonoides (quercetina)
8. Calibrar o espectrofotómetro com etanol a 85% (tubo 0 série A).
9. Fazer os espectros de absorção entre 320 e 550 nm para os padrões e as
amostras da série A.
10. Imprimir o espetro e os valores de absorvância.
11. Repetir os passos 9 a 11 para os tubos da série B (padrões e amostras).
Cálculos
12. Determinar a quantidade de quercetina em mg/g DW usando a equação da reta.
13. Comparar os conteúdos de quercetina obtidos com valores descritos na
bibliografia.
Você também pode gostar
- Potenciometria: aspectos teóricos e práticosNo EverandPotenciometria: aspectos teóricos e práticosAinda não há avaliações
- Síntese Do Cloreto de HexaaminocobaltoDocumento4 páginasSíntese Do Cloreto de HexaaminocobaltoMaiara SoaresAinda não há avaliações
- Desidrataçao de AlcooisDocumento3 páginasDesidrataçao de AlcooisEfrero RochyAinda não há avaliações
- Oxidação Do Mentol RelatórioDocumento7 páginasOxidação Do Mentol RelatórioStefany Thábian VieiraAinda não há avaliações
- Relatório 7 BioquimicaDocumento7 páginasRelatório 7 BioquimicaWeslei Bruno BoteroAinda não há avaliações
- Aula 3 - Estudos de Caso e Exercícios - v04Documento9 páginasAula 3 - Estudos de Caso e Exercícios - v04ALINE BEATRIZ SOARES PASSERINIAinda não há avaliações
- Laboratório de QuímicaDocumento4 páginasLaboratório de QuímicaDanielle BrandãoAinda não há avaliações
- Controle de Qualidade Físico-Quimico AdjuvantesDocumento6 páginasControle de Qualidade Físico-Quimico AdjuvantesasAinda não há avaliações
- Estudo Dirigido Reações OrgânicasDocumento30 páginasEstudo Dirigido Reações OrgânicasDanilo TourinhoAinda não há avaliações
- Relatorio BenzalacetonaDocumento3 páginasRelatorio BenzalacetonaJurandirGoisAinda não há avaliações
- QA SebentaDocumento8 páginasQA SebentaDiego FigueiraAinda não há avaliações
- Analise CloretoDocumento16 páginasAnalise CloretoRafamizutaAinda não há avaliações
- Introdução HidrocarbonetosDocumento10 páginasIntrodução HidrocarbonetosHadilson Chim Jin100% (1)
- Relatório Cloreto de Terc-ButilaDocumento6 páginasRelatório Cloreto de Terc-ButilaThais Almeida100% (1)
- Relatorio DibenzilacetonaDocumento11 páginasRelatorio DibenzilacetonaVictor Augusto Ferres ChaconAinda não há avaliações
- Pratica 8 CorretaDocumento10 páginasPratica 8 CorretalaisyAinda não há avaliações
- Relatório 2 - Acetilacetonato de Ferro III - OkDocumento13 páginasRelatório 2 - Acetilacetonato de Ferro III - OkJacyara Flores Arbues Carneiro100% (1)
- Exp. 6 - CR (Acac)Documento8 páginasExp. 6 - CR (Acac)Natalia VenelliAinda não há avaliações
- Relatório OrganicaDocumento11 páginasRelatório OrganicaChristiane Meire100% (1)
- Síntese Cloreto de Tec-Butila - GustavoDocumento8 páginasSíntese Cloreto de Tec-Butila - GustavoMarcel AmorimAinda não há avaliações
- MIA I - Teste II 2015 - PLab - 20.01.2016Documento2 páginasMIA I - Teste II 2015 - PLab - 20.01.2016Angelique ViannyAinda não há avaliações
- Relatório Obtenção Do Cloreto de T ButilaDocumento8 páginasRelatório Obtenção Do Cloreto de T ButilaBeatriz MonteiroAinda não há avaliações
- Praticas 7 e 8Documento4 páginasPraticas 7 e 8Fernando SimoniAinda não há avaliações
- Protocolo Analitico para AlcalinidadeDocumento4 páginasProtocolo Analitico para AlcalinidadeThay SantosAinda não há avaliações
- Apostila Quimica Organica IIDocumento14 páginasApostila Quimica Organica IIdanjxdAinda não há avaliações
- Roteiro Prtico 2Documento5 páginasRoteiro Prtico 2Mariana KattahAinda não há avaliações
- Relatorio Quali AcetilenoDocumento7 páginasRelatorio Quali AcetilenocandysuhAinda não há avaliações
- Relatório 4 - Análise InstrumentalDocumento7 páginasRelatório 4 - Análise InstrumentalFrancisco PalacioAinda não há avaliações
- Tulueno, Antraceno e AftalenoDocumento14 páginasTulueno, Antraceno e AftalenovaldemarbastanteAinda não há avaliações
- Experimento 9Documento5 páginasExperimento 9Talitha Ortiz100% (1)
- Preparação Do Cicloexeno - Amanda Rangel e Milena Amorim.Documento12 páginasPreparação Do Cicloexeno - Amanda Rangel e Milena Amorim.Amanda AlmerindoAinda não há avaliações
- Síntese Do Cloreto de Terc-Butila - Química - UTFPR - 2010Documento16 páginasSíntese Do Cloreto de Terc-Butila - Química - UTFPR - 2010joaomarcosls94% (17)
- Exercícios DestilaçãoDocumento12 páginasExercícios DestilaçãoVITORIA DE OLIVEIRA SOARESAinda não há avaliações
- Prática 3Documento4 páginasPrática 3Albert SantosAinda não há avaliações
- Artigo Magnésio No SoloDocumento12 páginasArtigo Magnésio No SoloDanyela CardosoAinda não há avaliações
- 8 HidroxiquinoleinaDocumento15 páginas8 HidroxiquinoleinaLubaki Francisco FranckAinda não há avaliações
- 2023 QA Lab 5 - Coeficiente de Partição Do Violeta de GencianaDocumento4 páginas2023 QA Lab 5 - Coeficiente de Partição Do Violeta de GencianaMartaAinda não há avaliações
- CiclohexenoDocumento3 páginasCiclohexenosegecsAinda não há avaliações
- Relatório 03 - Síntese Cloreto de Hexaminoníquel (II)Documento13 páginasRelatório 03 - Síntese Cloreto de Hexaminoníquel (II)Marcos Vinicius MarquesAinda não há avaliações
- DUREZADocumento6 páginasDUREZAAlisson AlmeidaAinda não há avaliações
- Revisão Unesp 2021Documento7 páginasRevisão Unesp 2021ALLANA OLIVEIRAAinda não há avaliações
- Relatório 4 - Síntese Do Composto DibenzalacetonaDocumento12 páginasRelatório 4 - Síntese Do Composto DibenzalacetonaMarcel Amorim0% (1)
- Preparação Do CicloexenoDocumento7 páginasPreparação Do CicloexenoGuilherme Romano De ChicoAinda não há avaliações
- Alcinos. 3º Grupo. Turma DD BiologiaDocumento11 páginasAlcinos. 3º Grupo. Turma DD BiologiaAlbino Sande FrançaAinda não há avaliações
- QUÍMICA - Mod9 - Propriedades Compostos OrganicosDocumento2 páginasQUÍMICA - Mod9 - Propriedades Compostos Organicosjade lopesAinda não há avaliações
- Síntese e Isomerização Do (Co (NH3) 5ONO3) Cl2Documento14 páginasSíntese e Isomerização Do (Co (NH3) 5ONO3) Cl2Lorena Tuane100% (1)
- Tecnico Laboratorio QuimicaDocumento12 páginasTecnico Laboratorio QuimicaFernandaAinda não há avaliações
- Metodo Flavonoides Totais - GeanDocumento3 páginasMetodo Flavonoides Totais - GeanLeonardo PennaAinda não há avaliações
- Obteção Do Cicloexeno A Partir Do CicloexanolDocumento8 páginasObteção Do Cicloexeno A Partir Do CicloexanolGabriel GumaAinda não há avaliações
- Lista de ExercíciosDocumento2 páginasLista de ExercíciosGiovanna Rodrigues CostaAinda não há avaliações
- RELATÓRIO QUÍMICA - Identificação de Grupos FuncionaisDocumento13 páginasRELATÓRIO QUÍMICA - Identificação de Grupos FuncionaisAmanda Ayumi0% (1)
- DocumentoDocumento14 páginasDocumentodeborahj4527jesusAinda não há avaliações
- Exercciodestilao 1Documento2 páginasExercciodestilao 1Débora QueirozAinda não há avaliações
- Relatorio Organica 5Documento11 páginasRelatorio Organica 5carolina gonçalvesAinda não há avaliações
- Especificação de Insumo - Meleato de EnalaprilDocumento2 páginasEspecificação de Insumo - Meleato de EnalaprilRamon barbosaAinda não há avaliações
- Óleo FuselDocumento3 páginasÓleo FuselharecbaAinda não há avaliações
- Lista de Exercícios - Balanço Material - BMEDocumento3 páginasLista de Exercícios - Balanço Material - BMEVinícius RibeiroAinda não há avaliações
- Prática 3 - PREPARAÇÃO DE CLORETO DE PENTAAMINOCLOROCOBALTO (III)Documento4 páginasPrática 3 - PREPARAÇÃO DE CLORETO DE PENTAAMINOCLOROCOBALTO (III)Aline ScarduaAinda não há avaliações
- As Plantas Medicinais Baseiam-Se Nas Propriedades de Metabolitos SecundáriosDocumento28 páginasAs Plantas Medicinais Baseiam-Se Nas Propriedades de Metabolitos SecundáriosMatheus AlmeidaAinda não há avaliações
- PDF-BM2-aula 8TDocumento18 páginasPDF-BM2-aula 8TMatheus AlmeidaAinda não há avaliações
- PDF-BM2-aula 9TDocumento31 páginasPDF-BM2-aula 9TMatheus AlmeidaAinda não há avaliações
- Sintese de Terpenoides: A Adição Repetitiva de Unidades em C5 É Realizada Por PreniltransferasesDocumento26 páginasSintese de Terpenoides: A Adição Repetitiva de Unidades em C5 É Realizada Por PreniltransferasesMatheus AlmeidaAinda não há avaliações
- 2 TerpenoidesDocumento13 páginas2 TerpenoidesMatheus AlmeidaAinda não há avaliações
- 2c-Cumarinas, Estilbe-Nos, Estirilpironas, e ArilpironasDocumento10 páginas2c-Cumarinas, Estilbe-Nos, Estirilpironas, e ArilpironasMatheus AlmeidaAinda não há avaliações
- 2b-Lignanas, Ligninas e Suberização: Tecido Suberizado Tecido LenhificadoDocumento26 páginas2b-Lignanas, Ligninas e Suberização: Tecido Suberizado Tecido LenhificadoMatheus AlmeidaAinda não há avaliações
- Método Filosofico X Método CientíficoDocumento1 páginaMétodo Filosofico X Método CientíficoMatheus AlmeidaAinda não há avaliações
- Metabolitos SecundáriosDocumento34 páginasMetabolitos SecundáriosMatheus AlmeidaAinda não há avaliações
- Síntese Dos Compostos de Cobalto Nitrato de Tetraamimcarbonatocabalto (Iii) e Cloreto de Pentaamimclorocobalto (Iii)Documento14 páginasSíntese Dos Compostos de Cobalto Nitrato de Tetraamimcarbonatocabalto (Iii) e Cloreto de Pentaamimclorocobalto (Iii)Luis ManoAinda não há avaliações
- Constituição, Propriedades e Classificação de SolosDocumento35 páginasConstituição, Propriedades e Classificação de SolosAngelica_RCunhaAinda não há avaliações
- Apostila de Bioquímica - PráticaDocumento18 páginasApostila de Bioquímica - PráticaRayssa LamaniereAinda não há avaliações
- Analítica A - Apostila LabDocumento27 páginasAnalítica A - Apostila LabLorraine OliveiraAinda não há avaliações
- Trabalho e Gênese Do Ser Social Na "Ontologia" de György LukácsDocumento305 páginasTrabalho e Gênese Do Ser Social Na "Ontologia" de György Lukácseditoriaemdebate100% (1)
- Revisitando A AtlântidaDocumento14 páginasRevisitando A AtlântidaMichael TuckerAinda não há avaliações
- Lista de Exercícios - Cinética QuímicaDocumento4 páginasLista de Exercícios - Cinética QuímicaMary Eduarda MoraesAinda não há avaliações
- Qumica de Coordenacao - Um Sonho Audacioso de Alfred WernerDocumento22 páginasQumica de Coordenacao - Um Sonho Audacioso de Alfred WernerNathalyAinda não há avaliações
- AcidezDocumento47 páginasAcidezNúbia NunesAinda não há avaliações
- Catalise em Compostos de CoordenaçãoDocumento42 páginasCatalise em Compostos de Coordenaçãonetochemistry0% (1)
- Complexo de CobaltoDocumento16 páginasComplexo de CobaltoCezar ManziniAinda não há avaliações
- Relatorio Hexaaquacobalto IIDocumento11 páginasRelatorio Hexaaquacobalto IIIbraima Bente DjaloAinda não há avaliações
- 5 Compostos de CoordenaçãoDocumento49 páginas5 Compostos de CoordenaçãoRipardoWembliAinda não há avaliações
- Aulas Praticas AnaliticaDocumento24 páginasAulas Praticas AnaliticaMah NovaesAinda não há avaliações
- Prova Química IIDocumento16 páginasProva Química IIAdryana SousaAinda não há avaliações
- Aspectos de Simetria Molecular e A Hibridizacao de Orbitais AtomicosDocumento6 páginasAspectos de Simetria Molecular e A Hibridizacao de Orbitais AtomicosTarso RezendeAinda não há avaliações
- Aula de Complexação Parte 1 - 1S2015Documento27 páginasAula de Complexação Parte 1 - 1S2015Neto GomesAinda não há avaliações
- Boro Quelato 1Documento3 páginasBoro Quelato 1Igor BiggieAinda não há avaliações
- Ácidos e Bases Duros e MolesDocumento21 páginasÁcidos e Bases Duros e MolesBruno Poleto0% (1)
- Prática 2 Química InorgânicaDocumento7 páginasPrática 2 Química InorgânicaRichard Gabriel Freitas GuedesAinda não há avaliações
- Slides Química de OrganometálicosDocumento106 páginasSlides Química de OrganometálicosLucas Ferreira da SilvaAinda não há avaliações
- Relatorio Leite em Pó COMPLEXAÇÃO PRONTODocumento12 páginasRelatorio Leite em Pó COMPLEXAÇÃO PRONTOthalita santos alvesAinda não há avaliações
- Relatório Cromatografia de Troca IônicaDocumento21 páginasRelatório Cromatografia de Troca IônicaErickson Azevedo Cristovão100% (1)
- Aula 02Documento187 páginasAula 02Anonymous UYDJtUnAinda não há avaliações
- Metaprojeto - Dijon de MoraesDocumento7 páginasMetaprojeto - Dijon de MoraesSergio SudsilowskyAinda não há avaliações
- Relatório Grupo 15 - Compostos de NitrogênioDocumento13 páginasRelatório Grupo 15 - Compostos de NitrogênioDimas BritoAinda não há avaliações
- BLOCO D E BLOCO FDocumento17 páginasBLOCO D E BLOCO FFabi MansillaAinda não há avaliações
- Volumetria de Complexacao (Reparado)Documento21 páginasVolumetria de Complexacao (Reparado)Arïgë Ussënë RæjæbœAinda não há avaliações
- Síntese e Caracterização Do Complexo K3Documento7 páginasSíntese e Caracterização Do Complexo K3Laís BarbosaAinda não há avaliações
- Compostos de CoordenacaoDocumento59 páginasCompostos de CoordenacaoDouglas Leonardo100% (1)